人参中五氯硝基苯残留的加工因子测定及其在膳食暴露评估中的应用
王 莹, 李耀磊, 于新兰, 王 赵, 金红宇∗, 马双成∗
(1.中国食品药品检定研究院中药民族药检定所,北京 100022;2.新疆维吾尔自治区食品药品检验所,新疆乌鲁木齐 830049)
2015年版 《中国药典》一部在药材人参正文项下增加了16种有机氯的农残限度检查[1]。基于前期数据监测,按照2015版药典规定人参中五氯硝基苯 (PCNB)不得过0.1 mg/kg的要求,人参中PCNB的超标率较高。PCNB属有机氯取代苯类杀菌剂,化学性质稳定,对人畜低毒,对皮肤有一定的刺激性。在土壤中相当稳定,其半衰期约为4~10 个月, ADI 为 0.01 mg/kg b.w.[2]。 但其杂质六氯苯是一种持久性有机污染物POPs,具有长期残留性、生物蓄积性和高毒性,能够导致生物体内分泌紊乱、生殖及免疫机能失调以及癌症等疾病[3]。PCNB在一些发达国家和地区已被列入环境激素污染物化学品目录中,在某些食品作物上禁用或限制使用。由于致癌以及环境因素等原因,日本、新西兰、瑞士、德国、韩国、印度及中国台湾地区已全面禁止PCNB的使用。目前在我国取得PCNB登记的产品有25个,PCNB并未在人参药材中登记。故从其危害性、高检出率、不规范使用等方面,人参中PCNB摄入风险评估具有重要意义。
农药残留风险评估是指通过测定农药的生物效应、毒理学、污染水平和膳食暴露量等数据,定性或定量描述农药残留对健康或生态的风险。随着农药残留超标现象日益严重,开展食品药品中农药残留风险评估成为当前关注的热点问题。值得关注的是,从人参药材到入口服用通常会经过加工处理(如水煎煮、乙醇提取、水浸泡等),这些加工方式会在不同程度上影响药材中的农药残留水平。在此过程中,若不考虑加工因素对农药残留的影响而直接进行膳食暴露评估,则会高估或低估农药残留的暴露风险。加工处理对农药残留的影响程度通常采用加工因子 (PF)来描述。将加工因子纳入暴露评估模型中,是国际上优化评估方法、提高评估结果准确性的通行做法[4-7]。德国联邦风险评估研究所 (BfR)在加工因子方面做了较多研究,其数据库提供了多种农药在不同产品中的加工因子[8],目前国外针对食品加工因子的研究也较多[9-10]。近些年来,中药中逐步开展了有害残留物风险评估的研究工作[11-15],但针对农药考虑加工因子的风险评估工作尚处于空白状态。
本研究测定了不同加工方式获得的人参产品中PCNB的残留量,得出PCNB不同加工过程中的加工因子,应用于暴露评估,并为其他中药材风险评估提供有益借鉴。
1 材料
789 0 A气相色谱仪配置电子捕获检测器、旋转蒸发器、超声仪、离心机 (美国Agilent公司)。丙酮、二氯甲烷、正己烷为色谱纯 (美国Fisher公司);浓硫酸 (优级纯,国药集团)。22种有机氯农药混标对照品 (约10 μg/mL,中国食品药品检定研究院)。10批人参饮片来源于市场抽样,经中国食品药品检定研究院中药民族药检定所康帅助理研究员鉴定为正品。
2 方法
2.1 农药标准溶液制备
2.1.1 农药工作对照溶液制备 精密量取22种有机氯农药混标1 mL至100 mL量瓶中,用正己烷稀释至刻度,摇匀,作为对照品工作溶液 (100 ng/mL)。
2.1.2 标准曲线制备 分别精密量取适量工作对照溶液,用正己烷稀释成 1、2、5、10、20、50 ng/mL的对照品溶液,进行标准曲线测定。
2.2 人参中PNCB残留测定方法
2.2.1 人参中PNCB测定前处理方法 取人参粉末约5 g,精密称定,置100 mL具塞锥形瓶中,加水30 mL,振摇10 min,精密加丙酮50 mL,称定质量;超声处理30 min,放冷,再称定质量;用丙酮补足减失的质量,再加氯化钠约8 g,精密加二氯甲烷25 mL,称定质量,超声处理15 min,再称定质量;用二氯甲烷补足减失的质量,振摇使氯化钠充分溶解,静置,离心 (3 000转/min)3 min,使完全分层,将有机相移入装有适量无水硫酸钠的具塞锥形瓶中,放置0.5 h。精密量取15 mL,于40℃水浴上减压浓缩至约 1 mL,加正己烷约5 mL,减压浓缩至近干,用正己烷溶解并转移至5 mL量瓶中,并稀释至刻度,摇匀。小心加入硫酸 1 mL, 振摇 1 min, 离心 (3 000 转/min)5 min,分取上清液,即得。
2.2.2 色谱条件 DB-1707毛细管柱(30 m×0.32 mm,0.25 μm), Ni-ECD 电子捕获检测器;进样口温度230℃;检测器温度300℃;进样量1 μL,不分流进样;色谱柱升温程序为初始60℃,60℃/min升至170℃,5℃/min升至220℃,保持13 min,5℃/min升至240℃,25℃/min升至280℃,保持5 min。
2.3 人参不同加工方式处理方法
2.3.1 水浸泡 精密称取人参粉末5 g,置200 mL烧杯中,加沸水 100 mL,加盖,静置1.0 h。取全部上清液至分液漏斗中,加入正己烷30 mL,振荡萃取2 min,取上层正己烷层至梨形瓶中。重复萃取操作3次,回收所有上层正己烷至梨形瓶中,50℃下减压浓缩至少许,移入25 mL量瓶中,用正己烷定容至刻度。取5 mL溶液至15 mL离心管中,再加入1 mL硫酸溶液,振荡1 min, 离心 (3 000转/min) 5 min, 取上清液,即得供试品溶液a。
2.3.2 水煎煮 精密称取人参粉末5 g,置500 mL烧杯中,加水100 mL,加盖置于电炉上加热。待水沸腾后,保持微沸煎煮1 h。静置取上清液至分液漏斗中,按 “2.3.1”项下方法配制,最终得供试品溶液b。
2.3.3 75%乙醇提取 精密称取人参粉末5 g,置150 mL锥形瓶中,加75%乙醇100 mL,加热回流2 h。待冷却后,取上清液至分液漏斗中,按“2.3.1”项下方法配制,最终得供试品溶液c。
2.3.4 加工后剩余粉末PCNB测定 将上述“2.3.1”至 “2.3.3”项中处理后的人参粉末,置于烘箱中,50℃干燥6 h,得干燥粉末。精密称取此粉末2 g,按 “2.2.1”项下方法操作。
2.4 暴露评估方法 农药残留膳食暴露评估通常是指对农产品或食品来源的农药残留可能摄入量的定量评价,即根据农药残留水平和人群膳食特点估计某农药的膳食暴露值。其中确定性评估也称为点评估,是以点值的形式对人群的暴露参数作出的简单描述。此种评估方法简单易操作,应用最为广泛。在点评估过程中,除了了解膳食量和最大残留量外,探索成品的加工因子,对于准确的进行暴露评估有重要意义。引入加工因子的点评估模型[5]如公式 (1)、(2) 所示。
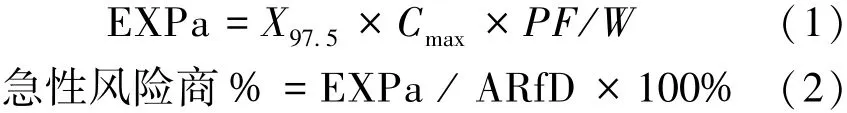
式中EXPa代表某种化学物的短期暴露量;X97.5代表食物消费量分布的97.5%分位数,本研究参考中国药典规定人参最大日用量,即9 g;Cmax代表食物中某一化学物的最大残留量,本实验采用了10批人参药材 PCNB的最大残留量,即14.0 mg/kg;PF代表成品的加工因子;W代表人群的平均体质量,以60 kg计。急性风险商为短期暴露量值与安全参考剂量ARfD的比值,当风险商小于1时,表明暴露风险可以接受。
3 结果
3.1 人参中PCNB测定方法的准确度 与2015版《中国药典》四部通则2531有机氯测定第一法相比,本研究对方法中的参数稍作改变,例如将正己烷代替石油醚作为最终定容溶液等,对本方法测定PCNB的灵敏度、准确性及线性进行考察。对6份空白样品采用加标回收方式,添加质量分数为0.1 mg/kg。结果显示PCNB回收率为103.3%,重现性2.13%,检测限为0.002 5 mg/kg,PCNB的线性方程为Y=7X-75.12,r=0.999。表明在1.0~100 ng/mL范围内,线性良好。该方法的准确度良好。
3.2 水及乙醇溶液中PCNB测定方法的准确性 采用空白试剂中加标回收方式,加标质量浓度为100 ng/mL,平行操作6份。结果表明,水及75%乙醇溶液中PCNB的提取回收率可达95%以上,RSD%小于4.0%。表明该方法准确度良好。
3.3 10批人参中PCNB测定结果 对市售的10批人参药材采用 “2.2.1”项下方法处理,每个样品平行处理2份,最终测得PCNB结果见表1。

表1 10批样品PCNB测定结果Tab.1 Results of PCNB residues in ten batches of samples
3.4 不同加工方式PCNB转移以及残留率 采用水浸泡、水煎煮、75%乙醇提取3种方法对人参中PCNB在药液中的转移及药材残渣中的残留情况进行测定,见图1。每种方法转移率重复测定3次,取平均值。根据加工因子的计算公式[5],即PF=加工产品中的农药残留量/初级原料中的农药残留量,见表2。
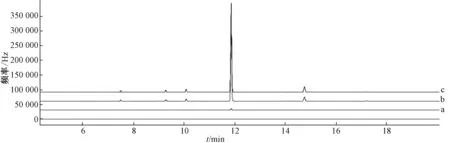
图1 样品中五氯硝基苯不同加工方式比较图Fig.1 Comparison of PCNB residues with different extract methods in samples
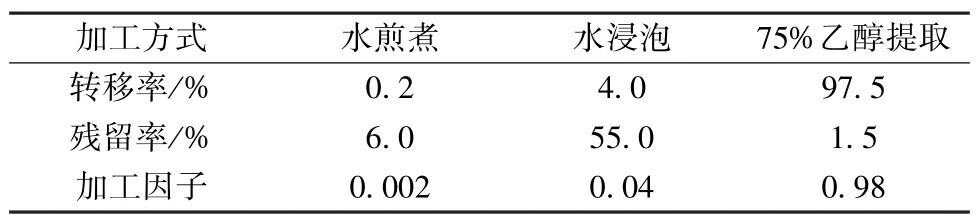
表2 不同加工方式PCNB转移率Tab.2 The transfer rates of PCNB residues with different extract methods
结果显示水煎煮、水浸泡2种情况下,转移至药液中的PCNB农药量极低,不到5%,可能主要是由于PCNB作为有机氯农药,其水溶性极差,即使在煎煮、浸泡过程中亦少有转移。采用水浸泡和煎煮方式后,药材中残留的PCNB量有所差别,煎煮后药材中PCNB很低仅为6%,而浸泡后PCNB在药材中的残留量依旧很高为55.0%,有可能在水煎煮这种剧烈的条件下,PCNB发生了分解。75%乙醇提取方式几乎将药材中绝大部分PCNB转移至药液中。一般情况下若加工因子小于1,则表明加工过程农药残留水平降低,反之则表示残留水平升高。
4 讨论
4.1 必要性 目前农药残留监测都是针对初级产品,未考虑加工过程对农药残留的影响,故在使用这些数据进行膳食暴露评估时,往往会导致高估、低估,同样不同加工方式也会影响产品中最大残留限量MRL的制定。如FAO/WHO规定戊唑醇在葡萄中的MRLs值为2 mg/kg,葡萄酒生产过程能降低其残留,显然用葡萄中MRLs值进行膳食暴露评估时会高估其对人体健康的影响,故Gonzalez-Rodriguez等[16]建议将葡萄酒中的戊唑醇MRLs值修订为0.25 mg/kg。本研究中,如果不考虑加工过程,则风险评估结果与实际摄入情况差异较明显,尤其是在水煎煮食用方式下,加工因子为0.002。评估人参水煎煮药液PCNB的每日摄入量时,是否引入加工因子这一因素,将导致结果相差500倍,即对风险明显的高估。因此,必须充分了解不同加工过程对农药残留的影响,才能准确的开展膳食暴露评估工作。
4.2 摄入风险评估 人参药材或饮片直接使用时,按照2015版中国药典煎服最大推荐用量为9 g计,研粉吞服的推荐量为2 g。国家风险评估中心张磊等[17]对全国各地区中草药食用方式进行调查,发出3 000多份调查问卷,得出结论中草药最常见的服用方法是煎服,约有49.1%的人曾采用过煎服的方式;其次是用中草药煮汤或者泡水的有39.4%。故对于药材采用了水煎煮、水浸泡、研粉吞服3种方式的风险分析。
进一步了解含人参中成药的工艺过程,查阅2015版 《中国药典》总结出目前所收录的中成药品种中有70个品种含有人参药材,而其中以原粉入药的炮制方式所占比例最大,达到81.4%,剩余为水煎煮和乙醇提取,见表3。

表3 中国药典中含人参中成药各制法所占比例Tab.3 Proportion of Chinese patent medicines containing P.ginseng in Ch.P
70种中成药中人参处方比例为0.2%~20%,按照药典用法用量对以上70种进行统计,原粉入药的成药人参日最大摄入量约2.5 g(参芩白术丸);75%乙醇提取入药的日最大摄入量为2 g(津力达颗粒);水煎煮入药的人参日最大摄入量约3 g。分别对3种方式的最大摄入值代入公式 (2)进行风险分析。由于缺少PNCB的ARfD值,本研究安全参考剂量采用了ADI值。将表2中得出的加工因子代入公式 (1)、(2),对中药材及含人参中成药不同加工方式PCNB的暴露量及急性风险商进行计算,见表4。
表4显示,按照风险商值进行判断,人参药材煎煮、泡水及通过煎煮制成中成药的方式,产生的风险商均很低,不到1.0%,可认为通过此类方式摄入人参产生风险极小。直接采用药材研粉吞服,以及原粉入药和75%乙醇提取制成中成药的方式,产生的风险商分别为4.67%、5.83%、4.57%,风险值亦较低。但考虑到联合风险评估,由于中药材摄入在人体总的膳食结构中所占比例很低,故此3种方式的风险仍需关注。比如按照2015版 《中国药典》四部9302通则,农药残留量最大限量制定时安全因子设为100,即认为每日由中药材及其制品中摄取的农药残留量应不大于日总暴露量的 1%[18]。
4.3 局限性 本研究中加工因子的测定为实验条件下进行,样品量均较小,且加工的重要参数亦与实际生产有所差异。而这些参数都会对结果产生一定影响,比如水煎煮、乙醇提取时间、提取溶剂体积、提取温度等。故要获得某一具体品种的PCNB加工因子,还应尽可能使实验室模拟的加工过程接近商业化加工过程,或者在工厂生产条件下,从中药材到成品分阶段对其中的农药残留量进行监控,从而得到更具有实际应用价值的结果。
本研究建立了人参粉末、人参药液、75%乙醇提取液中 PCNB的测定方法。对10批人参中PCNB残留量进行测定,不合格率较高达到50%。对不同加工方式中PCNB的转移进行测定,得出转移率及加工因子,通过点评估模式计算风险商。虽然人参中PCNB不合格率较高,但通过摄入人参中PCNB对人体产生风险的可能性很低。其中采用水煎煮、水浸泡方式,药液中PCNB量极低。人参药材研粉吞服、原粉入药、75%乙醇提取后中成药的风险相对较高,应引起关注,必要时应增加含人参此类工艺中成药的PCNB限度检查。

