硫酸钙链霉素的颗粒体外缓释性能的研究
陈勇忠 卫秀洋 翁少煌 刘永平


[摘要] 目的 了解载结核药链霉素的硫酸钙缓释颗粒在体外的药物缓释性能。 方法 实验组,将链霉素与医用硫酸钙混合制备成载药颗粒,将其置于模拟体液中,取1 d、2 d、3 d、1周、2周、4周、6周、8周、10周时缓冲液为样本,高效液相色谱法(HPLC)检测其中链霉素药物的浓度,绘制药物缓释曲线。空白组,医用硫酸钙制备成未载药颗粒。 结果 医用硫酸钙5 cc与链霉素1 g为最佳配比。载链霉素硫酸钙颗粒在模拟体液中浸泡,缓释颗粒3 d时累计释放量15.33%。在8周前的样本液中,药物浓度均较高;至8周时链霉素的释出浓度、仍达到的最小抑菌浓度,之后逐渐降低。未载链霉素的硫酸钙颗粒在有效检测时间内药物出峰时间处未见波峰出现。 结论 硫酸钙链霉素颗粒具有效缓释性能。8周内模拟体液中释出药物的浓度均可达到抑制结核分枝杆菌的浓度。
[关键词] 硫酸钙;链霉素;缓释;体外实验
[中图分类号] R969 [文献标识码] B [文章编号] 1673-9701(2019)01-0040-04
Study on the sustained release properties of calcium sulfate streptomycin particles in vitro
CHEN Yongzhong1 WEI Xiuyang1 WENG Shaohuang2 LIU Yongping1
1.Department of Orthopaedics,476 Hospital of Fuzhou General Hospital,Fuzhou 350002,China;2.College of Pharmacy,Fujian Medical University,Fuzhou 350002,China
[Abstract] Objective To understand the drug release properties of calcium sulfate sustained-release granules carrying the tuberculosis drug streptomycin in vitro. Methods In the experimental group, streptomycin was mixed with medical calcium sulfate to prepare drug-loaded granules, which were placed in simulated body fluids. The buffer at 1 day, 2 days, 3 days, 1 week, 2, 4 , 6, 8 and 10 weeks was used as a sample. The concentration of streptomycin was detected by high performance liquid chromatography(HPLC), and the drug sustained-release curve was drawn. In the blank group, medical calcium sulfate was prepared as unloaded particles. Results The medical calcium sulfate 5 cc and streptomycin 1g were the best ratio. The streptomycin calcium sulfate particles were soaked in the simulated body fluid, and the cumulative release of the sustained-release particles was 15.33%. In the sample solution before 8 weeks, the drug concentration was higher. Release concentration of streptomycin and still reached minimum inhibitory concentration at 8 weeks, and then gradually decreased. Calcium sulfate particles without streptomycin showed no peaks at the peak time of the drug during the effective detection time. Conclusion Calcium sulfate streptomycin granules have a slow release property. The concentration of the drug released in the simulated body fluid can reach the concentration of inhibiting tuberculosis within 8 weeks.
[Key words] Calcium sulfate; Streptomycin; Sustained release; In vitro experiments
脊柱是骨結核的好发部位之一,如果诊治不及时或不规范,极易造成椎体破坏、甚至累及椎管,压迫脊髓神经,造成瘫痪[1-2]。椎体的上下终板主要由软骨细胞、致密胶原及糖蛋白基质共同构成,自身修复困难。同时病灶周围坏死硬化的骨具有屏障作用,导致局部药物浓度过低或者不能达到病灶[3-4]。因此在治疗脊柱结核的时候,不仅要规范的抗结核,维持局部有效血药浓度,还要解决病灶填充、修复、成骨的问题。医用硫酸钙具有较好的抗压缩强度、组织相容性、缓释性能、成骨特性等优点,已成为近年研究的热点[5-9]。同时我院已将硫酸钙链霉素的颗粒已在临床应用,取得满意效果[10-11]。但是硫酸钙链霉素的颗粒缓释性能如何尚未见文献报道。本研究将载链霉素的硫酸钙颗粒浸泡在缓冲液中,在不同时间点取出缓冲液样本中,采用高效液相色谱法(high perfromance liquid chromatography,HPLC)测定药物浓度,评价其在体外的缓释性能。
1 材料与方法
1.1 主要仪器、材料与试剂
注射用硫酸链霉素(山东鲁抗医药股份有限公司,规格1 g/瓶,国药准字H37020187);医用硫酸钙(英国百赛公司,5 cc思迪骨粉,CS);岛津LC-15C型高效液相色谱仪(日本岛津公司);智能溶出实验仪(天大天发)。
1.2 不同规格的链霉素硫酸钙缓释系统的制作
不同规格的链霉素硫酸钙,如下方法制作成颗粒。用万能压力测试机测试各个比例材料颗粒的抗压强度和最大压缩力,并测得最佳混合配比(1 g链霉素注射粉剂:5 cc医用硫酸钙粉剂)。
以1 g 链霉素注射粉剂与5 cc医用硫酸钙粉剂,后加入2 mL配套的混合液(灭菌注射用水),搅拌至糊状,充填到模具中,10~15 min干硬后倒出便制成直径3 mm、厚3 mm的含链霉素的硫酸钙缓释颗粒,进行实验组实验。用同样方法制备不混合任何药硫酸钙固化颗粒,进行空白组实验。
1.3 缓释液的采集
取16块含链霉素的硫酸钙缓释颗粒,每块材料分别置入40 mL经 0.22 μm 滤器处理过的磷酸缓冲液(PBS,pH值7.3 5~7.40)模拟体液中,用生物半透膜包裹,避光放入37°C恒温振荡器中,转速设定为100 r/min 持续震荡于整个实验周期。每日取缓冲液5 mL,并回补PBS模拟体液5 mL。留取1 d、2 d、3 d、1周、2周、4周、6周、8周、10周各时间点缓冲液作为测定样本,用0.22 μm滤器过滤后加入l mL的进样瓶中避光保存,备高效液相色谱仪检测用。
1.4 缓释液药物浓度检测
采用高效液相色谱仪对不同时间点缓冲液样本中链霉素的药物浓度进行检测,计算单位时间段内药物的释放度。色谱条件:CN(5 μm)、250 mm ×4.6 mm色谱柱;流动相采用0.01 mol/L 庚烷磺酸钠(pH值3.0):乙腈=50:50;流速1.0 mL/min;检测波长203 nm;柱温30℃;进样体积10 μL。
利用HPLC 在上述色谱条件下检测已知浓度的链霉素溶液,进样本检测,通过测试设备软件分析进行数据处理,得出链霉素药物浓度的标准曲线方程。利用HPLC 在待检测样本,也在上述色谱条件下检测,不同时间点样本中链霉素对应的曲线峰面积,再通过标准曲线方程,换算得到各时间点缓冲液中药物的浓度。
1.5 统计学处理
采用SPSS 17.0 统计软件进行分析。计量资料以均数±标准差表示,用獨立样本t检验进行两组间的比较,计数资料采用频数和百分比表示。P<0.05为差异有统计学意义。
2 结果
2.1 硫酸钙链霉素颗粒的制备及体外内环境系统模型
硫酸钙链霉素颗粒的制备过程及颗粒的配比是在预实验下多次制作,重复性、稳定性良好。链霉素-硫酸钙颗粒电子显微镜下显示:结构其中以棒状结构为主,硫酸钙宽度为7.5 μm~10.0 μm,长40.0 μm~50.0 μm,链霉素为颗粒形状为主 5 μm×5 μm×5 μm。见图1a~c。
2.2 硫酸钙与链霉素颗粒的最佳混合比例
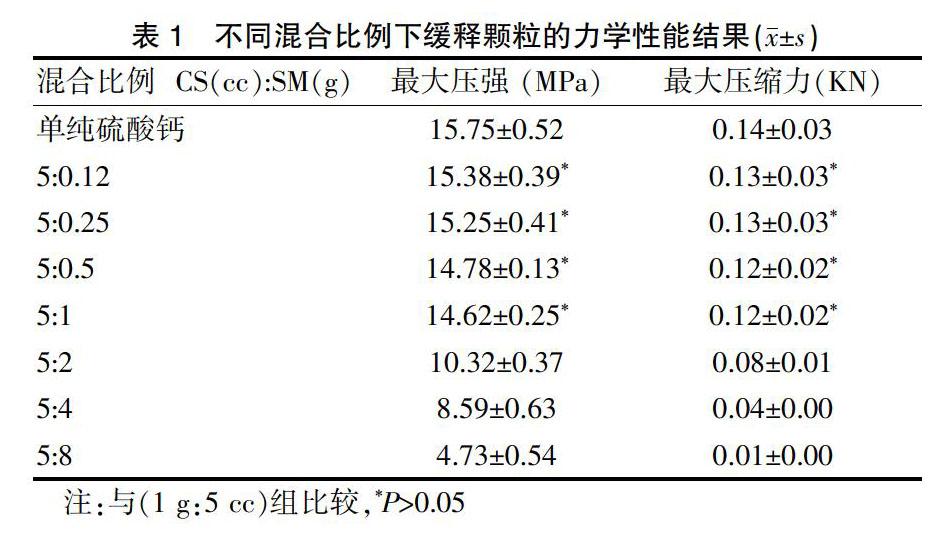
在缓释颗粒中,当链霉素与硫酸钙在比例在小于5 cc:1 g时缓释颗粒的抗压强度及最大压缩力,与单纯硫酸钙颗粒物无统计学意义(P>0.05)。当链霉素与硫酸钙在比例在大于5 cc:1 g抗压强度及最大压缩力开始下降。因此本研究认为缓释颗粒链霉素与硫酸钙在比例在大于5 cc:1g时为最佳配比。见表1。
2.2 硫酸钙链霉素颗粒与非载药硫酸钙HPLC 色谱图
硫酸钙链霉素颗粒缓冲液的色谱图显示,7.36 min为链霉素的药物峰。说明硫酸钙链霉素颗粒能够释药且能用HPLC法检测到药物浓度。未载药硫酸钙浸提液的色谱图显示,在7 min左右色谱图的未出现明显波峰,说明无药物峰,未检测到链霉素。见图1e~g。
2.3 载药人工材料体外缓释药物浓度
不同时间点浸提液中药物浓度。在前8周各个时间点的浸提液中药物浓度均较高至8周时链霉素的释出浓度均高于其10倍的最小抑菌浓度(MIC),之后逐渐降低。见表2。
2.4 载药人工材料体外缓释药物释放度
载链霉素硫酸钙颗粒在模拟体液中浸泡,缓释颗粒3 d时累计释放量15.33%。1周、2周时释放度分别为21.85%、62.31%。可见在1~2周时链霉素释放较快,存在一定的“突释”现象。之后逐渐平稳释放。在8周前的样本液中,药物浓度均较高;至8周时链霉素的释出浓度、仍达到的最小抑菌浓度,之后逐渐降低。见表2。
3 讨论
脊柱结核的治疗主要在于解决抗结核化疗、修复、脊柱稳定性的问题。通过手术固定可以获得脊柱稳定问题。手术后如何抗结核与骨修复成为治疗的热点。抗结核药物之一链霉素,临床常常采用肌肉注射。连续肌肉注射长达3个月,患者难以坚持。若在清除结核病灶后直接在创面撒上链霉素粉剂,有效药物浓度维持时间不够长;如果病灶内一次给予过量的药物,但其不良反应的发生率高。设计在病灶局部搭载含链霉素缓释药物人工骨支架植入是一种解决方案。本研究制备载了硫酸钙链霉素缓释颗粒,目的在于获得一种新型材料植人病灶清除之后的缺损部位,兼具抗结核和修复骨缺损的双重作用。硫酸钙是一种理想的骨替代材料,植骨效果与自体骨相当。广泛应用于口腔科和矫形外科[12-13]。选用其作为载体,可以修复病灶清除后的骨缺损。
实验设计原理是利用智能溶出实验仪,体外模拟体内环境,造出一个动态的内环境。将硫酸钙链霉素缓释颗粒在缓冲液内,每日提取部分缓冲液体,作为测量样本。同时补充缓冲液,模拟体内的液体交换。通过高效液相色谱法(HPLC)测定缓冲液,在不同时间点测定缓冲液体的药物浓度,评价酸钙链霉素颗粒在体外的缓释性能。
设计模型基本可以模拟体内环境。但是也存在局限性。体内环境较复杂,颗粒链霉素在体内不仅是代谢,吸收,还有伤口出血、渗出、引流丢失等。我们将每日提取缓冲液视为药物在体内的自然代谢。每次取样后在补充回缓冲液,以求保持体液的平衡。
在缓释颗粒中,硫酸钙作为载体,主要提供缓释效应,同时硫酸钙的量决定颗粒的硬度。颗粒的硬度又与颗粒的崩解时间正呈相关性。硫酸钙份量越大,颗粒硬度越硬,崩解时间相对持久。链霉素提供抗结核药物,链霉素总量决定局部药物浓度。链霉素的份量又与局部浓度呈正相关。链霉素份量越大,局部药物浓度相对较高。从颗粒力学性能结果显示,当链霉素与硫酸钙在比例在小于1 g:5 cc时缓释颗粒的抗压强度及最大压缩力,与单纯硫酸钙颗粒物无统计学意义(P>0.05)。当链霉素与硫酸钙在比例在大于1 g:5 cc抗压强度及最大压缩力开始下降。要做到缓释颗粒的持久缓释性能,既要保证颗粒的硬度,又要兼顾颗粒载药总量。因此我们认为缓释颗粒链霉素与硫酸钙在比例在大于1 g:5 cc时为最佳配比。
从药物缓释曲线显示,测定7周、8周时检测液中,链霉素的浓度9.01 μg/mL,0.07 μg/mL。链霉素的MIC为0.05 μg/mL。文献报道抗结核药物一般最低杀菌浓度MBC为最低抑菌浓度MIC的10倍[14]。所以在将近2个月内均能在最低杀菌浓度范围内。可见硫酸钙链霉素缓释颗粒这种缓释作用在抗结核疗程中具有重要临床意义的。
从绘制的药物释放度曲线显示,3 d、1周、2周时释放度分别15.33%、21.85%、62.31%。可见在1~2周时链霉素释放较快,存在一定的“突释”现象。之后药物释放度曲线逐渐平稳释放。药物的突释也是药物工作者共同存在的问题。突释效应一般出现在药物释放的最初阶段,在短时间内释放出大量的药物,产生全身不良反应。对于靶向缓释载体而言,这将导致靶部位有效药物质量的减少,最终削弱缓释载体的靶向作用。资料显示[15-16],药物突释的定义3 d内释放量比例不超过总量的40%。本缓释颗粒3 d时累计释放量15.33%,在药物突释的范围内。从实验观察结果显示,颗粒在缓冲液体内浸泡,在1~2周时出现崩解,颗粒碎裂,崩解后出现大量的小颗粒,小颗粒表面的链霉素大量释放,存在突释。之后曲线相对平稳,是由于颗粒在制作的过程中,通过加压,干燥过程,硫酸钙的棒狀结构和链霉素分子之间产生螯合作用,相互结合。虽然大颗粒遇水出现崩解,但是硫酸钙和链霉素小分子之间的螯合作用,硫酸钙分子逐渐释放出链霉素。同时颗粒在电镜下结构也显示,链霉素与硫酸钙棒状的分子结构,分子间相互交错成形,能够起到的缓慢释放作用的基础。
2005版《中国药典》规定体外药物释放开始0.5 h内的释放量应小于40%,对于安全性差的药物更应进行严格控制,相关文献也有诸多报到[17]。出于临床用药对人体绝对安全性的考虑,该钙链霉素缓释颗粒总药量小于每日临床口服与静脉滴注的用药量,且药物是在长时间内以相对稳定的速率释放的,保证单位时间内药物释放量处于安全范围内。
研究表明硫酸钙链霉素颗粒具有效缓释性能,模拟体液中释出药物的浓度可长期达到杀死结核分枝杆菌的浓度。课题也存在局限性,该颗粒的释放制作过程进一步优化,颗粒的配比需进一步细化,体外模拟装备不能完全等同体内实验。同时进行体内实验将后续报道。
[参考文献]
[1] Eva N,Paul N,FRC,et al. MDR tuberculosis critical steps for prevention and control[J]. N Eng J Med,2010, 363:1050-1058.
[2] 李大伟,马远征.骨关节结核局部药物缓释材料研究进展[J].中国防痨杂志,2013,35:(5):376-378.
[3] Diacon AH,Donald PR.The early bactericidal activity of antituberculosis drugs[J].Expert Rev Anti Infect Ther,2014,12(2):223-237.
[4] 王骞,耿广起,丛晓明,等. 载三联抗痨药硫酸钙/聚氨基酸缓释材料在兔脊柱结核模型体内的缓释性能[J].中国组织工程研究,2017,21(10):1520-1526.
[5] Mistry S,Roy S,Maitra NJ,et al. A novel, multi-barrier,drug eluting calcium sulfate/biphasic calcium phosphate biodegradable composite bone cement for treatment of experimental MRSA osteomyelitis in rabbit model[J].J Control Release,2016,239:169-181.
[6] Liu P,Jiang H,Li S,et al.Determination of anti-tuberculosis drug concentration and distribution from sustained release microspheres in the vertebrae of a spinal tuberculosis rabbit model[J].J Orthop Res,2017,35(1):200-208.
[7] 德向研,施建党,王自立,等. 载三联抗结核药硫酸钙/氨基酸聚合物人工骨体内缓释实验研究[J]. 中国脊柱脊髓杂志,2013,23(6):531-536.
[8] Wang P,Liu P,Peng H,et al.Biocompatibility evaluation of dicalcium phosphate/calcium sulfate/poly(amino acid)composite for orthopedic tissue engineering in vitro and in vivo[J].J Biomater Sci Polym Ed,2016,27(11):1170-1186.
[9] Wu CC,Hsu LH,Tsai YF,et al.Enhancement of biodegradation and osseointegration of poly(ε-caprolactone)/calcium phosphate ceramic composite screws for osteofixation using calcium sulfate[J].Biomed Mater,2016,11(2):125-132.
[10] 陈勇忠,王剑火,张朋,等.含链霉素医用硫酸钙人工骨修复胸腰椎结核骨缺损[J].中国组织工程研究,2014, 18(5):802-805.
[11] 陈勇忠,王剑火,张朋,等.一期后路病灶清除混合植骨内固定术治疗胸腰椎结核[J]. 临床骨科杂志,2014,17(6):626-632.
[12] 普有登,汤逊。硫酸钙骨移植替代材料的研究及应用进展[J].中国矫形外科杂志,2011,19(11):931-933.
[13] Yashavantha Kumar C,Nalini KB,Menon J,et al. Calcium sulfate as bone graft substitute in the treatment of osseous bone defects,a prospective study[J]. Journal of Clinical & Diagnostic Research Jcdr,2013,7(12): 2926-2928.
[14] 张俊山,王自力,施建党,等.复合三联抗抗结核药人工缓释材料体外抗结核性能[J].脊柱外科杂志,2014,12(6):380-384.
[15] 龙娜,吕竹芬.微球缓释系统的突释现象及其影响因素[J].中国药师,2010,13(3):421-423.
[16] 周林.抗结核药物研究进展[J].中国临床医生,2013,41(3):14-17.
[17] 刘海涛,施建党,王骞,等. 载三联抗痨药硫酸钙/聚氨基酸缓释人工材料体外缓释性能的观察[J].中国脊柱脊髓杂志,2015,25(3):239-244.

