SPF金黄仓鼠种群的建立及质量控制
张华琼, 夏 爽, 吴燕茹, 何 凡
(成都生物制品研究所有限责任公司, 成都 610023)
乙型脑炎(乙脑)活疫苗系用乙脑病毒减毒株(SA14-14-2株)接种原代仓鼠肾细胞,经培养、收获病毒液,加入适宜稳定剂冻干制成[1]。生产过程中使用的毒种、细胞基质、血清和胰酶等动物源性原材料的外源因子污染是所有活疫苗生产中普遍关注的问题。世界卫生组织(WHO)技术报告系列(TRS)现行版TRS980(附录7)为人用乙脑减毒活疫苗生产和质量控制提供了指南,其中,10~14日龄金黄仓鼠作为乙脑活疫苗生产用主要起始原材料,所用动物的13种病毒[2]应为阴性。为加速我国生产的人用疫苗得到世界的认可,2006年国药中生成都公司与美国适宜卫生科技组织(PATH)合作,开展乙脑活疫苗预认证工作。其中,建立SPF级金黄仓鼠种群是认证工作中的一个重要环节。
1 材料与方法
1.1 原有金黄仓鼠A种群
本单位金黄仓鼠一直用于乙脑减毒活疫苗的生产,并适应于SA14-14-2疫苗株的培养。种群最初来源于北京生物制品研究所,普通级,封闭群;2003年首次通过剖宫产手术净化,自建SPF金黄仓鼠种群(A),以降低疫苗外源因子污染的风险。A种群于屏障系统内饲养,常年保持4 000只繁殖母鼠,为乙脑疫苗生产提供10~14日龄动物。本研究随机选取20对40~60日龄A种群金黄仓鼠。
1.2 引进代乳鼠
根据动物生产的实际情况,结合外籍专家的建议,拟定6对动物按照既定的遗传矩阵配种,以建立新种群(B)。2010年10月从德国Charles River公司引进40~60日龄SPF级金黄仓鼠20只(8只雄性,12只雌性),于隔离器内饲养。
1.3 配种
2010年11月,代乳鼠先后2周分2批配种,每批6只雌鼠,用作代乳鼠。
本单位原有A种群金黄仓鼠20对分2批先后同步配种,作为供胎鼠,用于剖宫产。
1.4 剖宫产及代乳
检查受孕情况, 推算预产期, 一旦代乳鼠分娩,立即检查原有金黄仓鼠,结合腹部触诊,选择临产前母鼠实施剖宫产手术,取出仔鼠(定义为F0);同时淘汰代乳鼠的幼崽,将F0转移到代乳鼠笼盒内。因为代乳鼠只有7只先后妊娠,2010年12月,先后实施剖宫产手术一共代乳7窝(表1)。
1.5 传代
F0离乳后雌雄分别饲养,2个月后从2#~7#代乳鼠后代各挑选2对, 分别以A、C、E、G、I、K 表示F0(♀)遗传信息, 以L、B、D、F、H、J分别表示F0(♂)的遗传信息(表1), 按照既定的方式进行配种, 6 对 /组, 共两组(1 组备用), 生产出F1, 以此类推, 经过6次传代配种,F6具备全部6对动物(F0)的遗传信息(A~L)。具体配种方式见图1。

表1 金黄仓鼠的剖宫产和代乳情况Table 1 Caesarean and foster nursing in golden hamster 只

图1 配种矩阵图Figure 1 Mating matrix
1.6 扩群
自F6起,同窝留单一性别,随机交配,于2013年5月建立核心种群(312对),同时逐步转种到生产群(屏障环境),并于2014年7月全部替换原有A种群持续供应乙脑活疫苗生产。
1.7 种群质量控制措施
1.7.1 厂房设计 SPF动物生产二车间(B207)由法国Technip工程公司按照国际标准设计和监理,建筑面积3 700 m2,专门用于SPF金黄仓鼠生产繁殖。车间为局部二层结构,二楼为D级背景,内置28台隔离器(56个隔离包),用于核心群保种,配备UPS,确保不间断供电。一楼为屏障环境,有6个饲养单元(150 m2/单元),每个单元拥有独立的空调系统,常年保持4 000只母鼠繁殖,为乙脑疫苗生产提供10~14日龄幼鼠。
1.7.2 人员管理 人员经过充分培训, 持证上岗, 定期体检, 无人畜共患病, 人员经洗澡、更衣进入洁净区,隔离器操作戴手套,与动物无直接接触。
1.7.3 环境监测 饲养人员每日观察房间实际温湿度压差情况,中控报警系统24 h监控各项环境参数,确保符合国家标准规定。每月检测沉降菌,确保清洁消毒效果。
1.7.4 验证校验 定期验证校验, 确保HVAC、隔离器、高压锅、各种仪表正常有效运行。
1.7.5 维修维保 设施设备定期计划性维护保养, 日常故障及时维修处理。
1.7.6 消毒灭菌 各种物料(笼具、用具、饮水、垫料、饲料)进入洁净区前都必须经过清洁消毒/高压灭菌/辐照处理。不同种类消毒剂轮换使用; 消毒灭菌工艺经过验证; 对饮水、垫料的高压灭菌效果定期进行无菌检查; 对饲料原材料和成品料按要求进行营养成分分析和无菌检查。
1.7.7 3C管理 任何变更(CC)要进行风险评估, 及时发现不符合性(N C),并采取纠正预防措施(CAPA)。
1.8 动物质量检测
1.8.1 采用哨兵动物法监测动物种群质量 选取4~6周龄雌性仓鼠作为哨兵动物,每个隔离包1盒,每盒2~3只,笼盒搁置在离排风口较近的地方,在每次更换笼盒时, 将其脏垫料分散到被监控的全部动物的干净笼盒中,确保所有动物与哨兵动物“100%”接触,以最大限度地代表整个群体的质量。
1.8.2 本单位QC检测 每季度抽取哨兵动物,每个隔离包1~2只,按照国家标准要求采样,检测细菌、病毒、寄生虫。
1.8.3 委托检测 定期抽取哨兵动物,每个隔离包1只,采集被毛/皮屑、血清、气管/气管分泌物、肠道内容物等样品, 每半年国内委托检测1次, 每年国外委托检测1次。国外委托检测病毒学项目19个,细菌学项目16个,寄生虫学项目6个。
2 结果
2.1 核心群(隔离环境)
常年保持312对繁殖仓鼠,定期向生产群提供种子。
2.2 生产群(屏障环境)
常年保持4 000只繁殖母鼠,平均每窝产仔数11只,年供应10~14日龄仓鼠16~20万只。
2.3 国外委托检测
病毒学、细菌和寄生虫的检测方法及结果分别见表2,表3和表4。
3 讨论
预认证是指WHO通过对申请产品的安全性、有效性和免疫效果作出评价后,能够作为国际机构采购疫苗的资质确认,通过预认证后,疫苗可以由联合国相关机构采购提供给相关国家使用。其主要审核标准是TRS颁布的技术指导意见,这是世界各国专家组成员以个人身份在广泛的医疗和公共卫生问题方面向WHO提供的最新科学技术意见,其目的是确保联合国采购供应疫苗的安全性、有效性和 “100%”的质量保证[5]。
为贯彻执行《中国生物制品规程》( 2000年版) 于生物制品生产和检定用实验动物必须使用清洁级动物的规定,上海率先进行了普通级金黄仓鼠的净化[6],本单位于2003年建立SPF金黄仓鼠种群(A), 也是通过对普通级金黄仓鼠实施剖宫产、外购SPF金黄仓鼠代乳培育而成,微生物净化级别符合SPF动物国家标准要求,国外委托检测淋巴细胞脉络丛脑膜炎病毒、仙台病毒、小鼠肺炎病毒、呼肠孤病毒Ⅲ型、汉坦病毒、小鼠细小病毒、大鼠K病毒、猴病毒5、小鼠脑脊髓炎病毒、吐兰病毒、逆转录病毒等11种病毒阴性[7], 但是多瘤病毒、支原体、分支杆菌等项目[2]也是TRS980的要求, 而且在种群建立时没有进行遗传控制, 也没有建立完整的种群资料和记录。为配合乙脑项目WHO预认证,需要重新建立SPF金黄仓鼠种群(B)。

表2 病毒学检测方法及结果Table 2 Virological items, methods and results
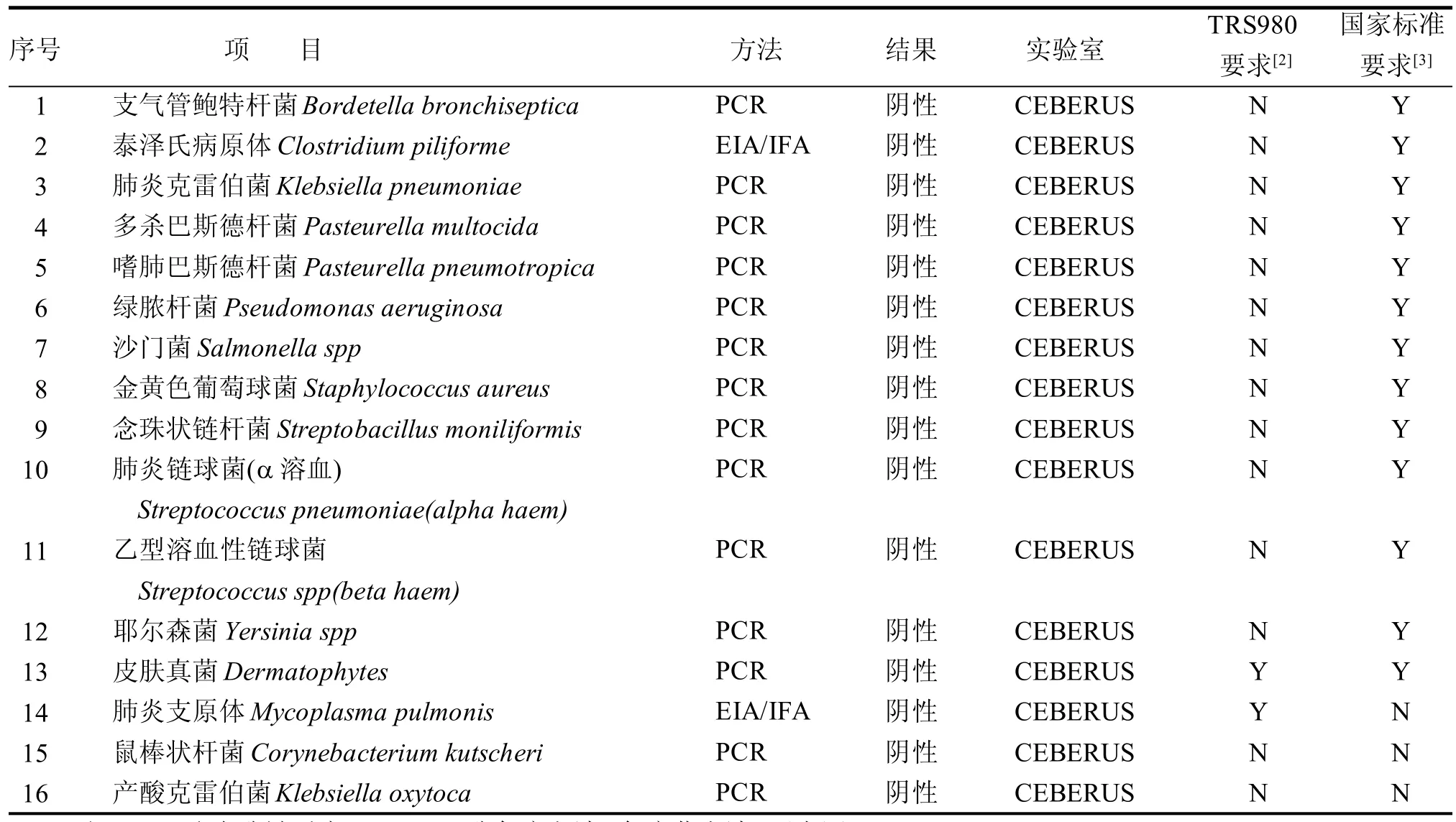
表3 细菌学检测方法及结果Table 3 Bacteriological items、methods and results

表4 寄生虫学检测方法及结果Table 4 Parasitological items、methods and results
剖宫产-代乳是常用生物净化方法之一,一方面要尽早淘汰代乳鼠自己的幼崽, 另一方面, 剖宫产取出的胎儿个体要足够大,数量不宜过多,以提高成活率。待手术的孕鼠数量要充足,如果剖宫取出的胎儿数量过多个体太小,则立即淘汰,另选其它孕鼠再实施剖宫产,以便选择较好的胎儿用于代乳。另外,将剖宫产的胎儿与代乳鼠的幼崽接触一下,可以减少代乳鼠“食仔”情况。
乙脑活疫苗生产使用的是原代仓鼠肾细胞(PHK), SPF金黄仓鼠的微生物携带状况直接影响产品,其中病毒直接影响疫苗的安全和质量, 所以病毒学项目的筛查尤为重要,新种群排除了19种病毒,远远多于国家标准要求的4种病毒。
按照国家标准要求,SPF金黄仓鼠需要排除13种细菌,同时WHO TRS980还特别要求排除支原体和分支杆菌,其中分支杆菌的检测是由本单位QC进行的, 主要采集仓鼠肾脏和肺脏直接培养,结果均为阴性。
国产疫苗国际化是中国疫苗界的梦想,疫苗生产单位如果要申请预认证,疫苗生产和检定用动物必须符合中国药典和WHO TRS980的要求,其中注射用活疫苗生产用金黄仓鼠必须至少排除以上13种病毒(表2序号1-13),尤其是逆转录病毒,此要求将载入2020年版中国药典。
本单位金黄仓鼠剖宫产净化手术一直选择原有种群, 外购动物仅仅用作代乳,一方面是为了确保遗传背景清楚, 另一方面是不用变更疫苗生产用原材料。本次剖宫产净化的金黄仓鼠B种群已先后送中国食品药品检定研究院和上海伯豪生物技术有限公司进行遗传检测,遗传质量分析工作还在进行中。

