Cu/ZnO/SBA-15催化剂的制备及碳酸酯加氢性能研究
李娜,宋磊,唐思扬
(四川大学 化学工程学院,四川 成都 610065)
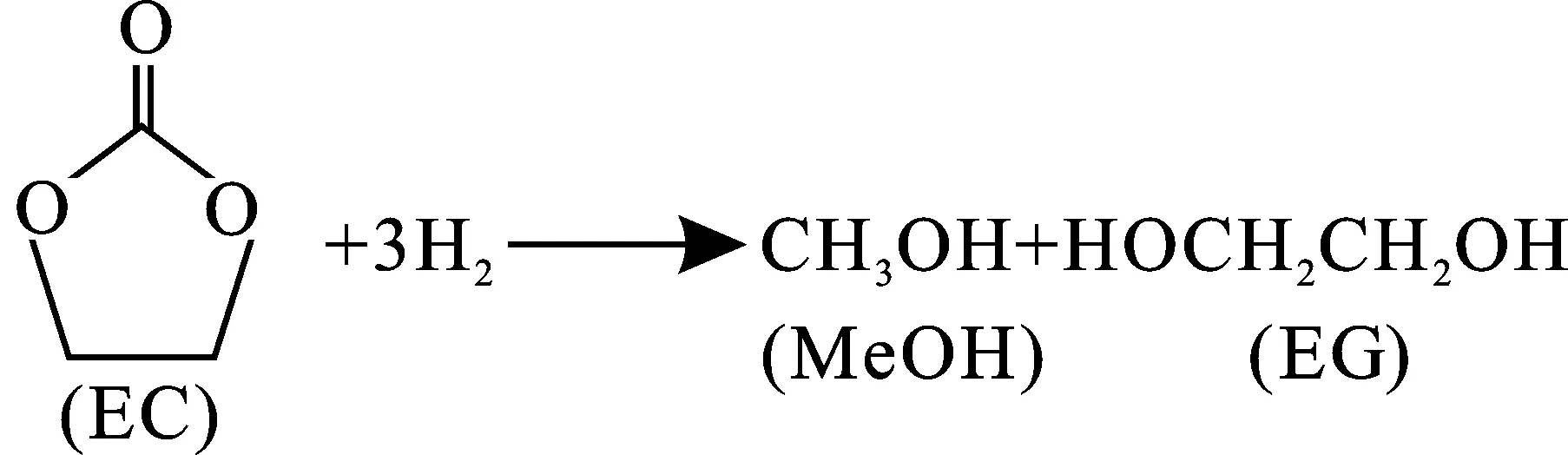
碳酸乙烯酯(EC)加氢反应是CO2与环氧乙烷合成EC,再与H2生成乙二醇(EG)和甲醇(MeOH)的关键步骤[1],该路线有望实现碳减排和制备高附加值化学品的综合目标[2-4]。目前,关于该反应的催化体系主要是均相RuII催化剂[5]以及CuCr2O4[6]、Cu-SiO2-PG[7]、Cu/HMS[8]、Cu/MCM-41[9-10]、Cu/堇青石[11]等铜基多相催化剂。其中,Cu基催化体系中Cu纳米颗粒粒径尺寸及其Cu0/Cu1活性中心对加氢转化有重要影响。Cu负载在ZnO上,ZnO的添加可使铜的活性和选择性得到提高[12-17]。
本文针对Cu/ZnO催化体系,采用大孔径、高孔容的SBA-15分子筛作为载体,考察了四种不同制备方法(体积浸渍法、过量浸渍法、旋转蒸发法和氨蒸法)对催化剂活性组分Cu分散度、Cu/ZnO比对EC加氢活性及产物选择性的影响。
1 实验部分
1.1 试剂与仪器
Cu(NO3)2·3H2O、Zn(NO3)2·6H2O、氨水(25%)、无水乙醇、SBA-15分子筛和四氢呋喃均为分析纯;碳酸乙烯酯(98%);H2(99.99%)。
ME204E/02电子天平;XL-3A马弗炉;DZF真空干燥箱;RE2000真空旋转蒸发器;GDC-1催化剂评价装置;SC-3000B气相色谱仪;SPECTRO ARCOS电感耦合等离子体发射光谱仪(ICP-OES);DX-2700丹东方圆射线衍射仪(XRD);Spectrum Two L1600300 Perkin Elmer傅里叶红外光谱分析仪(FTIR);Atuochem II 2920全自动程序升温化学吸附仪(H2-TPR)。
1.2 Cu/ZnO/SBA-15催化剂
选用SBA-15分子筛作为载体,分别采用氨蒸法、等体积浸渍法、过量浸渍法和旋转蒸发法制备纳米催化剂,铜和氧化锌的总量控制在催化剂总质量的20%。
1.2.1 氨蒸法 将Cu(NO3)2·3H2O和 Zn(NO3)2·6H2O溶解在去离子水中,搅拌下加入一定体积的25%氨水,形成锌氨和铜氨混合溶液,室温下搅拌20 min。加入4 g载体SBA-15,并用氨水将 pH 调至约12,室温下搅拌12 h。转移到 80 ℃水浴中进行蒸发除氨,待 pH 下降到7~8之间停止,沉淀物过滤,用去离子水、乙醇进行洗涤,于105 ℃下干燥8 h。得到催化剂前驱体(CZS-AE),于空气气氛中400 ℃下煅烧6 h,然后用氢气在300 ℃下还原2 h,得Cu/ZnO/SBA-15催化剂。
1.2.2 等体积浸渍法 将Cu(NO3)2·3H2O和Zn(NO3)2·6H2O溶解在16 g去离子水中,加入4 g分子筛,搅拌均匀,室温下干燥2 d,105 ℃下干燥8 h,得催化剂前驱体,于空气气氛中400 ℃下煅烧6 h。反应前用氢气在300 ℃下还原2 h,所得催化剂记为CZS-IWI。
1.2.3 过量浸渍法 将Cu(NO3)2·3H2O和Zn(NO3)2·6H2O溶解在50 mL去离子水中,加入4 g分子筛,室温下搅拌12 h,抽滤,用去离子水洗涤2次,在105 ℃下干燥8 h。所得催化剂前驱体于空气气氛中400 ℃下煅烧6 h,反应前用氢气在300 ℃下还原2 h,所得催化剂记为CZS-IM。
1.2.4 旋转蒸发法 将Cu(NO3)2·3H2O和Zn(NO3)2·6H2O溶解在50 mL去离子水中,室温下搅拌20 min。加入4 g分子筛,室温下搅拌12 h。放在旋转蒸发器中,在60 ℃下蒸发液体,随后于空气气氛中400 ℃煅烧6 h,反应前用氢气在300 ℃下还原2 h,所得催化剂记为CZS-XZ。
1.3 催化剂活性评价
将焙烧后的催化剂压片至6 MPa,用玛瑙研钵研磨,取40~60目的催化剂1.0 g装入直径8 mm的反应管中,催化剂体积约为3 mL。装填好的催化剂先用氢气预还原(300 ℃,2 h,氢气流量20 mL/min)。还原后将温度降至室温,然后以2 ℃/min的速度升温至180 ℃进行反应,氢气流量5.08 L/h,液体进料量1.08 mL/h。反应的质量空速0.1 h-1,氢酯比200,溶剂是四氢呋喃,碳酸酯在溶液中的含量为10%。待反应器的温度稳定后开始进料,出料用冷阱冷凝,每隔1 h取1次样(液体出料),用气相色谱定量分析组成,以四氢呋喃作为内标物,计算反应的转化率、甲醇和乙二醇的选择性。
1.4 催化剂表征
采用X-射线粉末衍射(XRD)、傅里叶变换红外光谱(FTIR)和程序升温还原(H2-TPR)技术对样品进行表征。
1.4.1 XRD测定 CuKα特征衍射辐射,工作电压40 kV,电流30 mA,扫描范围2θ= 10~90°。
1.4.2 FTIR分析 KBr压片,分辨率1 cm-1。
1.4.3 程序升温还原(TPR) 样品重量50 mg左右,用氮气在473 K下吹扫1 h后降至室温,再切换成5%H2/N2混合气进行程序升温还原,还原速率为5 K/min,热导检测器记录出峰信号。
1.5 分析方法
采用电感耦合等离子体发射光谱仪(ICP-OES)测定催化剂体相的Cu和Zn浓度。准确称取约0.1 g 焙烧后的干燥催化剂,转移到四氟乙烯杯中,依次加入1 mL硝酸、2 mL氢氟酸,加热直至白烟冒尽,取下冷却,加入去离子水,并定容到500 mL。
2 结果与讨论
2.1 制法对催化剂性能的影响
合适的催化剂的制备方法,要求活性组分达到高分散,优越的催化性能,提供足够的比表面和活性位。
ICP分析表明,用等体积浸渍法、旋转蒸发法和氨蒸法所得的催化剂的Cu含量相近,而过量浸渍法Cu含量仅有2.35%,Cu活性组分含量太少,催化活性低。
广角XRD分析(图1)表明,等体积浸渍法(IWI)和旋转蒸发法(XZ)制的2θ=35.6°和38.7°为氧化铜的峰,用Scherrer公式计算,得到IWI的粒径为29 nm,XZ的粒径为16 nm。而用氨蒸法得到的催化剂几乎看不到氧化铜的峰,而由于ICP表明Cu含量相似,可知氧化铜在载体上面分散度很高。为了提高铜的比表面积和活性,后续用于反应的催化剂均为氨蒸法所得。

图1 不同制备方法的Cu/ZnO/SBA-15催化剂XRD表征Fig.1 XRD characterization of Cu/ZnO/SBA-15prepared with different methods
2.2 Cu/ZnO比对催化剂性能的影响
为研究Cu/ZnO/SBA-15催化剂上不同的Cu∶ZnO的比例对催化剂的活性和选择性的影响,用蒸氨法制备Cu∶ZnO从低到高分别约为1∶5,1∶1,3∶2,2∶1,5∶2和100%六个系列的Cu/ZnO/SBA-15催化剂,分别命名为CZS-15,CZS-11,CZS-32,CZS-21,CZS-52和CZS-10。
2.2.1 FTIR分析 由图2可知,所有样品中均出现了1 080 cm-1处的强吸收峰和1 250 cm-1处的大肩峰,归因于Si—O—Si键的不对称伸缩振动引起。所有催化剂焙烧后在670 cm-1处均出现了归属于硅酸铜结构中的δOH特征峰,表明煅烧产物中仍有硅酸铜结构存在。根据相关文献报道[18],硅酸铜在500 ℃下进行煅烧仅能部分分解成CuO成分。本研究中采用的催化剂前驱体煅烧温度为400 ℃,因此,在催化剂煅烧产物中除含有硅酸铜成分外,还含有CuO成分。所有催化剂都在2 868,2 924 cm-1出现了氧化铜的吸收峰,可知催化剂煅烧后,铜物种以硅酸铜和CuO形式共同存在,还原后,硅酸铜成分会被全部还原成其他低价铜物种。

图2 不同Cu/ZnO比例的Cu/ZnO/SBA-15催化剂FTIR谱图 Fig.2 FTIR characterization of Cu/ZnO/SBA-15with different Cu/ZnO ratio
2.2.2 XRD分析 由图3可知,在2θ=22°附近较宽的衍射峰归属于无定型的二氧化硅,其余峰的强度均较弱,说明反应后的铜在载体上高分散,没有发生烧结。四种催化剂均在2θ=36.5°出现了可归属于Cu2O的(111)晶面的特征衍射峰,另外,在2θ=43.5°也出现了较弱的金属铜的特征峰,说明催化剂中同时存在Cu+和Cu0,二者共同起到催化作用。而且随着锌含量的增加,Cu2O和金属铜的峰强度逐渐减小,其粒径根据Scherrer公式计算也随锌含量的增加而尺寸变小,说明氧化锌的含量可以调变Cu2O和金属铜的分布,提升铜纳米颗粒的分散度。
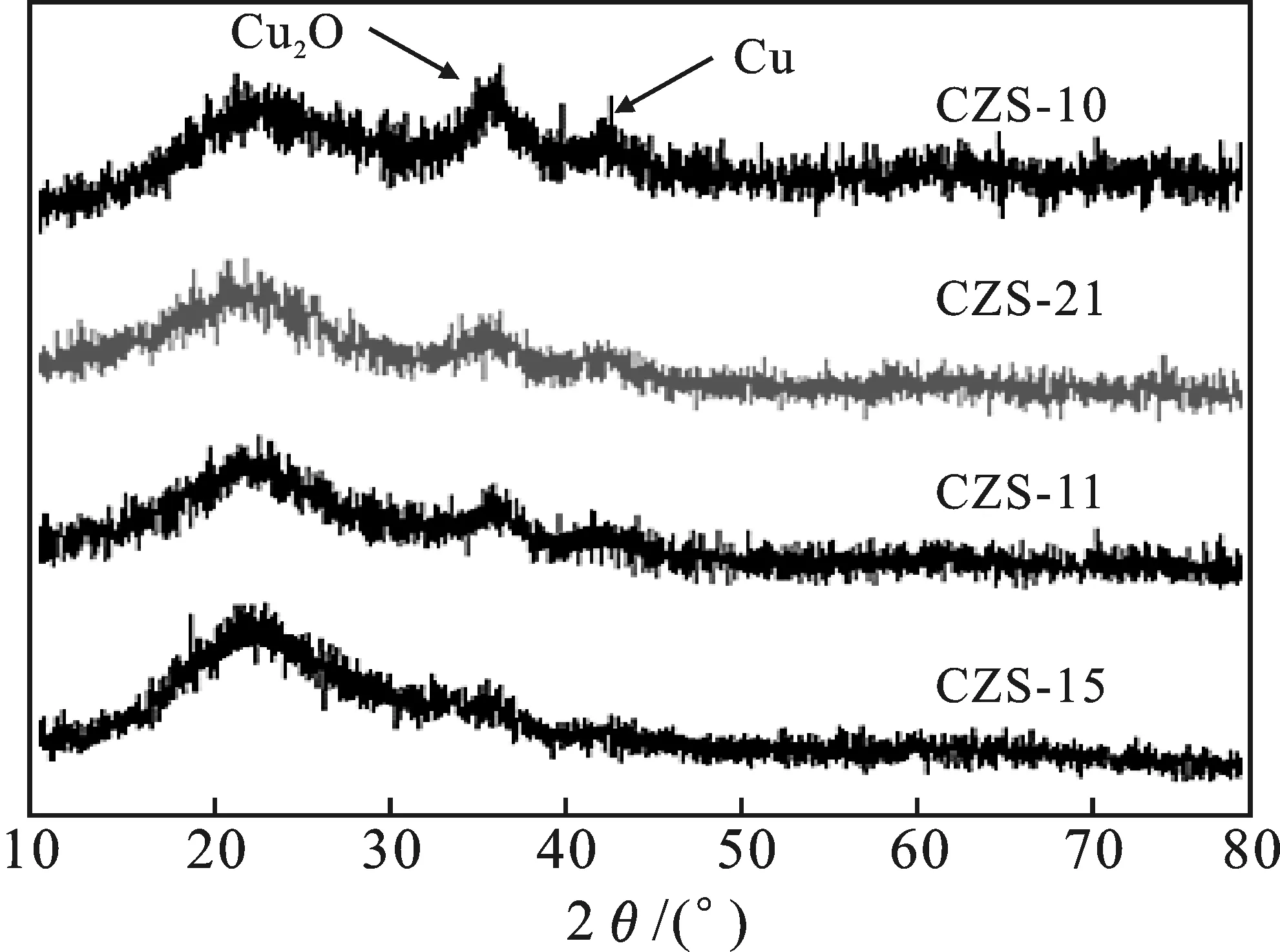
图3 不同Cu/ZnO比的Cu/ZnO/SBA-15催化剂XRD表征Fig.3 XRD characterization of Cu/ZnO/SBA-15with different Cu/ZnO ratio
2.2.3 H2-TPR表征 纯的氧化铜通常在390 ℃以内就能完成还原过程,前期研究表明,高分散的氧化铜温度一般为250 ℃,离子交换Cu—O—Si 还原成Cu+的温度也在250 ℃左右,若将Cu+进一步还原为Cu0则需要较高的温度(通常大于600 ℃)。本研究焙烧所得的CuO/ZnO/SBA-15催化剂中,所有的氧化铜均为高分散,当全部为氧化铜时,还原峰的温度约为250 ℃,但是当催化剂中的锌的含量增加时,还原峰的温度也随之增加(图4),说明了锌和铜之间存在较强的相互作用,阻碍了氧化铜的还原。已有报道中的锌助剂对铜催化剂的作用主要有两方面的观点,第一种是氧化锌可以促进铜的氢溢流,进而会降低氧化铜的还原温度[19],这种观点与本文得到的结果相悖。另一种观点为助剂锌的加入有利于催化剂生成铜锌复合氧化物[20],其还原生成铜锌合金的还原温度相对较低,所以锌含量的增加会提高还原峰的温度。CZS-15催化剂在350 ℃还原后会产生一部分淡黄色的粉末,可能是铜锌合金的颜色,也可证实这一推测。因此,推测在本实验中氧化锌会与铜氧化物生成复合氧化物,氧化锌也会被还原生成铜锌合金。
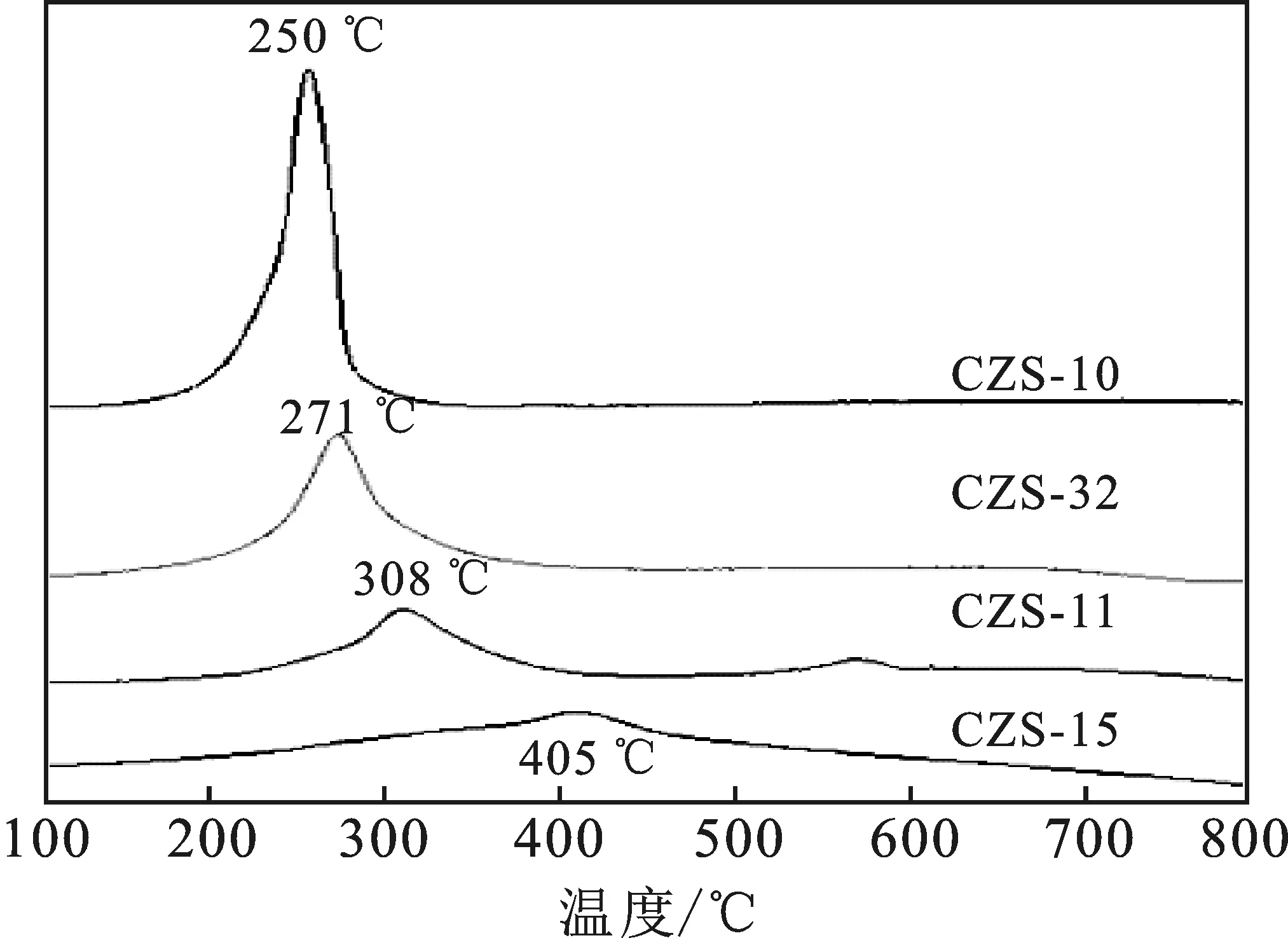
图4 不同Cu/ZnO比的Cu/ZnO/SBA-15催化剂的H2-TPR图Fig.4 H2-TPR characterization of Cu/ZnO/SBA-15with different Cu/ZnO ratio
2.3 Cu含量对催化剂性能的影响
对氨蒸法制备的催化体系的活性评价见表1。

表1 不同Cu/ZnO比的Cu/ZnO/SBA-15催化剂的催化活性Table 1 Catalytic behavior of ethylene carbonatehydrogenation over Cu/ZnO/SBA-15 withdifferent Cu/ZnO ratio
由表1可知,在铜和锌总的负载量不变的情况下,碳酸乙烯酯的反应转化率及甲醇和乙二醇的选择性先随着Cu/(Cu+ZnO)的增加而增加,随后降低。在Cu/(Cu+ZnO)=0.7时,活性和选择性最好,此时碳酸乙烯酯的转化率为100%,甲醇的选择性为69.7%,乙二醇的选择性为100%。在铜含量100%时,碳酸酯的转化率96.9%,甲醇的选择性66.2%,乙二醇的选择性90.4%。该结果说明:首先,催化剂的主要活性组分是铜,因为反应的活性在很大范围内随着铜含量的增加而增加;其次,氧化锌在一定范围内,对催化剂的活性和选择性有影响,因为在Cu/(Cu+ZnO)=0.7条件下,活性和选择性比铜含量为100%的高。
单质Cu和Cu+在碳酸酯加氢过程中起重要的作用[21-22],一般认为在酯加氢中,Cu0充当着反应的活性位点,而更多的是认为是Cu0和Cu+的共同作用促进了酯加氢反应的进行。ZnO中会存在Cu+,Cu+与Cu的协同作用会提高铜的活性[9-10,23],ZnO和Cu的界面存在特殊的活性位[22]或ZnO可以存储铜溢出的氢,反氢溢流提高铜的活性[23]。
3 结论
采用氨蒸法、等体积浸渍法、过量浸渍法和旋转蒸发法制作了CO2间接转化路线中碳酸酯加氢Cu/ZnO/SBA-15催化体系,研究发现,过量浸渍法制备的催化体系中铜负载量较低,等体积浸渍和旋转蒸发法得到的催化剂分散性不好,而氨蒸法可有效控制催化剂的颗粒在10 nm,也可保证催化剂的负载量依据铜氨溶液的浓度进行调节。
氨蒸法制备的铜和氧化锌的总量为20%,Cu/ZnO比为2∶1时,催化剂的活性和选择性最好,碳酸乙烯酯转化率为100%,甲醇选择性为69.7%,乙二醇选择性为100%,在一定范围内,氧化锌对铜的活性和选择性有提高。

