四氧化三锰工艺废水沉锰渣综合利用研究
银 瑰,刘维荣,木宗云,黄文杰
(湖南特种金属材料有限责任公司,湖南 长沙 410013)
现有四氧化三锰的主要生产工艺是金属锰粉悬浮液氧化法[1],该工艺由于使用了少量的铵盐作催化剂,水相(常称为母液)中的Mn2+很难彻底转化成四氧化三锰,始终约有500 mg/L的Mn2+残留。又由于原料电解金属锰片中带有杂质Mg、Ca,当母液循环利用多次以后,其中的Mg、Ca杂质被富集,影响到产品质量,这时需要让母液开路。开路出来母液必须进行除锰处理,从而产生沉锰渣,沉锰渣呈浆糊状,平均含水74.53%,其中的锰以多种价态的氧化锰和氢氧化锰形式存在,且成分构成不稳定。经干燥后的成分见表1。

表1 120℃烘干处理后渣中成分 %
沉锰渣水分含量大,且含有Mg、Ca、Si等杂质成分,不能直接使用,一方面浪费了其中的锰资源,另一方面也给环保处理造成负担。所以,对沉锰渣开展综合利用研究是很有必要的。
1 酸浸分离处理
沉锰渣中锰以多种形态存在,且含Mg、Ca等杂质,先开展酸浸试验研究。每次称取沉锰湿渣100 g(同步,取样送分析),按2∶1液固比将其浆化,常温下用1∶1 H2SO4调节pH值,选择主要杂质Mg为对比考察对象,不同pH值下,Mn、Mg进入液相的比例见表2。
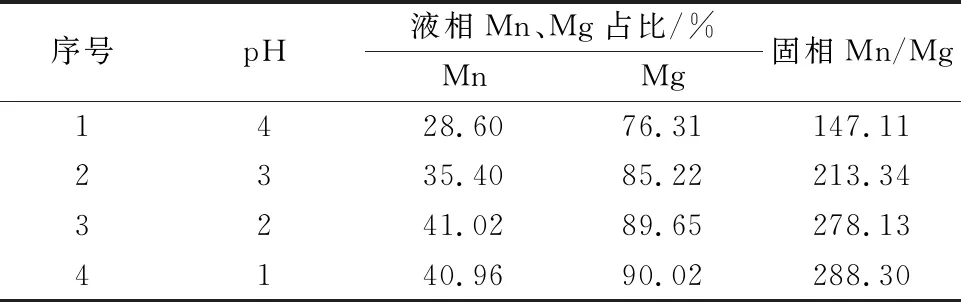
表2 进入液相的Mn、Mg比例及固相Mn/Mg值
由表2可看出:当pH值小于2时,约有41%的Mn进入液相,可溶锰也基本在41%左右,此时进入液相的Mg约90%,留在固相中的Mn和Mg的比例大幅提高。由此可以推断,先将可溶的Mn和Mg等杂质酸浸溶出,再将溶出的Mn2+转变成不溶的MnO2,而此时被溶出的Mg等杂质仍留在液相,这样便可实现Mn与杂质的分离。
2 酸浸—氧化试验[2-3]
2.1 烘焙干渣的酸浸—氯酸钠氧化
沉锰渣经120℃烘焙干燥,研磨破碎备用。每次取干渣50 g,加蒸馏水150 mL调浆,用1∶1 H2SO4调pH值至3~4,加氯酸钠(工业级)10.9 g,95℃下搅拌反应3 h,过程中适时补加蒸馏水,终点后过滤、洗渣、分析滤液,分析结果见表3。
表3结果表明:烘焙干渣经酸浸—氧化处理,有98%以上的锰留在固相中,但留在固相中的镁也有约33%。锰与镁实现了一定程度的分离,但仍不理想,且沉锰湿渣增加了烘干步骤,增加了处理的复杂程度。

表3 滤液中Mn、Mg分析及固相Mn/Mg
2.2 沉锰湿渣直接浆化—酸浸—氯酸钠氧化
每次取新压滤湿渣,称取100 g,按液相固比3∶1调浆,同时送样分析Mn、Mg含量,用1∶1 H2SO4酸化,加氯酸钠,95℃搅拌反应3 h,而后过滤分析滤液中Mn、Mg,结果见表4。
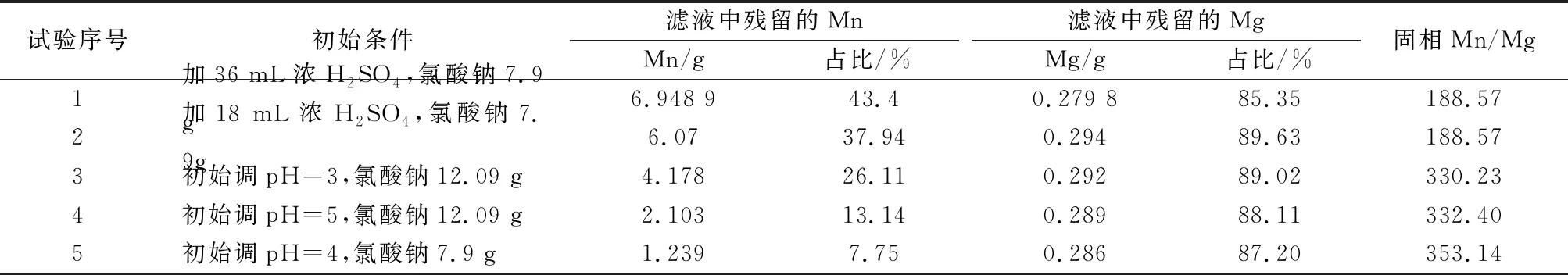
表4 滤液中Mn、Mg分析及固相Mn/Mg
表4结果表明:高酸性情况下Mn2+转化成MnO2比较困难,酸化pH值在4左右时,留在液相中的Mn降至7.75%,此时进入液相中的Mg达到87%,Mn与Mg实现了较大程度的分离,不过仍未达到满意的程度。
2.3 沉锰湿渣直接浆化—酸浸—W试剂氧化
每次取新压滤湿渣,称取100 g,按液相固比4∶1调浆,同时送样分析Mn、Mg含量,用1∶1 H2SO4酸化至pH=4,常温下加入W试剂,搅拌反应至控制点,过滤分析,结果见表5。

表5 W试剂处理结果
表5结果表明:当W试剂用量为过量理论值的1.5倍时,99.9%的Mn留在固相,而有近90%的Mg进入液相,分离效果比较理性。
表5中2号试验滤渣经洗涤烘干,检测成分见表6,X衍射分析结果见图1。

表6 表5中2号试验滤渣分析 %

图1 W试剂处理后滤渣X-射线衍射分析
图1中W试剂处理的滤渣X-射线衍射结果表明,固相中主要组分是r-MnO2。
2.4 W试剂处理所得MnO2返回制Mn3O4试验
按照表5中2号试验的条件,取2份各100 g沉锰渣制备MnO2(按沉锰渣的平均锰含量估测,可制得约25 g MnO2),反应到位后,过滤备用。从生产车间四氧化三锰反应槽中取2份各2 L已反应8 h的浆料(选取此种浆料的目的是考虑其中有未反应的Mn和Mn(OH)2,便于让MnO2转化成Mn3O4,按生产投料的液固比计称,2 L浆料含Mn转化成Mn3O4约500 g),分别盛于2 500 mL烧杯。分别加入1份前述制备的MnO2滤饼,于60℃温度条件下,搅拌、鼓空气反应5 h,适时补加蒸馏水,维持体积稳定,达到预定反应时间后、过滤、洗涤、烘干,取样分析,结果见表7。

表7 W试剂处理所得MnO2返回制Mn3O4分析结果
表7结果表明:按1/20的比例把W试剂处理沉锰制得的MnO2返回制Mn3O4,不会给产品带来影响。但MgO、SiO2已接近标准上限,宜适当降低加入比例。
3 结 论
1)采用湿渣直接浆化—酸浸—W试剂氧化处理,可将四氧化三锰废水沉锰渣中的锰制成MnO2,并且实现锰与主要杂质的有效分离。
2)将制得的MnO2以小于1/20的比例返回制备Mn3O4主流程,不会对Mn3O4质量带来影响。

