术后吉兰-巴雷综合征的临床及电生理特征分析
张锐毅 贾延劼
郑州大学第一附属医院神经内科,河南 郑州 450052
吉兰-巴雷综合征(Guillain-Barre syndrome,GBS)是一种累及周围神经的炎性脱髓鞘疾病,目前认为其病因是由于病原体的某些组分与周围神经髓鞘的某些组分相似,机体产生自身免疫性T淋巴细胞与自身抗体而导致针对自身组分的免疫应答。尽管大部分病例与病原体感染或感染后免疫有关,但仍有报道显示,非感染因素如创伤、手术也可引起GBS[1]。GENSICKE等[2]报道显示,术后发生GBS的风险是普通人的13倍,达到4.1/10万。目前关于术后GBS的国内相关文献还仅限于病例报道,缺乏系统研究。2013-11—2016-11郑州大学第一附属医院570 206台手术中,10例发生术后GBS,本研究对这些病例进行回顾性分析。
1 资料与方法
1.1研究对象选择2013-11—2016-11郑州大学第一附属医院10例由于手术引起的GBS患者。所有患者符合GBS诊断标准[3],并排除手术外其他可能引起GBS的危险因素。排除标准:前驱感染史,使用神经肌肉阻滞剂,注射神经节苷脂,接种疫苗,血肿瘤标志物、副肿瘤标志物异常等。回顾性分析患者的一般资料、临床表现、神经电生理检查、血清学抗神经节苷脂抗体、脑脊液检查结果及治疗情况。
1.2神经电生理检测神经电生理操作按照中华医学会神经病学分会制定的肌电图规范[4]进行,肌电图为Nicolet EDX型。主要检测包括神经传导速度(NCS)和H反射,患者均在发病10~14 d内进行检测。肢体温度控制在32 ℃以上,用表面电极及针极肌电图检测四肢近端、远端8条运动、感觉神经的传导(正中神经、尺神经、胫神经、腓深神经/腓肠神经)。测量运动神经远端潜伏期(DL)、运动神经动作电位波幅(CMAP)、运动神经传导速度(MCV),以及感觉神经动作电位波幅(SNAP)、感觉神经传导速度(SCV)。数值落在均值±2.5个标准差外视为异常。根据HADDEN等[5]提出的标准诊断轴索或髓鞘损伤。
1.3血清抗神经节苷脂抗体抽取血清,以酶联免疫法(ELISA)检测血清抗神经节苷脂抗体,ELISA检测的抗原为GM1、GD1b和GQ1b,各200 ng。本研究选择IgG抗体阳性为病理学意义。
2 结果
2.1一般资料入组患者年龄33~78岁,平均54.2岁,均为择期手术患者无外伤史,在GBS临床症状出现前已苏醒、生命体征平稳并无神经功能缺损。患者编号按照时间顺序,#1和#4患者全麻下行人工股骨头置换手术;#2患者全麻下行双侧股内侧抽脂术;#3患者全麻下行腹腔镜胆囊切除术;#5患者局麻下行人工流产术;#6患者全麻下行颈前路椎体次全切除+内固定术;#7患者全麻下行腰椎间盘突出髓核摘除术+内固定术;#8患者局麻下行肠息肉内镜切除术;#9患者腰麻下行剖宫产术;#10患者全麻下行脾脏切除术。
患者主要临床症状为进行性对称性肢体无力伴不同程度的肌肉萎缩,腱反射减弱或消失,下肢为著。具有以下特点:(1)急性或亚急性发病,术后第3~30天发病,平均9.8 d;(2)进展迅速,程度重;(3)脑神经受累多;(4)呼吸肌麻痹的发生率高;(5)并发症多(表1~2)。

表1 10例手术后GBS患者资料
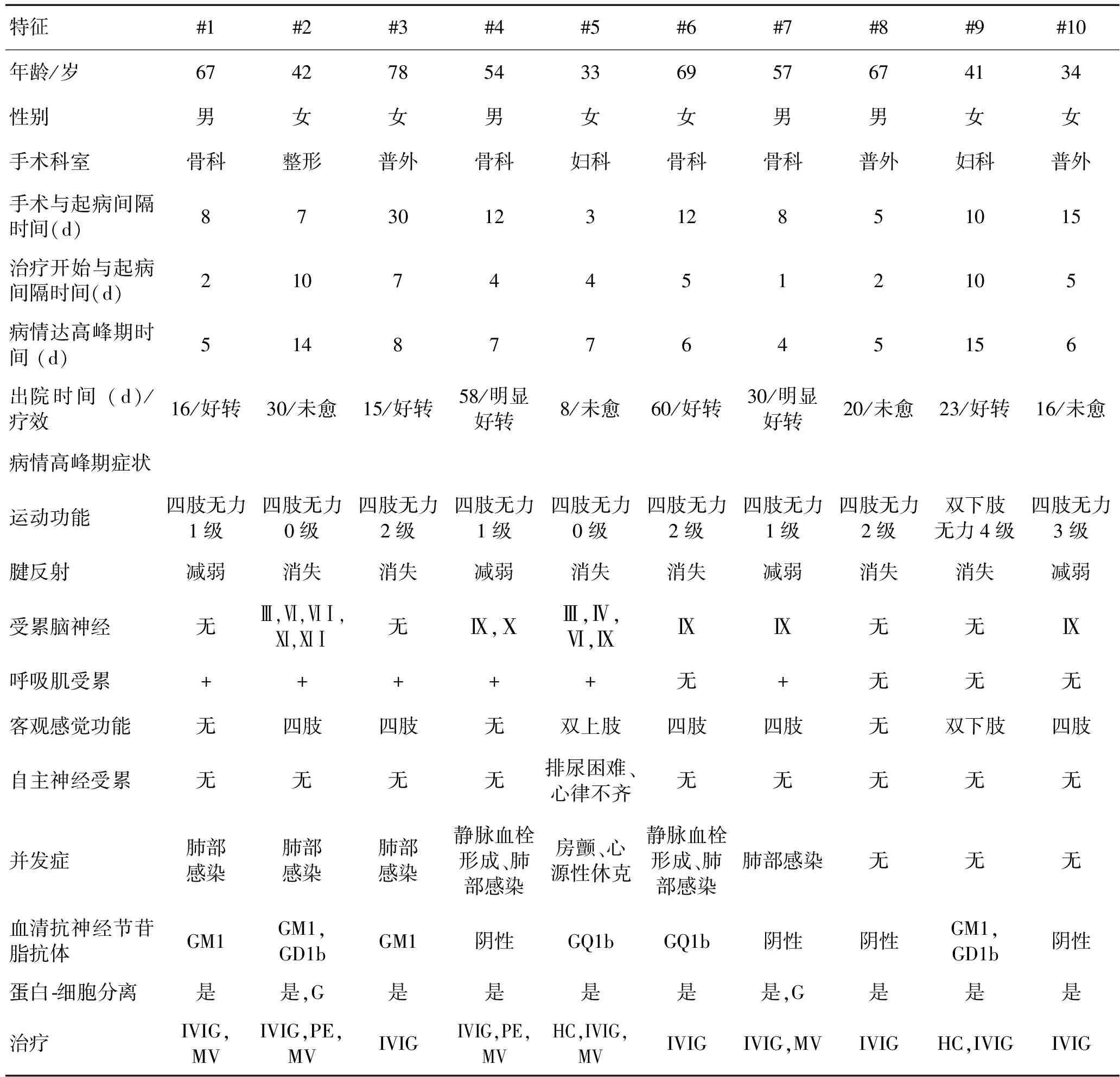
表2 10例手术后GBS患者的详细资料
注:IVIG:静脉注射免疫球蛋白;MV:机械通气;HC:激素冲击;PE:血浆置换;G:脑脊液寡克隆区电泳阳性
2.2神经电生理特点如表3所示,8例患者住院期间进行了肌电图检查,从起病到NCS异常的平均时间为8.75 d。在感觉神经中,SNAP幅度在上肢和下肢都相对保留,7例(#1、#3、#4、#6、#7、#8、#10)保持正常。相反,所有受试者的H反射均未引出。另外,针极肌电图均呈神经源性损害。
2.3抗神经节苷脂抗体6例血清抗神经节苷脂抗体阳性。其中,#1、#2患者的靶抗原为GM1,#2、#9患者的靶抗原为GD1b和GM1,#5、#6患者靶抗原为GQ1b。
2.4脑脊液实验室检查所有患者于发病14 d后行腰椎穿刺术,均出现蛋白-细胞分离现象,其中2例出现脑脊液寡克隆电泳阳性。
2.5治疗及预后经确认的GBS患者,立即给予0.4 g/kg的人免疫球蛋白静脉注射5 d,其中#1、#2进行了两轮注射治疗,其中#1患者16 d后好转出院,另外,#2、#4患者同时给予血浆置换(#4患者58 d后好转出院),#5、#9患者同时给予大剂量激素冲击治疗(#9患者23 d后好转出院)。 虽然所有患者静脉注射免疫球蛋白治疗后有不同程度的临床改善,但仍有4例症状改善不明显,预后较差。
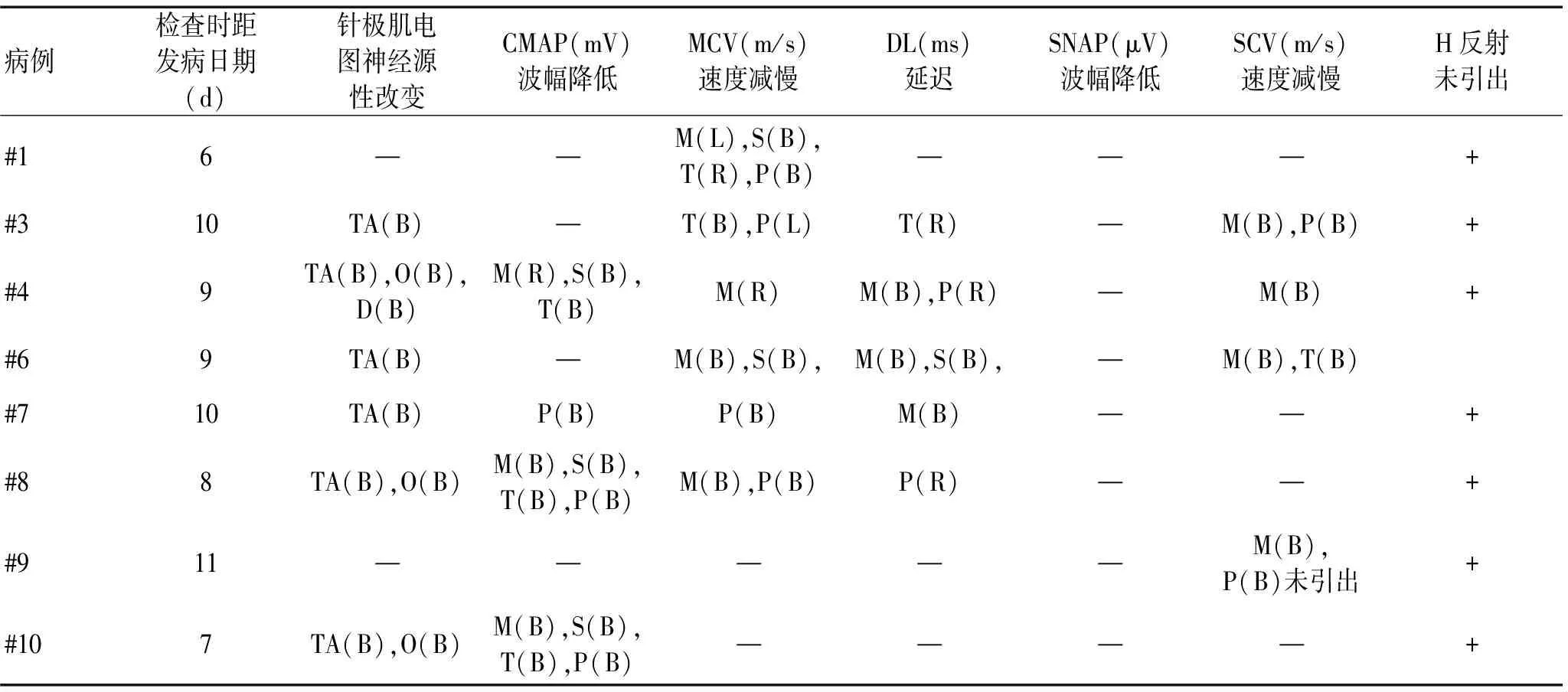
表3 8例GBS患者的神经电生理特征
3 讨论
GBS病因尚未充分阐明,以往认为多与感染后免疫反应有关,同时也发现创伤可以引发炎症性神经病变,包括GBS[6-11]。WIEDERHOLT等[12]在1965年首次报道了手术后GBS的病例。过去几十年中,多种类型的手术,如脑外伤术、冠脉搭桥术、脊髓手术、腰椎手术、抽脂手术、牙体种植、肝移植术后GBS患者陆续被报道[13-24]。国内也报道了急性硬膜下血肿术、肾移植、动脉栓塞术、甲状腺切除加双侧颈部淋巴结清扫术等引起GBS的个案[25-35]。手术相关的GBS发病率极低,缺乏详细的流行病学数据[36]。按照本研究选取的单中心570 206台手术量计算,发生率为1.8/10万,低于国外报道[2,37]。另外,其发生与手术、麻醉方式无关,手术分级和科室无规律可循,甚至腹腔镜手术、人工流产术等相对创伤小的手术也可发生,因此各手术科室均需要加以防范。也有研究指出,术后GBS与骨骼及消化器官手术的相关性可能更高[38]。
根据神经电生理诊断标准[3-5],本研究GBS患者主要影响运动纤维,而且神经轴索损伤较脱髓鞘损伤更常见,与STAFF等[7]报道一致,也是术后GBS预后不良的原因之一。本研究发现,手术类型、大小与神经损伤程度相关性不高,推测造成神经损伤的原因可能非手术直接导致。目前术后GBS的机制仍不明确,可能是创伤导致的暂时免疫抑制和临床或亚临床外源性感染的增加联合所致[39-41]。免疫抑制可诱导免疫耐受性的改变,外源感染可引起交叉反应性抗体[41],两者共同促进对周围神经的自身免疫性攻击,导致GBS。
本研究中6例(60%)检测到IgG抗神经节苷脂抗体。GQ1b抗体阳性者均有感觉神经受累。以往报道约50%的GBS患者神经节苷脂的血清抗体阳性,包括GM1、GM1b、GM2、GD1a、GalNAc-GD1a、GD1b、GD2、GD3、GT1a和GQ1b[3,42]。
术后GBS吉兰-巴雷综合征往往被原来疾病症状或术后不适症状掩盖,及早识别尤为重要。因此,当术后有无法解释的进行性肌无力时,应考虑GBS,及时给予心电监护,尽早识别呼吸衰竭,必要时及时转入重症监护病房。对于术后GBS患者的治疗及预后目前仍无系统研究。尽管静脉注射免疫球蛋白能改善大部分患者预后,但大剂量激素冲击或血浆置换联合治疗是否优于单独使用免疫球蛋白还有待探索。对于创伤后GBS的临床特点和发病机制仍需后续大样本临床研究和基础实验阐明。

