金梅清暑颗粒的定性定量方法研究
徐向平,胡展晴,叶惠煊,刘淑妦,张振贤,黄 胜*
(1.九芝堂股份有限公司,长沙 410021;2.中南大学湘雅药学院,长沙 410013)
金梅清暑颗粒现收载于《卫生部药品标准》中药成方制剂第十四册,是九芝堂股份有限公司的独家生产品种,标准编号为WS3-B-2725-97-2014Z。其处方由金银花、乌梅、淡竹叶和甘草4味中药组成,具有清暑解毒和生津止渴的功效,临床上常用于治疗夏季暑热、口渴多汗、头昏心烦和小便短赤,并防治沙痱和暑症[1-2]。
1 仪器与试药
1.1仪器 Waters 2695-2998高效液相色谱仪(美国沃特世公司);DZKW型电热恒温水浴锅(北京市永光明医疗仪器有限公司);KQ-300DV型数控超声波清洗器(昆山市超声仪器有限公司);AY220型电子分析天平(日本岛津公司);CP225D型电子分析天平(德国赛多利斯公司);Merck硅胶G薄层层析板(德国默克公司)。
1.2试药 山银花对照药材(批号121595-201202),灰毡毛忍冬皂苷乙(批号111814-201303)和绿原酸(批号110753-201415),均为中国食品药品检定研究院生产;金梅清暑颗粒(九芝堂股份有限公司生产,规格:15 g·袋-1);乙腈为色谱纯;水为超纯水;其他试剂均为分析纯。本实验样品所涉及的药材均由九芝堂股份有限公司质量中心按照《中国药典》2015年版一部相应品种项下的质量标准检验合格后使用。
2 方法与结果
2.1山银花TLC鉴别
2.1.1色谱条件 采用硅胶G薄层板,以三氯甲烷-甲醇-水(6∶4∶1)10 ℃下放置的混合溶液为展开剂,展开,取出,晾干,喷以质量分数为10%的硫酸乙醇溶液,在105 ℃下加热至斑点显色清晰。
2.1.2对照品溶液的制备 取灰毡毛忍冬皂苷乙对照品适量,加体积分数为50%的甲醇使溶解,摇匀,制成质量浓度为0.6 mg·mL-1的对照品溶液。
2.1.3对照药材溶液的制备 精密称取山银花对照药材1 g,加入40 mL乙醚使溶解,超声处理15 min,滤过,滤渣挥干残留的乙醚后,加甲醇30 mL继续超声处理20 min,滤过,水浴蒸干滤液,残渣加纯化水40 mL使溶解,再用水饱和的正丁醇振摇提取3次,每次20 mL,合并正丁醇液,加纯化水洗涤2次,每次20 mL,正丁醇液回收溶剂至近干,残渣加甲醇5 mL使溶解,作为对照药材溶液[3]。
2.1.4供试品溶液的制备 称取金梅清暑颗粒10 g,研细,按照2.1.3项下方法制成供试品溶液。
2.1.5阴性对照溶液的制备 取处方中除去山银花的全部药味,按照处方比例制成缺山银花的阴性对照样品。称取阴性对照样品10 g,研细,按照2.1.3项下方法制成阴性对照溶液。
2.1.6实验结果 取连续生产的3批样品(批号:20160301,20160302和20160303),按照2.1.4项下方法分别制成相应的供试品溶液。按照TLC法(《中国药典》2015年版四部通则0502)实验,吸取对照品溶液和对照药材溶液各5 μL、供试品溶液和阴性对照溶液各10 μL,按照2.1.1项下色谱条件进行TLC法实验,结果显示,在供试品色谱中,与对照药材和对照品色谱相应位置上,显相同颜色的斑点,而阴性对照色谱中则未见明显干扰,表明该方法专属性良好,见图1。

图1TLC鉴别
1.灰毡毛忍冬皂苷乙对照品;2.山银花对照药材;3.阴性对照;4~6.金梅清暑颗粒样品。
Fig.1 TLC chromatogram
1.macranthoidin B reference substance;2.LoniceraeFlos reference material;3.negative sample;4-6.Jinmeiqingshu Granules sample.
2.2绿原酸HPLC含量测定
2.2.1色谱条件 采用Inertsil ODS-3(250 mm×4.6 mm,5 μm)色谱柱;以乙腈-4 mL·L-1磷酸溶液为流动相,等度洗脱,洗脱体积比为8∶92;柱温为35 ℃;流速为1.0 mL·min-1;检测波长为327 nm;进样量为5 μL。
2.2.2对照品溶液的制备 精密称取绿原酸对照品适量,置于棕色量瓶中,加甲醇溶解,制成质量浓度为0.283 0 mg·mL-1的对照品储备液。精密量取上述对照品储备液5~50 mL,置于棕色量瓶中,加甲醇稀释定容并摇匀,制成质量浓度为0.028 30 mg·mL-1的对照品溶液,备用。
2.2.3供试品溶液的制备 取样品粉末0.25 g,精密称定,置于具塞锥形瓶中,精密加入体积分数为30%的甲醇25 mL,称定质量,超声处理(功率300 W,频率25 kHz)30 min后冷却至室温,再加甲醇补足减失的质量,摇匀,滤过,取续滤液,备用。
2.2.4阴性对照溶液的制备 取处方中的全部药味,按照处方比例制成缺山银花和乌梅2味药材的阴性对照样品,按照2.2.3项下制备方法制得阴性对照溶液。
2.2.5线性关系考察 分别精密吸取对照品溶液2,5,5,1和1 mL,分别置于5,50,100,25和50 mL的棕色量瓶中,加甲醇稀释定容并摇匀,分别进样5 μL,测定,以进样质量浓度为横坐标(x)、绿原酸的峰面积为纵坐标(y),进行线性回归,并绘制标准曲线。其回归方程为:y=107x-930.94,r=1.000。结果表明,绿原酸含量在28.3~566.0 μg范围内线性关系良好。按照信噪比(S/N)的3和10倍考察检测限(n=2)和定量限(n=6),结果检测限和定量限分别为4.245和11.320 ng。
2.2.6专属性实验 取对照品溶液、供试品溶液和阴性对照溶液,按照2.2.1项下色谱条件进样,HPLC图见图2。结果显示,阴性对照溶液的HPLC图中,在绿原酸色谱峰保留时间附近无其他色谱峰干扰,表明该方法专属性良好。
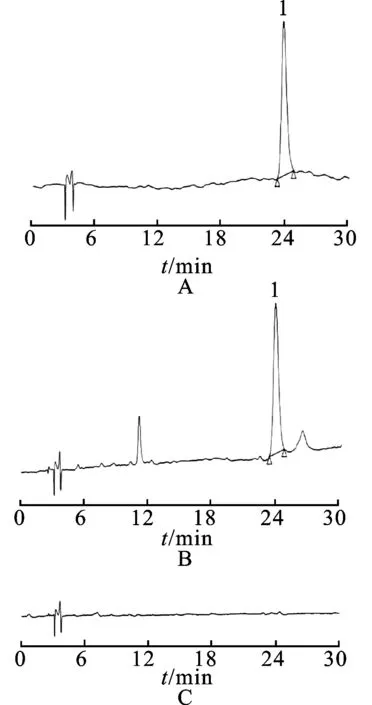
图2HPLC图
A.对照品;B.金梅清暑颗粒样品;C.阴性样品;1.绿原酸。
Fig.2 HPLC chromatograms
A.reference substance;B.Jinmeiqingshu Granules sample;C.negative sample;1.chlorogenic acid.
2.2.7精密度实验 精密吸取2.2.3项下制备的供试品溶液5 μL,连续进样6次,计算得供试品中绿原酸峰面积的RSD值为1.51%(n=6),结果表明,该仪器精密度良好。
2.2.8稳定性实验 取同一室温下放置的供试品溶液,精密吸取5 μL,分别在0,2,4,6,8,12和24 h后进样,计算其RSD值。结果,绿原酸峰面积的RSD值为1.91%,表明供试品溶液在24 h内稳定。
2.2.9重复性实验 取同一批样品(批号20160302),按照2.2.3项下方法平行制备6份供试品溶液,测定,结果绿原酸峰面积的RSD值为1.80%(n=6),表明该方法重复性良好。
2.2.10加样回收实验 取样品(批号20160302,绿原酸含量为 1.58 mg·g-1)0.125 g,共6份,精密称定,分别加入对照品溶液(含绿原酸0.198 1 mg),按照2.2.3项下方法制备供试品溶液,进样测定并计算,结果绿原酸的平均回收率为104.56%,RSD值为2.53%。见表1。
表1绿原酸加样回收实验结果
Tab.1 Results of recovery test of chlorogenic acid (n=6)

样品取样量/g样品中绿原酸含量/mg添加绿原酸量/mg实测绿原酸量/mg回收率/%平均回收率/%RSD/%10.123 70.195 40.198 10.404 0105.30104.562.5320.122 80.194 00.198 10.401 4104.6930.122 10.192 90.198 10.400 0104.5440.116 20.183 60.198 10.399 6109.0450.127 00.200 70.198 10.402 2101.7260.124 80.197 20.198 10.399 4102.07
2.2.11耐用性实验 选择2种不同品牌的色谱柱,对已建立的方法耐用程度进行考察。结果显示,不同条件下,绿原酸色谱峰的对称因子、分离度和理论塔板数均达到准确定量要求,表明该方法耐用性良好。见表2。
表2耐用性实验结果
Tab.2 Results of robustness test (n=2)

色谱柱不同批号的绿原酸含量/mg·g-1201603012016030220160303Inertsil ODS-3(250 mm×4.6 mm,5 μm)3.621.613.21Kromasil 100-C18(250 mm×4.6 mm,5 μm)3.661.672.98RSD/%0.551.833.72
2.2.12含量测定 按照2.2.3项下方法平行制备供试品溶液2份,按照2.2.1项下色谱条件分别进样测定,采用外标一点法计算金梅清暑颗粒中绿原酸的含量,结果10批金梅清暑颗粒样品中绿原酸的含量分别为3.66,1.67,2.98,1.78,1.86,2.54,2.52,3.63,3.82和4.00 mg·g-1,平均值为2.85 mg·g-1。考虑到绿原酸化学性质不稳定,受热易分解[4-6],且该制剂的整个工艺过程较为复杂,会导致绿原酸进一步分解,故按照成品含量平均值的70%折算为1.995 mg·g-1。因此,暂拟定本品山银花和乌梅以绿原酸(C16H18O9)计含量不得少于2.0 mg·g-1。
3 讨论
3.1TLC专属性考察 近年来,市场上金银花和山银花药材混用的现象较为严重[7-8],使用金银花或山银花药材作为原料的中药制剂更是难以辨别[9-10]。如不能将二者准确区分开,易对患者的用药安全埋下隐患。笔者通过前期文献调研发现,二者虽然为同属植物,但化学成分有较大区别[11-16]。其中,灰毡毛忍冬皂苷乙是山银花的特征性成分[17-20],而金银花中不含有此成分,故可将灰毡毛忍冬皂苷乙是否检出作为区分本制剂中为金银花还是山银花投料生产的有效鉴别手段。本实验建立的TLC鉴别方法特征斑点明显,分离效果好,能够作为该制剂中山银花的专属性鉴别。
3.2TLC温度考察 TLC实验中使用了三氯甲烷-甲醇-水(6∶4∶1)为展开剂,发现在室温条件下重复性较差,样品图谱易拖尾,影响结果判定。而将样品放置在10 ℃以下保存的展开剂中展开,则重复性良好,故采用其作为展开条件。
3.3HPLC流动相的选择 HPLC实验中比较了3种不同的流动相系统,分别是乙腈-4 mL·L-1磷酸、甲醇-4 mL·L-1磷酸和甲醇-水-冰醋酸。结果表明,在乙腈-4 mL·L-1磷酸流动相系统下,绿原酸色谱峰的保留时间适宜,分离度良好。
3.4HPLC前处理条件优化 在建立HPLC法测定山银花和乌梅中绿原酸含量的方法中,笔者进行了以下单因素系统考察实验:体积分数为30%的甲醇、体积分数为50%的甲醇、体积分数为70%的甲醇、甲醇和乙醇共5种提取溶剂;超声和回流2种提取方法;不同提取时间(30,45和60 min)。结果表明,在提取溶剂为体积分数为30%的甲醇、超声提取30 min的条件下,金梅清暑颗粒中的绿原酸提取率达到最佳。
本实验方法首次建立了投料药材为山银花的金梅清暑颗粒的定性定量质量控制方法,结果快速、简便、灵敏度高,为金梅清暑颗粒质量标准修订的提升提供参考,同时也对其他含山银花中药制剂的质量控制提供参考依据。

