合成单位点钴基催化剂Co-NG实验
温旭东, 吴淑杰, 管景奇
(吉林大学 化学学院, 吉林 长春 130021)
金属-空气电池作为一种干净的电源设备,由于其独特的半开式系统,直接将燃料中的化学能转化为电能,被认为是有效和清洁能源转化的候选者之一[1]。在其空气电极上消耗大量的氧气,从而实现高能量密度。特别是锌-空气燃料电池,由于材料成本低廉,环境友好且易操作而受到越来越多的关注和深入研究。然而,氧气还原反应(ORR,O2+H2O +4e-→ 4OH-)和氧气释放反应(OER,4OH-→ O2+H2O +4e-)动力学缓慢阻碍了锌-空气燃料电池的实际开发,这是因为高的OO键能(498 kJ·mol-1),这种双键在放电和充电过程中很难被破坏。因此,Pt/Ir基贵金属催化剂尽管非常昂贵、稀缺且具有有限的可用性和稳定性,但也已被广泛用于ORR/OER。经实践证明,通过使用简便技术将N掺杂的、原子分散的Co负载在石墨烯基质上来合成Co-NG(NG表示N掺杂石墨烯),已经成为电催化剂中ORR活性部位的潜在替代物[2]。
当纳米材料缩小到原子尺度时,会出现意想不到的特性[3]。为了获得金属单位点催化剂,原子分散的金属原子的生成可以通过物理或化学方法来实现[4]。金属单位点的稳定化主要基于自下而上的策略,在此过程中,金属前驱体被支撑物吸收、减少并被限制[5]。在酸性或碱性介质中,金属支撑的N掺杂碳材料替代Pt基催化剂是具有实际意义的材料之一。
“单位点钴基催化剂的制备”涉及到了实验室的基本操作过程,“氧还原反应”的应用已经成为国内许多高校必修的物理化学基础实验内容之一,本实验创新地将“单位点钴基催化剂应用在氧还原反应”中,具有全面性和综合性。本实验方法良好且具有实施性,可以推广[6]。
1 实验原理
金属-空气电池,也称为空气去极化电池,由金属阳极(负)和氧阴极(正)构成。锌-空气燃料电池是更成熟的金属-空气燃料电池技术之一。锌-空气燃料电池电极反应式:
阴极:O2+ 2H2O + 4e-= 2OH-
阳极:2Zn + 4OH-= 2ZnO + 2H2O + 4e-
总反应:2Zn + O2= 2ZnO
典型的锌-空气燃料电池由碱性电解质、可替换的阳极、空气阴极组成。锌-空气燃料电池的充/回收过程包括[7]:
(1) 拆解使用的锌源(通常80%的锌利用率);
(2) 锌阳极氧化产物(ZnO)与电解质(KOH)的反应:
ZnO+2KOH + 2H2O = K2Zn(OH)4;
(3) 电解锌酸盐溶液:
2K2Zn(OH)4=2 Zn + 4KOH + 2H2O +2O2;
重新组装含有电解锌的Zn源与质子交换膜燃料电池(PEM-FC)相比,锌-空气燃料电池的商业化已经开始应用。
氧还原反应的测试涉及到电化学,用于诊断电化学机制的常用方法是Koutecky-Levich(K-L)方法[8]。该方法基于电流密度j的倒数与旋转盘电极的旋转速率ω的平方根的倒数(1 /j-ω-1/2)的外推,从这个曲线的截距和斜率可以得到几个机械参数,例如速率常数、扩散系数和转移电子数(但最后2个在同一时间)[9]。
K-L方程如下:
根据南山终端中水系统试运行期间出现的问题,及时采取有针对性的改进措施,对工艺系统进行了优化改造,改进转水方式、采用硝化与反硝化同步工艺,采取多项措施降低系统的耗电量及淡水消耗量,并优化系统的运行管理方式,中水回收率高,产水水质合格,解决了系统运行不稳定、氨氮含量偏高、回收率低、运行成本偏高等问题。措施可操作性较强,系统运行经济性强,实现了生活污水零排放,既是南山终端持续推进低碳、清洁生产的手段,也是油气田降本增效的一项重要措施。
式中:F是法拉第常数,F=9.6485×104C/mol;D为氧气扩散系数,cm2/s;υ为溶液黏度系数,cm2/s;C为氧分子体积浓度,mol/cm3;n为电子转移个数,jk为动力学极限电流密度。
一般情况下,通过1/j对ω-1/2作图求斜率,斜率k=1/jlim,要求D、υ、C是已知参数,从斜率中得到n。
经查文献[10],当电解质为0.1 mol/L KOH时,C= 1.2×10-6mol/cm3,D=1.9×10-5cm2/s,υ= 0.01 cm2/s。
利用K-L方程来计算在碱性电解液(0.1 mol/L KOH)中ORR过程电子转移个数。首先根据K-L求出斜率k,然后根据jlim=1/k=0.62nFD2/3υ-1/6。得到n= 1/(0.11k),可求出电子转移个数n。
2 实验
2.1 实验仪器与试剂
仪器:烘箱,电热恒温油浴锅,循环水真空泵,旋转蒸发仪,超声器,管式炉,电化学工作站,红外光谱仪。
试剂:六水合硝酸钴(Co(NO3)2·6H2O),氧化石墨烯(GO),蒸馏水(DI),硝酸,氮气纯度99.999%),NH3(纯度99.999%)。所有试剂均为AR级。
2.2 实验
2.2.1 Co-NG的合成
将100 mg GO溶于500 mL水中,超声30 min;然后加入0.04 mmol Co(NO3)2·6H2O,超声20 min;再通过旋转蒸发仪在80 ℃条件下除去水,并将其在70 ℃下干燥2 h;然后将样品在NH3气氛下以5℃/min的加热速率从室温加热至750 ℃,维持1 h;最后冷却至室温,干燥称重并计算产率。
电化学工作站为上海辰华仪器有限公司制造,在标准的三电极电池中进行。所述三电极电池具有所需样品涂覆的玻璃碳电极(GCE)作为工作电极(WE),作为对电极的铂,在碱性溶液中使用饱和甘汞电极(SCE)作为参比电极。为了制备工作电极,将1 mg催化剂加入到质量分数为1%的Nafion溶液(50 μL)的乙醇溶液(150 μL)中,超声20 min;之后,将5 μL的混合液在玻碳电极上;最后在0.1 mol/L的KOH电解质溶液中线性扫描曲线。
2.2.3 红外光谱表征
取适量的Co-NG进行KBr压片(质量比约为1∶100),然后进行红外光谱测试。
3 实验结果与讨论
3.1 产率
产率的计算以样品反应前加入量为基准。通过收集实验数据进行统计分析,大部分学生的产率达到40%~50%。部分学生产率较低,主要原因有以下几点:(1) 反应过程中未控制好温度,温度过高,使溶液溅出容器,产率必然下降;(2)在抽滤过程中样品损失过多,洗涤时将样品损失;(3)在管式炉中焙烧时,样品挂于石英管内壁。
3.2 表征
图1为样品红外光谱图。从图中可获得在波数σ为1 457,1 506,1 540,1 575和675 cm-1处有明显吸收峰,归属于碳环上的CC及C—H键弯曲振动[11]。在1 605 cm-1处的吸收峰归因于CN键,而在2 359 cm-1处出现明显的吸收峰归属于CO。
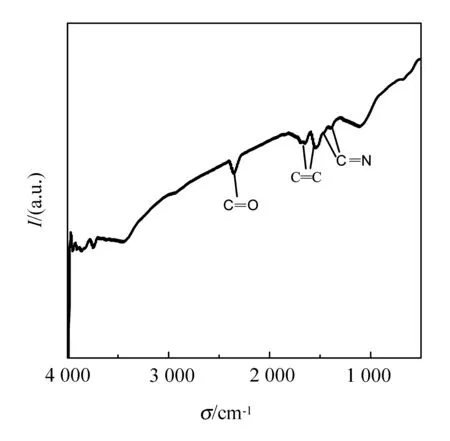
图1 Co-NG样品红外光谱
为了更好地了解Co-NG催化剂的结构,对其形貌及物象进行表征(见图2)。Co-NG的透射电子显微镜图中没有发现明显的纳米颗粒,证明Co是一种高分散的状态。球差电镜可以直接看到很多亮点,为钴离子。该结果表明金属钴离子是一种单位点分布的。通过扫描电子显微镜以及元素分布进行能谱表征确认了C、N、Co元素是均匀分布的。

图2 Co-NG样品透射电镜图、球差电镜图、扫描电子显微镜图和C,N,Co元素分布
3.3 ORR性能
图3显示样品在0.1mol/L KOH溶液中、在不同的电极转速下电流密度曲线。从图3可以看出,随着旋转圆盘电极转速从600 r/min增加到3 000 r/min,Co-NG的电流密度逐渐增加,这是由于电解质和电极之间界面浓度极化的减少。并且起始电位V约为0.98 V(vs RHE),优于商业Pt/C催化剂。相关的K-L曲线(图4)揭示了不同电位值中反转电流密度(j-1)与旋转速度的平方根(ω-1/2)相反的函数。它在不同转速下表现出良好的线性,且在0.40~0.60 V的电压范围内n值约为3.44,表明由Co-NG催化的ORR过程包括两电子与四电子混合的一种转移途径。

图3 Co-NG在不同转速下的电流密度曲线
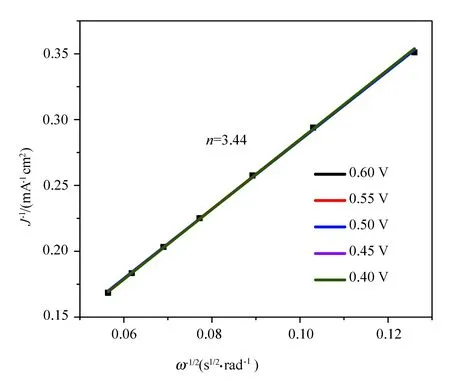
图4 Co-NG在不同电位值下K-L曲线
通过简单经济的合成路线,合理设计具有理想氧还原反应(ORR)性能的且具有成本效益的非贵金属基催化剂是未来燃料电池和金属空气电池商业化的一大挑战[12]。
4 结论
利用焙烧法制备了单位点钴基催化剂Co-NG,具有很高的原子利用率,碱性锌-空气燃料电池的ORR反应显示出优异的催化活性。通过对Co-NG催化剂的表征,结果表明金属Co离子高度分散在氮掺杂的石墨烯上,该催化剂表现出高效的ORR活性,起始电位约为0.98 V(vsRHE),优于商业Pt/C催化剂。通过K-L方程计算得到电子转移数为3.44,表明ORR包括两电子与四电子混合的一种转移途径。
本实验创新地制备了高效廉价的单位点催化剂,并且在氧还原反应中表现出优越的催化性能,为燃料电池中氧还原电极材料工业生产提供了一条途径。

