五氧化二氮/硝酸体系中活性质点的分析与研究
李永祥, 郭昊琪, 柴笑笑, 曹端林, 王建龙, 王松林
(中北大学 化学工程与技术学院, 山西 太原 030051)
0 引 言
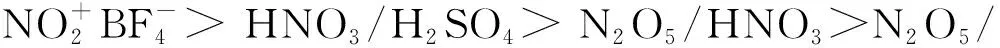
采用N2O5作硝化剂的新工艺是当前具有代表性的新型硝化技术[5]. N2O5/HNO3溶液是一种强有力的硝化体系, 其硝化能力等同于硝硫混酸的硝化能力[6]. 又因其硝化有较强选择性, 反应温度易控制, 基本不放热, 可在低温下进行, 不发生氧化等副反应, 硝化产物得率较高[7]. N2O5独特的性质使它在硝化反应中有着广泛的应用前景, 鉴于其在硝化领域中的重要性, 越来越多的科研工作者研究了N2O5的硝化特性[4].
当前制备N2O5的主要方法[8-9]有HNO3经P2O5脱水法, 直接蒸馏法, N2O4臭氧化法与电解法. 本文采用P2O5与98%浓HNO3混合制备N2O5, 配置不同浓度的N2O5/HNO3体系硝化乌洛托品, 通过红外、 拉曼光谱分析研究N2O5/HNO3体系中各活性质点硝化机理.
1 实 验
1.1 N2O5的制备及不同浓度N2O5/HNO3溶液配制
1.1.1 N2O5的制备
将P2O5与98%浓HNO3混合来制备N2O5.
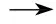
将40 mL 98%浓HNO3倒入四口烧瓶并将其放入恒温-10 ℃的冷阱中, 将120 g P2O5缓慢加入并搅拌至加料完成. 将瓶内混合原料取出放至恒温29 ℃的水浴锅中, 采用P2O5作为干燥剂于-10 ℃冷阱中收集, 收集得到25.4 g N2O5.
1.1.2 不同浓度N2O5/HNO3溶液配制
低温准确称取不同质量的N2O5固体, 量取不同体积的98%浓HNO3溶液, 室温20 ℃下将N2O5溶入浓HNO3中得到配置溶液. 用红外、 拉曼光谱测试配置出的5%, 10%, 15%, 20%, 25%, 30%六种不同浓度的溶液和98%浓HNO3, 并且用该样品硝化乌洛托品.
1.2 光谱检测
红外光谱是吸收光谱, 而拉曼光谱是散射光谱. 原则上, 拉曼光谱的频率(波数)和有机官能团的对应关系与红外光谱是一样的. 但对于特定的结构质点, 没有红外特征吸收频率, 要从分子光谱中得到结构信息, 必须借助于拉曼光谱. 拉曼光谱的峰比红外光谱尖锐, 分辨比较容易, 尤其是在低波数的指纹区域, 红外光谱峰太多, 难以分辨, 而在低波数的拉曼光谱则清晰得多. 因此用以下两光谱结合的方式对反应体系中活性质点进行分析与研究.
1.2.1 红外光谱检测
通过红外光学仪器将不同浓度N2O5/HNO3体系溶液及98%浓HNO3采用KBr压片法, 利用FTIR-7600型红外光谱仪, 在4 000~5 000 cm-1范围内进行扫描, 得到不同浓度红外光谱, 7种样品测试结果如图 1 所示.
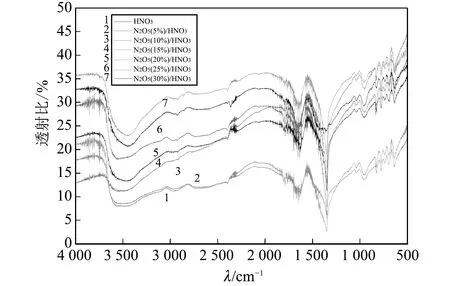
图 1 5%~30%N2O5/HNO3体系溶液及98%浓HNO3的红外光谱图Fig.1 Infrared spectrum of 5%~30% N2O5/HNO3 system solution and 98% HNO3
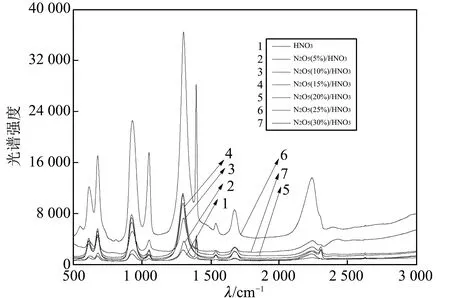
图 2 5%~30%N2O5/HNO3体系溶液及98%浓HNO3拉曼光谱Fig.2 Raman spectrum of 5%~30% N2O5/HNO3 system solution and 98% HNO3
1.2.2 拉曼光谱检测
毛细管采样, 通过德国布鲁克激光共聚焦拉曼光谱仪(stenterra.bruker), Ar离子激光源, 在室温20 ℃条件下, 扫描波长532 nm, 扫描时间10 s, 叠加三次, 得出不同浓度拉曼光谱, 7种样品测试结果如图 2 所示.
2 结果与讨论
2.1 光谱分析
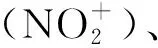
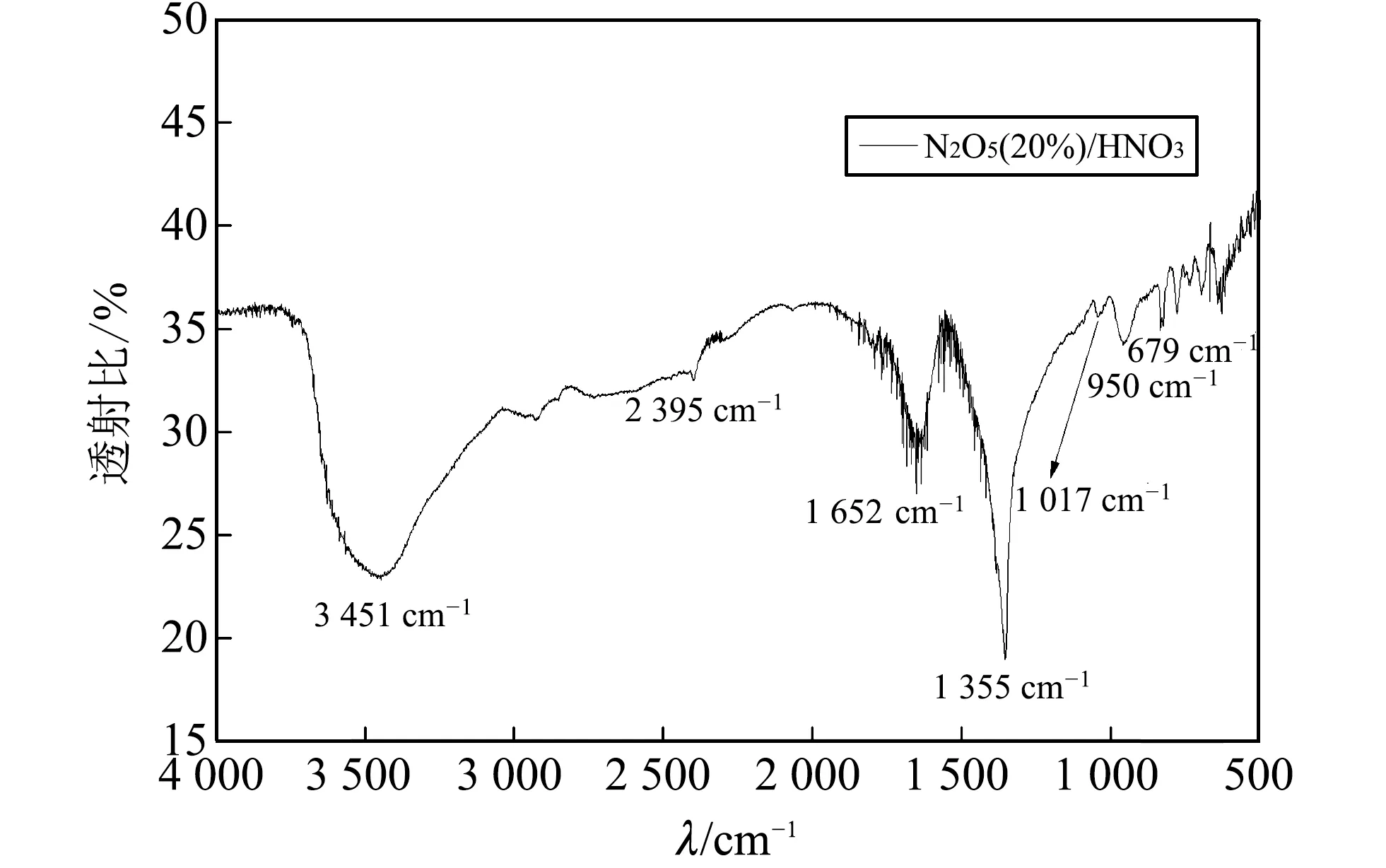
图 3 20% N2O5/HNO3体系溶液红外光谱Fig.3 Infrared spectrum of 20% N2O5/HNO3 system solution

图 4 20% N2O5/HNO3体系溶液拉曼光谱Fig.4 Raman spectrum of 20% N2O5/HNO3 system solution
2.1.1 硝酰阳离子

2.1.2 硝酸合氢离子
硝酸合氢离子的存在(它们以缔合的双分子硝酸, 即在1 017 nm红外光谱上的强度)从拉曼光谱图像上无特征峰, 而通过红外光谱, 可以观测到1 017 nm红外吸收光谱的强度, 且通过不同浓度红外光谱图对比, 硝酸合氢离子特征峰变化不明显.
2.1.3 硝酸根离子
其拉曼光谱在峰值1 287 cm-1,1 051 cm-1附近, 出现特征峰, 与文献描述一致[10]. 而通过和拉曼图像对比分析, 两组硝酸根离子与硝酰阳离子的规律相类似, 特征峰强度呈先线性增加后降低的规律.
2.1.4 亚硝酸根离子
峰值在1 655 cm-1附近, 出现特征峰, 通过特征基团拉曼频率表[12], 亚硝酸根特征峰在1 660~1 620 cm-1附近, 可推断此1 655 cm-1特征峰为亚硝酸根离子. 根据拉曼光谱检测, 随着N2O5浓度变化, 特征峰强度无明显变化规律.
2.1.5 HNO3分子及其他配合物离子
通过与98%浓HNO3溶液对照分析, 红外与拉曼光谱均可在峰值与679 cm-1, 932 cm-1, 1 538 cm-1检测出HNO3特征峰, 且随着N2O5浓度增加, 特征峰均存在先增强后减弱的趋势.
除此之外, 98%浓HNO3可能含有其它配合物离子, 从红外与拉曼光谱中检测不明显, N2O5容易分解成的NO2及N2O4均未从图像中检测出来, 通过拉曼光谱测定, 尤其在810 cm-1, 1 380 cm-1[13]处未能检测出N2O4特征基团, 可推断即便分解成N2O4, 含量也极低.

2.2 硝解法制备RDX的N2O5/HNO3反应体系中各活性质点反应机理

硝酸硝化乌洛托品生成黑索今的反应中, 存在大量副反应, 生成大量副产物, 当硝酸浓度为95%~100%时, 主要生成黑索今反应. 当大量高浓度硝酸对乌洛托品进行硝解作用时, 赖特[14]认为反应机理如图 5 所示.

图硝化乌洛托品反应机理Fig.5 The reaction mechanism of nitration of urotropine by


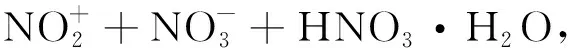
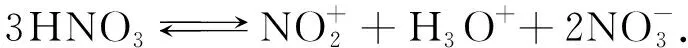


表 1 不同体系中拉曼特征峰波数及强度
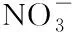
表 2 不同浓度体系溶液中拉曼特征峰波数及强度




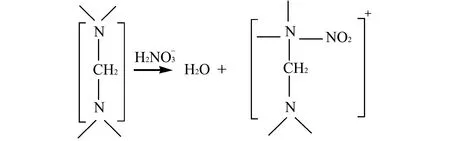
图硝化乌洛托品反应机理Fig.6 The reaction mechanism of nitration of

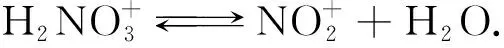
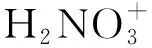
2.2.3 硝酸分子的作用


图 7 直接法制备RDX得到的中间产物Fig.7 The intermediate products of preparing RDX by the direct method
乌洛托品合成黑索今的反应, 是多种并行的反应交织在一起的, 反应途径随反应条件变化而有差别. 乌洛托品与硝酸的生成反应很快, 1 mol硝酸与1 mol乌洛托品可以生成中性的乌洛托品一硝酸盐(HADN), 而加入过量的硝酸, 可以生成乌洛托品二硝酸盐. 在一般的硝解条件下, 硝酸浓度通常很高, 乌洛托品与两分子硝酸合成乌洛托品硝酸盐, 主反应最先直接生成乌洛托品二硝酸盐, 最终生成RDX. 因此, 硝酸分子也可作为反应中活性质点存在.
2.2.4 其他活性质点及相关物质


从拉曼及红外光谱中还可观察到亚硝酸根离子. 而亚硝酸根特征基团明显, 但又无法从光谱中检测到N2O4特征峰, 可推断出亚硝酸中电离出的硝酰阳离子含量很低, 可以不计.
(8)
因此, 硝酸的其他水合质子配合物及亚硝酸根等物质随着N2O5浓度增加亚硝酸强度变化不明显, 对于硝化乌洛托品生成RDX无明显作用.
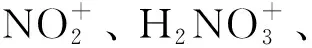
3 结 论


3) 采用N2O5/HNO3溶液体系进行硝化, N2O5的存在不会使硝酸浓度降低, 能够有效减少硝酸用量, 抑制副产物的生成, 降低废酸生成量, 增加RDX得率.

