外源水杨酸预处理对低温胁迫下甜瓜幼苗生长及其抗逆生理特性的影响
刁倩楠,蒋雪君,陈幼源,张永平*
(1 上海市农业科学院园艺研究所,上海市设施园艺技术重点实验室,上海201403;2 上海市金山区农业技术推广中心,上海201599)
甜瓜(Cucumismelo)属葫芦科甜瓜属,一年生蔓性草本植物,甜瓜喜温耐热, 生育期适温为25~35 ℃,在世界园艺生产中占有重要地位,甜瓜具有很高的营养价值和药用价值。甜瓜栽培历史悠久,中国作为甜瓜生产大国,栽培面积和产量历年均居世界首位。但在甜瓜栽培过程中, 尤其是早春栽培中, 经常遇到低温危害, 导致生长发育受到抑制,果实品质受到影响,进而降低经济效益。低温不仅对作物的光合能力、抗氧化酶活性产生影响,还能诱导活性氧大量产生, 造成氧化伤害, 甚至导致植株死亡[1]。水杨酸(salicylic acid, SA),作为一种简单的酚类衍生物, 广泛存在于高等植物体中,不仅能参与植物体内多种生理过程,还与植物抗逆性之间存在密切的关系[2]。研究发现,外源施用SA能通过提高抗氧化酶活性,增加渗透调节物质的含量来减轻干旱、盐害、低温等胁迫对植株造成的伤害[3-6]。前人研究表明,适应浓度的SA能通过激活抗氧化酶活性,调节渗透调节物质的含量,加强光合效率来增强番茄[7]、黄瓜[8]、萝卜[9]和甜瓜[10]等作物的耐低温性。然而,Janda等的研究发现,正常条件下施用SA后,玉米植株的净光合速率、气孔导度和蒸腾速率都发生了下降[11],说明SA也可能产生毒害作用。低温会严重影响甜瓜的产量与品质。外源施用SA能有效提高多种植物的抗逆性,然而不同作物,不同环境条件下SA的保护作用不尽相同。因此,本研究以甜瓜幼苗为试材,通过外源喷施的方法,比较不同浓度SA对低温胁迫下甜瓜幼苗生长、膜系统、渗透调节物质及活性氧清除系统的影响,旨在寻求外源SA诱导甜瓜幼苗耐低温性的最佳浓度阈值,为外源施用SA缓解低温伤害提供理论依据。
1 材料和方法
1.1 材料培养与处理
供试的甜瓜品种为‘红优’,种子由上海市农业科学院园艺研究所提供;SA购买于上海源叶生物有限公司, 用蒸馏水配制1 000 mmol·L-1的母液, 4 ℃保存, 用时按试验所需浓度进行稀释。试验在上海市农业科学院园艺研究所进行,2017年12月27日将饱满、整齐一致的种子浸种催芽, 出芽后播于10 cm×10 cm的塑料营养钵中,以蛭石作基质,然后置于光照培养箱中进行幼苗培养,温度设置为昼(28±1)℃/夜(22±1)℃, 光照12 h,光照强度为400 μmol·m-2·s-1左右。
2018年1月22日, 当幼苗长到3~4片真叶时, 选取生长一致的幼苗用浓度分别为0、0.1、0.5、1.0、2.0 mmol·L-1的水杨酸(SA)溶液(含1/8浓度日本园试营养液)喷施甜瓜幼苗,每株50 mL, 连续喷施3 d, 以便甜瓜幼苗充分吸收SA,分别置于昼(28±1)℃/夜(22±1)℃,光照强度为400 μmol·m-2·s-1左右的光照培养箱内,3 d后将处理的幼苗进行昼(12±1)℃/夜(6±1)℃[12]低温处理。以喷施1/8浓度日本园试营养液,置于昼(28±1)℃/夜(22±1)℃幼苗为对照(CK)。每种处理50株, 3次重复。低温处理与对照培养箱除温度不同外, 光照和湿度状况均一致。低温培养7 d后温度调为昼(28±1)℃/夜(22±1)℃, 进行7 d恢复处理。低温处理7 d和恢复7 d时分别取样进行各项指标的测定。
1.2 测定项目与方法
1.2.1生长量每处理取6株,用直尺测量幼苗株高(子叶节至生长点); 利用游标卡尺测量茎粗, 即子叶展开方向的子叶节的直径; 用去离子水冲洗植株并吸干水分, 称地上鲜重。
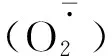
1.2.3抗氧化系统活性超氧化物歧化酶(SOD)活性采用四唑氮蓝法[18]测定;过氧化物酶(POD)的活性采用愈创木酚显色法测定[19];过氧化氢酶(CAT)活性的测定参照Dhindsa等的方法[20];抗坏血酸过氧化物酶(APX)活性的测定参照Nakano和Asada的方法[21];抗坏血酸(AsA)含量的测定参考Law等的方法[22];还原型谷胱甘肽(GSH)含量参照Griffith等的方法[23];单脱氢抗坏血酸还原酶(MDHAR)活性的测定参照Nakano 和 Asada的方法[21]:脱氢抗坏血酸还原酶(DHAR)活性的测定参照Hossain等的方法[24]。
1.3 数据统计分析
每个指标测定重复3次,取平均值。数据采用Origin软件绘图,用SPSS统计软件对平均数用Duncan’s 新复极差法进行多重比较。
2 结果与分析
2.1 外源SA对低温胁迫下甜瓜幼苗生长的影响
如表1所示, 经过低温胁迫及恢复处理7 d后,T0处理甜瓜幼苗的株高与对照(CK)相比分别显著降低了28.47%、36.36%(P<0.05),地上鲜重则分别显著降低36.80%、34.92%,而低温对植株茎粗影响不显著。与T0处理相比,不同浓度SA处理均能诱导低温胁迫甜瓜幼苗的形态指标不同程度增加,且随SA浓度增加呈先升后降的变化趋势,但仍低于对照。其中,1.0 mmol·L-1SA处理(T1.0)作用最为突出,其低温胁迫7 d幼苗株高、茎粗和地上鲜重与相应T0处理相比分别增加了36.24%、5.21%和51.89%,恢复7 d幼苗则分别增加了40.34%、7.66%和38.21%。由此说明,低温胁迫处理使甜瓜幼苗的生长受到显著抑制,而外源SA能够缓解这种抑制作用,其中以1.0 mmol·L-1SA处理的效果最好。
2.2 外源SA对低温胁迫下甜瓜幼苗叶绿素含量的影响
图1显示,在单独低温处理下(T0),甜瓜幼苗叶片的叶绿素a、叶绿素b及叶绿素a+b含量均显著降低,低温处理7 d幼苗与对照相比分别下降了29.26%、49.17%和34.81%,恢复7 d幼苗则分别降低27.54%、42.95%和31.63%。低温胁迫下施用不同浓度SA均能不同程度增加甜瓜叶片的叶绿素a、b和a+b含量,但各低温处理仍明显低于对照(CK);1.0 mmol·L-1SA 处理的增幅最大,其低温处理7 d幼苗叶绿素a、b和a+b含量分别比T0处理显著增加27.66%、59.49%和34.60%,其恢复7 d幼苗则分别比相应T0处理显著增加19.68%、58.96%和28.37%。可见,低温胁迫能诱导甜瓜幼苗叶片叶绿素含量显著降低,而外源SA能够缓解这种下降趋势,并以1.0 mmol·L-1SA处理的效果最好。
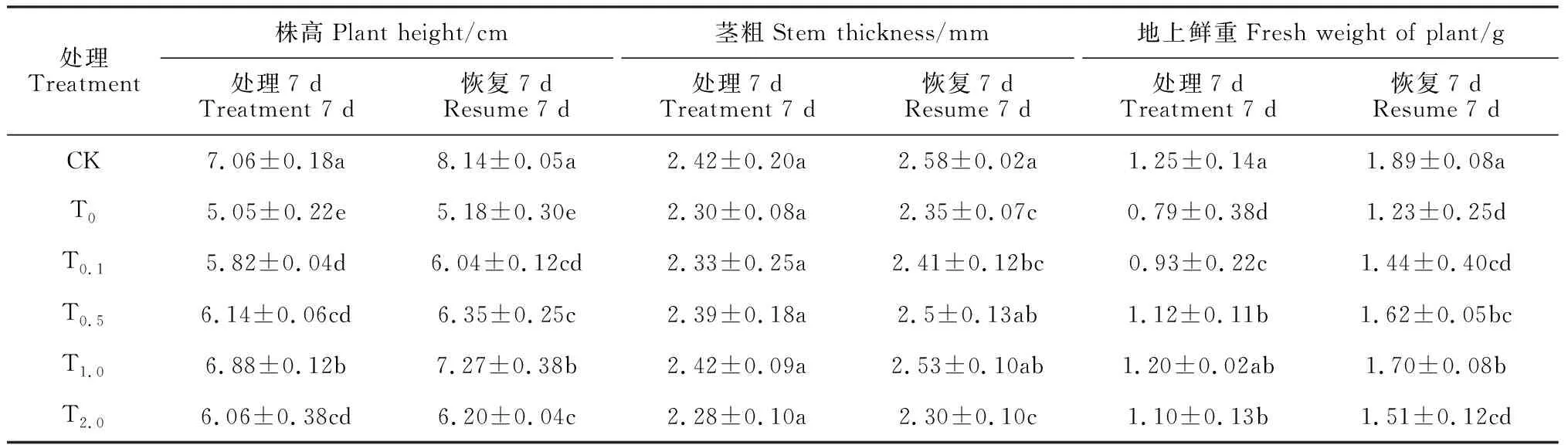
表1 外源SA预处理对低温胁迫以及恢复处理的甜瓜幼苗生长的影响
注:CK.对照,无低温和外源SA处理;T0.单纯低温处理;T0.1. 0.1 mmol·L-1SA+低温处理;T0.5. 0.5 mmol·L-1SA+低温处理;T1.0. 1.0 mmol·L-1SA+低温处理;T2.0. 2.0 mmol·L-1SA+低温处理;相同处理时间内不同小写字母表示处理间差异达0.05显著水平;下同
Note: CK. Control,without chilling stress and SA treatment; T0. chilling stress; T0.1. 0.1 mmol·L-1SA+ chilling stress; T0.5. 0.5 mmol·L-1SA+ chilling stress; T1.0. 1.0 mmol·L-1SA+ chilling stress;T2.0. 2.0 mmol·L-1SA+ chilling stress; The different normal letters within the same treatment time indicate significant difference among treatments at 0.05 level. The same as below
2.3 外源SA对低温胁迫下甜瓜幼苗渗透调节物质含量的影响
从图2可知,与对照(CK)相比,低温处理7 d后甜瓜叶片中可溶性糖和脯氨酸含量分别显著提高12.22%和27.63%,而其可溶性蛋白含量却显著降低了39.66%。与单独低温胁迫(T0)相比,外源SA能够不同程度地增加甜瓜叶片中可溶性糖、可溶性蛋白和脯氨酸含量,且随浓度的增加呈先上升后下降的趋势,1.0 mmol·L-1SA处理的可溶性糖、可溶性蛋白和脯氨酸含量最高,与T0相比分别显著增加了68.97%、58.10%和44.30%。恢复处理7 d后,各处理甜瓜幼苗叶片可溶性糖、脯氨酸、可溶性蛋白含量的变化趋势与低温胁迫处理7 d相似,1.0 mmol·L-1SA处理的可溶性糖、可溶性蛋白和脯氨酸的含量分别比T0处理显著增加了54.79%、66.92%和44.86%,并高于相应的对照水平。说明低温胁迫下施用不同浓度的SA能够增加甜瓜叶片中渗透调节物质的积累,减轻低温对甜瓜幼苗造成的伤害,且1.0 mmol·L-1SA处理作用最明显。

Ⅰ.处理7 d;Ⅱ.恢复7 d。下同图1 外源SA预处理对低温胁迫以及恢复处理的甜瓜幼苗叶绿素含量的影响Ⅰ. Treatment 7 d; Ⅱ. Resume 7 d. The same as belowFig.1 Effects of exogenous SA pretreatment on chlorophyll contents of melon seedlings under chilling stress and resume treatment
2.4 外源SA对低温胁迫下甜瓜幼苗活性氧和膜脂过氧化的影响
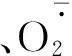
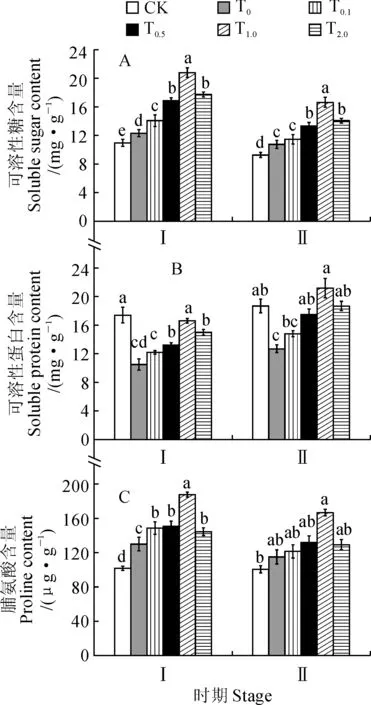
图2 外源SA预处理对低温胁迫以及恢复处理的甜瓜幼苗渗透调节物质含量的影响Fig.2 Effects of exogenous SA pretreatment on osmotic adjustment substances of melon seedlings under chilling stress and resume treatment
2.5 外源SA对低温胁迫下甜瓜幼苗抗氧化酶活性的影响
图4显示, 与常温对照(CK)相比, 低温胁迫7 d后, 单独低温胁迫(T0)甜瓜幼苗叶片SOD、POD、CAT、GR和DHAR活性分别降低23.80%、20.95%、29.63%、68.42%和54.54%, 而APX活性则升高26.83%;低温胁迫下经不同浓度SA处理的甜瓜幼苗叶片中各抗氧化酶活性均比T0处理不同程度增加,且活性随SA浓度的增加呈现先上升后下降的变化趋势,并在SA浓度为1.0 mmol·L-1时各抗氧化酶活性均达最大值,此时比单独低温处理分别提高了36.31%、118.07%、55.26%、48.08%、233.33%和100.00%。在恢复7 d后, 除CAT以外,甜瓜幼苗叶片其他抗氧化酶活性与低温胁迫7 d相比均有不同程度的增加,它们随SA浓度的变化规律与低温胁迫7 d相似, 同样以1.0 mmol·L-1SA处理的甜瓜幼苗叶片抗氧化酶活性最大, 且与常温对照相比显著增加(CAT和DHAR活性除外)。以上结果表明低温胁迫下喷施不同浓度的SA能诱导甜瓜幼苗抗氧化酶活性明显增强, 其中以1.0 mmol·L-1SA处理的作用最为显著。
2.6 外源SA对低温胁迫下甜瓜幼苗抗坏血酸-谷胱甘肽循环的影响
图5表明, 低温胁迫7 d时, 单独低温胁迫处理甜瓜幼苗叶片中ASA、GSH含量及ASA/DHA、GSH/GSSG比值与对照相比均显著降低, 降幅分别为68.29%、74.51%、76.37%和82.81%;同时,低温胁迫下外源施用SA提高了甜瓜幼苗叶片中的ASA、GSH含量及ASA/DHA、GSH/GSSG,且各指标随SA浓度的增加呈现先升高后降低的变化趋势,其中在1.0 mmol·L-1SA处理时达到最大值,此时比单独低温处理分别提高了2.20、2.04、2.86和3.11倍。恢复7 d后,除了ASA含量外,甜瓜幼苗叶片中的GSH含量及ASA/DHA、GSH/GSSG比值与低温胁迫7 d相比均有所降低,单个值的变化规律与低温胁迫7 d相似,仍以1.0 mmol·L-1SA处理的甜瓜幼苗叶片中ASA、GSH含量及ASA/DHA、GSH/GSSG比值最大,与常温对照相比无显著性差异,与单独低温胁迫相比显著提高,增幅分别为1.09、0.30、1.24和1.35倍。以上结果表明低温胁迫下施用不同浓度的SA能激活抗坏血酸-谷胱甘肽循环系统,有效减轻低温胁迫对甜瓜幼苗引起的过氧化伤害。
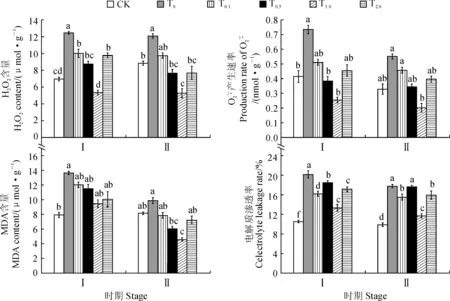
图3 外源SA预处理对低温胁迫以及恢复处理的甜瓜幼苗活性氧及膜脂过氧化和透性的影响Fig.3 Effects of exogenous SA pretreatment on H2O2 and MDA contents, production rate of and electrolyte leakage of melon seedlings under chilling stress and resume treatment
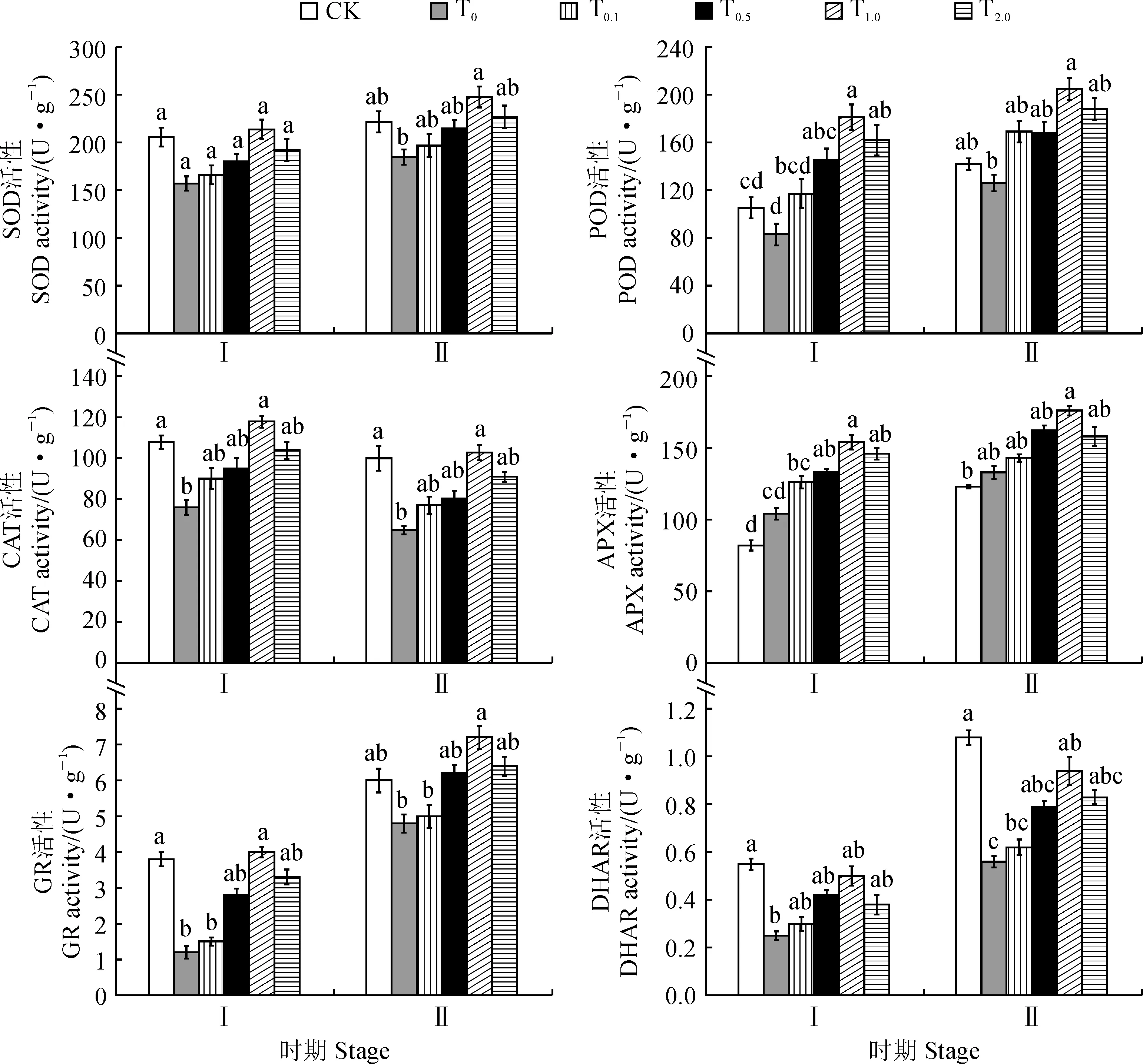
图4 外源SA预处理对低温胁迫以及恢复处理的甜瓜幼苗抗氧化酶活性的影响Fig.4 Effects of exogenous SA pretreatment on antioxidant enzyme activities of melon seedlings under chilling stress and resume treatment
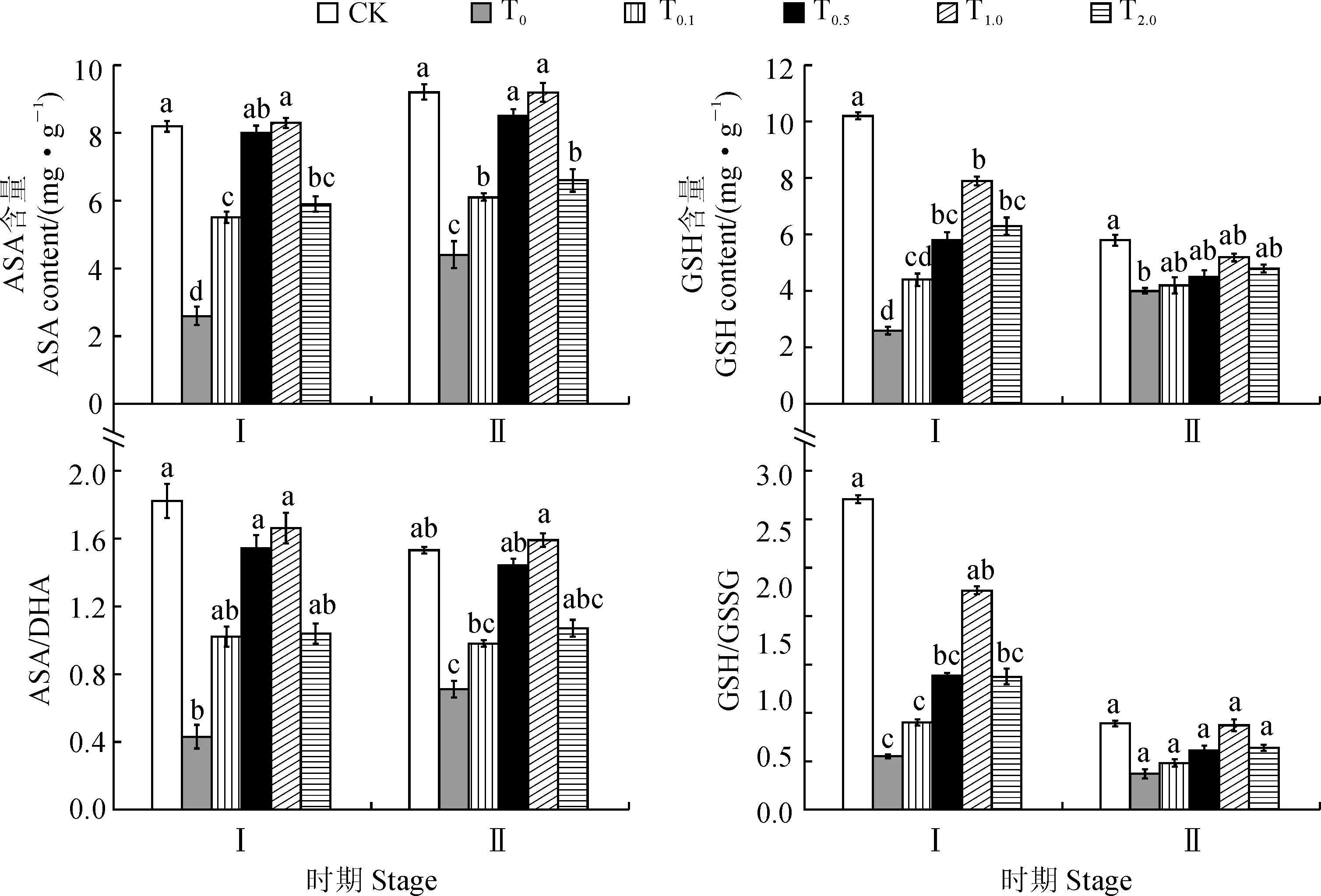
图5 外源SA预处理对低温胁迫以及恢复处理的甜瓜幼苗抗坏血酸-谷胱甘肽循环的影响Fig.5 Effects of exogenous SA pretreatment on ASA-GSH cycle of melon seedlings under chilling stress and resume treatment
3 讨 论
植物的生长发育除了受到遗传因素调控外,还会受到环境条件的影响,低温胁迫是影响设施栽培蔬菜作物优质高产的主要限制因子。前人研究已经证明,低温胁迫会导致植物发生一系列生理生化变化,造成生理功能紊乱。本研究中,与常温对照相比,低温胁迫处理明显抑制了甜瓜幼苗的生长,植株的株高、茎粗和地上鲜重显著低于对照,即使经过恢复处理也无法达到对照水平。同时,低温胁迫还降低了甜瓜幼苗叶片中的叶绿素含量。此外,经过低温胁迫处理7 d后,甜瓜幼苗叶片的相对电导率明显高于对照,说明长期低温胁迫会使细胞膜受到损伤,细胞膜透性增大,使甜瓜幼苗产生冷害性状。这与前人在黄瓜和水稻等作物上的研究结果一致[25]。在本研究中,低温胁迫下施用不同浓度的外源SA均能有效缓解低温对甜瓜幼苗的伤害,并以1.0 mmol·L-1SA的效果最显著;与单独低温胁迫相比,低温胁迫下施用1.0 mmol·L-1SA能显著提高甜瓜幼苗的生长量和叶绿素含量,同时增加可溶性糖、可溶性蛋白及脯氨酸等渗透调节物质的含量,降低叶片的相对电导率,从而提高甜瓜幼苗的耐冷性,这与辛慧慧等在棉花上[26]、刘晓静等[27]在甘蔗上的研究结果一致。
综上所述,对低温胁迫下甜瓜幼苗叶片喷施适当浓度的外源SA后,可以明显改善低温下甜瓜幼苗的生理特性,明显提高其渗透调节物质含量,显著增强SOD、POD、CAT、APX等抗氧化酶活性,激活ASA-GSH循环,显著降低了活性氧的产生和膜脂过氧化伤害,从而有效缓解低温胁迫对甜瓜幼苗的损害,明显提高幼苗的耐寒能力。

