腹腔镜全结肠切除术经自然腔道取标本的应用效果分析
胡俊杰,鲁 力,熊治国,阮 戈,朱光胜,张 弛,斯迪克江,魏少忠
(湖北省肿瘤医院,湖北 武汉,430079)
全结肠切除术是家族性腺瘤性息肉病、林奇综合征相关结直肠癌及部分结肠多原发癌的主要治疗方法[1]。腹腔镜全结肠切除术是结直肠手术中难度最大、操作最复杂的术式之一,涉及右半结肠、左半结肠及直肠切除术的技术要点与难点,操作创面范围广,对结直肠外科医师要求高[2]。经自然腔道取标本手术(natural orifice specimen extraction surgery,NOSES)是近年结直肠微创外科领域的重要技术创新,由于避免了传统腹腔镜辅助手术所需要的取标本腹部小切口,从而进一步增加了腹腔镜外科的微创优势[3-4]。全结肠切除术的手术标本较大且纵轴长,传统理念认为很难将其经自然腔道取出,且由于术式的复杂性,该类术式报道较少。本中心共完成15例经自然腔道取标本的腹腔镜全结肠切除术,现将开展初期的结果及体会报道如下。
1 资料与方法
1.1 临床资料 2015年1月至2018年6月湖北省肿瘤医院胃肠外科共完成15例无腹部辅助切口的腹腔镜全结肠切除手术,标本经自然腔道取出。15例患者中家族性腺瘤性息肉病 8例,多原发结直肠癌5例,林奇综合征相关结直肠癌2例。标本在腹腔内完整游离后,经肛门取出11例,经阴道取出4例。本中心挑选合适的患者施行全结肠NOSES,条件如下:(1)术前CT、MRI或内镜超声考虑恶变肿瘤临床分期cT1~3;(2)肿瘤最大径≤5 cm;(3)直肠壶腹无恶变病灶或腺瘤数量少,可电灼处理;(4)内脏脂肪厚度适宜;(5)经评估可耐受常规腹腔镜手术;(6)术前需取得患者知情同意。
1.2 手术方法 均气管插管静脉复合全身麻醉,患者取截石位。脐下缘1 cm穿刺10 mm Trocar作为观察孔并建立气腹,压力维持在15 mmHg。采用5孔法施术,分别于右下腹及左上腹穿刺12 mm Trocar作为操作左半及右半的主操作孔,分别于右上腹及左下腹穿刺5 mm Trocar作为辅助操作孔。游离顺序为逆时针方向,术者开始立于患者右侧,扶镜手立于头侧,显示器置于尾侧,首先游离直肠,然后依次游离乙状结肠;调整显示器放置于头侧,扶镜手转至尾侧,继续向上依次游离降结肠、结肠脾区及横结肠左半,完成左半结肠游离后,术者转至患者左侧,继续游离右半结肠,直至全结肠游离后应用切割闭合器闭合离断末端回肠(图1),最后调整显示器至尾侧,扶镜手转回至头侧,术者立于患者右侧行消化道重建。经肛门取标本及消化道重建过程:直肠上段切开直肠,经肛门置入切口保护套,吻合器钉砧头经肛门置入腹腔,卵圆钳经肛门夹住标本远端向外拖出标本(图2),腔内切割闭合器闭合直肠残端(图3)。于末端回肠断端5 cm切开末端回肠,置入钉砧头并手工腔镜下荷包缝合固定(图4),经肛门置入吻合器完成末端回肠-直肠侧-端吻合(图5)。经阴道取标本及消化道重建过程:直肠上段切割闭合器闭合离断直肠完全游离全结肠标本。阴道经稀释碘伏水消毒冲洗后用超声刀切开阴道后穹隆(图6),置入切口保护套,吻合器钉砧头经阴道置入腹腔,卵圆钳经阴道夹住标本远端向外拖出标本(图7)。倒刺线缝合阴道后穹隆切口(图8)。消化道重建方法同前。
1.3 统计学处理 应用SPSS 19.0软件进行数据分析,计量资料以均数±标准差进行描述,或以中位数描述,计数资料采用频数及百分比描述。

图1 闭合离断末端回肠 图2 切开直肠后经肛门置入保护套,经肛门取出标本(右上角小图为会阴组医师拖标本情况)

图3 闭合直肠残端 图4 钉砧头置入末端回肠并荷包缝合固定
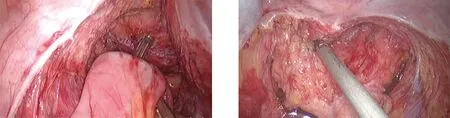
图5 经肛门置入吻合器完成末端回肠-直肠侧-端吻合 图6 切开阴道后穹隆

图7 经阴道置入保护套,取出标本 图8 腹腔镜下倒刺线连续缝合关闭阴道切口
2 结 果
手术均顺利完成,无一例中转开腹,术中无副损伤、出血及死亡病例。15例患者中女9例,男6例; 26~75岁,中位年龄56岁。BMI平均(22.9±2.6)kg/m2。根据国际抗癌联盟2017年第八版TNM分期:Ⅰ期5例,Ⅱ期6例,Ⅲ期4例。5例多原发癌患者肿瘤发病部位:结肠肝曲+直肠2例,升结肠+降结肠1例,横结肠+乙状结肠1例,横结肠+降结肠+直肠1例。肿块最大径平均(3.1±1.0)cm。手术时间平均(180.8±13.2)min,术中出血量平均(128.0±71.5)mL,淋巴结清扫数量平均(45.3±17.2)枚。术后排气时间平均(2.3±0.6)d,术后进流质时间平均(2.6±0.6)d,术后平均住院(9.7±2.0)d。术后1例(6.7%)出现并发症,为术后第4天出现吻合口漏,行回肠造口术治疗,患者顺利出院。本组均无肺部感染、盆腔脓肿、肠梗阻发生。
患者术后均获随访,随访3~45个月。术后3个月排便次数为3~10次/d,中位次数为6次/d。经调整饮食结构并改变生活习惯,每日排便次数有逐渐减少趋势。患者均无排尿困难、性功能障碍及大便失禁。肿瘤学结果方面,1例多原发癌患者术后12个月出现肝转移,另1例多原发癌患者术后18个月出现肺转移,余者随访过程中均未见局部复发及远处转移。
3 讨 论
结直肠NOSES是近年结直肠微创外科领域的一大发展热点,其注重标本取出途径的创新,是外科医师对微创效果不断追求的产物[5-6]。由于标本经自然腔道取出,避免了腹部辅助切口,不仅为患者获取了良好的美容效果,同时减轻了术后疼痛与心理压力,加快了术后恢复[7-8]。2017年中国NOSES联盟制定了首版NOSES手术专家共识[9],根据取标本方式及切除肿瘤部位将NOSES进行分类命名,全结肠切除术经肛门取标本被命名为NOSES Ⅸ式,经阴道取标本被命名为NOSES Ⅹ式,也被认为是腹腔镜结直肠手术操作技术要求最高的术式之一。
NOSES的一大技术难点在于能否将标本从自然腔道取出,大标本往往很难经狭窄的自然腔道取出,因此对于全结肠切除术而言,由于标本长、体积大,且横结肠附着大网膜肥厚,往往被认为很难经肛门或阴道取出。本中心尝试开展15例NOSES全结肠切除术,最初经阴道拖出标本获得成功,后经肛门取标本过程依然比较顺利,证实患者如满足NOSES的手术适应证:肿瘤最大径不超过5 cm、内脏脂肪厚度适宜,全结肠标本经充分游离展开后,沿肠管长轴方向经肛门或阴道拖出标本技术上是可行的。本中心经肛门或阴道放置切口保护套,对取出通道起到一定程度的支撑作用,利于标本的取出,同时在保护套内侧面涂抹石蜡油润滑,则更加有助于取出标本。此外,我们选择直肠壶腹无恶变病灶或腺瘤数量少的患者施行NOSES,主要考虑保留直肠壶腹对患者术后排便、控便功能具有重要意义,且拖出标本后可较方便地在腔镜下闭合直肠残端完成回肠直肠的侧-端吻合。
目前关于经自然腔道取标本的全结肠切除的研究报道较少,Palanivelu等[10]报道了7例家族性腺瘤性息肉病合并直肠癌患者,在腹腔镜下行全结直肠切除术,标本经阴道取出,术后阴道切口均愈合,无阴道瘘发生,因此认为经阴道取标本的全结肠切除术是安全、可行的。本研究中4例女性患者标本经阴道取出,我们体会阴道壁扩张性良好,较经肛途径取标本更为容易,因此如肿瘤体积偏大,考虑经肛门拖出标本存在一定难度时可考虑选择经阴道取标本。阴道后壁血运充分,组织愈合能力强,只要保证肠道吻合口的血运与张力适宜,肠道吻合时勿夹入阴道后壁组织,并不会因为经阴道取标本增加直肠阴道瘘的机会。本中心关闭阴道切口是在腹腔镜下用倒刺线连续单层缝合,未观察到阴道切口愈合相关并发症发生。
术后并发症方面,本组15例患者中术后仅1例(6.7%)出现吻合口漏,经回肠造口术治疗好转出院,均无腹盆腔感染等其他并发症发生,已体现出良好的短期疗效。随访结果显示,2例多原发癌患者术后出现转移,而其他患者随访最长达45个月均未见肿瘤转移。近期韩国Park等[11]报道了NOSES与传统腹腔镜手术的对比研究,两组术后并发症发生率差异无统计学意义,且经过中位随访时间57个月的观察,结果显示138例直肠NOSES患者5年局部复发率仅为4.1%,5年无病生存率高达89.3%,与传统腹腔镜手术无明显区别。
综上所述,尽管腹腔镜全结肠NOSES的操作较传统腹腔镜手术复杂,但其代表了现代微创外科发展的方向,可给患者带来大手术无疤痕的效果。结合我们完成的15例腹腔镜全结肠NOSES的经验,我们认为严格把握手术适应证,挑选合适的患者开展,全结肠标本能较容易地经肛门或阴道取出,且不增加患者并发症,在有经验的中心开展此类复杂手术依然是安全、可行的。

