薄膜扩散梯度(DGT)
——技术进展及展望
李 财,任明漪,石 丹,王 燕,3,杨丽原,丁士明*
(1.济南大学水利与环境学院,济南 250022;2.中国科学院南京地理与湖泊研究所,南京 210008;3.南京智感环境科技有限公司,南京 210008)
薄膜扩散梯度(Diffusive Gradients in Thin-films,DGT)技术主要利用自由扩散原理(Fick第一定律),通过对目标物在扩散层的梯度扩散及其缓冲动力学过程的研究,获得目标物在环境介质中的(生物)有效态含量与空间分布、离子态-络合态结合动力学、以及固-液之间交换动力学的信息[1-3]。DGT装置由固定层(即固定膜)和扩散层(扩散膜和滤膜)叠加组成,目标离子以扩散方式穿过扩散层,随即被固定膜捕获,并在扩散层形成线性梯度分布(图1)。DGT装置对目标物的扩散通量(FDGT)可用公式(1)和公式(2)计算:

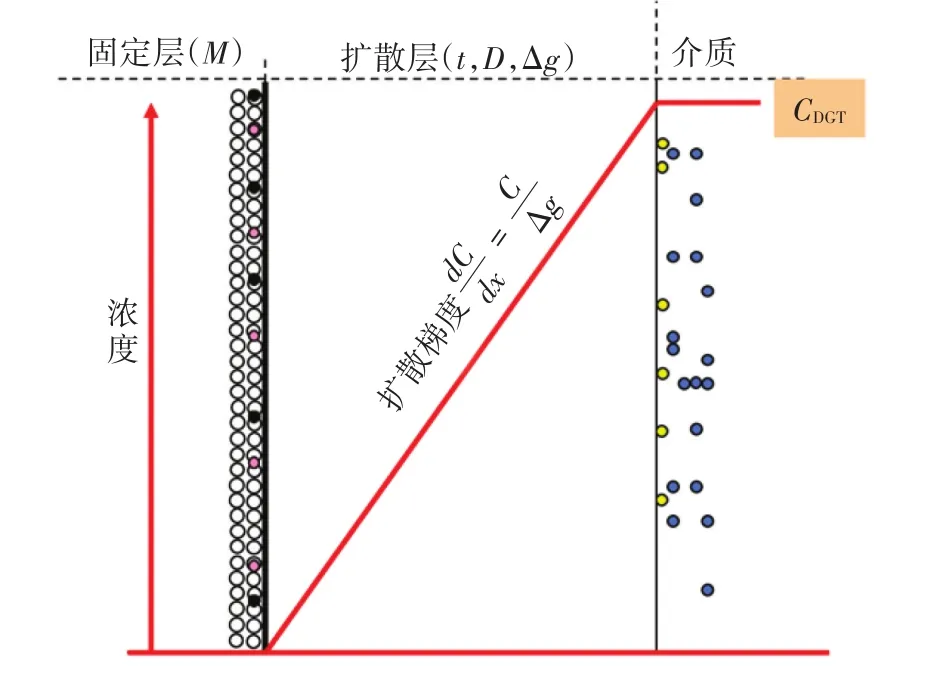
图1 薄膜扩散梯度原理示意图Figure 1 Schematic diagram of diffusive gradients in thin-films
式中:t为DGT装置放置时间,s;M为DGT装置放置时间段固定膜对目标离子的积累量,μg;A为DGT装置暴露窗口面积,cm2;Δg为扩散层厚度,cm;D为目标离子在扩散层中的扩散系数,cm2·s-1;CDGT为扩散层线性梯度靠近环境介质一端的浓度,mg·L-1。
将公式(1)和公式(2)结合,得到CDGT的计算公式(3):
固定膜中目标离子积累量(M)一般采用溶剂提取的方法,根据公式(4)计算得到:

式中:Ce为提取液浓度;Ve为提取剂体积;Vg为固定膜体积;fe为提取剂对固定膜上目标离子的提取率。
当DGT装置测定水体时,DGT吸收目标物中的自由离子态组分,将促使弱结合络合物的解离,因此FDGT/CDGT反映水体目标物自由离子态组分的含量及弱结合络合物对该形态的解离和缓冲能力。当DGT装置测定土壤、沉积物时,DGT吸收造成孔隙水中目标物溶解态组分降低,导致固相弱结合态组分通过解吸或溶解对溶解态组分进行缓冲,因此FDGT/CDGT反映土壤、沉积物中溶解态的含量及固相弱结合态对其溶解态的缓冲能力。
DGT技术首先应用于检测水环境中的金属阳离子,并在1995年获取了DGT野外测量结果[1,4]。1997年,Davison等[5]将DGT应用到沉积物中,获得了重金属离子的高分辨分布信息。1998年,Zhang等[6]利用DGT测定了土壤中重金属的生物有效性,将DGT技术拓展到土壤领域。此后经过大量研究人员的改进和扩展,DGT技术可测定的目标物已从常规的金属阳离子拓展到贵金属[7-8]、有机金属[9-11]、氧化性阴离子[12-13]、放射性物质[14-15]、营养盐[16-18]、有机物[19-20]以及稀土元素[21-22]等。
DGT技术自1994年发明以来,已有二十多年的发展历史,并发表了多篇DGT技术原理和应用的综述[23-31]。其中,有关DGT技术材料、装置和测定流程的论述还较为缺乏。尽管该技术的发展速度较快,但在装置构型和测定流程等方面还存在一定的不足,造成测定结果常出现偏差,又难以被研究者注意。本综述将集中探讨DGT技术在装置构型、固定相和扩散相材料制备、样品测定流程等方面的研究进展,并对未来的发展进行展望。
1 DGT装置的发展
目前,DGT装置主要有四种类型,分别是活塞式(Piston type)、双模式(Double mode)、平板式(Flat type)和液体固定相装置,前两种装置用于土壤和水体的测定,第三种装置用于沉积物、湿地土壤的测定,最后一种装置主要用于水体的测定。
1.1 活塞式DGT装置
如图2a所示,活塞式DGT装置由底座和盖帽两部分组成,底座上依次放置固定膜、扩散膜和滤膜,并用盖帽固定3层膜。活塞式DGT装置的暴露窗口直径为20 mm,面积为3.14 cm2,暴露窗口直接与环境介质(土壤、水体等)接触,目标物通过该窗口扩散通过扩散层,被结合相固定。该装置可以通过尼龙线、塑料网条、有机玻璃板等方式进行固定后放置在天然水体中,用于水体的测定[7,32-34]。同时,可以通过用手按压的方式将装置与土壤(调节水分后)接触,用于土壤的测定[35-36]。然而,使用按压的方式接触土壤样品时,可能因为操作者使用力度的不同会改变土壤层的紧实度,从而改变目标离子在土壤层(靠近DGT装置暴露面)的扩散速率,造成测定误差[37]。Ding等[37]利用人工污染土壤测试时,使用活塞式DGT装置获得磷、砷、镉、铅DGT浓度的平均误差(相对标准差)为5.57%。考虑到人工污染土壤降低了仪器的分析误差,对自然土壤的测定误差可能会增加。
1.2 双模式DGT装置
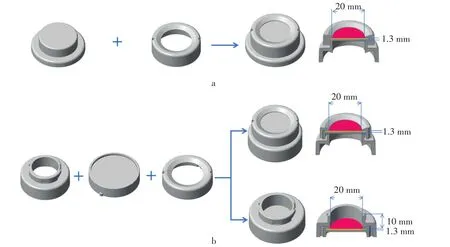
图2 活塞式DGT装置(a)和双模式DGT装置(b)(图片改自Ding等[37])Figure 2 Piston type DGT device(a)and Double mode DGT device(b)(the figures were modified according to Ding et al.[37])
Ding等[37]对传统的活塞式DGT进行了改进,以降低人为按压造成的测定误差。如图2b所示,双模式DGT主要由放置3层膜的DGT核心模块(DGT Core)、支撑核心的底座(Base)组成(参考www.easysensor.net)。双模式DGT有两种组装方式:一种是将DGT核心模块置于底座之上,形成传统的活塞式DGT,适用于水体和溶液中溶质的测定;另一种是将DGT核心模块镶嵌在底座下方的凹槽内,形成开放式内腔(Open Cavity);内腔的直径为20 mm,与活塞式装置暴露窗口的直径一致,高度为10 mm。土壤调节水分后,按其重力自然填满到内腔中。采用内腔式放置土壤的方式克服了活塞按压式的缺陷,包括:(1)土壤仅凭借其重力与DGT暴露面自然接触,避免按压产生的人为误差;(2)土壤层的厚度统一为10 mm,避免了土壤层厚度不统一产生的误差;(3)土壤与DGT暴露面的接触面积严格控制在3.14 cm2,避免土壤层侧向扩散对测定的干扰。Ding等[37]对比发现,采用内腔式方式放置土壤时,测定获得的磷、砷、镉、铅DGT浓度的平均误差仅为3.37%,比活塞式放置的误差降低42%。
1.3 平板式DGT装置
对于沉积物、湿地土壤等空间异质性大的环境介质,需采用平板型DGT装置获取目标物的垂向或者二维剖面的信息。如图3a所示,传统的平板式DGT装置由底板和盖板组成,固定膜、扩散膜和滤膜依次放置在底座上,并用盖板固定,形成暴露窗口的面积为150 mm×18 mm(长×宽)。该装置可以插入沉积物(柱样)中进行采样[38],也可以通过潜水员[39]或者DGT投放装置[17,40]在野外进行原位投放。传统的平板式DGT装置暴露面低于盖板形成的外围,这种结构使得底部形成横向凸起(图3a)。当DGT装置垂向插入时,会不同程度地造成沉积物剖面结构的变形,并且有可能造成:(1)沉积物界面固相颗粒物被带到下层。由于界面附近固相颗粒物的有机质含量高,界面颗粒物被带到下层后,将会造成生物地球化学过程与强度的变化;(2)上覆水通过缝隙向下引灌。当上覆水体含有氧气等电子受体时,其引灌将会氧化下层的沉积物,改变沉积物生物地球化学性质和营养盐、重金属的迁移活性;(3)由于剖面结构的变形,通过DGT获得的剖面信息存在不同程度的空间错位。如获取的空间分辨率要求很高时(如亚毫米级),这种错位造成的信息失真将会非常严重。
为克服传统平板式DGT装置的缺陷,Ding等[37]发展了新型平板式装置(图3b;参考www.easysensor.net),主要改进措施包括:(1)去掉了底部凸起结构,使暴露面至装置底部完全处于同一平面上;(2)装置底部的背面呈30度楔形结构,当装置插入时,这种结构可产生对暴露面的挤压力,确保装置暴露面与沉积物的紧密接触。此外,为便于和活塞式、双模式装置的参数进行统一(直径20 mm),改进后的DGT装置暴露窗口的宽度增加到20 mm。进一步对比发现,新型平板装置插入沉积物时,界面上溶解态和颗粒态硫化物(负载在沙粒上)在沉积物中的渗透深度仅是传统装置的33%和20%。当使用传统装置时,沉积物界面以下5 mm范围内出现硫的富集层,可能是沉积物界面上富含硫的动物粪便在装置插入时带到沉积物界面以下,粪便通过快速降解释放硫化物造成的。当使用新型平板装置时,硫的富集现象消失,说明传统装置插入造成的测定误差需要引起高度重视,同时凸显出新装置使用的优越性。
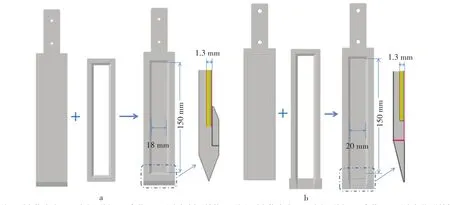
图3 传统平板式DGT装置(a)和新型平板式DGT装置(b)(图片改自Ding等[37])Figure 3 Traditional(a)and new(b)flat-type DGT devices(The figures were modified according to Ding et al.[37])
除上述两种研究者使用较多的平板型装置外,Docekal等[41]基于DET设计原理设计了限制型DGT探针装置,主要将DGT结合凝胶注入密集的细条型凹槽中,该设计主要是为了对DGT固定膜进行分割,以便准确获取沉积物剖面目标物的垂向分布信息。装置回收后,需要将每一凹槽中固定膜(凝胶)进行回收,操作较为繁琐,同时回收过程中凝胶可能存在一定程度的损失,产生分析误差。
1.4 液体结合相DGT装置
活塞式、双模式、平板式DGT装置的固定相均是凝胶。Li等[42]在2003年发展了一种以聚4-苯乙烯磺酸盐(PSS)溶液作为固定相的新型液体结合相DGT技术。如图4所示,液体固定相DGT装置由容纳固定相溶液的基底、硅胶垫片、渗析膜以及密封盖帽组成[43]。固定相液体填充到基底中,依次盖上硅胶垫片和渗析膜(该膜作为扩散层),将盖帽与基底固定,固定相溶液被密封于基底中。液体结合相DGT装置提供了聚合物溶液和扩散层之间的良好接触,克服了凝胶的易碎性和溶胀问题,并且固定相溶液可直接用于分析目标物含量,不需要洗脱步骤,简化了分析流程[44-46]。但是,由于液体的流动性,液体固定相DGT局限于水体的测定,目前难以获取沉积物/湿地土壤的剖面信息。此外,目标离子在透析膜中耐受的环境条件(如pH、离子强度)有限,限制了这类技术的应用范围。
2 DGT固定相和扩散相材料的发展
DGT由固定相和扩散相(扩散膜和滤膜)组成,固定相一般是由吸附材料嵌入凝胶中制成,其对目标离子的测定依赖于固定材料的类型。目前,多种类型的固定相应用于DGT的测定,包括单一固定材料(表1)、复合固定材料(表2)以及液相吸附材料(表3)。
2.1 单一固定材料

图4 液体结合相DGT装置Figure 4 The liquid binding phase DGT device
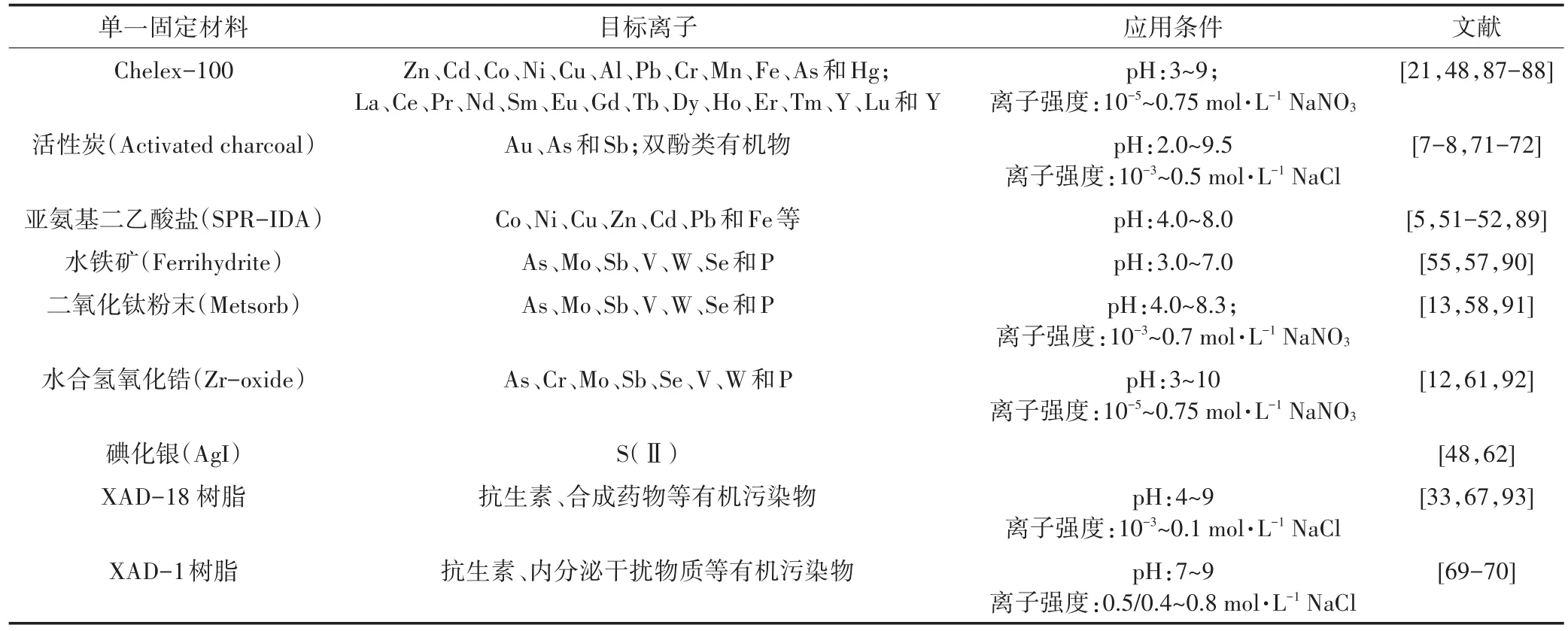
表1 DGT固定相使用的单一固定材料Table 1 Single binding materials for DGT use

表2 DGT固定相使用的复合固定材料Table 2 Mixed binding materials for DGT use
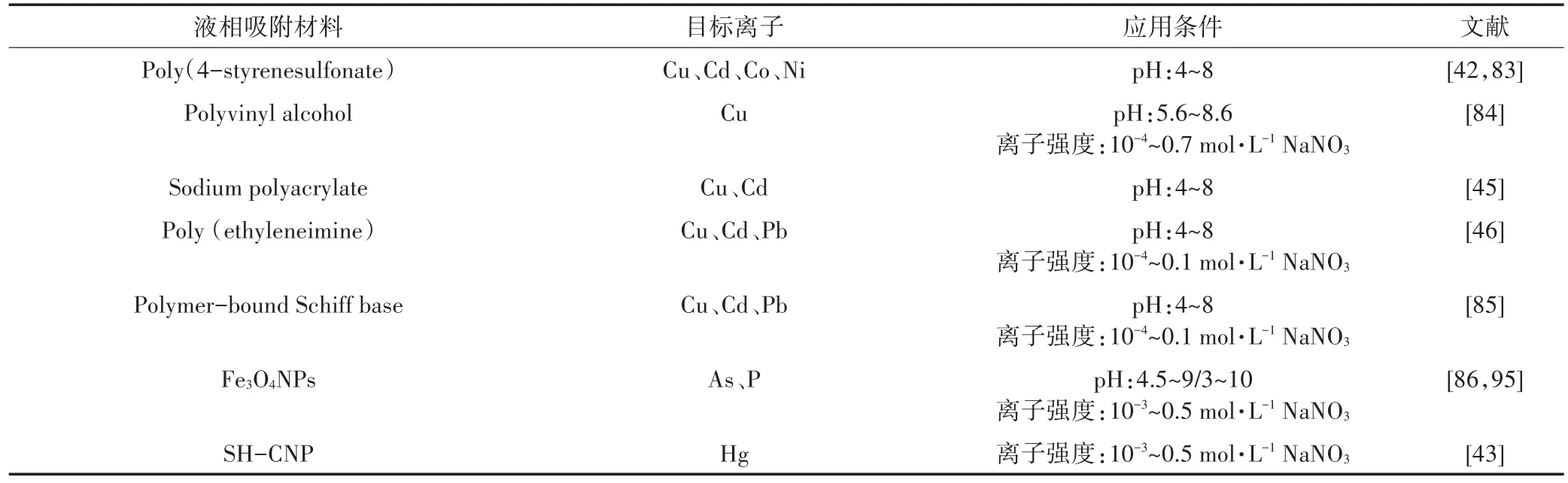
表3 DGT使用的液相固定材料Table 3 Liquid binding phase materials for DGT use
Chelex-100树脂是发展最为成熟的金属阳离子吸附材料,能够用于十几种金属阳离子的测定,例如Zn、Cd、Co、Ni、Cu、Al、Pb、Cr、Mn、Fe、As 和 Hg等[6,47-48]。Yuan 等[21]通过比较多种吸附材料,发现Chelex-100 DGT对15种稀土元素具有很高的吸收效率和环境抗干扰能力(pH 3~9,离子强度 3~100 mmol·L-1)。以活性炭作为固定相的DGT可以测定Au、As和Sb,并且对环境具有很强的耐受性(pH 2~9)[7-8]。此外,悬浮颗粒试剂——亚氨基二乙酸盐(SPR-IDA)可用于金属阳离子Co、Ni、Cu、Zn、Cd、Pb、Mn和Fe等的测量[49-51]。相比于粒径约为100 μm的Chelex-100树脂,SPR-IDA的粒径约为0.2 μm,可结合激光剥蚀-电感耦合等离子体质谱联用技术(LA-ICP-MS)获取土壤或者沉积物中金属离子的亚毫米级二维分布信息[52-54]。
除了金属阳离子之外,一些特异性吸附氧化性阴离子材料被应用于DGT的固定相。以水铁矿(Ferri⁃hydrite)作为固定剂的DGT(Fe-oxide DGT)技术最早被用于测定磷(PO3-4-P),并被拓展到As、Mo、Sb、V、W和Se的测定[55-56]。在20世纪90年代末至2010年期间,Fe-oxide DGT作为测定阴离子的经典技术,在拓展DGT应用功能方面发挥了重要作用[55,57]。然而,该技术有3个方面的不足:(1)容量较低,对P的DGT测定容量仅有2~7 μg·cm-2(包括沉淀型Fe-oxide DGT,简称为PF DGT),以常规的放置时间24 h计算,理论上Fe-oxide DGT只能满足最高浓度1.4 mg P·L-1的测定。在实际环境中,由于溶解态有机碳和竞争性离子的干扰,实际的DGT测定容量会进一步降低,因此该技术在应用到高磷含量的环境介质(如富营养化水体、施肥的土壤等)时,很可能因为超出DGT容量造成测定结果出现较大的偏差。通过在合成淡水和海水中的测试发现,Fe-oxide DGT不能有效测定Sb(Ⅴ)、Mo(Ⅵ)和W(Ⅵ)[13]。(2)非晶型的水铁矿寿命较短(小于40 d),在存放时间内将逐渐向针铁矿和赤铁矿转变,降低DGT的测定容量;(3)Fe-oxide DGT与还原性的环境介质(如沉积物)接触后,固定膜中的水铁矿有可能被还原,从而影响沉积物的生物地球化学过程,干扰铁和其他目标物(如氧化性阴离子)的测定。
另外一种发展较成熟的技术是Metsorb DGT(Metsorb是二氧化钛的商品名)。该技术可测定As、Mo、Sb、V、W、Se和P等多种氧化性阴离子[13,58]。Pan⁃ther等[59]和 Price等[60]详细比较了 Fe-oxide DGT和Metsorb DGT的性能,发现两者DGT测定容量的差异不大(Metsorb DGT对P的测定容量是12 μg·cm-2),但Metsorb对某些阴离子(如Sb)的亲和力比水铁矿强,因而适用的阴离子种类比Fe-oxide DGT多。在高pH值和高离子强度的海水中,竞争性阴离子对Metsorb DGT的干扰程度有所降低,仅发现Metsorb DGT不能测定Mo(Ⅴ)[13]。当使用Metsorb DGT测定多种阴离子时(如P和Sb),需要使用1 mol·L-1NaOH和1 mol·L-1NaOH-1 mol·L-1H2O2分别提取24 h(总计48 h),耗费时间较长,同时提取溶液中Na+的含量高,要对提取溶液稀释很大倍数才能避免Na+对ICP-MS测定的干扰。
Ding等[61]首次利用水合氢氧化锆(Zr-oxide)固定剂开发了Zr-oxide DGT,用于多种氧化性阴离子的测定[12]。作为Fe-oxide DGT、Metsorb DGT的相同类型技术,Zr-oxide DGT 具有明显的优势:(1)Zr-oxide DGT对P具有高的测定容量,在pH 4.2、pH 7.1和pH 9.2条件下测定容量分别为>330、130 μg·cm-2和 95 μg·cm-2,在pH中性条件下分别是泥浆型和沉淀型Fe-oxide DGT的65倍和19倍,是Metsorb DGT的11倍[16]。当同步测定As、Cr、Mo、Sb、Se、V、W和P等8种阴离子时,Zr-oxide DGT的容量分别是Mestorb DGT和Fe-oxide DGT的29~2397倍和7.5~232倍[12]。这一优势使得Zr-oxide DGT可以应用到目标物含量很高的环境介质中(如污染或富营养化的土壤和沉积物);(2)Zr-oxide固定剂对氧化性阴离子的亲和力强,因此对竞争性阴离子的抗干扰能力强,如测定P时对SO2-4的耐受浓度高于 16.2 mg·L-1,而 Metsorb DGT和Fe-oxide DGT(沉淀型)仅有5.4 mg·L-1和0.6 mg·L-1,因此Zr-oxide DGT显著提升了对海水中氧化性阴离子的监测能力[16]。(3)当同步测定As等8种阴离子时,Ding等[12]开发了 0.2 mol·L-1NaOH-0.5 mol·L-1H2O2一步提取方法,提取时间仅用3~5 h(Metsorb DGT需要48 h),且提取溶液中Na+含量大幅度降低(仅为Metsorb DGT的1/5),有利于ICP-MS对金属目标物的检出;(4)Zr-oxide对阴离子的吸附性能非常稳定,存放2 a后没有发现DGT测定容量有显著的降低,因此与Fe-oxide DGT相比优势明显。
此外,Teasdale等[62]在早期(1999年)利用AgI作为固定剂开发了DGT测定还原态硫S(Ⅱ)的技术。S(Ⅱ)与淡黄色的AgI发生特异性的沉淀反应,形成黑色的Ag2S物质,其积累量与固定膜表面的光密度(颜色)可以建立定量关系,因此可以结合计算机成像密度法(CID)获取S(Ⅱ)在环境中的二维分布信息[31,62-63]。Ding等[64-65]将磷钼蓝比色法与CID技术结合,将Zr-oxide DGT功能拓展到可以二维、高分辨(亚毫米分辨率)测定P。Yao等[66]基于Zr-oxide DGT,结合二苯基卡巴肼染色技术与CID技术进一步开发了Cr(Ⅵ)的二维高分辨率测定。
2012年以来,DGT技术开始拓展到有机污染物的测定。XAD-18树脂和XAD-1树脂是应用最广泛的吸附材料。Chen等[20]使用XAD-18树脂作为DGT固定相测量水中的磺胺甲唑抗生素,与高效液相色谱的测量结果具有很好的一致性。目前,XAD-18固定相的目标分析物已经拓展到几十种抗生素以及违禁药品等有机污染物[19,33,67-68]。XAD-18 树脂在较高离子强度下(>0.5 mol·L-1)具有较弱的吸附能力,难以应用于海水等高离子强度环境中[20,69]。Xie等[69-70]进一步将XAD-1树脂作为DGT的固定相,利用DGT在海水中测定了多种抗生素以及内分泌干扰物质。活性炭(Activated charcoal,AC)作为固定相除了能够测定Au、As以及Sb外[7-8],Zheng等[71]和Guan等[72]进一步将活性炭拓展到测定水体和土壤中的苯酚类有机物,对BPA、BPB和BPF的吸附容量分别能达到192、140、194 μg·凝胶盘-1。Guibal等[73]使用 Oasis®HLB和Oasis®MAX作为DGT固定相测定水环境中的4种阴离子农药,经实验验证在pH 3~8以及0.01~1 mol·L-1的离子强度下具有较高的测量精度。
2.2 复合固定材料
当测定不同类型目标物时,需要同时使用几种单一固定材料的DGT装置。对于沉积物、根际土壤等空间异质性大的环境介质,通过几种DGT装置测定不同类型目标物时存在空间错位,从而在对研究多种目标物的耦合关系时形成较大的障碍。因此,采用多种固定材料配制复合型DGT固定相,利用复合DGT在同一时空位置和尺度上同步获取多种目标物的信息,是DGT技术发展的重要方向。
2005年,Mason等[74]首次使用Fe-oxide和Chelex-100树脂作为DGT吸附材料制备复合固定膜,用于同时测定 5种痕量金属(Cd、Cu、Mn、Mo和 Zn)和 P。Huynh等[75]将其拓展到As、Cd、Cu、Pb和Zn的同步测定,并成功应用到水体和土壤中。Panther等[76]以Che⁃lex-100和Metsorb为吸附材料制备了Chelex-Metsorb复合固定相,开发了能够同步测定6种痕量金属(Mn、Co、Ni、Cu、Cd和Pb)和6种氧化性阴离子(V、As、Mo、Sb、W和P)的DGT技术。并且Chelex-Metsorb DGT在pH 5.03~8.05和离子强度0.001~0.7 mol·L-1下能够保持良好的性能。相比于Fe-oxide和Chelex-100复合固定相,Chelex-Metsorb复合固定相具有明显的优势,首先Metsorb和Chelex-100可通过商业途径获取,不需要单独制备;其次,Chelex-Metsorb能够测定Fe,同时对淡水和海水中一些氧化性阴离子的测定拥有更高的精度[76]。然而,包括Chelex-Metsorb DGT在内,能够测定的目标物元素最多只有12种,且由于使用了Ferrihydrite、Metsorb等固定剂,存在DGT容量低、测定时间过长等不足。
Xu等[77]使用Zr-oxide和Chelex-100树脂制备了ZrO-Chelex复合固定膜,实现了P和Fe(Ⅱ)的同步测定。该技术对P和Fe(Ⅱ)的测定容量分别是90 μg·cm-2和75 μg·cm-2。在此基础上,Wang等[78-79]将ZrOChelex DGT拓展到同步测定8种金属阳离子(Fe、Mn、Co、Ni、Cu、Zn、Pb和Cd)和8种氧化性阴离子(P、As、Cr、Mo、Sb、Se、V和W)。通过优化配制方法,增加Zroxide和Chelex-100的配制量,最终定型的ZrO-Chel⁃ex DGT对P的测定容量达到130 μg·cm-2,远高于其他类型的单一和复合DGT(≤12 μg·cm-2);对Fe(Ⅱ)和 Cd(Ⅱ)的测定容量达到 100 μg·cm-2和 301 μg·cm-2,是经典型 Chelex DGT(45 μg Fe·cm-2;DGT Re⁃search Ltd.提供)的2.2倍和1.2倍。由于容量的提高,ZrO-Chelex DGT对环境条件的耐受能力显著优于其他复合DGT。此外,采用两步提取方法,即分别用1.0 mol·L-1HNO3和 0.2 mol·L-1NaOH-0.5 mol·L-1H2O2溶液提取阳离子和阴离子,所用时间控制在24 h内,少于Chelex-Metsorb DGT方法的48 h(不包括Sb分析)和60 h(包括Sb分析)[76]。Wang等[121]进一步以Zr-oxide、Chelex-100树脂和AgI为吸附材料制备了ZrO-CA DGT,用于同时测定S(Ⅱ)、8种金属阳离子以及8种氧化性阴离子。相比于ZrO-Chelex DGT,ZrO-CA DGT对氧化性阴离子表现出更快的吸收速率,并且当ZrO-CA DGT对S(Ⅱ)吸附饱和时,对金属阳离子表现出更快的吸收速率。
与此同时,Ding等[64]利用Zr-oxide和AgI作为固定剂,开发了ZrO-AgI DGT复合技术,用于同步测定P和S(Ⅱ)。将该技术与二维切片-微量比色方法、CID结合,可以用于获取沉积物等环境介质中P和S(Ⅱ)的二维分布信息。利用该技术测定了太湖沉积物剖面P和S(Ⅱ)的分布,首次观察到两者同步释放的新现象。Xu等[80]使用ZrO-AgI DGT研究了As和S(Ⅱ)在沉积物中的释放规律,也观察到两者同步释放的现象。Kreuzeder等[81]利用Zr-oxide和SPR-IDA作为固定剂,研发了一种复合型DGT。将该技术与LA-ICP-MS结合,可用于高分辨、二维获取P、As、Co、Cu、Mn和Zn的分布信息。
2.3 液相固定材料
液体结合相DGT的固定相是聚合物溶液,将吸附剂或具有吸附性能的纳米颗粒物溶于水溶液中制备而成。
Li等[42]第一次将聚4-苯乙烯磺酸盐[Poly(4-sty⁃renesulfonate),PSS]溶液作为DGT的固定相,用于测定水体中的Cu和Cd[82]。Chen等[83]将PSS DGT的目标物扩展到同步测定4种金属离子(Cu、Cd、Co和Ni)。Fan等[84]使用聚乙烯醇(Polyvinyl alcohol,PVA)溶液作为液体结合相测量环境中的Cu;使用聚丙烯酸钠(Sodium polyacrylate,PA)溶液测量水中的Cu和Cd,与火焰原子吸收光谱法(FAAS)测定的结果具有很好的一致性[45]。Sui等[46]使用聚乙烯亚胺[Poly(ethyle⁃neimine),PEI)]溶液作为固定相测定了水中Cu、Cd和Pb。Fan等[85]进一步通过将2-吡啶甲醛(2-pyridine⁃carboxaldehyde,Py)和聚乙烯亚胺缩合制备聚合物结合的席夫碱(Py-PEI)来测定有效态的Cu、Cd和Pb,并且经测试,Py-PEI的吸附容量均高于PA DGT、PSS DGT以及PEI DGT。
近几年,纳米颗粒材料也已经应用于液体固定相。相比聚合物溶液,均匀悬浮溶液中的纳米颗粒材料具有大的表面积、丰富的官能团以及高的移动性,非常适用于DGT的液体固定相。Fe3O4纳米颗粒(Fe3O4NPs)悬浮溶液已经用于测定As和P,稳定性(>24个月)、对P的吸附容量(15.4 mgP·cm-2)以及抗干扰能力(pH 3~10)均高于Ferrihydrite和Metsorb固定相[86]。Wu等[43]研发了巯基修饰的碳纳米颗粒物(SH-CNP)悬浮溶液作为DGT的液体固定相吸附Hg离子,并且该固定相不受Cd、Cr、Cu和Pb等潜在干扰离子的影响,具有高的特异性。
2.4 扩散相材料的发展
与固定相类似,扩散相是DGT技术的基本构成部分。由公式(3)可知,扩散层的厚度和目标离子在扩散层中的扩散系数是DGT定量计算的基础。因此,扩散层厚度和扩散性能参数是否稳定,对于控制DGT的测定误差至关重要。
目前,通过凝胶制备的DGT扩散膜已被广泛应用,主要有两种类型:一是琼脂糖交联的聚丙烯酰胺(APA)水凝胶;二是琼脂糖凝胶(浓度一般为1.5%)。APA凝胶是一种经典的DGT扩散膜,由丙烯酰胺和琼脂糖交联剂制备成水凝胶,然后加入过硫酸铵引发剂和TEMED催化剂制备而成;该凝胶具有>5 nm的孔径,水合后膨胀3.2倍,含水率>95%,并在pH 2~9范围内保持厚度稳定[4,79]。APA适用于环境中多种阴阳离子的测定,且已被广泛应用[22,60]。APA对痕量金属离子(尤其是Cu)及其富里酸络合物有特异性、低容量的吸附,同时存在静电作用[96]。当溶液离子强度低于1 mmol·L-1时,这些作用会干扰DGT的吸收,延迟扩散梯度的建立[97]。因此,APA扩散膜组装的DGT装置要求在离子强度高于1 mmol·L-1的环境中使用。由于APA凝胶中的酰胺等基团会与一些目标离子结合,因此 APA 凝胶不能用于汞[9,98-99]、铵[18]以及有机污染物(抗生素、内分泌干扰物等)[19,72,100]的测定。值得注意的是,同一目标物在APA扩散膜中的扩散系数报道有比较大的差异,通过扩散杯测定的误差(相对标准偏差)在6.49%~20.71%之间(表4),通过DGT法测定得到的误差在6.23%~16.36%(表5)。考虑到其他误差(如操作差异性以及扩散层厚度、提取率、目标物分析误差等),DGT的整体分析误差将会被进一步放大。
琼脂糖凝胶是将琼脂糖溶于热水中制备而成,制作步骤简单,水合后不发生膨胀。相比于APA凝胶,琼脂糖凝胶具有更大的孔径(>20 nm),较低的弯曲度以及更高的含水率(>99%),有利于目标离子的扩散。琼脂糖分子中带有巯基基团,与痕量金属离子会发生微弱的络合作用;琼脂糖分子中主要的结合位点来自带负电荷的pyruvate基团,通过形成Donnan势与阴离子和阳离子分别产生排斥和吸附作用。当离子强度升高时,特异性和静电结合的作用会减弱消失[101-102]。Wang等[79]系统研究了琼脂糖扩散膜厚度的稳定性和对阴阳离子的扩散性能,发现在pH 2~11,离子强度0~1.0 mol·L-1,温度4~40 ℃以及储存300 d等条件下,琼脂糖的厚度变化均控制在0.7%以内(RSD%)[72],因此厚度非常稳定;当溶液中离子强度高于1 mmol·L-1和2~3 mmol·L-1时,琼脂糖对阳离子和阴离子的特异性或静电作用消失,因此琼脂糖扩散膜对阴离子和阳离子的测定需要在离子强度高于1 mmol·L-1和2~3mmol·L-1的条件下进行,与APA扩散膜的适用条件(1 mmol·L-1)基本一致。利用改进型Chelex DGT和Zr-oxide DGT获得16种阴阳离子在琼脂糖扩散膜中的扩散系数(表6),其平均值是APA扩散膜的1.10倍,说明阴阳离子在琼脂糖扩散膜中的扩散系数略高于APA扩散膜中的扩散系数。值得一提的是,利用Chelex DGT获得的扩散系数适用于ZrO-Chelex DGT的测定,说明琼脂糖扩散膜的扩散性能稳定。Wang等[79]发现,将不同类型滤膜与琼脂糖扩散膜组合,利用DGT测定得到Cu、Cd、As的扩散系数存在显著差异,说明在应用层面,DGT装置使用的滤膜类型和型号应该固定和统一。目前,DGT主要使用的滤膜包括Durapore®聚偏氟乙烯(PVDF)滤膜(孔径0.45 μm,厚度 100 μm,Millipore)、PES(孔径 0.45 μm,厚度 140 μm,Supor 450)和硝酸纤维素膜(孔径0.45 μm,厚度130 μm)。利用琼脂糖扩散膜组装的DGT已被用于测定多种阴离子和阳离子[78-79]、有机物金属离子[10-11]、NH+4[18]、汞[103-104]以及多种有机污染物[67,93],已经成为除APA外另一种被广泛用于DGT测试和应用的标准扩散膜。
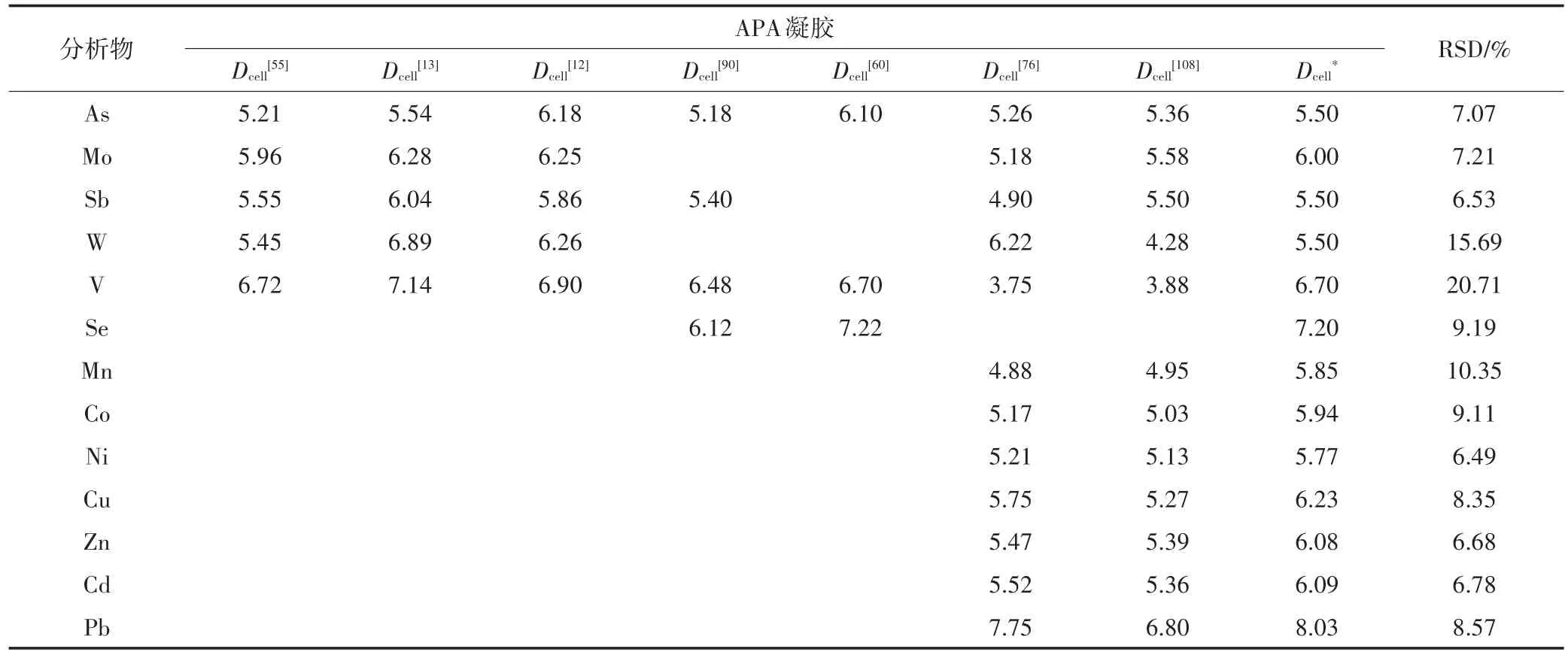
表4 使用扩散杯法得到的阴阳离子在APA扩散膜中的扩散系数(Dcell,×10-6cm2·s-1,25℃)Table 4 Diffusion coefficients of anions and cations in APA gel(Dcell,×10-6cm2·s-1,25 ℃)
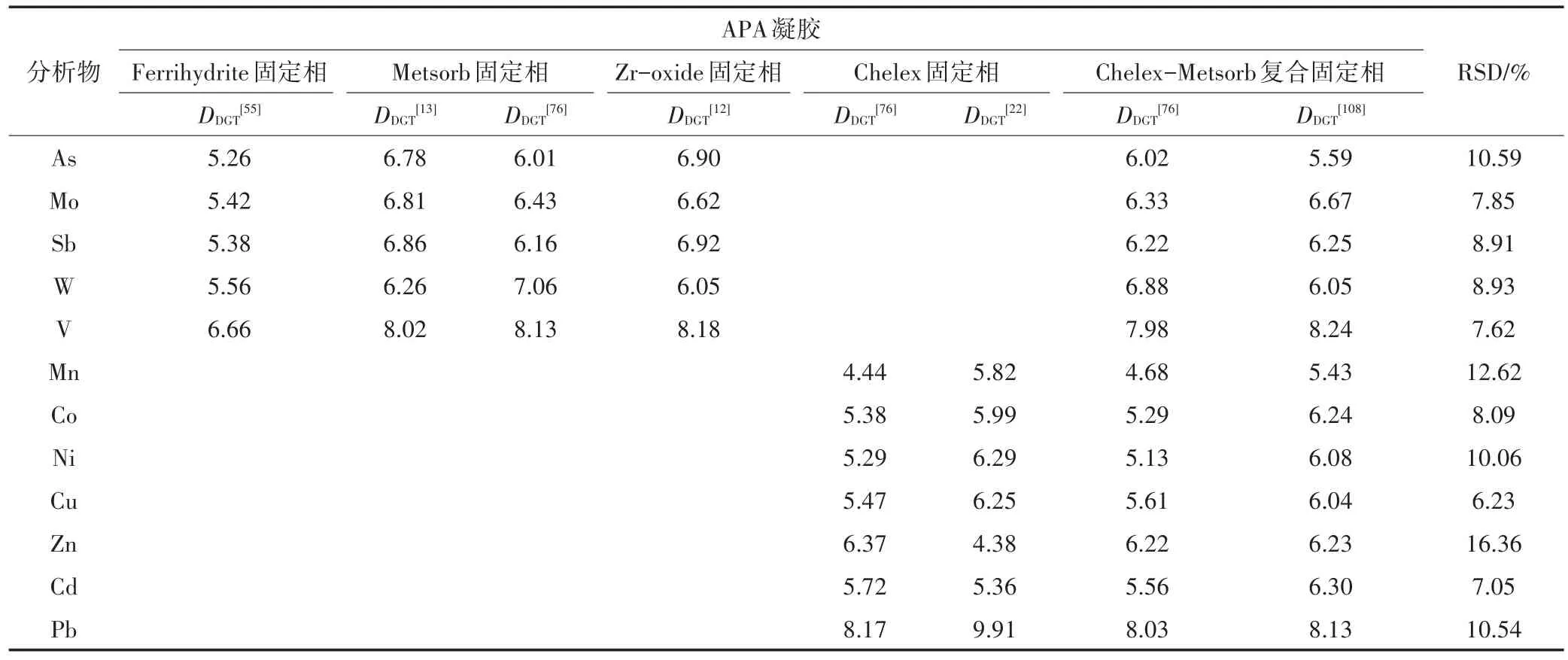
表5 使用不同固定相组装的DGT装置测得阴阳离子在APA扩散膜中的扩散系数(DDGT,×10-6cm2·s-1,25℃)Table 5 Diffusion coefficients of anions and cations in APA gel using different binding phase(DDGT,×10-6cm2·s-1,25 ℃)
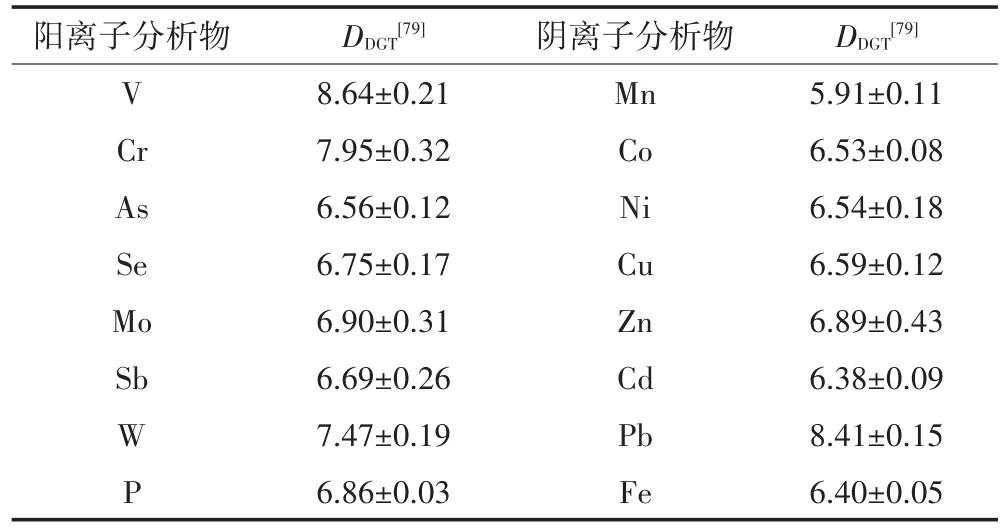
表6 使用DGT装置测得的阴阳离子在琼脂糖扩散膜中的扩散系数(DDGT,×10-6cm2·s-1,25 ℃)Table6 Diffusioncoefficientsofanionsandcationsinagarose diffusiongeldetectedusingDGTmethod(DDGT,×10-6cm2·s-1,25 ℃)
DGT获取空间信息的分辨率与扩散层厚度有关。当目标离子通过扩散层时,离子不仅向固定相方向发生垂直扩散,同时发生侧向扩散,造成空间分辨率的降低。当使用标准的DGT装置时,扩散层的厚度约为0.90 mm,所获得的目标物空间分辨率在1.0 mm左右[48,105]。因此,为了获得亚毫米(0.1~0.5 mm)信息,需要将扩散层厚度降低到0.5 mm以内,由此促进了超薄扩散相在DGT技术领域的应用。Lehto等[53]使用0.01 mm厚度的Nuclepore膜组装DGT,用于获取金属离子在土壤和沉积物中的二维分布;Ding等[106]直接使用0.10 mm厚度的Durapore®PVDF膜获取了Fe和P在沉积物中的二维分布信息。在使用超薄扩散膜时,利用公式(3)计算得到的目标物DGT浓度要远小于孔隙水中的溶解态浓度。这是因为扩散层变薄后,DGT的吸收通量会大幅加快,造成DGT装置表面目标离子的溶解态浓度快速衰减。由于DGT浓度与孔隙水溶解态浓度两者之间缺乏可比性,使用超薄扩散膜时DGT测定结果通常用扩散通量表示[公式(1)][106-107]。
3 DGT的测定
3.1 DGT在旱作土壤中的测定
DGT在旱作土壤中的测定流程主要包括7个步骤(图5):(1)土壤研磨过2 mm筛;(2)测定土壤最大田间持水量;(3)根据最大田间持水量加入去离子水,调节土壤含水率;(4)手工或者机械搅拌土壤样品;(5)DGT装置与土壤样品接触,通常放置24 h;(6)取出DGT装置的固定膜,提取并测定固定膜上的目标物积累量;(7)根据DGT方程计算目标物的含量(具体操作及测定流程参考www.easysensor.net)。
根据DGT装置构型的不同,DGT装置与土壤样品接触的方式有两种:一种是将土壤加去离子水湿润后,将活塞式DGT暴露面按压在土壤表面进行测定;另一种是将土壤湿润后,将湿润的土壤填充至双模式DGT装置的内腔中(内腔式)进行测定。目前,DGT测定使用的土壤含水率还没有统一的标准。Zhang等[109]用去离子水调节土壤的最大田间持水量至100%,并在室温下平衡24 h后进行测量;Luo等[36]和Guan等[110]分别将干燥土壤的最大田间持水量调节至60%和50%培养48 h后,再将土壤含水率调节至80%和90%,平衡24 h后进行测量。Kalkhajeh等[111]将土壤的最大田间持水量调节至50%培养48 h后,再调节至100%,平衡24 h后进行测定。值得注意的是,土壤含水率过高,可能导致土壤缺氧,影响目标离子的形态和移动性,造成DGT测定结果与实际情况有差异。Zhang等[112]为使得DGT测量结果与实际情况接近,将土壤含水率调节到最大田间持水量的70%,采用“内腔式”方式放置土壤,可使得多数土壤样品能够与DGT膜心的暴露面紧密接触,装置在恒温下放置48 h后进行测定,所用时间比其他研究者缩短24 h。在加入去离子水后,传统上使用玻璃棒来调节土壤含水率,这种方式耗费人力,同时效率低,不适用大批量样品的处理;建议使用电动非金属搅拌器进行混匀(参考www.easysensor.net),可以极大地节省人力,提高处理样品的效率。

图5 活塞型与内腔式DGT的操作流程(参考www.easysensor.net)Figure 5 Operation step for the piston-type and open cavity-type DGTs(www.easysensor.net)

图6 平板型DGT的操作流程(参考www.easysensor.net)Figure 6 Operation details for the flat-type DGT(www.easysensor.net)
3.2 DGT在沉积物/湿地土壤中的测定
对沉积物、湿地土壤的测定,主要使用平板式DGT装置,主要流程(图6)包括:(1)DGT装置组装、充氮去氧后,放置在0.01 mol·L-1NaCl溶液中;(2)将DGT装置手工插入或者现场投放到沉积物中,暴露面保留2~4 cm在上覆水体中,放置一段时间(一般24 h);(3)取出DGT装置,清洗装置表面,将固定膜取出后,密封保存;(4)对固定膜进行切片,测定固定膜切片上目标物的积累量;(5)根据DGT方程计算目标物的含量或者通量(参考www.easysensor.net)。
目前,有两点原因限制了DGT在现场的应用:一是DGT装置现场投放缺乏可靠的方法,人工潜水成本高,同时不适合大范围的应用;二是现场识别沉积物-水界面的难度非常大,在装置回收的过程中,水流会冲刷附着在DGT装置滤膜上的沉积物颗粒,使对沉积物-水界面位置的判断十分困难。为克服这些困难,Ding等[17]开发了一种重力投放装置,适合水深在10 m以内的DGT装置的投放。同时,为解决沉积物-水界面精确识别的问题,Ding等[40]开发了一种沉积物-水界面标识装置,通过后盖板将海绵固定在DGT平板装置的背面,同时加载可以覆盖DGT装置的塑料膜。将DGT装置插入沉积物时,沉积物颗粒将渗透进入海绵孔洞中,从而保留沉积物的深度信息;当DGT装置从沉积物中取出时,塑料薄膜立即覆盖装置的暴露面和背面,保护渗入海绵孔洞中的沉积物颗粒不被水流冲刷,从而使得沉积物-水界面位置得到保存。
与土壤测定相比,对沉积物/湿地土壤DGT测定的操作更为复杂,不仅体现在DGT装置的投放环节,同时在DGT样品的处理环节也存在很大的难度。通常使用平板型DGT装置的目的是为了获取目标物在沉积物中的垂向分布信息,当空间分辨率提高到毫米级时,一是对固定膜的切片要求非常高,二是将产生大量的切片样品(当分辨率为1 mm时,单个DGT装置将产生150个样品),且通常每个切片产生的提取溶液体积很少(数百微升),因此如何实现微量体积样品的大批量测定,是面临的技术难题。
对于固定膜的切片,一般使用单个特氟龙涂层剃刀对固定膜垂向方向依次进行切割,必要情况下需要通过称重标定固定膜切片的宽度[47]。该方法处理样品的效率低,且使用金属剃须刀片时,容易造成铁等金属对固定膜样品的污染。此外,Gao等[48,113]使用有机玻璃凝胶切割机对固定膜进行切割,切片宽度精确但费用较高。为克服上述缺陷,Ding等[106]开发了陶瓷排刀,由厚度为1.0 mm的陶瓷刀片叠加组装形成,通过调节相邻陶瓷刀片的间隔,可以将切片的分辨率设在1.0~5.0 mm之间(参考www.easysensor.net)。将固定膜整张平铺到陶瓷排刀上,沿垂向方向依次按压固定膜,即可将整张固定膜按照既定的分辨率快速进行切片。该方法与传统方法相比,切片效率和准确度有了极大提高;由于刀片是用陶瓷材料制作而成,切片时不会产生任何金属污染[12,106]。
固定膜切片后,通常需要对每个切片的目标物进行提取分析。为解决微量提取液样品的大批量分析难题,Ding等[65]改进了微孔板分光光度法,可以一次性实现96个或者384个样品的测定,测定时间仅为1 min左右,所需的样品体积可以低至10~200 μL。该方法可以测定Fe、P,同时可以拓展硝酸根、硫化物等常规的离子。与传统的分光光度法相比,该方法测定样品的效率有了极大提高。
此外,将Zr-oxide固定膜着色与电脑密度成像计量(CID)技术结合,可以利用DGT实现P的二维高分辨测定[17]。Zr-oxide固定膜着色的原理与溶液中磷钼蓝反应原理一致,在Zr-oxide膜表面直接生成蓝色络合物,事先将扫描获得的灰度值与单位膜面积P的累积量建立校正曲线,利用校正曲线将Zr-oxide固定膜表面的灰度转换成积累量,从而实现沉积物/湿地中有效P亚毫米分布信息的大批量获取。该技术已被大量应用到沉积物和湿地土壤 P 的研究[40,106,114-115]。
3.3 DGT在水体中的测定
当DGT装置放置在水中时,水溶液会附着在滤膜的表面形成扩散边界层,从而影响溶质的扩散速率[57]。一般使用不同厚度的扩散膜组装的DGT放置于水体中,通过公式(5)推导扩散边界层的厚度(δ),并进一步获得 DGT 浓度[4,116]:
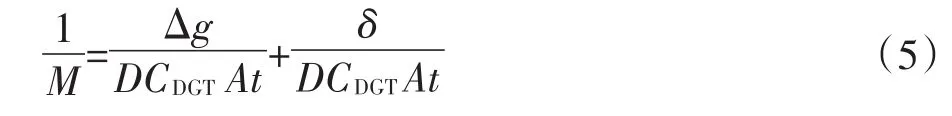
式中:M是DGT吸附的目标离子的总量;D是目标离子在扩散层的扩散系数;A是DGT暴露窗口的面积;Δg是扩散层的厚度;t是DGT的放置时间;CDGT是DGT测得的浓度。
Davison和Zhang[117]总结了不同水环境条件下扩散边界层的厚度:在充分搅拌的溶液中约为0.2 mm,在快速流动的水体中约为0.26 mm;在缓流水体中厚度会增加,例如在湖泊中约为0.31 mm,在停滞的池塘中约为0.39 mm。Huang等[118]最近发现,在一些池塘和湿地水体中,扩散边界层的厚度甚至与标准DGT扩散层的厚度(0.9 mm)相当。然而,许多研究忽视了扩散边界层的存在,导致使用DGT对水体目标物浓度的测定存在较大的不确定性。另外,DGT装置在水体中的放置时间一般要一周以上,当时间过长时,DGT滤膜表面将着生生物膜,影响目标物向DGT装置内部的扩散。Feng等[119]发现磷酸根的扩散系数随着生物膜厚度的增加而降低。有研究者采用了一些措施用于消除生物膜的影响,如校正扩散系数、使用聚碳酸酯膜、对滤膜进行预处理等,其实际效果需要做进一步验证[32,119-120]。
4 展望
与传统的测定技术相比,DGT技术能够在原位(原状)条件下较为真实地反映环境介质中目标物的可移动性和生物可利用性,从而能够更加准确地反映环境介质的营养或污染水平。DGT的富集过程可以在一定程度上模拟目标物在环境中的固-液交换动力学与土壤-根系动力学吸收过程,分析结果更加科学可靠,而这一特点正是传统有效态测定方法所欠缺的。DGT测定流程较为简单,操作环境要求低,具备较强的推广性,未来有替代传统分析方法的潜力。从技术发展层面,以下几个方面将可能成为主要发展方向:
(1)研发新型固定相,将DGT技术的测定功能拓展到更多类型的目标物,始终是DGT技术发展的主要方向。目前,部分研究者的兴趣已经从无机转移到有机化合物。
(2)近年来,复合固定相的发展使得对环境中多种元素耦合关系的研究成为可能。因此,使用复合固定相同步测定多种类型的目标物仍然是DGT发展的主要方向。与单一固定相相比,新型复合固定相的发展需要克服不同固定剂之间的干扰,同时分析流程应尽可能简化。
(3)结合分子印迹等技术,针对某一目标物发展高选择性的DGT测定技术。在该领域,重点是要研发有高选择性的固定相,将该类型DGT与普适性DGT结合,可以实现某一目标物形态和价态的区分。
(4)DGT具有空间高分辨分析的功能,一般采用SPR-IDA固定相和LA ICP-MS分析得到,但高成本制约了其应用。CID技术的发展极大地促进了DGT对磷、硫的测定应用,未来需要发展更多低成本、可替代的技术,包括固定相和高分辨分析技术。另外,DGT高分辨分析需要采用超薄扩散层,其测定值(通量)不能反映目标物在环境介质中的实际含量,需要拓展其测定结果的物理意义。

