乙酰氨基阿维菌素原位凝胶注射剂中乙酰氨基阿维菌素含量的HPLC测定
张振东,杨亚军,刘希望,马 宁,申栋帅,李剑勇
(中国农业科学院兰州畜牧与兽药研究所/农业部兽用药物创制重点实验室/甘肃省新兽药工程重点实验室,甘肃兰州 730050)
乙酰氨基阿维菌素是由默克公司1997年开发出的大环内酯类体内外杀虫剂,是一种高效、广谱、低残留的兽用新一代抗寄生虫药物[1-3]。乙酰氨基阿维菌素具有广谱、高效、用量小和安全程度高等优点,对线虫、昆虫及螨虫均具有高效杀灭作用[4]。目前,国内商品化的制剂只有1% EPR注射液,其作为国家二类新兽药由河北威远动物药业有限公司等注册生产[5]。临床主要应用于奶牛、肉牛等动物,在羊、猪、兔等其他动物上进行的试验也取得了较好的治疗效果[6-7]。但EPR注射液皮下注射给药,生物利用度低、药效维持时间短,从而给临床治疗效果带来严重影响。因此,提高生物利用度和延长有效血药浓度的EPR新剂型开发成为近年来国内外防治寄生虫病的研究热点[8]。本团队开发了一种EPR原位凝胶注射剂,拟用于奶牛、肉牛寄生虫病的治疗。本试验在前期研究的基础上,采用一种快速简便、专属性强、灵敏度高、重复性好的高效液相色谱法测定EPR原位凝胶注射剂中有效成分EPR的含量,可用于EPR原位凝胶注射剂的质量控制[9],旨在为该原位凝胶注射剂的进一步应用提供检测方法。
1 材料与方法
1.1 材料
1.1.1 药物 乙酰氨基阿维菌素对照品(B1a含量为95.4%,B1b含量为2.37%,批号K0471411),中国兽医药品监察所产品;EPR原位凝胶注射剂3批(批号170816、170919、171016),由中国农业科学院兰州畜牧与兽药研究所兽药研究室研制。
1.1.2 主要仪器 Agilent-LC 1290Ⅱ高效液相色谱仪(G7120A泵,G7114B紫外检测器,OpenLAB CDS中文色谱工作站),美国安捷伦科技有限公司产品;CPA224S电子天平,德国赛多利斯公司产品;优普超纯水机,四川优普超纯科技有限公司产品。
1.1.3 主要试剂 乙睛,甲醇(色谱纯),赛默飞世尔科技(中国)有限公司产品;水为超纯水,其余试剂均为分析纯。
1.2 方法
1.2.1 液相色谱条件 色谱柱:ZORBAX Eclipse Plus C18柱(2.1 mm×50 mm,1.8 μm);流动相:乙腈∶水∶甲酸(60 mL∶40 mL∶0.04 mL);流速:0.4 mL/min;紫外检测波长:245 nm;柱温:35℃,进样量:2 μL。
1.2.2 对照品溶液的制备 精密称取乙酰氨基阿维菌素标准品102 mg,加无水乙醇定容至100 mL,得浓度为1.02 mg/mL的标准品储备液。使用前用流动相稀释成系列浓度的标准品工作液。
1.2.3 供试品溶液的制备 EPR原位凝胶注射剂摇匀,用移液管精确量取1 mL,置50 mL容量瓶中,用无水乙醇25 mL,分5次洗涤移液管内壁,洗液并入容量瓶中,摇匀,置水浴中超声10 min,加无水乙醇缓慢稀释至刻度,摇匀。精确量取1 mL,置10 mL容量瓶中,加无水乙醇稀释至刻度,摇匀,即得供试品溶液。
1.2.4 标准曲线的绘制 精确量取标准品储备液适量加到流动相中,得浓度分别为200、100、50、25、12.5、6.25、3.125、1.562 5 μg/mL的对照品溶液,各取2 μL进样测定,以峰面积(y)对EPR浓度(x)进行线性回归,并绘制标准曲线。
1.2.5 精密度试验 取EPR对照品溶液,连续重复进样6次,进样量2 μL,依法测定峰面积,观察其峰面积测量值的相对标准偏差。
1.2.6 稳定性试验 分别在供试品溶液制备0、4、8、12、24 h后,精确量取2 μL,依法测定峰面积,考察其稳定性[10-11]。
1.2.7 重复性试验 取同一批次EPR原位凝胶注射剂6份,按照1.2.3中的方法制备供试品溶液,并进样测定峰面积,计算其RSD。
1.2.8 加样回收率试验 精确取EPR对照品和辅料适量,按处方制成EPR原位凝胶注射剂的样品,然后制备高、中、低3种浓度共9份供试品溶液,测定EPR的含量,与加入值进行比较,计算回收率。
1.2.9 样品含量测定 取不同批次的样品制成供试品溶液,分别精确量取2 μL,依法测定。
1.2.10 专属性试验 按处方比例精确称取EPR
原位凝胶注射剂中除EPR原料药外的其他成分,同EPR原位凝胶注射剂工艺制备,再按供试品溶液的制备方法处理,即获得阴性样品溶液。分别精密吸取乙酰氨基阿维菌素对照品溶液、供试品溶液及阴性样品溶液各2 μL,按1.2.1中的色谱条件,注入高效液相色谱仪,记录色谱图。
2 结果
2.1 EPR含量测定的标准曲线
以峰面积(y)对EPR浓度(x)进行线性回归,回归方程为y=10 830x+6 492.8,r=0.999 8,进样量在1.562 5 μg/mL~200 μg/mL范围内线性关系良好(图1和表1)。

图1 乙酰氨基阿维菌素标准曲线

序号 №123456789进样量/μg Injection volume11.562 53.1256.2512.52550100200峰面积/(mAU·s-1) Peak area11 09321 09639 81274 689149 003283 500557 1491 068 5652 179 571
2.2 精密度测定
EPR峰面积RSD为1.48%(n=6),表明仪器精密度符合要求。
2.3 稳定性测定
测定液室温放置24 h,与零时比较含量无显著变化,EPR峰面积RSD为0.26%,表明样品溶液在本试验条件下,至少可以稳定24 h。
2.4 重复性试验
重复性试验结果见表2。EPR含量的RSD为0.48%,说明此方法重复性良好。
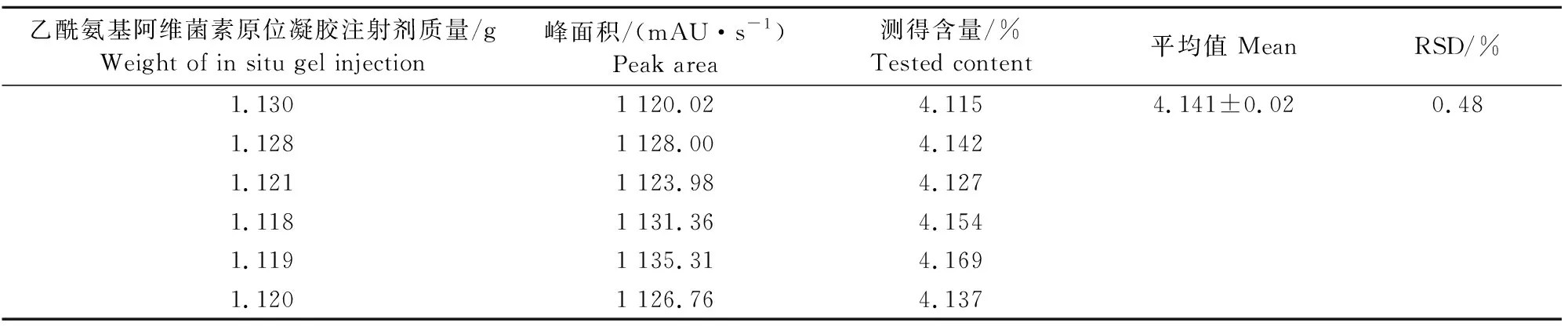
表2 乙酰氨基阿维菌素原位凝胶注射剂中乙酰氨基阿维菌素的重复性试验测定结果
2.5 加样回收率测定
加样回收率试验结果见表3,平均回收率为99.61%,RSD为0.47%(n=9),说明本试验的准确性高。
2.6 样品含量测定
3批次EPR原位凝胶注射剂含量测定结果见表4,测得EPR原位凝胶注射剂的平均含量为5.118%,RSD为0.23%,说明该测定方法准确、可靠,可用于EPR原位凝胶注射剂中EPR含量的测定。
2.7 专属性试验
阴性样品溶液、对照品溶液和供试品溶液的色谱图见图2,EPR分离度良好,峰形尖锐,保留时间5.1~5.2 min,阴性样品溶液和供试品溶液中的其他组分对EPR的测定无干扰,方法专属性良好。

表3 乙酰氨基阿维菌素原位凝胶注射剂中乙酰氨基阿维菌素的加样回收率测定结果

表4 乙酰氨基阿维菌素原位凝胶注射剂中乙酰氨基阿维菌素含量的测定结果
3 讨论
EPR标准品溶液经紫外可见分光光度计扫描,在240 nm~250 nm的波长处有吸收峰[12]。最初选择242 nm作为检测波长,在色谱条件优化时发现,当选择245 nm作为检测波长时,检测的灵敏度显著提高,故最终将检测波长定为245 nm。为避免EPR和注射剂中辅料的色谱行为相互干扰,筛选了甲醇-水、乙腈-水、丙二醇-水等流动相[13-15],并根据色谱分离效果调整流动相组分的体积比,最终确定流动相为乙腈∶水∶甲酸(60 mL∶40 mL∶0.04 mL)。在此色谱条件下,EPR与杂质分离效果良好,回收率、精密度、稳定性等试验结果进一步验证了试验所建立的方法专属性良好。本研究采用HPLC-外标法测定EPR原位凝胶注射剂中EPR的含量,方法具有快速简便、专属性强、灵敏度高、重复性好的特点,可在EPR原位凝胶注射剂的质量控制实践中应用。
A.阴性样品;B.对照品;C.供试品
A.Negative sample; B.Eprinomectin standard; C.Tested sample
图2乙酰氨基阿维菌素原位凝胶注射剂中
乙酰氨基阿维菌素的HPLC色谱图
Fig.2 HPLC chromatogram of eprinomectin
in situ gel injection

