AECOPD患者并发呼吸衰竭相关危险因素分析
张恒
COPD是一种由有害气体或颗粒所引起的以气道阻塞为特征的呼吸系统疾病。其死亡率在我国城市和农村中分别为第4位和第3位[1]。COPD患者病程为慢性逐年加重过程, 发作时病情复杂, 治疗不当可进一步出现缺氧缺血性脑病、心功能异常和呼吸衰竭[2], 而并发呼吸衰竭时, 患者死亡率明显增高, 成为呼吸科常见的危重症。本研究回顾性收集了本院近几年AECOPD患者的临床资料, 进一步探讨了AECOPD合并呼吸衰竭的相关危险因素, 为诊断和治疗提供相关参考, 报告如下。
1 资料与方法
1. 1 一般资料 本次以本院2013年1月~2017年12月临床确诊的AECOPD患者为研究对象, 共60例, 以有无呼吸衰竭分为观察组(存在呼吸衰竭, 30例)与对照组(无呼吸衰竭, 30例)。
1. 2 纳入及排除标准 纳入标准:①临床明确诊断为COPD的患者[呼吸衰竭诊断标准主要通过患者动脉血气分析进行诊断, 符合第8版《内科学》参考标准, 即血氧分压(PaO2)<60 mm Hg(1 mm Hg=0.133 kPa)或伴二氧化碳分压(PaCO2)>50 mm Hg];②目前处于急性发作期, 短期内出现咳嗽、气喘症状加重;③患者的血气分析和血生化检测均为入院后24 h内检测。排除标准:①患者存在自发性气胸、肺部感染、间质性肺炎、胸部外伤等其他肺部疾病所致的呼吸衰竭;②存在神经系统、消化系统、血液系统疾病等系统性疾病所致的呼吸衰竭和血生化异常。
1. 3 方法 收集两组患者的性别、年龄、COPD病程、糖尿病史、高血压病史、心脏疾病史、白细胞计数、血红蛋白量、血钾、血尿素、血清白蛋白量等临床资料, 并进行分类整理,比较两组差异, 分析AECOPD患者并发呼吸衰竭的危险因素。
1. 4 统计学方法 采用SPSS17.0统计学软件进行数据分析。计量资料以均数±标准差(±s)表示, 采用t检验;计数资料以率(%)表示, 采用χ2检验;通过Logistic多因素回归分析其独立影响因素。P<0.05表示差异具有统计学意义。
2 结果
2. 1 两组患者基线资料比较 观察组患者中有心脏疾病占66.7%(20/30)明显多于对照组的36.7%(11/30), 差异具有统计学意义(P<0.05);两组性别、年龄、COPD病程、有无糖尿病及高血压情况比较差异无统计学意义(P>0.05)。见表1。
2. 2 两组患者相关生化指标水平比较 两组白细胞计数、血钾、血尿素、血清白蛋白量比较差异具有统计学意义(P<0.05);两组血红蛋白量比较差异无统计学意义(P>0.05)。见表2。
2. 3 AECOPD患者并发呼吸衰竭危险因素的多因素Logistic回归分析 将上述结果中有明显差异的指标, 即心脏疾病史、白细胞计数、血钾、血尿素、血清白蛋白量等因素集中, 再设定无呼吸衰竭为0、有呼吸衰竭为1, 无心脏疾病的为0、有心脏疾病的为1, 白细胞计数、血钾、血尿素、血清白蛋白量为对应数值。以AECOPD是否合并呼吸衰竭为应变量, 上述有意义的因素为自变量, 进一步行多因素Logistic回归分析, 发现合并心脏疾病、高血尿素、低蛋白血症是AECOPD患者并发呼吸衰竭的独立危险因素(P<0.05)。见表3。
表1 两组患者基线资料比较[n(%), ±s]
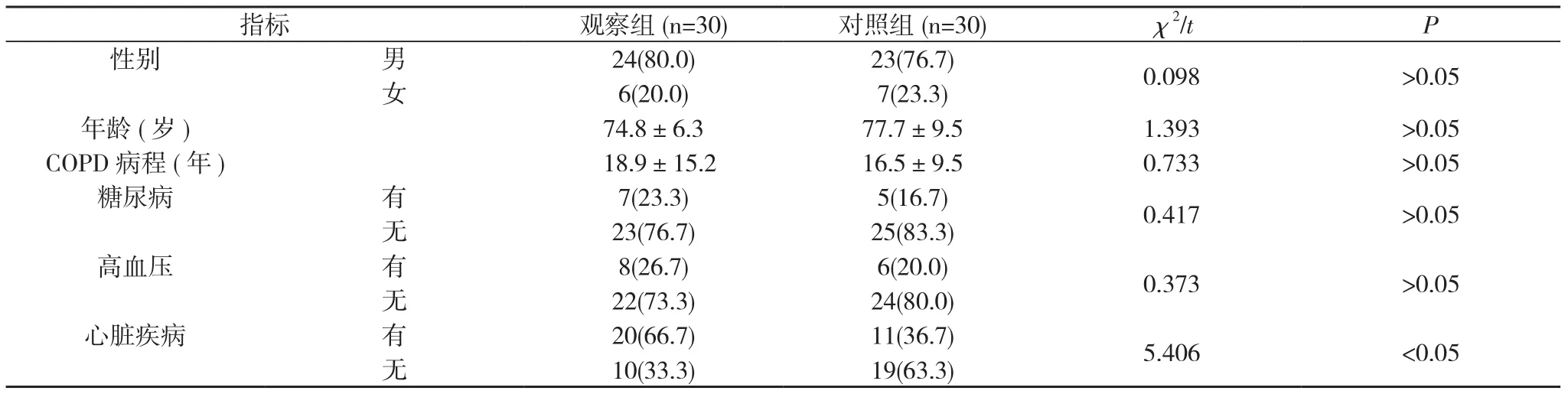
表1 两组患者基线资料比较[n(%), ±s]
注:两组心脏疾病情况比较, P<0.05
指标 观察组(n=30) 对照组(n=30) χ2/t P性别 男 24(80.0) 23(76.7) 0.098 >0.05女6(20.0) 7(23.3)年龄(岁) 74.8±6.3 77.7±9.5 1.393 >0.05 COPD病程(年) 18.9±15.2 16.5±9.5 0.733 >0.05糖尿病 有 7(23.3) 5(16.7) 0.417 >0.05无23(76.7) 25(83.3)高血压 有 8(26.7) 6(20.0) 0.373 >0.05无22(73.3) 24(80.0)心脏疾病 有 20(66.7) 11(36.7) 5.406 <0.05无10(33.3) 19(63.3)
表2 两组患者相关生化指标水平比较( ±s)

表2 两组患者相关生化指标水平比较( ±s)
注:与对照组比较, aP<0.05
指标 观察组(n=30) 对照组(n=30) t P白细胞计数(×109/L) 11.81±5.40a 8.97±3.94 2.327 <0.05血红蛋白量(g/L) 144.8±16.7 136.9±18.5 1.736 >0.05血钾(mmol/L) 3.81±0.87a 4.20±0.50 2.129 <0.05血尿素(mmol/L) 8.10±3.30a 5.85±1.95 3.215 <0.05血清白蛋白量(g/L) 35.22±4.36a 40.11±3.76 4.652 <0.05

表3 AECOPD患者并发呼吸衰竭危险因素的多因素Logistic回归分析
3 讨论
COPD做为临床上可预防和控制的常见病, 具有高发病率和高死亡率的特点[3]。由于其具有不完全可逆性, 病程呈现慢性、逐年加重的发展趋势, 且患者在受凉感染等诱因下可出现急性发作, 而后可能并发呼吸衰竭、缺氧缺血性脑病等, 导致病情进一步加重, 甚至出现死亡, 是呼吸科常见的急重症。
目前COPD患者多为中老年人[4], 该类患者多可合并高血压、糖尿病、冠心病等疾病, 这些疾病均可能为COPD发作时的危险因素, 故对其相关危险因素的防治亦相当重要。本研究发现合并心脏疾病的AECOPD患者更容易出现呼吸衰竭, 考虑该类患者在COPD发作期时由于心肌缺氧症状加重, 导致乳酸堆积、心脏负荷增加及心脏泵血功能下降, 以及高碳酸血症、感染进一步损伤心肌, 心功能可出现明显下降, 进一步影响肺循环, 从而使肺功能下降导致呼吸衰竭;同时也有研究显示[5]COPD也可引起心血管疾病, 可见两者相互影响, 由此可见对合并心脏疾病的AECOPD患者进行心脏功能的改善至关重要。
在COPD患者慢性发展的过程中, 可伴有长期慢性缺氧,在长期低氧情况下可出现消耗增加, 继发出现体重减轻、营养不佳[6]。目前已有研究提示, 低蛋白血症可造成COPD合并呼衰的死亡率增加[7], 低蛋白血症更易并发呼吸衰竭、心力衰竭、电解质紊乱等, 与本研究结果基本一致;因此对于COPD的患者更应注重稳定期的氧疗、缓解症状减少疾病的消耗及白蛋白的补充等处理。血尿素是肾功能的重要指标,尿素升高提示肾功能下降, 肾功能的下降可引起体内酸碱平衡的调节能力下降, 进而使AECOPD患者更易并发呼吸性酸中毒和呼吸衰竭;同时肾脏由于其自身特点, 对缺氧较敏感[8], 部分COPD患者由于长期缺氧可出现一定程度的肾损伤, 故对肾功能的保护仍然不能忽视。
综上所述, AECOPD患者存在心脏疾病、高血尿素、低蛋白血症时更易并发呼吸衰竭, 临床对于有心脏疾病的患者应积极治疗心脏问题, 并积极纠正低蛋白血症, 对于存在肾功能异常的患者应注意慎用肾毒性药物, 同时应长期氧疗改善低氧血症对心脏、肾脏等器官的损伤, 避免进一步加重COPD患者的病情进展。

