超快速液相色谱-三重四极杆/线性离子阱质谱法同时测定不同贮藏条件下红参中17种人参皂苷类成分
石婧婧,陈舒妤,邹立思,刘训红*,唐仁茂,马继梅,严 颖,赵 慧
(1.南京中医药大学 药学院,江苏 南京 210023;2.江苏苏中药业集团股份有限公司,江苏 泰州 225500)
红参是我国名贵中药材之一,系五加科植物人参PanaxginsengC.A.Mey.的栽培品经蒸制后的干燥根和根茎,具有大补元气、复脉固脱、益气摄血的功效,用于治疗体虚欲脱、肢冷脉微、气不摄血、崩漏下血等症[1]。现代研究表明,红参的主要药效成分为人参皂苷类,具有抗肝毒活性、抗糖尿病、抗衰老、抗氧化、抗疲劳、抗肿瘤等药理作用[2]。中药疗效的发挥是多种活性成分综合作用的结果,针对红参多种药效成分的特点,建立多种药效成分同时测定的方法,对探讨多指标成分的综合评价体系具有实用性和有效性。
药材的品质受种质资源、生态环境、采收加工、贮藏保管等因素的影响,其中贮藏保管是药材品质形成的重要环节。关于红参的品质形成研究,种质资源、生态环境和药材采收等方面的研究较成熟,且普遍得到公认,以上研究多集中于加工对红参品质的影响[3-4],贮藏条件对商品药材品质变化的影响常被忽略。科学的贮藏方法可以减少药材存放过程中由于自身特点及贮藏环境因素对其质量产生的不良影响,确保临床用药的疗效[5-7]。红参的质量评价多以含量较高的几种人参皂苷为指标[8-11],尚少见基于多种人参皂苷同时测定考察与评价红参药材贮藏的研究报道[12]。本实验基于超快速液相色谱-三重四极杆/线性离子阱质谱(UFLC-QTRAP-MS/MS)技术,建立了同时测定红参中原人参二醇型皂苷(人参皂苷Rb1、Rc、Rb2、Rd、F2、20(S)-Rg3、20(R)-Rg3、CK)、原人参三醇型皂苷(人参皂苷Re、Rg1、Rf、20(S)-Rg2、20(S)-Rh1、20(R)-Rg2、20(R)-Rh1、F1)、齐墩果烷型皂苷(人参皂苷Ro)17种指标成分含量的方法,并结合主成分分析(PCA)和聚类分析法(HCA)对不同贮藏(不同包装材料和贮藏温度)条件下的红参药材进行比较与综合评价,旨在为红参贮藏方法和条件的优选提供基础资料,同时为红参药材内在质量的综合评价和全面控制提供新的方法参考。
1 实验部分
1.1 仪器与试药
液质联用系统:Shimadzu SIL-20A XR 超快速液相色谱仪(日本岛津公司)包括LC-20AD二元输液泵、STL-20A XR 自动进样器。CTO-20AC柱温箱;AB QTRAP 5500 三重四极杆线性离子阱质谱仪(美国AB Sciex 公司),配有电喷雾离子源及Analyst 1.5.2软件。KQ-500B超声波清洗机(昆山超声仪器有限公司,超声功率500 W,40 kHz);BSA2245型电子分析天平(十万分之一,德国赛多利斯公司);ME36S型电子分析天平(百万分之一,德国赛多利斯公司);H1650-W高速离心机(湖南湘仪实验室仪器开发有限公司);SHZ-D(Ⅲ)循环水式真空泵(巩义市英峪仪器厂);Q-500B高速多功能粉碎机(上海冰都电器有限公司);Milli-Q超纯水制备仪(美国Millipore公司)。
人参皂苷Rb1(Rb1,批号:16060402)、人参皂苷Rc(Rc,批号:15121701)、人参皂苷20(R)-Rg3(20(R)-Rg3,批号:15121701)、人参皂苷Rd(Rd,批号:16051604)、人参皂苷Rf(Rf,批号:16052502)、人参皂苷CK(CK,批号:16072902)、人参皂苷20(S)-Rg2(20(S)-Rg2,批号:15123004)、人参皂苷20(S)-Rh1(20(S)-Rh1,批号:16081802)、人参皂苷Re(Re,批号:16081605)、人参皂苷F2(F2,批号:16081105)、人参皂苷Rg1(Rg1,批号:15121303)、人参皂苷Rb2(Rb2,批号:16061503)、人参皂苷Ro(Ro,批号:16050405)、人参皂苷20(R)-Rh1(20(R)-Rh1,批号:15121903)、人参皂苷20(S)-Rg3(20(S)-Rg3,批号:16012405)、人参皂苷20(R)-Rg2(20(R)-Rg2,批号:17022103)、人参皂苷F1(F1,批号:16081205)经HPLC测定纯度均大于98%,购自南京良纬生物科技有限公司。实验用水为超纯水;乙腈、乙醇、甲酸为色谱纯,其余试剂均为分析纯。
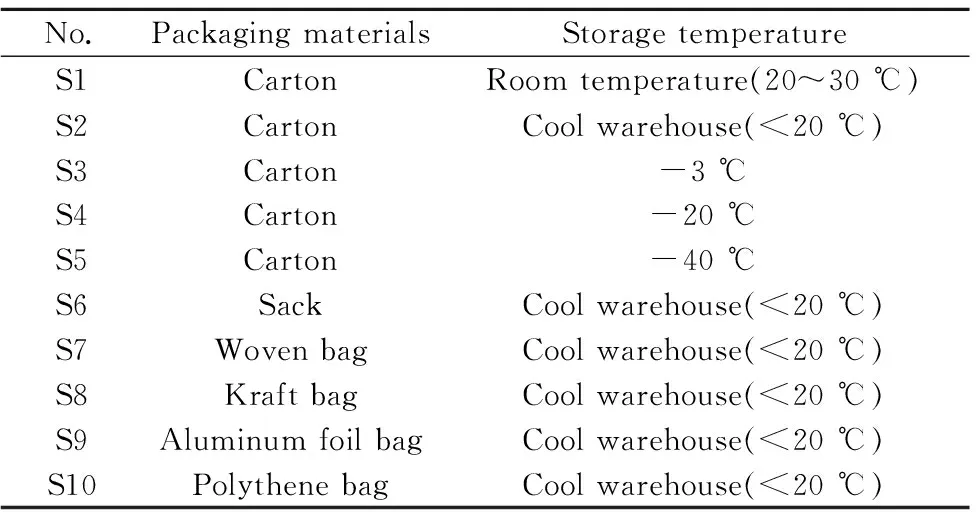
表1 不同贮藏条件的样品信息Table 1 Information of samples under different storage conditions
实验样品(人参)采自吉林省长白市靖宇县人参规范种植基地,经南京中医药大学药学院刘训红教授鉴定为五加科植物人参PanaxginsengC.A.Mey.的根及根茎,按产地的传统加工方法加工成红参药材。通过产地和市场调研,结合实际设计贮藏考察方法,各取红参药材500 g,按不同贮藏条件(包装材料及贮藏温度)避光贮藏半年后取出,样品信息见表1。留样凭证存放于南京中医药大学中药鉴定实验室。
1.2 溶液制备
1.2.1对照品溶液的制备分别称取人参皂苷Re、Rg1、Rf、20(S)-Rg2、20(R)-Rg2、20(S)-Rh1、Rb1、20(R)-Rh1、Rc、Ro、Rb2、F1、Rd、F2、20(S)-Rg3、20(R)-Rg3和CK对照品适量,精密称定,加60%乙醇配制成质量浓度分别为956、992、1 036、1 004、966、988、922、954、948、974、1 042、1 010、996、952、1 070、1 056、980 mg/L的对照品母液;取适量的各对照品母液,加甲醇配制成含上述对照品的混合储备液,并逐级稀释,得到一系列的混合对照品溶液,于4 ℃保存,备用。
1.2.2供试品溶液的制备取干燥至恒重的样品粉碎,过60目筛,精密称定0.5 g样品粉末,置于100 mL具塞锥形瓶中,加入25 mL 60%乙醇,于室温下超声(500 W、40 kHz)提取2 h后取出,放至室温以60%乙醇补足失重,静置冷却,4 ℃保存,12 000 r/min离心10 min,取上清液过 0.22 μm微孔滤膜,即得供试品溶液。
1.3 实验条件
1.3.1色谱条件色谱柱:SynergiTMHydro-RP 100 Å柱(100 mm×2.0 mm,2.5 μm);流动相:0.1%甲酸水(A)-乙腈(B);梯度洗脱:0~0.01 min,10%B;0.01~2.0 min,10%~25%B;2.0~11.0 min,25%B;11.0~13.5 min,25%~45%B;13.5~15.5 min,45%B;15.5~16.5 min,45%~98%B;16.5~18.0 min,98%~10%B;柱温40 ℃;流速0.4 mL/min;进样量2 μL。
1.3.2质谱条件使用AB Sciex QTRAP 5500 三重四极杆线性离子阱串联质谱仪在电喷雾负离子(ESI-)模式下进行多反应监测模式(MRM)检测,气帘气(CUR)压力为241.4 kPa,雾化气(Gas1)压力为379.3 kPa,辅助气(Gas2)压力为379.3 kPa,温度(TEM)为550 ℃,喷雾电压为5 500 V。
2 结果与讨论
2.1 色谱-质谱条件的优化
考察了水-甲醇、水-乙腈和0.1%甲酸水-乙腈作为流动相时的分离效果。结果表明,乙腈作为流动相时的分离效果明显优于甲醇,在流动相中加入一定量的甲酸可以减少色谱峰的拖尾,提高分离效果和检测灵敏度。因此,本实验最终采用0.1%甲酸水-乙腈作为流动相。
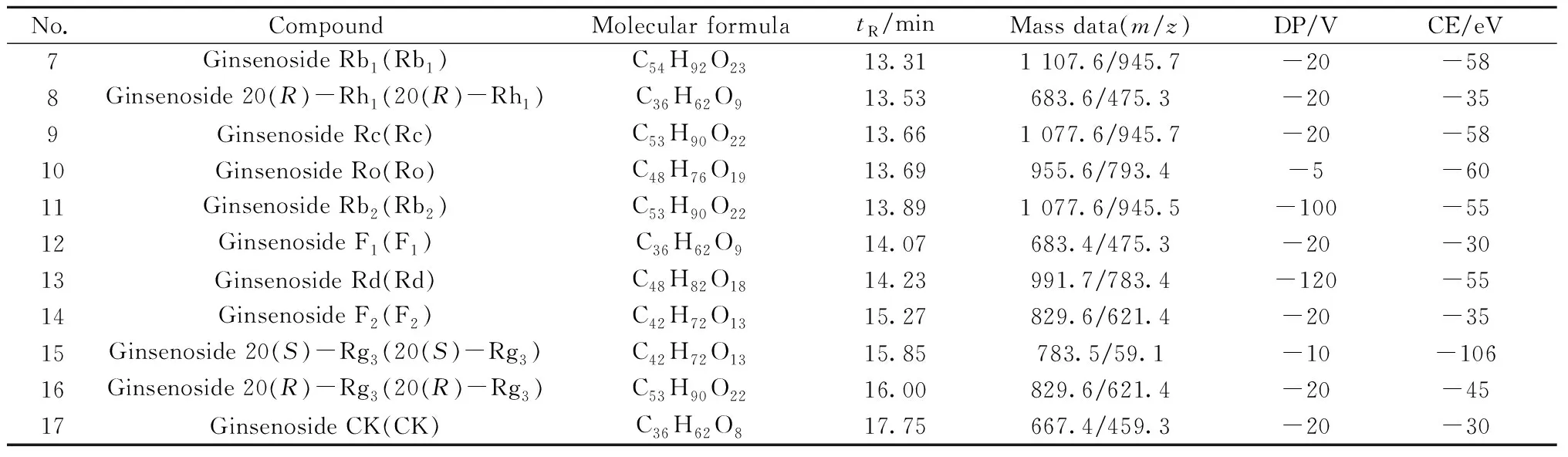
采用正、负两种离子模式测定17种化学成分的含量,经过反复试验,发现各成分在负离子模式下检测具有较高的稳定性、较高的响应值和较好的峰形,因此选择负离子模式检测。17种人参皂苷类成分的具体质谱参数及其MRM色谱图见表2及图1。

表2 17种目标成分的质谱分析参数Table 2 MS/MS parameters of seventeen components
(续表2)
No.CompoundMolecular formulatR/minMass data(m/z)DP/VCE/eV7Ginsenoside Rb1(Rb1)C54H92O2313.311 107.6/945.7-20-588Ginsenoside 20(R)-Rh1(20(R)-Rh1)C36H62O913.53683.6/475.3-20-359Ginsenoside Rc(Rc)C53H90O2213.661 077.6/945.7-20-5810Ginsenoside Ro(Ro)C48H76O1913.69955.6/793.4-5-6011Ginsenoside Rb2(Rb2)C53H90O2213.891 077.6/945.5-100-5512Ginsenoside F1(F1)C36H62O914.07683.4/475.3-20-3013Ginsenoside Rd(Rd)C48H82O1814.23991.7/783.4-120-5514Ginsenoside F2(F2)C42H72O1315.27829.6/621.4-20-3515Ginsenoside 20(S)-Rg3(20(S)-Rg3)C42H72O1315.85783.5/59.1-10-10616Ginsenoside 20(R)-Rg3(20(R)-Rg3)C53H90O2216.00829.6/621.4-20-4517Ginsenoside CK(CK)C36H62O817.75667.4/459.3-20-30
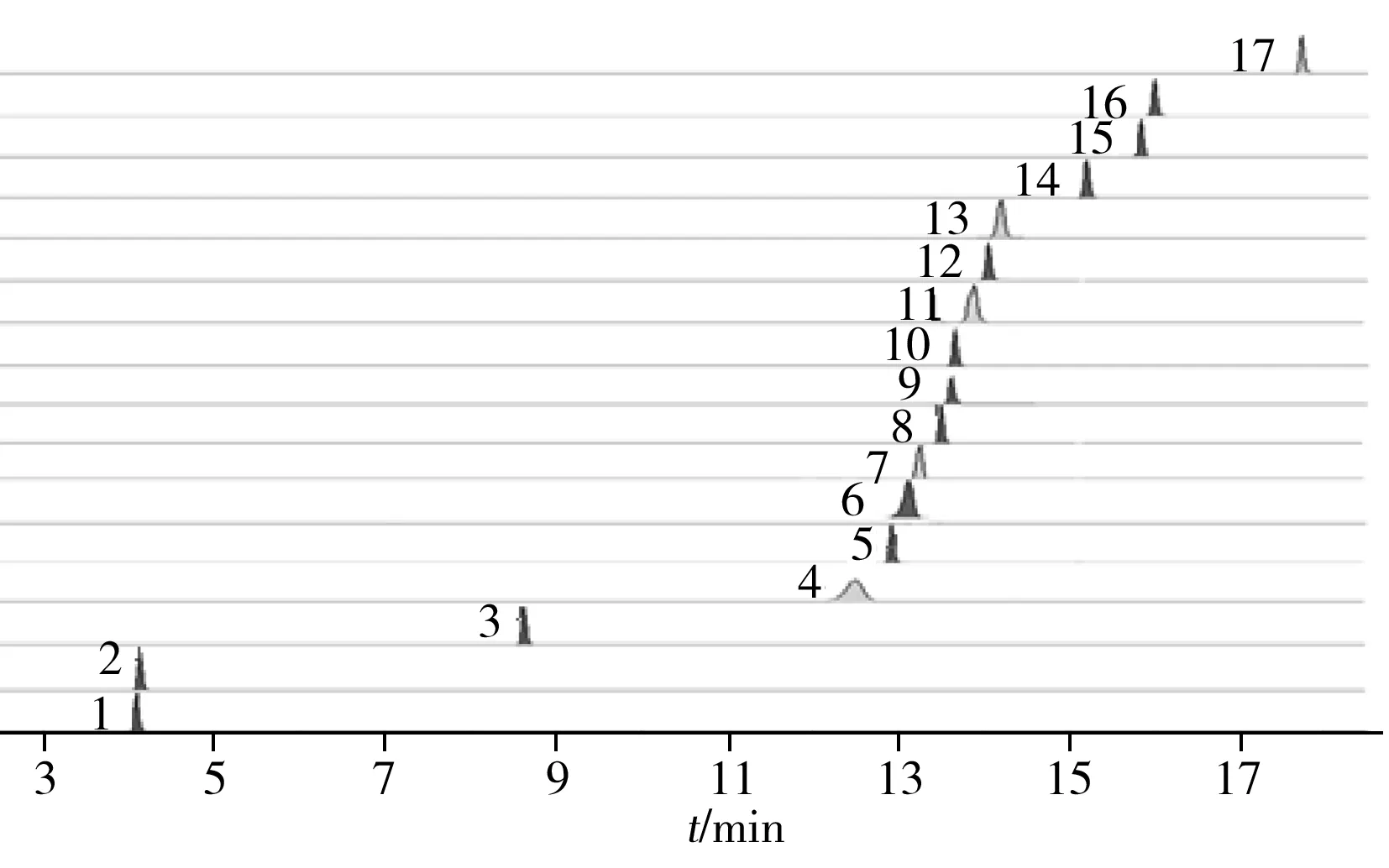
图1 17种目标成分的混合对照品的MRM色谱图Fig.1 MRM chromatograms of seventeen components in reference substancesthe peak numbers(1-17) denoted were the same as those in Table 1
2.2 供试品制备方法的优化
实验对提取溶剂(60%乙醇、70%乙醇、80%乙醇)、料液比(1∶20、1∶30、1∶50)及提取时间(1、1.5、2 h)进行正交实验考察,以人参皂苷Rb1、人参皂苷Re、人参皂苷Rg1的含量总和为指标。结果表明,最佳提取溶剂为60%乙醇,料液比为1∶50,提取时间为2 h。
2.3 方法学考察
2.3.1线性关系、检出限与定量下限精密吸取“1.2.1”中不同浓度系列的对照品溶液及混合对照品储备液各2 μL,按“1.3”色谱、质谱条件进行测定,以对照品的峰面积(Y)对相应的质量浓度(X,μg/L)进行线性回归,线性方程、相关系数及线性范围结果见表3。17种人参皂苷类成分均呈良好的线性关系,相关系数(r)均大于0.999 0。以信噪比(S/N)约为3计算各成分的检出限(LOD),以S/N≈10计算各成分的定量下限(LOQ),结果见表3。17种人参皂苷类成分的LOD为0.73~27.81 μg/L,LOQ为3.87~84.12 μg/L。

表3 17种化合物的线性关系、检出限和定量下限Table 3 Linear relations,LODs and LOQs of seventeen components
2.3.2精密度、重复性与稳定性试验精密吸取一定浓度的混合对照品溶液,连续进样6次,测定各对照品峰面积,计算得17种目标成分峰面积的相对标准偏差(RSD)为0.77%~2.6%(表4),说明仪器精密度良好;称取同一红参样品6份,每份0.5 g,精密称定,分别按“1.2.2”制备供试液,进样测定,计算得17种目标成分含量的RSD为1.2%~2.4%(表4),表明该方法重复性良好;取同一红参样品供试品溶液,分别在0、2、4、8、12、24 h进样分析,测定峰面积,计算得17种目标成分峰面积的RSD为1.0%~3.8%(表4),表明供试品溶液在24 h内具有较好的稳定性。
2.3.3加标回收率试验精密称取已知含量的红参样品0.25 g(9份),精密称定,分别加入低、中、高3个质量浓度的对照品溶液(分别相当于样品中各对照品含量为50%、100%、150%),每个浓度平行制备3份,按“1.2.2”制备加标回收供试品溶液并进行测定,计算回收率及相对标准偏差(表4)。17种人参皂苷类成分的平均回收率为96.4%~103%,RSD为0.68%~4.3%。结果表明该方法的准确度和精密度良好,可以满足日常样品的分析要求。

表4 精密度、重复性、稳定性及加标回收率结果Table 4 Precision,repeatability,stability and recovery of the method
2.4 样品含量的测定
取供试品溶液2 μL,注入液相色谱-质谱联用仪,按照优化条件进行测定,根据相应的线性关系计算供试样品中17种目标成分的含量,结果见表5。结果表明,不同贮藏条件下红参样品中17种人参皂苷类成分差异明显,其中人参皂苷Re、人参皂苷Rg1、人参皂苷Rb1的含量较高,分别为6 983.81~11 538.24、3 801.15~6 093.83、7 937.33~10 492.05 μg/g。从17种人参皂苷总量来看,以纸箱为包装,贮藏于-20 ℃条件下的红参样品(S4)总含量最高,达到53 835.10 μg/g;以牛皮纸袋为包装,贮藏于阴凉库(<20 ℃)条件下的红参样品(S8)总含量最低,仅4 4603.17 μg/g。由此可见,不同的贮藏条件会影响红参药材中人参皂苷类成分的含量。

表5 不同贮藏条件下红参样品的测定结果(μg/g,n=3)Table 5 Contents of samples under different storage conditions(μg/g,n=3)
(续表5)

CompoundS1S2S3S4S5S6S7S8S9S10Rd8 151.286 535.777 128.528 644.655 750.687 213.667 458.555 755.286 053.376 380.15F234.8436.9823.5927.1623.7720.0120.3911.6420.2114.1120(S)-Rg3887.241 683.64232.30984.501 056.85989.841 259.321 168.811 460.181 331.6320(R)-Rg32 207.311 622.232 165.322 410.291 789.931 942.932 164.021 777.512 095.651 761.19CK17.4310.9320.5616.1222.5021.1421.0921.0520.7521.36Sum47 833.4548 151.1846 493.1853 835.1044 766.0349 106.2746 988.6644 603.1746 157.9245 024.72

图2 不同贮藏条件下红参样品的聚类分析谱系图Fig.2 Dendrogram of Ginseng Radix et Rhizoma Rubra under different storage conditions
2.5 聚类分析
根据不同贮藏条件红参样品中各目标成分含量的测定结果,用聚类分析中的 Ward 法,利用 SPSS 中的 Hierarchical Cluster分析,对10个样品进行聚类分析。聚类的原则是相近的聚为一类,即距离最近或最相似的聚为一类,距离值越小,个体或变量之间越相近[18]。当临界值为20~25时可将不同贮藏方法的红参样品分为2类,S1、S4聚为一类,其他样品聚为一类(图2),结果表明不同贮藏条件下红参样品的质量存在一定差异。
2.6 主成分分析
主成分分析是一种降维或将多个指标转化为少数几个综合指标的方法,有利于克服单一指标的局限性,通过综合多种指标来准确、可靠地评判药材品质[13-14],对于红参质量的综合评价具有重要意义。
本文以人参皂苷类成分为指标,对不同贮藏条件下红参药材中17种指标成分进行主成分分析。通过SPSS 16.0计算主成分的特征值、贡献率和累积贡献率,结果如下:第一主成分的特征值为5.406,方差贡献率为31.801%;第二主成分的特征值为3.228,方差贡献率为18.991%;第三主成分的特征值为2.793,方差贡献率为16.431%;第四主成分的特征值为1.947,方差贡献率为11.450%;第五主成分的特征值为1.531,方差贡献率为9.007%;其他主成分特征值的贡献率依次减少。前5个主成分的累积贡献率达87.681%,且特征值均大于1,满足主成分的选取要求[15],表明前5个主成分可以反映17种人参皂苷的综合质量。
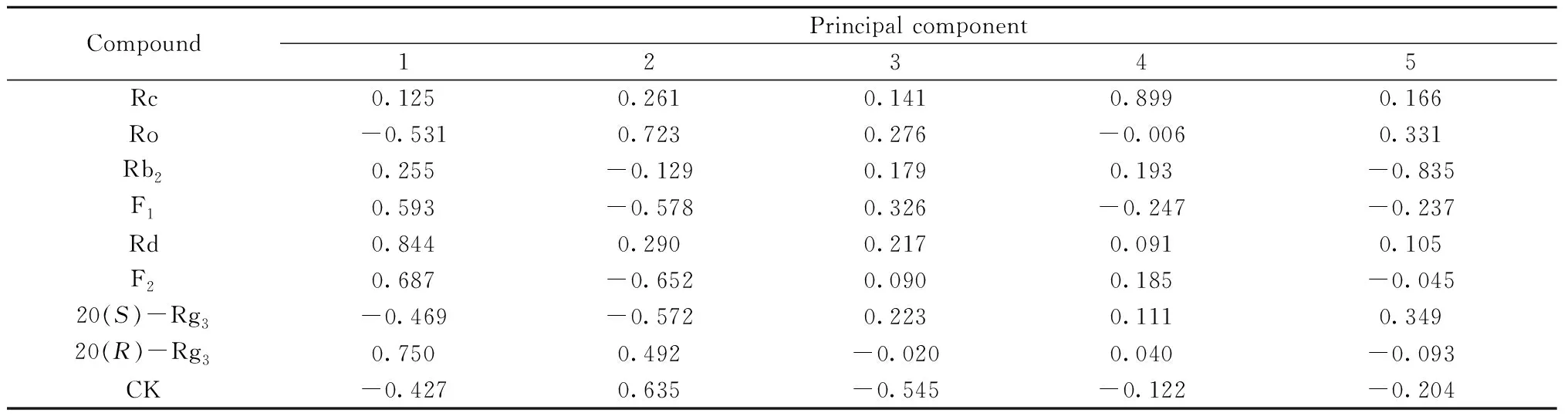
每个主成分均为原始变量的线性组合,线性组合中各变量对主成分的影响用载荷表示,载荷绝对值越大,其影响越大[16],在主成分分析中,一般认为大于0.30,表明载荷显著[17]。不同贮藏条件下17种人参皂苷的载荷如表6所示,在第一主成分中,人参皂苷20(S)-Rh1和Rd的因子载荷量最大,说明第一主成分主要反映了人参皂苷20(S)-Rh1、Rd的信息;同理,第二主成分主要反映了人参皂苷Ro、CK的信息;第三主成分主要反映了人参皂苷Re、20(S)-Rg2的信息;第四主成分主要反映了人参皂苷Rc、Rb1的信息;第五主成分主要反映了人参皂苷Rb2、20(R)-Rg2的信息。前5个主成分基本包含了大部分成分的信息。

表6 初始因子载荷矩阵Table 6 Component matrix
(续表6)
CompoundPrincipal component12345Rc0.1250.2610.1410.8990.166Ro-0.5310.7230.276-0.0060.331Rb20.255-0.1290.1790.193-0.835F10.593-0.5780.326-0.247-0.237Rd0.8440.2900.2170.0910.105F20.687-0.6520.0900.185-0.04520(S)-Rg3-0.469-0.5720.2230.1110.34920(R)-Rg30.7500.492-0.0200.040-0.093CK-0.4270.635-0.545-0.122-0.204
2.7 综合评价
不同贮藏条件下红参样品的主成分各因子总得分见表7,可根据权重系数计算得出各样品的综合得分。权重系数的计算依据其方差贡献的大小,即各主成分的贡献率与5个主成分的总贡献率之比,第一主成分的权重为31.801%/87.681%=0.362 7,同理可得第二、三、四、五的权重为0.216 7、0.187 4、0.130 6、0.102 7。各主成分的因子得分与其权重乘积之和相加,得出各红参样品的总因子得分F,得分越高,表明质量越好[18]。由表7可知,以纸箱为包装,贮藏于-20 ℃和常温条件下的红参样品(S4、S1)综合得分较高,说明这两种贮藏条件下的红参样品整体质量较好。以纸箱为包装,贮藏于-40 ℃下的红参样品(S5)综合质量较差。-20 ℃与-40 ℃均为冷冻贮藏,但-20 ℃为缓冻,-40 ℃为速冻,两者的冰冻速度有差异,这有可能是-20 ℃与-40 ℃贮藏条件下的红参样品质量相差较大的原因[19]。
聚类分析结果表明,以纸箱为包装,贮藏于-20 ℃和常温条件下的红参样品(S4、 S1)聚为一类,说明这两个样品之间的相似性较高。综合评价得分结果表明,以纸箱为包装,贮藏于-20 ℃和常温条件下的红参样品(S4、 S1)整体质量较好。但本文只考察了半年的贮藏期,若贮藏期更长,常温贮藏下的红参样品可能会出现虫蛀、发霉等现象[20],所以在短期贮藏中,考虑以纸箱为包装,存放于-20 ℃或常温条件下;但需要长期贮藏时,以纸箱为包装,存放于-20 ℃条件下较为合适,这与已有文献报道结果一致[21]。
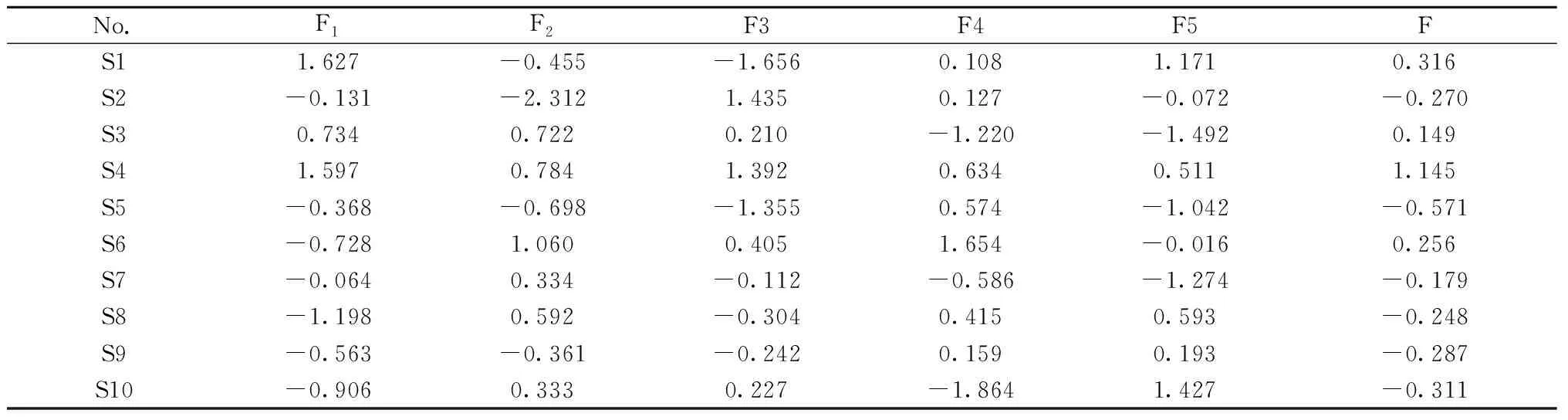
表7 不同贮藏条件红参主成分的得分和综合得分Table 7 Component scores and comprehensive scores of samples
3 结 论
本文建立了UFLC-QTRAP-MS/MS法同时测定红参中人参皂苷Rb1、Rc 、Rb2、Rd、F2、20(S)-Rg3、20(R)-Rg3、CK、Re、Rg1、Rf、20(S)-Rg2、20(S)-Rh1、20(R)-Rg2、20(R)-Rh1、F1、Ro 17种指标成分含量的方法,并结合主成分分析和聚类分析法对不同贮藏条件下红参药材进行比较分析与综合评价。本研究可为红参适宜贮藏条件的优选提供基础资料,同时为红参药材内在质量的综合评价和全面控制提供新的方法参考。

