镁-铝-镧三元类水滑石的制备及其在PVC中的应用
羌惜晨 ,肖 尖 ,王 凯 ,俞 强 ,陈 强
(1.常州大学材料科学与工程学院,江苏常州213164;2.常州南京大学高新技术研究院)
水滑石类化合物(LDHs)是一类无毒、环保、层板可控的无机材料[1]。由于其在阻燃、吸附、催化、离子交换等领域具有良好的前景而得到国内外学者广泛的关注和研究[2-3]。水滑石层板上的金属离子可被半径及电荷类似的金属离子所替代[4]。水滑石的层间碳酸根和层板均可与聚氯乙烯(PVC)降解产生的氯化氢发生反应,进而提高PVC的长期热稳定性,因此被广泛用作PVC辅助热稳定剂[5-6]。稀土元素La3+可以和水滑石其他金属离子组成MO6八面体筑成层板,且La3+较大的离子半径使它能通过静电引力和PVC活泼Cl-配位,显著抑制了HCl的脱附[7-9]。
目前,针对MgAlLa-CO3-LDHs的研究较少,La3+掺杂的稀土水滑石作为PVC热稳定剂的研究尚未见报道。本文采取共沉淀离心水热法制备出典型层状结构、晶型完整的MgAlLa-CO3-LDHs,并研究共沉淀温度、共沉淀时间、水热温度及水热时间对产物晶型的影响,将所得产物与PVC复配,通过静态热烘箱实验和刚果红实验研究其对PVC热稳定性能的影响。
1 实验
1.1 主要原料
六水合氯化镁(MgCl3·6H2O)、七水合氯化镧(LaCl3·7H2O)、六水合氯化铝(AlCl3·6H2O)、NaOH、Na2CO3、硬脂酸钙、邻苯二甲酸二正辛酯(DOP)、硬脂酸锌,均为分析纯;抗氧剂1010、液体石蜡、钛白粉、PVC(SG-5 型),均为工业级。
1.2 镁-铝-镧水滑石的制备
1.2.1 共沉淀法
称取3.05 g六水合氯化镁、1.74 g七水合氯化镧和0.11 g六水合氯化铝,倒入装有30 mL去离子水的烧杯中搅拌至溶液澄清。再称取2.4 g碳酸钠和1.59 g氢氧化钠,倒入装有30 mL去离子水的烧杯中充分搅拌至溶液澄清,冷却至室温。将上述制得的盐和碱溶液分别移入恒压滴液漏斗中,以1滴/s的速度滴入一定温度下的三口烧瓶中。打开磁力搅拌,强力搅拌2 h,用去离子水洗涤、抽滤3~4次,直到pH呈中性,所得固体在70℃下干燥12 h,研磨过筛至粒径≤200 μm,得到白色粉末MgAlLa-CO3-LDHs。
1.2.2 水热法
称取3.05 g六水合氯化镁、1.74 g七水合氯化镧和0.11 g六水合氯化铝,倒入装有30 mL去离子水的烧杯中搅拌至溶液澄清。再称取2.4 g碳酸钠和1.59 g氢氧化钠,倒入装有30 mL去离子水的烧杯中充分搅拌至溶液澄清,冷却至室温。将上述制得的盐和碱溶液分别移入恒压滴液漏斗中,以1滴/s的速度滴入一定温度下的三口烧瓶中。打开磁力搅拌,滴加结束后将混合液迅速转移至水热反应釜中,在150℃的烘箱中反应10 h。待其冷却至室温后,打开水热反应釜,将产物用去离子水充分洗涤、至pH呈中性,抽滤,所得固体在70℃下干燥12 h,研磨过筛至粒径≤200 μm,得到白色粉末MgAlLa-CO3-LDHs。
1.2.3 共沉淀-水热法
称取3.05 g六水合氯化镁、1.74 g七水合氯化镧和0.11 g六水合氯化铝,倒入装有30 mL去离子水的烧杯中搅拌至溶液澄清。再称取2.4 g碳酸钠和1.59 g氢氧化钠,倒入装有30 mL去离子水的烧杯中充分搅拌至溶液澄清,冷却至室温。将上述制得的盐和碱溶液分别移入恒压滴液漏斗中,以1滴/s的速度滴入一定温度下的三口烧瓶中。搅拌2 h后将混合溶液直接转移至水热反应釜中,在150℃烘箱中反应10 h。待其冷却后,将产物用去离子水充分洗涤、至pH呈中性,抽滤,所得固体在70℃下干燥12 h,研磨过筛至粒径≤200 μm,得到白色粉末MgAlLa-CO3-LDHs。
1.2.4 共沉淀-离心-水热法
称取3.05 g六水合氯化镁、1.74 g七水合氯化镧和0.11 g六水合氯化铝,倒入装有30 mL去离子水的烧杯中搅拌至溶液澄清。再称取2.4 g碳酸钠和1.59 g氢氧化钠,倒入装有30 mL去离子水的烧杯中充分搅拌至溶液澄清,冷却至室温。将上述制得的盐和碱溶液分别移入恒压滴液漏斗中,以1滴/s的速度滴入一定温度下的三口烧瓶中。搅拌2 h后,将反应液离心所得固体重新分散到60 mL的去离子水中,再将溶液转移至水热反应釜中,在150℃烘箱中反应10 h。待其冷却后,将产物用去离子水充分洗涤、至pH呈中性,抽滤,所得固体在70℃下干燥12 h,研磨过筛至粒径≤200 μm,得到白色粉末MgAlLa-CO3-LDHs。
1.3 性能测试
将1 g硬脂酸锌、1.5 g硬脂酸钙、0.2 g抗氧剂1010、2 g钛白粉、100 g PVC以及一定量的MgAlLa-CO3-LDHs混合均匀后,再加入0.4 g液体石蜡和25 g的DOP充分机械搅拌后,180℃下密炼3 min。随后将其在180℃下平板硫化制成1 mm厚度的薄片,热压1 min,冷压1 min。待其冷却将其裁成2 cm×2 cm的样品。
参照GB/T 9349—2002《聚氯乙烯、相关含氯均聚物和共聚物及其共混物热稳定性的测定》,采用静态热烘箱实验法测试不同添加量MgAlLa-CO3-LDHs对PVC的热稳定性能的影响。
参照ISO182-1:1900标准,采用刚果红实验法测试不同添加量MgAlLa-CO3-LDHs对PVC的热稳定性能的影响。
1.4 表征
采用D/max 2500 PC型X射线衍射仪对产物的物相结构进行表征。采用JSM-6360LV型场发射扫描电镜观察产物形貌。
2 结果与讨论
2.1 不同制备工艺对比对水滑石性能的影响
以六水合氯化镁、六水合氯化铝及七水合氯化镧为原材料,n(Mg2+)∶n(Al3+)∶n(La3+)=48∶23∶1,分别采用共沉淀法、水热法、共沉淀-水热法、共沉淀-离心-水热法制备MgAlLa-CO3-LDHs,并通过XRD表征,结果见图1。从图1可以看出,4种方法制备的水滑石样品均有明显的特征衍射峰,这些主衍射峰主要对应于 MgAlLa-CO3-LDHs 的(003)、(006)、(110)和(113)等衍射 晶 面,4 种 方 法所制 备 的MgAlLa-CO3-LDHs衍射谱图均在19°附近出现了La3+的衍射峰,说明这4种方法均成功制备出了MgAlLa-CO3-LDHs。由图1还可以看出,利用共沉淀法、水热法还有共沉淀-离心-水热法制备样品在15.8°处均含有微弱的La(OH)3杂相,用共沉淀法和水热法制备的样品在43.16°附近有NaClO3杂质峰,利用共沉淀-离心-水热法制备的样品衍射强度大、无杂相峰且衍射基线平稳,说明共沉淀-离心-水热法可以明显改善MgAlLa-CO3-LDHs的结晶度并提高晶体结构规整度。
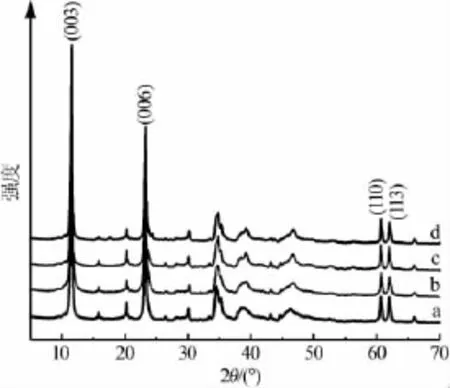
图1 不同方法制备的MgAlLa-CO3-LDHs的XRD谱图
图2是采用4种方法制备的MgAlLa-CO3-LDHs样品的SEM照片。由图2a可见,共沉淀法制备出的样品形貌很不规整,大小不均一,且片层大部分都比较大。由图2b可见,水热法制备的样品大小也不均匀,形貌无规则。由图2c可见,共沉淀-水热法制备的样品片层出现了水滑石特征的六边形和圆形,但是大小仍不够均一。由图2d可见,共沉淀-离心-水热法制备的样品均达到纳米级,且表面规整大小均匀,片层形貌呈六方片状,粒径为100~150nm。

图2 不同方法制备的MgAlLa-CO3-LDHs的SEM照片
2.2 共沉淀温度对水滑石形成的影响
实验分别在 60、70、80、90 ℃下共沉淀反应 2 h,考察了共沉淀温度对MgAlLa-CO3-LDHs的影响,结果见图3。由图3可见,共沉淀温度为60℃时,产物中除MgAlLa-CO3-LDHs外,在43.16°附近还有NaClO3杂相峰,在 15.8°附近仍有 La(OH)3杂峰,主晶相MgAlLa-CO3-LDHs衍射峰强度弱;随着温度升高,La(OH)3及 NaClO3等杂相含量逐渐减少,主晶相MgAlLa-CO3-LDHs衍射峰强度变强,70℃时为单相的MgAlLa-CO3-LDHs,其峰形尖锐且对称,衍射强度很强;主晶相MgAlLa-CO3-LDHs衍射峰的强度和对称性均随着温度升高而提升,说明其结晶度和结构的规整性同时提高;继续升高温度至90℃时,虽然水滑石相衍射峰明显且对称性良好,但是衍射强度变弱。

图3 不同共沉淀温度下MgAlLa-CO3-LDHs的XRD谱图
反应温度比较低,会造成体系内离子的运动速度较慢,使晶粒生成速度也变慢,最终导致产物结晶度不高、晶型不好且产生杂质。适当提升反应温度,体系内离子的运动速度变快,可使晶粒的生成速度变快,产物结晶度变高且晶型也趋于规整。但是如果反应温度过高,则会导致体系中水滑石分子动能增加过快,不利于形成规整、稳定且较大的水滑石晶粒。因此,实验选择适宜的共沉淀温度为70℃。
2.3 共沉淀时间对水滑石形成的影响
采用共沉淀-离心-水热法,在70℃下进行共沉淀反应,实验考察了共沉淀时间(1、2、3、4 h)对MgAlLa-CO3-LDHs样品的影响,结果见图4。从图4可以看出,反应时间为1 h时,除主晶相MgAlLa-CO3-LDHs外,还有大量明显的杂相La(OH)3存在,且主晶相衍射峰强度弱;共沉淀时间延长至2 h时,主晶相MgAlLa-CO3-LDHs的衍射峰强度并未有多大的变化,15.8°附近的杂相La(OH)3的衍射峰已经消失,水滑石基线平稳,几乎无杂峰;共沉淀时间为3 h时,主晶相的衍射峰强度明显变强,但是在44.7°附近又产生了杂相;共沉淀时间为4 h时,衍射谱图为单相的MgAlLa-CO3-LDHs,衍射峰变化不大。随着反应时间的延长,衍射峰的衍射强度变强,杂峰消失,峰形窄而尖,说明晶面生长的有序程度在提高,结晶度变好。2 h后继续延长反应时间,谱图中则未观察到变化。因此,实验选择适宜的共沉淀时间为2 h。
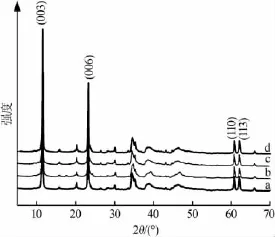
图4 不同共沉淀时间下MgAlLa-CO3-LDHs的XRD谱图
2.4 水热温度对水滑石形成的影响
为了考察水热温度对锌镁铝水滑石的影响,实验将离心所得沉淀物重新分散在纯水中,再转移至水热反应釜中,分别在 110、130、150、170℃下水热反应10 h,分析水热温度与结晶度的关系,结果见图5。由图5可见,当水热温度为110℃时,产物中除MgAlLa-CO3-LDHs外,在 26.8°附近产生了 Al(OH)3杂峰、15.8°附近有 La(OH)3杂相,还含有 Mg(OH)2杂相,并且主晶相MgAlLa-CO3-LDHs衍射峰强度弱。随着温度升高,Mg(OH)2等杂相含量逐渐减少,主晶相MgAlLa-CO3-LDHs衍射峰强度变强;150℃时为单相的MgAlLa-CO3-LDHs,峰形尖锐且对称,此时衍射强度很强。继续提升水热温度,则对衍射峰强度影响较小。因此,实验选择适宜的水热温度为150℃。

图5 不同水热温度下MgAlLa-CO3-LDHs的XRD谱图
2.5 水热时间对水滑石形成的影响
水热时间对晶体的生长有很大的影响,为此实验将重新分散的沉淀物转移至水热反应釜,并在150℃下分别反应 5、10、15 h制备 MgAlLa-CO3-LDHs。图6即为不同反应时间下产物XRD结果。从图6可看出,反应时间为5 h时,除MgAlLa-CO3-LDHs为主相外,16.7°附近还有大量明显的杂相La(OH)3峰且 19°附近 La3+衍射峰强度弱;当水热时间延长至10 h时,主晶相MgAlLa-CO3-LDHs衍射峰强度稍微变弱,杂相La(OH)3的衍射峰已经消失;水热时间为15 h时,主晶相MgAlLa-CO3-LDHs衍射峰强度变化不大且有杂峰。因此,实验确定适宜的水热反应时间为10 h,此时峰强度高、杂相少、峰形完整、产品结晶度高。
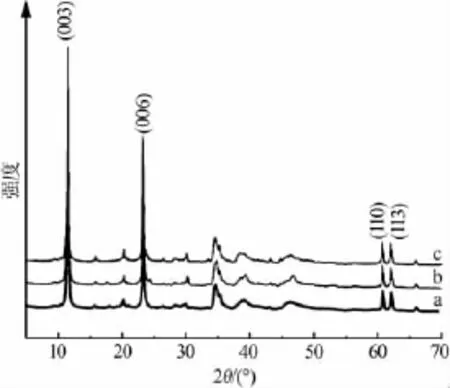
图6 不同水热时间下MgAlLa-CO3-LDHs的XRD谱图
2.6 对PVC热稳定性能影响
按照100 g PVC添加30 g DOP、1.5 g硬脂酸钙、1 g硬脂酸锌、0.5 g石蜡、2 g钛白粉、0.2 g抗氧剂1010和不同添加量(0~5%,与100 g PVC的质量比,下同)的MgAlLa-CO3-LDHs热稳定剂进行复配。密炼,平板硫化后制成2 cm×2 cm的1 mm样片后,置于(180±1)℃的鼓风恒温烘箱进行热老化实验。每20 min取出一个样片,观察并记录其颜色。PVC出现黑化点为临界点,以此作为热老化时间。通过观察可见,只添加了硬质酸钙、硬质酸锌和DOP及抗氧剂的PVC样品的初期颜色较浅,呈乳白色,说明未添加MgAlLa-CO3-LDHs的PVC初期着色性较好。但是60 min后就开始出现黑化点;添加1%MgAlLa-CO3-LDHs复配后,PVC呈浅粉色。不过PVC的热稳定性大大改善,比未添加水滑石的PVC热老化时间延长了40 min左右。添加了2%MgAlLa-CO3-LDHs的PVC样品初期着色较浅,80 min时后颜色才微微发黄,120 min后才出现黑化临界点;添加了3%MgAlLa-CO3-LDHs的PVC样品热稳定时间达到了140 min。将分别添加了4%和5%的MgAlLa-CO3-LDHs复配的PVC样品做对比发现,PVC颜色均为逐步加深,热稳定时间都达到了180 min。说明继续提高MgAlLa-CO3-LDHs的添加量对PVC热稳定时间的延长意义不大。因此PVC中适合的MgAlLa-CO3-LDHs添加量为4%左右。综上所述,La添加的镁铝水滑石作热稳定剂能大大提高PVC的热稳定性能,PVC的热稳定时间可以延长至180 min。较未添加水滑石的PVC的热稳定时间增加了2 h。这主要是因为MgAlLa-CO3-LDHs中的La元素可以和PVC主链上活泼的Cl元素进行一个配位作用,水滑石特殊的层板结构中的羟基又可以与PVC释放出的HCl中和,抑制自催化。从而使PVC的降解速率显著降低,MgAlLa-CO3-LDHs有效地提高了PVC的热稳定性能。
表1是不同添加量(1%~5%)的MgAlLa-CO3-LDHs对PVC热稳定性能影响的刚果红实验结果。由表1可以看出,刚果红测试的结果和热老化的结果基本吻合,未添加MgAlLa-CO3-LDHs复配的PVC样品热稳定时间较短,只有59 min,随着MgAlLa-CO3-LDHs的添加量增加,PVC的热稳定时间也逐步延长,当添加量达到了4%~5%时,热稳定达到了170 min以上,差异不大。因此,实验选择适宜的MgAlLa-CO3-LDHs水滑石添加量为4%。

表1 刚果红实验结果
3 结论
本文通过共沉淀-离心-水热法可以制备出晶型完整、高纯度、粒径均一的MgAlLa-CO3-LDHs。其最佳制 备条 件:n(M2+)∶n(M3+)=2∶1,pH≥10,n(La3+)∶n(Al3+)=1∶23,70 ℃共沉淀温度下反应 2 h,150℃水热温度下反应10h。通过静态热烘箱与刚果红实验,每100 g PVC添加4 g的MgAlLa-CO3-LDHs能将PVC在180℃下的耐热时间提高到177 min,对PVC的加工稳定性有显著提升作用。

