新型左室四极导线在心脏再同步化治疗中的疗效观察
李庆宽 覃绍明 胡昌兴 韦开福
心脏再同步化治疗(cardiac resynchronization therapy,CRT)是伴有机械心室收缩不同步的心力衰竭(简称心衰)患者的一种有效的治疗措施。然而,虽然经过严格的病例筛选,仍有部分患者出现CRT不应答现象而影响疗效,其中很大部分原因是由于左室导线起搏位点选择不恰当所致[1]。新型的左室四极导线,由于其更多的左室起搏位点、最小化膈神经刺激等特点,使其在CRT中具有明显优势,并有取代传统左室导线的趋势。笔者就新型左室四极电极导线在CRT中的疗效进行临床观察。
1 资料与方法
1.1研究对象
收集2016年5月至2017年6月在广西壮族自治区人民医院心血管内科使用新型左室四极导线行CRT的心肌病心衰患者共5例(表1),病因均为扩张型心肌病,其中男性2例,女性3例,均行CRT-D植入术,其手术指征均符合《2016年ESC急慢性心力衰竭诊断和治疗指南》[2]中关于CRT的推荐,同时也符合埋藏式心脏转复除颤器(ICD)植入的推荐。收集患者基本临床特征、血生化指标及临床用药情况。

表1 患者基本临床特征
1.2CRT-D植入术
①首先在局部麻醉下进行左侧胸前皮下切口 ,穿刺左锁骨下静脉,经左锁骨下静脉植入电极,左锁骨下行起搏器囊袋制作;②使用冠状窦电极或Amplatz导管寻找冠状窦,使用球囊封堵后行冠状静脉窦逆行造影,显示冠状静脉窦血管分支情况,使用左室四极导线(Quartet,St.Jude);③右室电极植入心尖部;④右房采用被动电极,植入右心耳。
1.3评估与随访
术前对患者进行充分评估,术后1、3及6个月嘱患者返院进行起搏器程控,术后6个月进行随访,评估和随访的内容包括:①用药情况,包括β受体阻滞剂、血管紧张素转换酶抑制剂/血管紧张素受体阻滞剂(ACEI/ARB)及醛固酮受体拮抗剂使用情况;②功能状态,明尼苏达生活质量评分(MLHFQ)和6 min步行实验(6MWT);③心衰进展指标,左室射血分数(LVEF)、左室舒张末内径(LVEDD)、二尖瓣返流量(MR)及血浆N末端B型利钠肽前体(NT-proBNP)浓度;④心衰预后,6个月内的再住院率。
2 结果
2.15例患者均成功完成CRT-D植入术,左室电极的植入:其中4例植入左室侧壁,1例植入左室后侧壁,见图1。术中左室电极阈值、阻抗及感知良好。手术时间95~135 min,曝光时间60~90 min,无感染、电极移位等并发症发生。术前及术后心电图见图2。
2.2随访结果
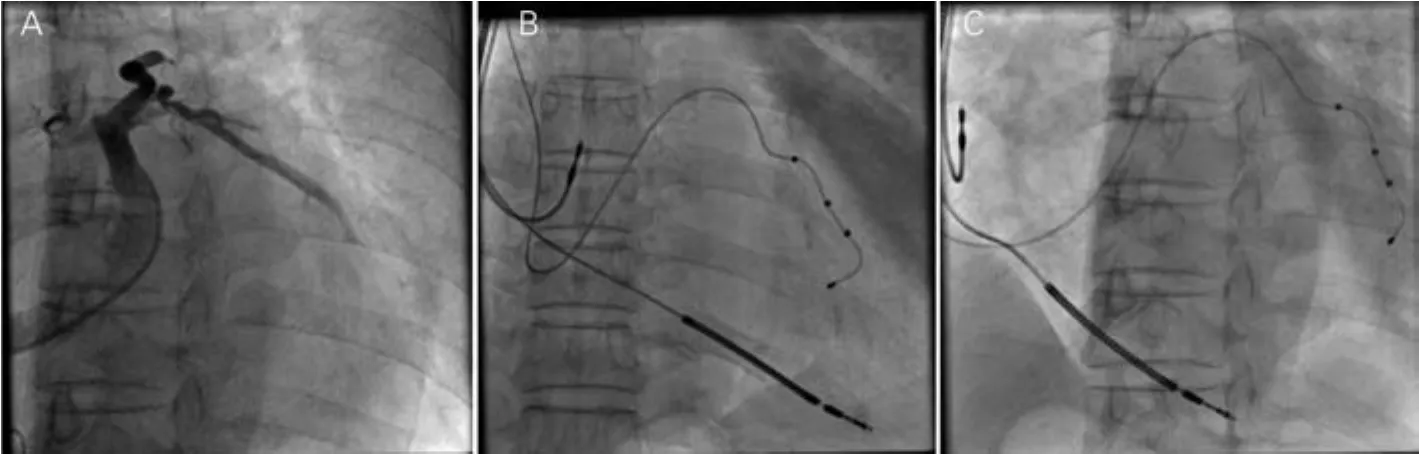
图1 患者胸部影像
2.2.1程控结果 新型左室四极导线具有自动测试右室-左室传导时间,可以检测左室电极传导最延迟的位点,再结合阈值及有无膈肌起搏等选择最佳起搏位点,5例左室导线程控结果见表2。随访第1个月,患者4因左室起搏位点阈值升高(3.25V、0.5ms),而改变起搏位点(由中间3-右室线圈改为中间2-右室线圈),改变起搏位点后阈值为1.75V、0.5ms。患者1术前伴有频发室性早搏(简称室早)(24 h 22 467搏),双心室起搏比例为78.9%,术后一个月室早减少为24 h 8 894搏,后联合使用胺碘酮治疗室早明显减少(24 h 2 349搏),双室起搏比例达90%以上。具体程控结果见表2及图3。
2.2.2用药情况 5例患者术前均使用有利尿药物及螺内酯,由于血压偏低,使用的美托洛尔缓释片及培哚普利剂量偏少(不使用至一片不等),2例患者需使用地高辛(每日半片)治疗。术后均继续优化药物治疗,均使用托拉塞米10 mg每日一次、螺内酯20 mg,每日1次,培哚普利4~8 mg,每日1次、美托洛尔缓释片95~142.5 mg,每日1次(逐渐加量)。血压110~120/60~85 mm Hg,静息心率55~65次/分,术后复查肾功能及电解质均未见明显异常。
2.2.3功能状态 术后6个月患者MLHFQ减低和6MWT增加,具体结果见表3。
2.2.4心衰进展指标 术后6个月5例患者心脏彩超各指标及血浆NT-proBNP浓度均较前明显改善,具体结果见表3。
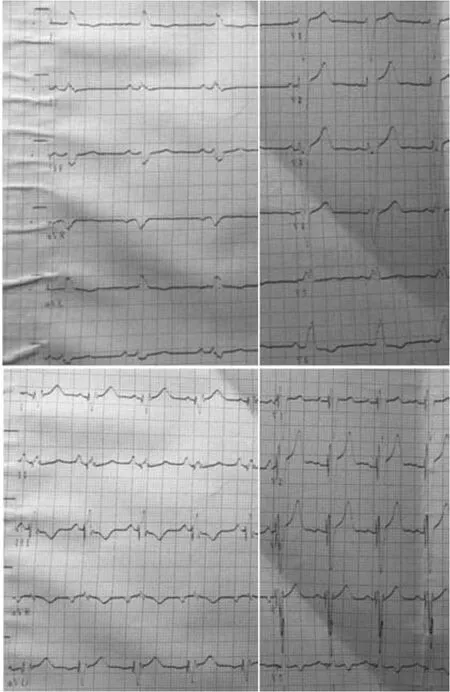
图2 患者5术前及术后心电图
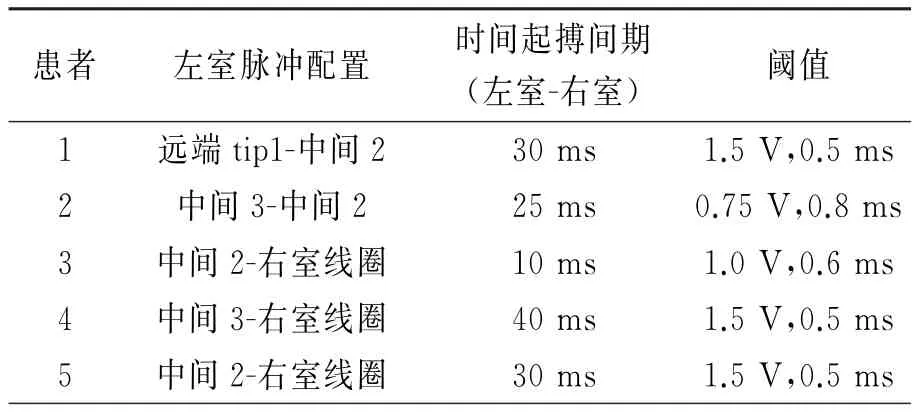
表2 CRT左室电极程控结果

图3 患者5的程控结果

表3 CRT治疗后6个月各指标改变情况
2.2.5心衰预后 5例患者术前因心衰年均住院2~3次,术后6个月内均未因心衰再次入院。
3 讨论
传统的左室电极仅有两极,起搏位点的选择有限,因此要求术者术中尽量选择良好的起搏位点,加上膈神经刺激、左室导线不稳定及有可能出现的心尖部起搏等因素导致手术难度的增大,同时还要面临术后可能会出现阈值升高的问题,等等这些因素都会影响CRT的疗效。新型左室电极具有四极,分别为远端头端电极D1、中部电极环2-M2、中部电极环3-M3及近端电极环-P4,借助四极电极,CRT-D可以从10个向量测试左室起搏阈值,从而获得更多的左室起搏位点。术中可以将导线的头端固定于选定血管的远端,以获得更好的稳定性,而起搏使用中部或近端的环状电极以求获得无膈神经刺激及非心尖部的起搏位点。其还可以自动测量右室-左室四个电极位点的电学延迟,作为左室起搏位点选择的依据,这种简化的方式可以改善CRT血流动力学和提高CRT疗效[3-4]。而更多的左室起搏位点的选择,可以通过非介入方法解决术后面临的阈值升高问题。
我们观察的5位患者均使用左室四极电极完成CRT-D术,手术时间及X线曝光时间较传统的左室二极导线明显缩短。手术均顺利完成,没有并发症发生。术后共随访6个月,这5位患者术前年人均因心衰入院2~3次,CRT治疗后随访的6个月内无一患者因心衰再次入院,患者生活质量提高、心衰进展延缓、再住院率及病死率降低,与国内马继芳等[5]的研究结果一致。5位患者随访期间,患者4术后1个月出现左室电极阈值升高,经过程控后选用新的阈值良好的起搏位点,后续随访,起搏阈值保持稳定。患者1术前伴有频发多源室早,经CRT治疗1个月后,室早较前明显减少。室早的减少考虑与患者血流动力学改善及心功能提高有关,这与In-Sync-III Marquis研究结论相似,即CRT治疗可以减少室早发生,提高室早及室性心动过速/心室颤动的治疗率[6]。但是残余的频发室早,会减少CRT双心室起搏的百分比,从而降低CRT疗效,因此我们加用胺碘酮协同治疗,随访6个月室早明显减少,CRT双心室起搏百分比达90%以上。患者4经CRT治疗后疗效极为显著,心脏彩超结构及功能参数恢复正常范围,心功能明显改善,是CRT超反映者。CRT术后超反映的发生率约为8%~30%,对于这类患者术后是否仍需继续双心室起搏研究偏少,尚无定论。少数研究认为,CRT带来的左室结构与功能的的改善是一种缓解状态而非痊愈[7-8],因此对于超反映者仍需持续的双心室起搏以保持改善后的状态,因此对于患者4我们仍继续开通CRT-D功能。
使用CRT治疗轻度或重度心衰均可显著改善临床疗效和预后,但最佳药物治疗是应用CRT治疗的先决条件。5位患者术前均使用“金三角”药物治疗,由于心功能欠佳,血压偏低,β受体阻滞剂及ACEI类药物均为小剂量使用,术后由于心功能改善,逐渐加大上述药物剂量,术后6个月β受体阻滞剂(美托洛尔缓释片)剂量为每日95~142.5 mg。患者术后治疗药物剂量的逐渐增加,说明CRT可以短时间内改善患者血流动力学、提高患者心功能,而长期最大耐受剂量药物的使用则能与CRT协同改善患者的预后,两者在心衰患者的治疗中起协同作用,缺一不可。
我们的观察证实新型左室四极电极在CRT治疗中是安全有效的,且能够很好地解决传统左室电极所遇到的膈神经起搏、左室电极不稳、心尖部起搏及阈值升高等问题,同时能够缩短手术时间,提高手术成功率,这与国内李杨等[9]的研究结果一致,值得临床推广应用。而且采用左室四极导线具有自动测量右室-左室四个电极位点的电学延迟功能,作为左室起搏位点选择的依据,可以改善CRT血流动力学和提高CRT疗效。本研究的局限在于研究例数偏少,但我们相信,随着临床应用经验的增多,在不久的将来,左室四极导线必将成为CRT治疗的标配。

