粗硫酸镍的提纯工艺研究
吴晓莉
(江西铜业集团公司 贵溪冶炼厂,江西 贵溪 335424)
1 引言
硫酸镍主要用于电镀和高纯镍盐生产的原料,生产上对其杂质元素的含量有严格的要求[1-2]。在铜电解精炼过程中,为稳定电解液的物理化学性质,采用冷冻结晶工艺,定期从铜电解液中分离得到的粗硫酸镍结晶(NiSO4·6H2SO4)含有大量的杂质元素[3](Cu、As、Sb、Bi、Zn、Fe、Co、Ca、Mg、Pb),杂质元素的存在,直接影响粗硫酸镍结晶在电镀和高纯镍盐生产工业中的应用,为使其成分符合国标要求,须对其进行脱杂提纯处理。资料对粗硫酸镍的精制与提纯工艺已有研究[4-7],笔者在前人研究的基础上,采用硫化除杂、氧化水解沉铁钴、氟化除钙镁、萃取除锌工艺对粗硫酸镍进行精制提纯实验,探索了工艺最佳控制条件,分析讨论了影响实验结果的可能因素。
2 实验
2.1 实验试剂与仪器
(1)实验用试剂如下:Na2S(工业级,含量大于60%)、H2SO4、NaOH 分析纯、Cl2、NaF分析纯、P204(D2EHPA)、氨水、磺化煤油等,实验用粗硫酸镍为铜电解液净化过程采用冷冻结晶工艺所得NiSO4·6H2SO4结晶,其成分含量如表1所示。
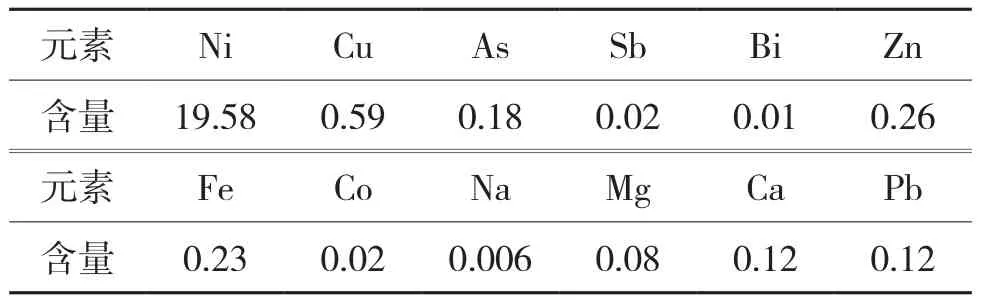
表1 粗硫酸镍成分 %
(2)实验仪器如下:启普发生器、烧瓶、电磁搅拌器、电热炉、集气瓶、烧杯、梨形分液漏斗、滤瓶、真空泵等。
2.2 实验方法
(1)实验流程如图1所示。
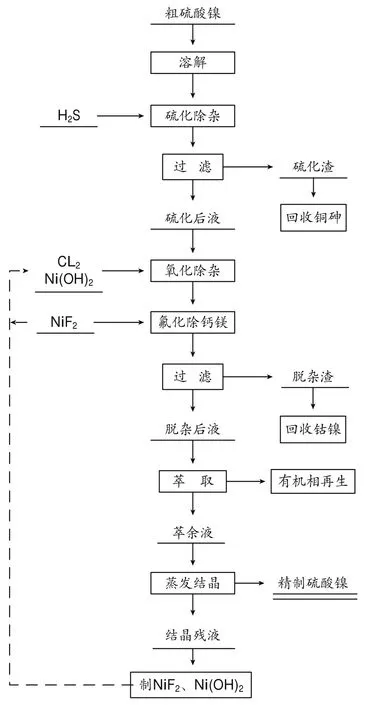
图1 粗硫酸镍提纯实验流程
(2)实验步骤。
①粗硫酸镍用水充分溶解,配得镍浓度大于80g/L的硫酸镍溶液;②硫酸镍溶液于常温常压下,在烧瓶内进行硫化除杂反应,尾气以高浓度NaOH溶液吸收,充分反应后精密过滤,得硫化后液;③硫化后液以Ni(OH)2调节pH值,通Cl2氧化除杂,尾气以高浓度NaOH溶液吸收;④氧化充分后,用Ni(OH)2调节pH值,向浆液中加入NiF2继续反应,充分反应后精密过滤,得脱杂后液;⑤脱杂后液以氨皂化P204萃取除锌,分相后得萃余液;⑥萃余液蒸发浓缩,得精制硫酸镍。
Ni(OH)2与 NiF2用浓缩结晶残液分别与 NaOH溶液和NaF反应制得,使用前水洗脱钠。
3 结果与分析
3.1 硫酸镍溶液的配制
粗硫酸镍加水充分溶解,得到的硫酸镍溶液成分如表2所示。
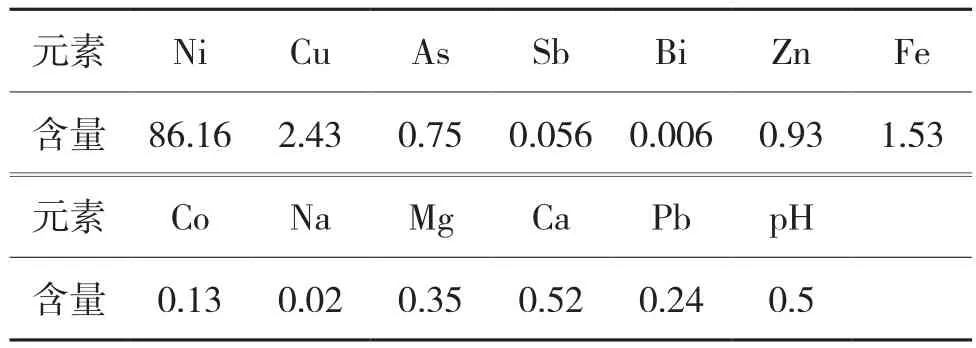
表2 硫酸镍溶液成分表 g/L
3.2 硫化脱杂实验
金属离子硫化物不溶于水(T=293K时,Ksp(CuS)=8.5×10-45、Ksp(As2S3)=4.45×10-22、Ksp(Bi2S3)=1.56×10-20、Ksp(Sb2S3)=1.0×10-18、Ksp(PbS)=6.77×10-13),通过向 pH=0.5 的硫酸镍溶液中通入H2S气体,使铜、砷、锑、铋、铅生成对应的硫化物沉淀,而镍由于在pH=0.5的溶液中不与H2S反应将留在溶液中,从而达到镍与铜、砷、锑、铋、铅分离的目的,其主要反应方程式如式(1)~(6)所示。
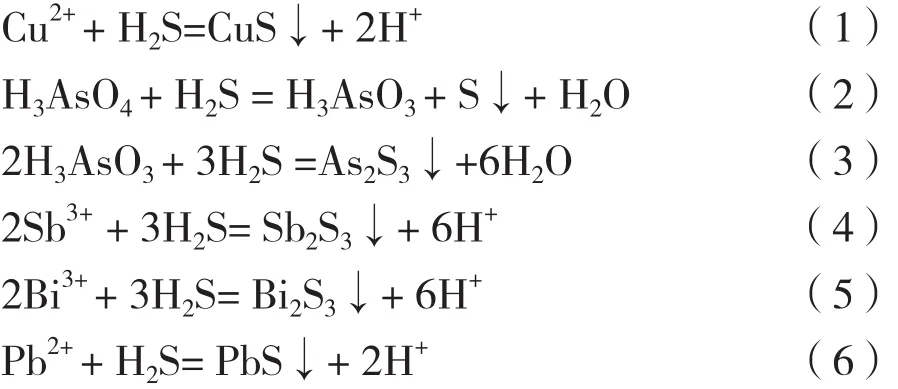
常温常压下,向2000mL硫酸镍溶液中通入H2S气体,控制气体流量2.0L/min,反应时间2h, 所得硫化后液成分如表3所示。
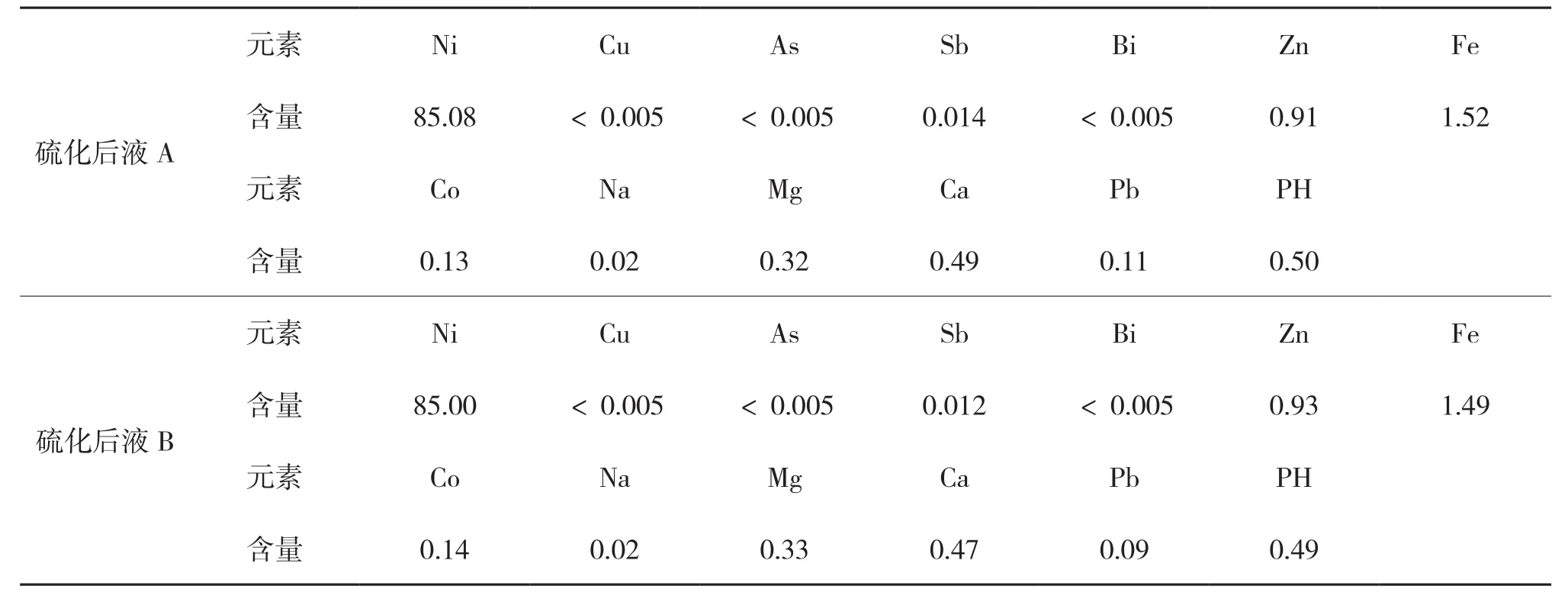
表3 硫化后液成分g/L
由表3可知,采用硫化除杂工艺,以H2S为硫化剂对硫酸镍溶液进行脱杂处理,铜、砷、铋脱除率大于99.9%,硫化后液铜、砷、铋浓度小于0.005g/L,锑脱除率约75%,硫化后液含锑小于0.020g/L,铅脱除率大于50%,硫化后液含铅约0.10g/L,镍直收率98.75%,其他元素含量无明显变化。
3.3 氧化脱杂实验
根据变价金属高价态离子易于水解沉淀的性质,通过向硫化后液中通入强氧化性气体Cl2,把溶液中Fe2+和Co2+全部氧化成Fe3+和Co3+,通过控制溶液 pH 值,使之水解成 Fe(OH)3和 Co(OH)3,从而沉淀脱除,在Cl2通入后,硫化后液中残余的锑、铅也将全部被氧化成高价态离子,进而形成沉淀脱除,其主要反应方程如式(7)~(15)所示。
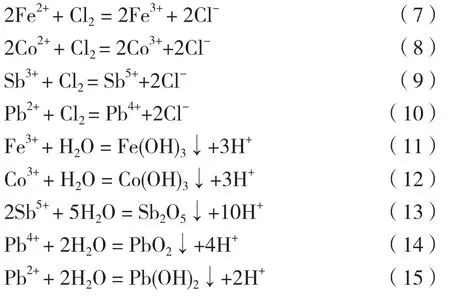
实验控制反应温度70℃,反应时间6h,氧化过程通过加入 Ni(OH)2浆液控制反应 pH=4.5~5.0,反应完成后取氧化液样,其成分如表4所示。
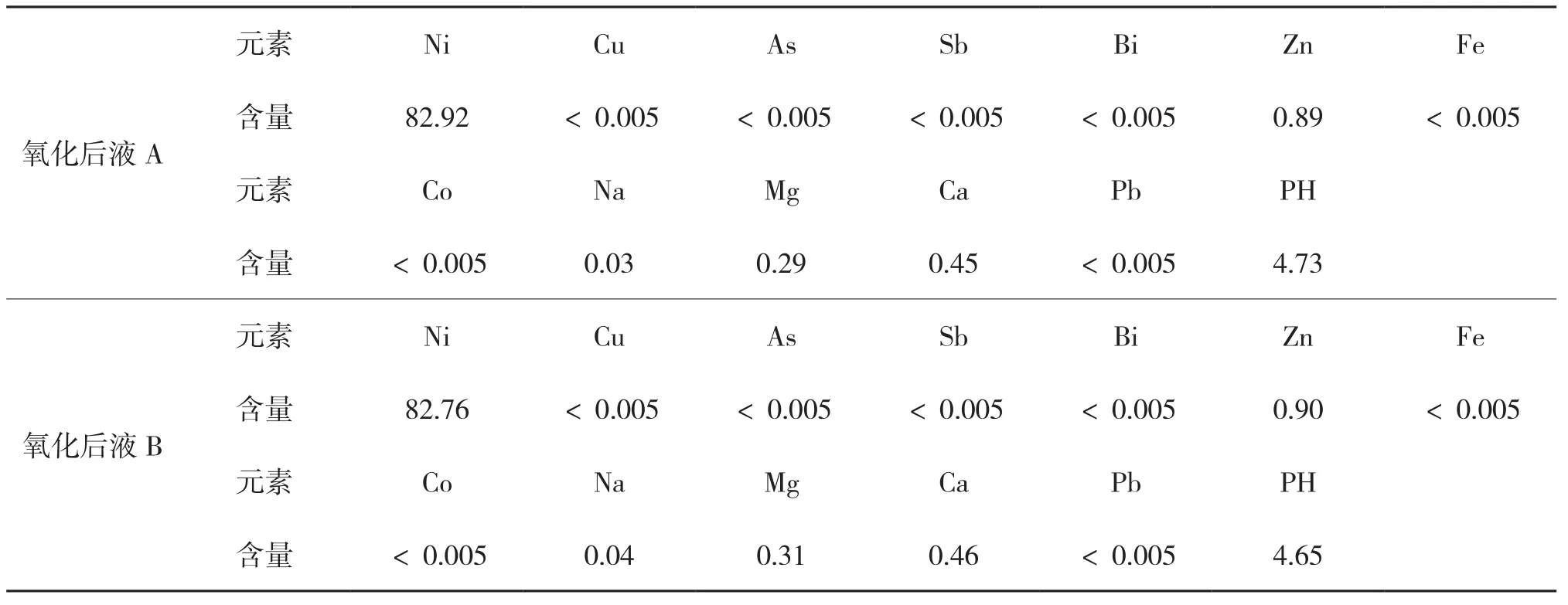
表4 氧化后液成分g/L
由表4可知,采用氧化水解除杂工艺,以Cl2为强化氧化剂处理硫化后液,溶液中铁、钴脱除率大于99.95%,氧化后液中铁、钴含量小于0.005g/L,同时,锑、铅也被脱除至0.005g/L以下,溶液中Ni2+因浓度过高,部分被氧化成Ni3+,进而水解生成 Ni(OH)3,造成镍沉淀损失。
3.4 氟化除钙镁实验
碱土金属氟化物溶度积小(T=293K时,Ksp(CaF2)=3.95×10-11、Ksp(MgF2)=6.4×10-9), 通 过 向氧化浆液中添加NiF2,使Ca2+、Mg2+生成CaF2和MgF2沉淀脱除,其主要反应方程式如式(16)、(17)所示。
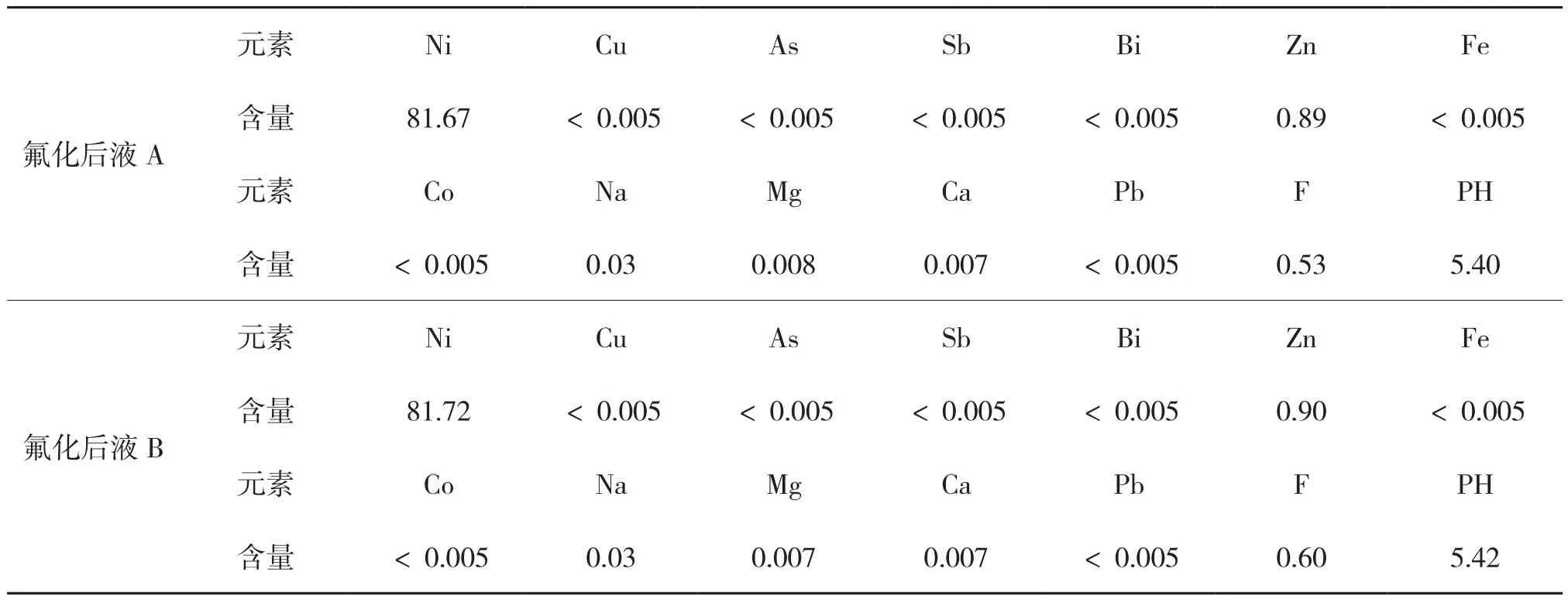
表5 氟化后液成分g/L

实 验 先 以 Ni(OH)2调 节 浆 液 pH5.0~5.5,NiF2按理论需求量1.5倍加入,控制反应温度90℃,反应时间2h,所得氟化后液成分如表5所示。
由表5可知,向氧化浆液中添加NiF2,可以有效地脱除溶液中的Ca2+和Mg2+,Ca2+脱除率98.44%,Mg2+脱除率97.24%,反应后液中Ca2+、Mg22+残余浓度小于0.01g/L,镍直收率95.99%。
3.5 萃取除锌实验
P204在硫酸盐溶液中对某些金属离子的萃取率与平衡pH值关系如图2所示。
由图2可知,在硫酸体系溶液中,通过控制溶液pH值,可使Zn2+优先于Ni2+被P204萃取,从而达到Zn2+、Ni2+分离的目的。
实验控制萃取原液pH4.5~5.0,相比O/A=1∶4,萃取剂浓度15%,皂化率70%,在梨形瓶中进行一级萃取,实验结果如表6所示。
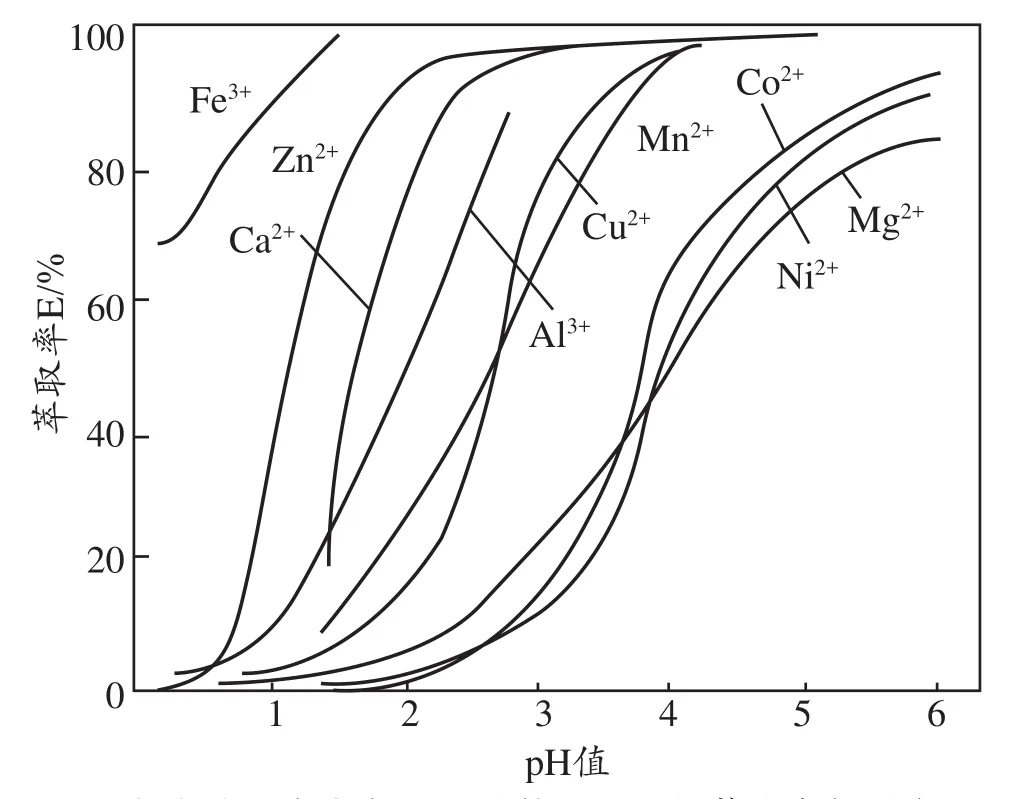
图2 在硫酸盐溶液中P204对某些金属的萃取率与平衡pH的关系

表6 萃余液成分g/L
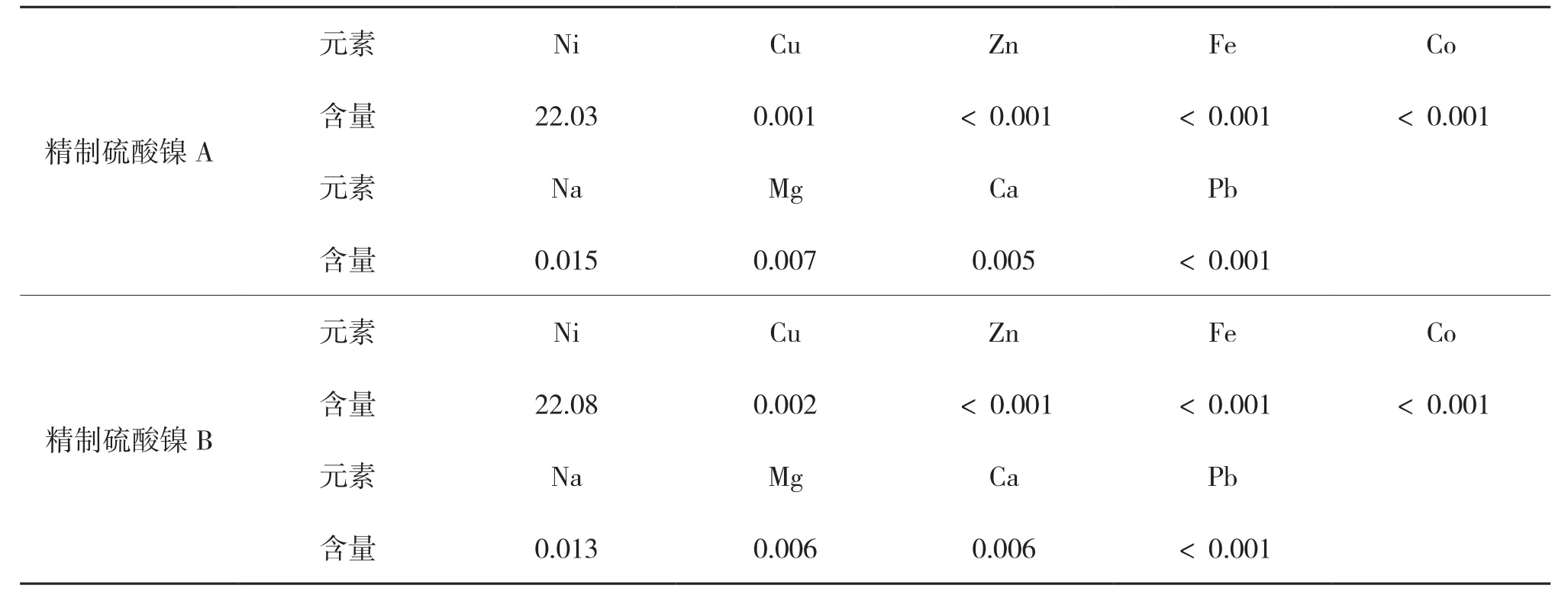
表7 精制硫酸镍成分%
由表6可知,采用萃取工艺,以P204作萃取剂,可以有效地萃除溶液中的Zn2+,Zn2+萃除率大于99.9%,萃余液含Zn2+小于0.005g/L,镍直收率大于98.50%。
3.6 蒸发结晶实验
萃余液蒸发浓缩,至2/5体积,冷却结晶,得到精制NiSO4·6H2SO4结晶,其成分如表7所示。
4 结论
采用“硫化除杂——氧化除铁钴——氟化除钙镁——萃取除锌——蒸发结晶”工艺处理粗硫酸镍结晶,可有效地脱除其所携带的杂质金属,得到的精制硫酸镍主品位大于22.00%,锌、铁、钴、铅含量小于0.001%,铜含量小于0.005%,钠小于0.015%,镁小于0.01%,钙小于0.01%,镍回收率大于93.50%。

