强生干化学分析仪开放通道检测血清淀粉样蛋白A的性能验证
黄 迪,尚陈宇,万泽民,柯培锋
(广东省中医院检验科,广州 510120)
血清淀粉样蛋白A(serum amyloid A,SAA)是一种十分敏感的急性时相反应蛋白,在炎性反应中的浓度会比健康状况下增加1 000倍[1]。SAA可与白细胞计数(WBC)、C反应蛋白(CRP)、降钙素原(PCT)等联合检测,多用于门急诊病人感染的鉴别诊断。近年来呼吸系统感染每年均有暴发出现的情况,临床对该指标越来越重视。SAA试剂盒一般搭载在检验科用于急诊检测的设备上。Ortho干式生化分析仪是美国强生公司生产的临床实验室检测设备,主要用于临床生化、免疫学的常规或急诊检测。Vitros 5.1 FS是该公司近年来推出的首款配备有“湿化学”检测通道的全自动生化免疫一体机。本实验拟在该款仪器进行SAA检测,本文将对其开放通道装载国产SAA试剂的检测性能进行分析、探讨,以期在我院开展该项目并进行后期科学研究。
1 材料与方法
1.1 标本来源 采集于广东省中医院住院、门急诊患者及体检合格的健康人标本,分离胶或肝素锂抗凝,离心后获取无溶血、无脂浊的血清或血浆。所有血清或血浆分管至洁净、干燥的分装管中,仅保留性别、年龄与结果数据,确保无法追踪受检者其他信息。
1.2 仪器与试剂 美国强生Vitros 5.1 FS全自动生化免疫分析仪(简称Vitros 5.1)。宁波普瑞柏生物技术公司胶乳增强免疫比浊法SAA检测试剂盒及配套稀释液、校准品和质控液。
1.3 方法
1.3.1 精密度验证:参考NCCLS EP15-A2文件要求[2]。原装两种浓度质控品,每天采用相同操作各复融1支,连续检测5天。每天每个浓度检测3次,获得两种浓度质控品检测数据各15个,根据公式计算总均值、S批内、S总和验证值[3]。
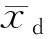
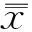
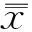

V=D×(n-1)
其中V为自由度,C为根据自由度和测定的浓度水平数查分布表所得百分位点;

其中T为自由度。
建立Levey-Jennings质控图,每天进行室内质控监测。根据Westgard设定失控规则,只有在当天质控在控的情况下,实验数据才有效。
1.3.2 准确度验证:参照卫生部WS/T 420-2013比较试验[4]的方法进行评估。选取20份不同浓度的患者血浆标本,要求覆盖该试剂盒声明的线性范围。分别在Vitros 5.1和另一溯源至参考物质的检测仪器进行检测。两组检测结果进行相关与回归分析。
1.3.3 线性范围验证:参照卫生部WS/T 408-2012线性评价[5]指南进行评估。根据厂家提供的理论线性范围,选取一份接近上限的高值标本H(92.59 mg/L)和一份接近下限的低值标本L(5.99 mg/L),使用专用稀释液,按照一定比例混合10个浓度(1H+9L,2H+8L,3H+7L,4H+6L,5H+5L,6H+4L,7H+3L,8H+2L,9H+1L,H),每个混合物重复检测2次(取均值),以X表示各样本的理论预期值,以Y表示各样本的实测值,进行线性拟合及差异限分析。
1.3.4 最大稀释倍数验证试验[6]:选择在分析测量范围(AMR)上限附近的样品,以专用稀释液进行2,4,6,8,10倍稀释,依据系列稀释浓度计算各系列样品的分析物浓度的预期值。比较各个稀释度样品的检测值和预期值,分别计算比值(R=检测值/预期值)。厂家要求为R≥85%,R<85%的相应稀释度为不可接受稀释度,其上一级别的稀释度即为该测试的最大稀释度。
1.3.5 生物参考区间验证:挑选1~62岁,男女比例大致相等且无基础疾病、表观健康的体检样本共23份为参考个体。统计各参考个体检测值,与试剂说明书参考区间比较,计算比率(r=检测值在引用参考区间的参考个体数/总的参考个体数)。若r≥90%,则验证结果可以接受。
1.4 统计学分析 线性拟合采用Excel软件进行,相关及回归分析、个体分布频率采用SPSS 20.0统计软件进行分析。
2 结果
2.1 精密度验证 见表1。批间精密度和总重复性均小于厂家声明范围,验证通过。

表1精密度验证结果
2.2 准确度验证 见表2。本实验室与对照实验室比对结果见图1。部分诊断切点水平相对误差值(TE%)。

表2部分诊断切点水平相对误差值

图1 准确度验证结果
2.3 线性范围 测量结果及偏差见表3。目测理论值与实测值呈直线相关,进行二元一次拟合见图2。
2.4 最大稀释倍数 见表4。 5个稀释梯度的R比值均大于厂家要求,最大稀释倍数可验证至10倍。

表3线性范围验证数据表

表4梯度稀释测定结果
2.5 参考区间验证 厂家推荐参考区间为0~10 mg/L。23例健康个体中有22例检测结果在厂家声明的参考区间之内,1例超出。检测结果分布见图3。r=95.7%,表明参考区间验证结果可以接受。

图2 线性拟合
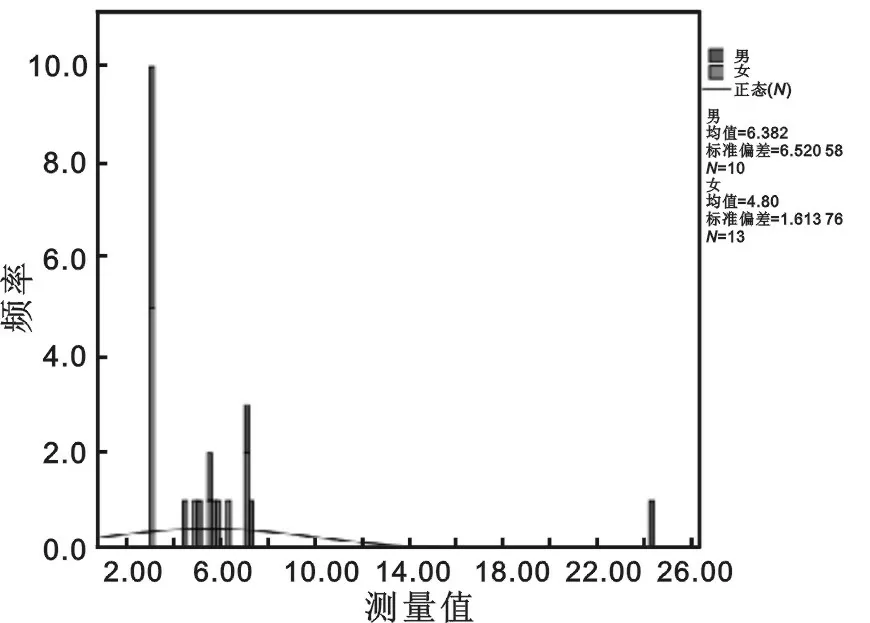
图3 参考个体结果分布图
3 讨论
SAA属于载脂蛋白家族中的异质类蛋白质,相对分子质量约12 000。在急性时相反应中,经IL-1,IL-6和肿瘤坏死因子(TNF)等细胞因子刺激,在肝脏中合成,炎性反应时SAA可与高密度脂蛋白(HDL)结合,形成SAA/HDL复合体,这使得其对巨噬细胞的亲和力增加2~3倍,调节HDL的代谢,对炎症细胞产生趋化作用[7]。文献报道,联合检测SAA和CRP等指标对感染性疾病的鉴别诊断有意义[8~10]。另外,近年来的流行病学研究发现,肥胖、糖尿病、心血管疾病和其他代谢综合症等患者SAA亦显著增高[11,12]。按《医疗机构临床实验室管理办法》和医学实验室ISO 15189《医学实验室质量和能力认可准则》的要求,新的检测系统或指标进行常规工作前应对其分析性能进行验证,以满足预期要求[13]。干式生化分析仪无需纯水,不产废液,使得其在临床实验室常规检测中有着独特优势。但也正因如此,限制了其临床应用范围。Vitros 5.1配备有“湿化学”检测通道,在一定程度上弥补了这一不足,使得市面上质优价廉的液体试剂用于干式生化仪检测成为可能。普瑞柏公司生产的SAA试剂,采用两点终点比浊法进行检测,已在部分知名品牌生化分析仪上使用,本次实验是该公司在干式生化分析仪上进行的首次尝试,对其他有意愿使用该试剂的实验室有一定的参考价值。Vitros 5.1加样、吸试剂以及比色均使用一次性耗材,有效避免了交叉污染和携带污染。所以本文仅进行了精密度、准确度、可报告范围和生物参考区间验证。
精密度是检测系统最基本的分析性能,是其他分析性能评价的基础,其目的是分析实验室内检测系统的精密度情况[14]。精密度不佳,其他性能指标无从谈起。三大性能指标之二是准确度,准确度是指在一定实验条件下多次测定的平均值与真实值相符合的程度,是测量结果中系统误差(正确度)与随机误差(精密度)的综合[15]。方法学比对试验可以用于准确度验证。美国临床实验室标准化委员会(CLSI)于2002年颁布的EP9-A2文件即《用患者样本进行方法学比对及偏倚评估-批准指南》第二版,该指南详细介绍了比对的实验方法[16]。线性范围是另一个很重要的仪器及方法学性能指标,在一定区间内,其能提供测量结果与样本中测量物的量值直接成比例,它允许对样本进行稀释、浓缩或其他预处理[17]。厂家声明的批内CV应≤8%,批间CV应≤10%,换算为标准差分别为S批内≤1.43,S批内≤3.81和S总低≤1.79,S总高≤4.76,本次实验批间精密度和总重复性均符合要求,验证通过。仪器说明书声明的线性范围为5~100 mg/L,在此范围内选取的高、低值样本进行线性验证。根据指南要求,若R2>0.990,则可初步判断厂家提供的线性范围符合要求;统计不同浓度处的值都在厂家声称的浓度误差范围内(±10%),则可直接判断测定方法在实验所涉及的浓度范围内成线性。本次实验R2=0.999 9,实测值与理论值偏差绝对值均<10%,本次线性验证范围为5.99~92.59 mg/L。最大稀释倍数实验5个梯度浓度的比值均≥85%,可认为本次试验的最大稀释倍数10倍也是可靠的。本次实验通过以上性能指标的验证实验,表明该分析系统检测能力能满足临床需求,可以用于实验室常规标本检测。通过对23例参考个体的检测结果进行统计,也验证了厂家说明书的参考区间(≤10 mg/L),实验室可以采纳。
我院临床科室对SAA急诊检测的需求越来越迫切,本实验室正式开展该项目后还需做进一步深入研究。

