Hybrid手术在复杂Stanford B型夹层中的临床应用
王贤灿,尚玉强,李 炳,易 凡,戴仕林,吴 伟,程 龙
临床上根据内膜撕裂后剥离的范围是否累及升主动脉分为Standford A型和Standford B型。我们定义累及主动脉弓部分支血管,导致锚定区不足15 mm的Standford B型夹层为复杂Standford B型夹层。胸主动脉腔内修复术(thoracic endovascular aortic repair,TEVAR)操作相对简单、安全,可以有效封闭破口,恢复远端真腔,对于主动脉夹层的治疗作用已经得到广泛认可[1]。但是,Stanford B型夹层破口多累及主动脉弓部分支血管,单纯的TEVAR术受限于15 mm有效锚定区,不能有效解决此类累及主动脉弓部分支血管的复杂Stanford B型夹层。近年来,随着心脏外科“杂交”(Hybrid)技术的飞速发展,Hybrid技术充分结合TEVAR术和外科By-pass术的优势,达到操作简单化,创伤最小化,疗效最优化[2]。2014年1月—2016年1月武汉市中心医院对87例近端锚定区不足的患者进行Hybrid手术,效果满意,现报道如下。
1 资料与方法
1.1 临床资料 回顾分析2014年1月—2016年1月武汉市中心医院收治87例复杂Stanford B型主动脉夹层的患者进行Hybrid手术,其中,男性68例,女性19例,年龄29~67(54.3±19.7)岁,所有患者均有胸背部剧烈疼痛病史,发病时间2 h~14 d,术前合并高血压 79例(90.8%),糖尿病 17例(19.5%),慢性肾功能不全9例(10.3%),慢阻肺11例(12.6%),术前给予双抗治疗(波立维、阿司匹林)4例(4.6%)。
1.2 方法
1.2.1 术前准备 入院后给予镇静、镇痛、控制性降压、控制心率治疗,完善主动脉计算机断层扫描血管造影(computed tomography angiography,CTA)(飞利浦128排CT、碘海醇注射液)及心脏彩超(飞利浦IE Elite)检查,87例患者均明确诊断为Stanford B型夹层,破口累及主动脉弓部,主动脉瓣未受累。依据Ishimaru锚定区分区法,夹层破口累及Z0区9例,Z1区23例,Z2-3区55例(该组患者破口位于Z3区,但锚定区不足15 mm);87例患者中,Willis环均衡型73例,左椎动脉优势型9例,右椎动脉优势型5例(图1);对11例需要支架覆盖T8-L1的患者行Adamkiewicz动脉CTA三维重建,指导术中精确定位,有效避免Adamkiewicz动脉发出肋间被封闭。
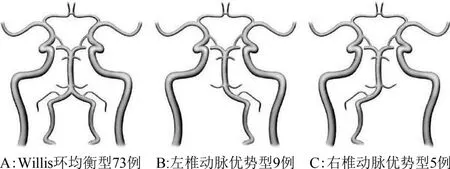
图1 Stanford B型主动脉夹层分型
1.2.2 麻醉 全组患者均在气管插管静脉复合全身麻醉下行Hybrid手术,根据患者夹层破口累及分区情况,决定血管重建策略。
1.2.3 手术方案 (1)Z0区(9例):①正中开胸,夹层破口处上侧壁钳;②行头臂干(brachiocephalic trunk,BCT)转移至升主动脉;③做Y形桥接:BCT与左颈总动脉(left common carotid artery,LCCA)做端侧吻合(BCT-LCCA),BCT与左锁骨下动脉(left subclavian artery,LSA)做端侧吻合(BCT-LSA);④沿BCT吻合口远端行TEVAR术。(2)Z1区(23例):①沿颈部横切口做 By-pass:BCT-LCCA-LSA;②沿BCT远端行TEVAR术。(3)Z2-3区(55例):①沿左颈部斜切口做By-pass:LCCA-LSA端侧吻合或侧侧吻合;②沿LCCA远端行TEVAR术。图2。

图2 破口累及范围
1.2.4 术后随诊 术后早期口服阿司匹林规律抗凝,根据患者基因印记杂交技术,提供患者阿司匹林个体化服药剂量推荐值,避免抗凝不足容易导致血栓形成、旁路血管闭塞[3]以及抗凝过量引起脏器出血、远端夹层破裂。术后3个月、半年、1年随诊主动脉CTA检查,动态观察患者破口闭合情况、分支血管通畅情况、夹层假腔血栓化程度或远端夹层病情进展程度以及支架置入后是否存在移位和形态改变;术后3个月、半年、1年随诊患者椎动脉窃血症状发生情况,左肩背部发冷,左上肢麻木刺痛以及肌力下降等症状的发生情况[4]。
2 结果
本组共87例患者(图3),手术顺利,9例累及Z0区患者,17例术前血氧饱和度明显下降(含11例既往有慢阻肺病史患者),共计26例患者术后带气管插管返回监护病房呼吸机辅助治疗,均于术后次日顺利脱机拔管;其中3例患者术中输血(均为Z0区患者);术后均于次日顺利转出监护病房,并于1周后顺利出院。
术后随访6~48 个月不等,于术后 3、6、12、24 个月来院复查主动脉CTA。术后并发症情况:死亡0例;肾衰3例(3.4%),经透析治疗后,其中2例在2周后恢复肾功能,1例需长期透析治疗;肺部感染5例(5.7%),此5例患者经监测体温、胸片检查及监测血常规明确诊断为肺部感染,经抗感染治疗1周后均痊愈;意识障碍7例(8.1%),患者术后早期出现谵妄、幻视等症状,持续3~5 d,经改善脑循环治疗后均痊愈;脑梗1例(1.1%),该例患者术后1周突发大面积脑梗,经积极治疗后仍存在左侧肢体肌力明显下降;内漏1例(1.1%),该例患者行LCCA-LSA转流+TEVAR术,于术后3个月出现近端内漏,内漏范围局限,患者夹层破口累及LSA,LCCA与LSA距离约5 mm,目前患者远端假腔血栓化,内漏局限,密切监测内漏发展情况。
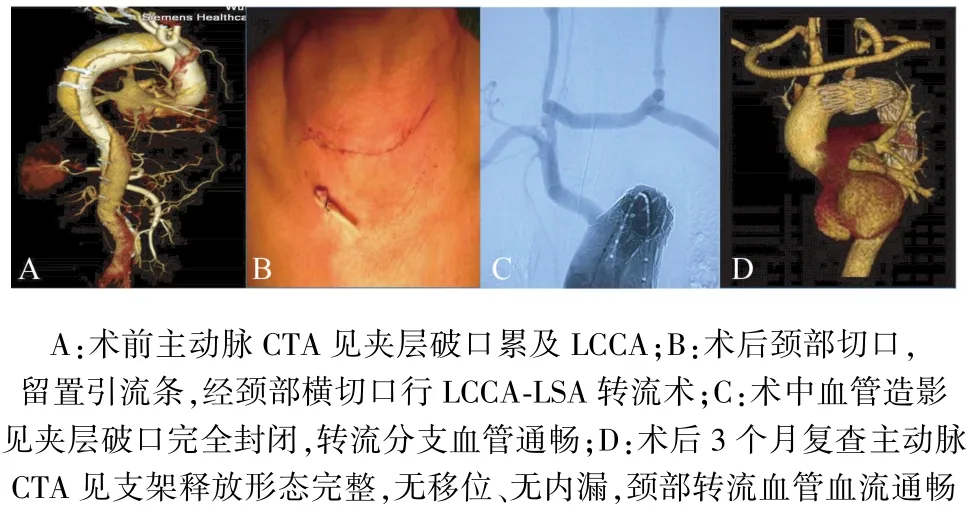
图3 Hybrid手术治疗复杂Stanford B型主动脉夹层
3 讨论
3.1 Hybrid手术的必要性 对于Stanford B型夹层患者,4/5经保守药物治疗,能安全度过急性期,故大部分患者均可采取择期手术;根据临床研究发现,Willis环均衡型占82%,左优势型占11%,右优势型占7%;美国血管外科学会临床指南建议:对于择期手术应该常规重建LSA,以避免LSA和左椎动脉缺血性并发症的发生。对于累及主动脉弓分支血管的Stanford B型夹层患者,目前能重建LSA和左椎动脉血供的方法包括:烟囱技术、开窗技术、带分支支架技术和Hybrid技术[5]。
3.1.1 烟囱技术 实施烟囱技术[6-7]有2个重要条件:①主动脉弓比较陡翘;②靶分支血管与主动脉弓部成角<30度;若主动脉弓部平坦,或靶分支血管与主动脉弓部成角较大,甚至成垂直,则植入的血管支架容易出现近端内漏,而且会影响远期的支架血管通畅率;所以,在采用烟囱技术处理这些主动脉夹层患者的时候,其远期疗效取决于近端内漏与支架锚定长度,之间达成有效平衡。
3.1.2 开窗技术 凭借支架所采用的记忆合金,具备优良的径向张力,在主动脉腔内治疗过程中,能有效将支架贴附于主动脉动脉壁上,起到封堵主动脉内膜破口、防止血流持续灌注主动脉夹层假腔、避免主动脉继续扩张甚至破裂的风险。腔内治疗的2点关键因素为:充分封闭破口,支架形态合适、稳定。而复杂Stanford B型夹层,其分支血管本身已受累,开窗技术破坏了支架的完整性,且对支架的径向扩张度和锚定部位、角度要求高,不仅是手术操作难度大,术后夹层假腔血栓化与支架微小移位,均会导致内漏或分支血管闭塞的风险。
3.1.3 带分支支架技术 该种支架分为主体和支体2部分,颈部分支血管直接供应脑部血流,任何操作或支架移植物的失败都会引发致残性的脑血管并发症,风险极高,因而对这一领域的研究仍处于探索阶段。
3.1.4 Hybrid技术 因弓部手术涉及众多重要血管,常规手术操作复杂,难度极大,一直以来,对于主动脉弓部的外科处理,是外科领域的棘手问题和研究热点。Hybrid技术[8-9]只需在颈部行1~2个小切口,完成主动脉弓部血管的转流,然后应用腔内技术修复胸主动脉病变,既避免了传统手术必需的开胸,又满足了此类患者足够锚定区的要求[10]。
3.2 手术时机的选择 在患者起病后的急性期内(发病后14 d),由于急性期主动脉壁处于炎性反应水肿期,导管导丝操作和支架释放容易造成血管壁的破裂,所以急性期过后再行腔内治疗更安全。近年来镇静、止痛、降压暨控制心率理论的发展,大多数患者可安全度过急性期。
3.3 手术注意事项 术前精确测量主动脉直径,评估破口位置以及破口位置与重要分支血管的解剖关系,选择合适大小与长度的血管支架。血管支架的直径关系到支架释放后与管壁的贴合程度,既能预防内漏,又不至于撑破血管壁;目前临床上一般认为使用直径比主动脉大15%~20%是最合适的。合适的长度关系到满足主动脉破口处足够的锚定区,又不至于覆盖Adamkiewicz动脉引起截瘫。
3.4 并发症的预防
3.4.1 意识障碍 Stanford B型夹层术后患者的意识障碍多表现为意识模糊或谵妄状态,术后3 d~1周多能自行恢复[11]。对于该组夹层患者中,意识障碍的原因与术后体内麻醉药物代谢、术中颈动脉阻断、围术期血压波动等因素有关。针对以上因素,对于全麻患者按体表面积精确给予合适剂量,并优先采用局麻方式;术前根据颈动脉CTA结果,评估Willis环类型,保证颈动脉逐个阻断过程中颅脑的血供充足,同时控制单根颈动脉阻断时间在12 min以内;血压管理方面,术前根据患者意识、神志的临床改变情况,尽可能保持较低水平,术中在颈动脉吻合过程中,在术前血压水平基础上升高10~20 mmHg[12];术后根据患者入院前最适血压水平,酌情控制。
3.4.2 内漏 大量研究结果表明,内漏的持续存在将导致动脉瘤晚期破裂,积极防治内漏有利于改善腔内治疗的远期效果。预防内漏主要有以下措施:①术前根据CTA检查结果,仔细评估夹层破口的位置、形态以及颈部分支血管的解剖结构和受累情况,指导术中精确定位支架位置、形态;②术中谨慎提供手术方案,确定足够、安全的锚定区(>15 mm),选择合适的支架型号(使用直径比主动脉大15%~20%的支架型号),提供个体化颈部血管转流方案;③依据Wheat等提出的降低血压和左室压力上升速率(dp/dt)可以将夹层破裂的危险降至最低的理论,围手术期积极予以控制性降压(患者耐受程度的低血压)、控制心率治疗,对于部分出现内漏患者,予以球囊扩张或放置Cuff。
3.4.3 截瘫 无论传统开放手术还是腔内治疗,截瘫都是备受关注的问题,一旦发生将严重影响患者的远期生活质量。截瘫原因主要由于肋间动脉被覆盖,阻断了Adamkiewicz动脉的血供,引起脊髓缺血所致。Adamkiewicz动脉一般起源于T8~L1之间,理论上在T8以上放置支架是比较安全的。对于术前主动脉CTA检查明确病变需要覆盖T8-L1区域的患者,做行Adamkiewicz动脉CTA三维重建,指导术中精确定位,有效避免Adamkiewicz动脉发出肋间被封闭。同时,该类患者行术中脑脊液测压、术后脑脊液引流,维持脑脊液压力在6~18 cmH2O,防止脊髓灌注压减少导致截瘫[13]。
3.4.4 肾衰 主动脉夹层患者术后发生肾衰主要有2个原因:①夹层累及肾动脉,导致肾脏血流灌注严重减少,TEVAR术后不能缓解肾动脉血供问题,导致肾衰发生;②碘对比剂肾毒性,包括化学毒性(离子性、含碘物质)、渗透毒性及粘滞度相关毒性。在TEVAR术中,预防肾衰的原则,主要从针对以上2个原因开展:①恢复肾动脉血供,根据术中观察肾动脉狭窄程度,选择放置肾动脉支架;②对于存在甲亢等禁忌证的患者,禁用碘对比剂;对于存在碘对比剂使用高危风险的患者,术前估算碘对比剂使用剂量(Max)[剂量=5 W(体重:kg)/Cr(mg/dl)],避免大剂量或短期内重复使用碘对比剂,建议2次对比剂应用间隔时间≥14 d,使用碘对比剂时应充分水化,在使用碘对比剂前6~12 h至使用后24 h内,对患者给予1 500 mL晶体液水化。
3.4.5 远端夹层 由于远端破口常累及腹腔干、肠系膜上动脉、肾动脉和髂动脉等重要分支动脉,使得远端破口的处理显得相当棘手。部分患者假腔内的逆向血流,可以经假腔为分支动脉提供血供,能起到逆灌的作用。但是,持续存在的远端破口及假腔,从患者的心理恐惧以及姑息性临床思维角度,均不是完美的解决方案。目前临床采用的开窗技术、裸支架支撑等姑息性治疗手段,仍存在内漏、远期分支血管闭塞等严重风险;二期胸腹主动脉置换术,因其巨创、手术技巧难度大,临床开展并不广泛;而3D打印分支支架技术尚不成熟,临床技术推广及远期疗效有待进一步考证。
综上所述,Hybrid手术作为治疗复杂Stanford B型主动脉夹层的一种手段,具有微创、安全、有效的策略优势,同时,在处理夹层破口、修复主动脉形态以及恢复重要脏器血供方面具有可靠的临床疗效[14]。根据患者的夹层解剖学范围以及患者的综合条件,选择个性化的Hybrid手术策略[15],是手术成功的关键。

