二水氯化钙中氯化钙含量分析方法探讨
,
(连云港碱业有限公司,江苏连云港 222042)
氯化钙含量是工业二水氯化钙产品的主要指标,其含量的高低直接影响到我厂产品的市场竞争力和经济效益。目前,工业二水氯化钙产品中氯化钙含量测定是采用EDTA配位滴定法,即在试验溶液的pH约为12的条件下,以钙羧酸为指示剂,用EDTA标准滴定溶液滴定钙,该测定方法缓慢,终点易返难掌握,该方法测定CaCl2含量会受到很多条件制约,导致测定误差较大,因此选择在最佳条件下测定氯化钙含量,提高测定准确度对满足用户要求和指导化工操作意义重大。
1 检验方法
1.1 测定原理
在pH=12时,加入钙指示剂,与Ca2+离子形成红色络合物, 随着EDTA试剂的加入,Ca2+离子与EDTA形成更稳定的络合物,终点时完全释放出钙指示剂,溶液呈现纯蓝色,测得Ca2+离子的含量。
1.2 试剂
1.2.1 盐酸:1+3
1.2.2 三乙醇胺:1+2
1.2.3 氢氧化钠:200 g/L
1.2.4C(EDTA):0.02500 mol/L
1.2.5 钙示剂羧酸钠盐指示剂(1+100)
1.3 分析操作步骤
称取样品10 g,精确至0.0002 g,置于250 mL烧杯中,加水溶解全部转移至1 000 mL容量瓶中,混匀,用水稀释至刻度,摇匀。此溶液为试验溶液A,用于氯化钙含量的测定。
移取10 mL试验溶液A置于250 mL锥形瓶中,用盐酸溶液(1+3)调节pH为3~5,加水约50 mL,加5 mL三乙醇胺溶液、2 mL氢氧化钠溶液、约0.1 g钙试剂羧酸钠盐指示剂,用EDTA标准滴定溶液滴定,溶液由红色变为纯蓝色即为终点。消耗EDTA标准滴定溶液体积为V。
试点地区按照《实行最严格水资源管理制度考核办法》(国办发〔2013〕2 号,以下简称《考核办法》)要求,结合当地实际,将水资源管理情况与地方政府绩效挂钩,制定本行政区域内最严格水资源管理制度考核办法,这些办法除了对《考核办法》细化外,还各有特色。河北省增加了地下水开采量指标,监测评估目标还包括万元GDP用水量、城市供水管网漏损率、饮用水水源地水质达标情况。湖北省规定考核实行百分制,其中公众满意率10分,并且考核结果向社会公布。天津市探索建立了水资源管理和河道水生态环境管理行政首长负责制,把考核任务分解到基层,区县长、乡镇长作为第一责任人对所辖河道水生态环境管理负总责。
同时做空白试验。空白试验除不加试样外,其它操作加入的试剂均与试验溶液相同。消耗EDTA标准滴定溶液体积为V0。
1.4 结果计算
氯化钙含量以氯化钙(CaCl2)的质量分数W1计,数值以%表示。
式中:V——滴定试验溶液消耗EDTA标准溶液的体积,单位为毫升(mL);
V0——空白试验消耗EDTA标准溶液的体积,单位为毫升(mL);
C——EDTA标准滴定溶液浓度,单位为摩尔每升(moL/L);
m——称取的试样质量,单位为克(g);
M——氯化钙的摩尔质量,单位为克每摩尔(g/moL)(M=111.0);
W2——测得的碱度以Ca(OH)2计的质量分数,数值以%表示;
取平行测定结果的算术平均值为测定结果,两次平行测定结果的绝对差值不大于0.2%。
2 几种分析过程的影响
2.1 样品粒度大小的影响
在氯化钙包装口取氯化钙样品,充分混匀后分成两份,一份充分研细,此样品为1#样;另一份保持原样片状,按第1.3节的测定步骤测定样品中氯化钙含量,两份样各测定八平行,结果统计如表1。
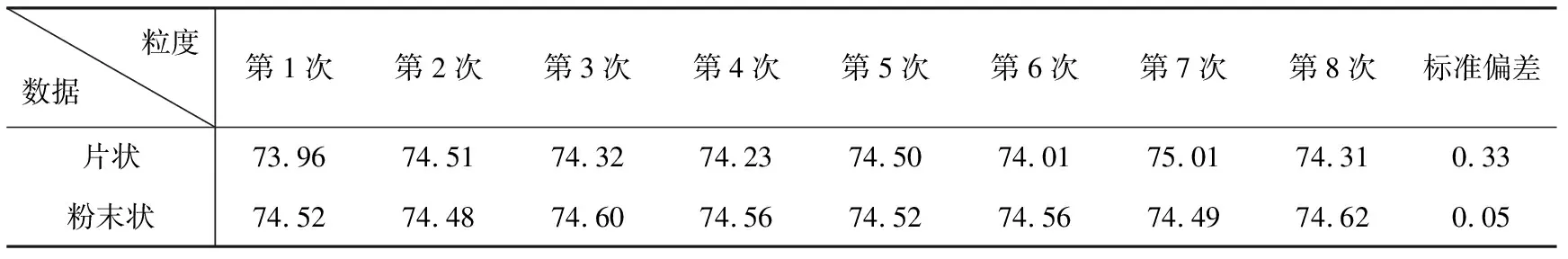
表1 不同粒度下测定的氯化钙含量
从以上数据可以看出,颗粒较大的片状试样测定结果重现性不好,且两次平行测定结果的绝对差值有的大于0.2%,不能满足测定要求;而粉末状试样测定结果精密度较好,两次平行测定结果的绝对差值均小于0.2%,满足试样测定要求。
2.2 滴定速度的影响
在pH=12时,试样中Ca2+与EDTA发生1∶1配位反应,配位反应速度比中和反应、沉淀反应速度偏慢,滴定过程中如果滴定速度偏快,容易造成局部EDTA浓度偏高,过早夺取氯化钙与钙试剂形成配合物中Ca2+,游离出蓝色指示剂颜色,终点过早出现。
每天在氯化钙包装口取一个氯化钙样品,充分混匀研细,置于1 000 mL的干燥磨口瓶中,连续7天取7样品,分别为2#~8#样品。按第1.3步骤用不同滴定速度测定1#~8#样品中氯化钙含量,测定结果如表2。
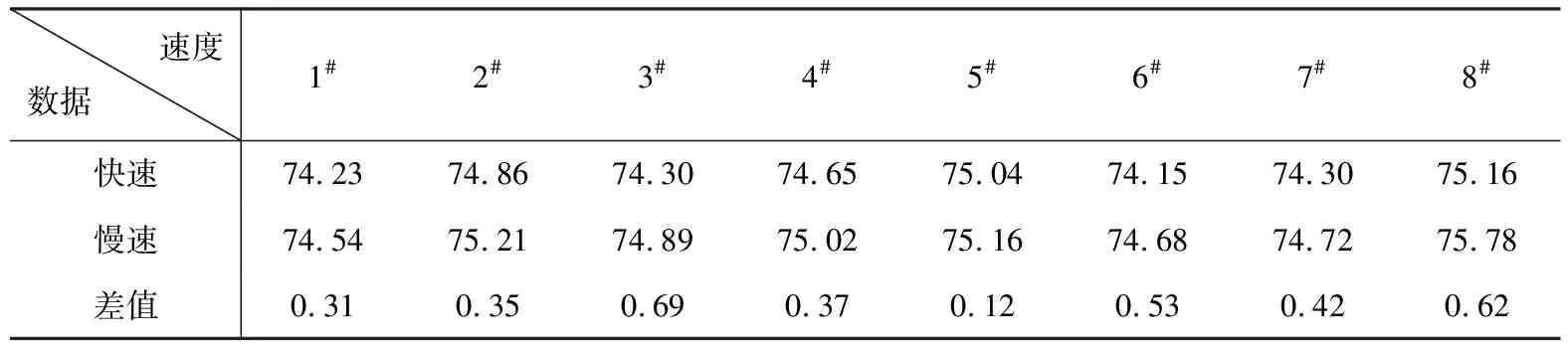
表2 不同滴定速度下测定的氯化钙含量
从表2可以看出滴定速度快慢,对测定结果影响较大,滴定速度偏快测定结果偏低,所以在滴定过程中速度不能偏快,接近滴定终点时更应一滴一滴地滴加EDTA标准溶液。滴定速度偏快时变色时间容易偏长,到达滴定终点后溶液颜色易返回紫色。
2.3 三乙醇胺用量的影响
EDTA具有很强配位能力,能与很多种金属离子形成稳定的配合物。在pH=12时测定试样中氯化钙含量,需要用三乙醇胺掩蔽溶液中干扰离子,防止干扰离子与EDTA、钙羧酸指示剂发生反应,保证EDTA与Ca2+发生定量反应。因此三乙醇胺加入的量的多少会对测定结果有影响。
试验中取1#样品做平行测定,按第1.3节的步骤溶于1 000 mL容量瓶中,取10.00 mL试液,在加入的步骤中分别加入三乙醇胺3 mL、5 mL、7 mL测定氯化钙含量,空白试验也加入对应量的三乙醇胺。测定的氯化钙含量如表3。
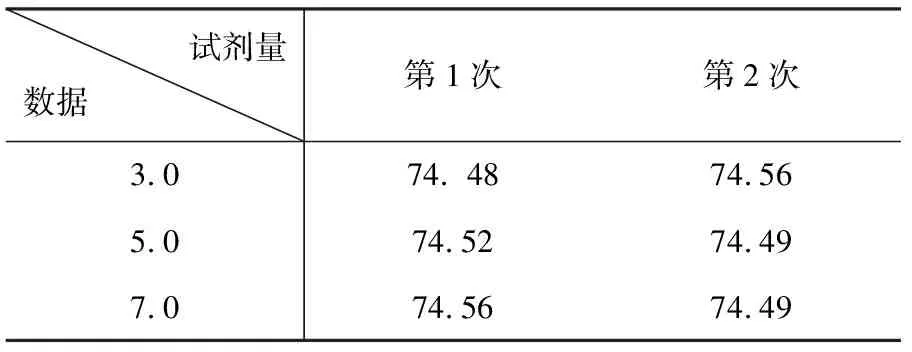
表3 不同量三乙醇胺下测定的氯化钙含量
由表3可以看出加入不同量三乙醇胺测定结果没有变化。所以在考虑生产质量波动时,二水氯化钙中氯化钙含量在合格品时的情况,选择加入5.0 mL三乙醇胺适宜。
2.4 溶液酸度的影响
在测定试样中氯化钙含量时,移取10.00 mL试样A置于250 mL锥形瓶中,用盐酸溶液调节试样pH为3~5,加水约50 mL,再加入三乙醇胺。这时溶液的pH值必需为3~5的弱酸性,如果酸性太强,与后面加入的2 mL氢氧化钠溶液发生中和反应,消耗较多的氢氧化钠溶液,实际上氢氧化钠的量不足2 mL,氢氧化钠控制溶液pH值达不到要求,滴定时其它干扰离子容易与EDTA发生配位反应,影响测定结果准确度。三乙醇胺是在碱性溶液中掩蔽Fe3+,如果溶液呈中性或碱性,已水解的金属离子不易被三乙醇胺掩蔽,与指示剂发生反应,产生指示剂封闭或僵化现象,或终点不明显,造成测定误差,影响测定结果准确度,所以在操作过程中控制溶液pH为3~5。
3 精密度的试验
按照第1.3步骤对1#、2#样各平行测定5次,测定结果如表4。
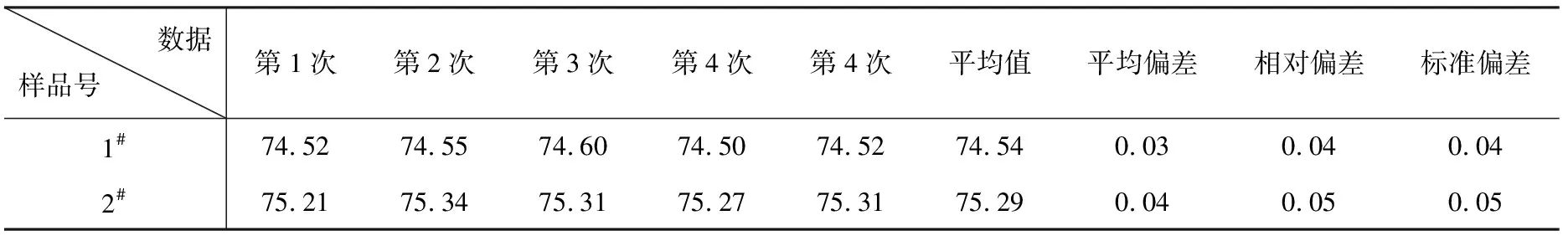
表4 精密度的试验
由表4可以看出,分析结果的精密度较高,能满足氯化钙生产中对氯化钙含量的控制要求,起到指导生产作用;同时满足工业氯化钙GB/T26520-2011标准6.4.4节,测定结果取平行测定结果的算术平均值,两次平行测定结果的绝对差值不大于0.2%的要求,能够严把产品销售质量关。

