N-(5-芳基-1,3,4-噁二唑-2-基)-N'-α-萘氧乙酰基硫脲的合成及生物活性
孙光文,覃章兰
(1.湖北三峡职业技术学院,湖北 宜昌443000;2.华中师范大学化学学院,湖北 武汉430079)
含氮杂环农药的开发研究仍是当今农药创制的重点之一[1]。而酰基硫脲和1,3,4-噁二唑类化合物具有较强的杀菌、杀虫活性[2-5]。为了设计合成生物活性更强的化合物,作者按照活性因子叠加的原理,在前文[6-7]工作基础上,将α-萘氧基、1,3,4-噁二唑引入到酰基硫脲中,合成了10个新的具有较好生物活性的化合物。
目标化合物的合成路线如下:
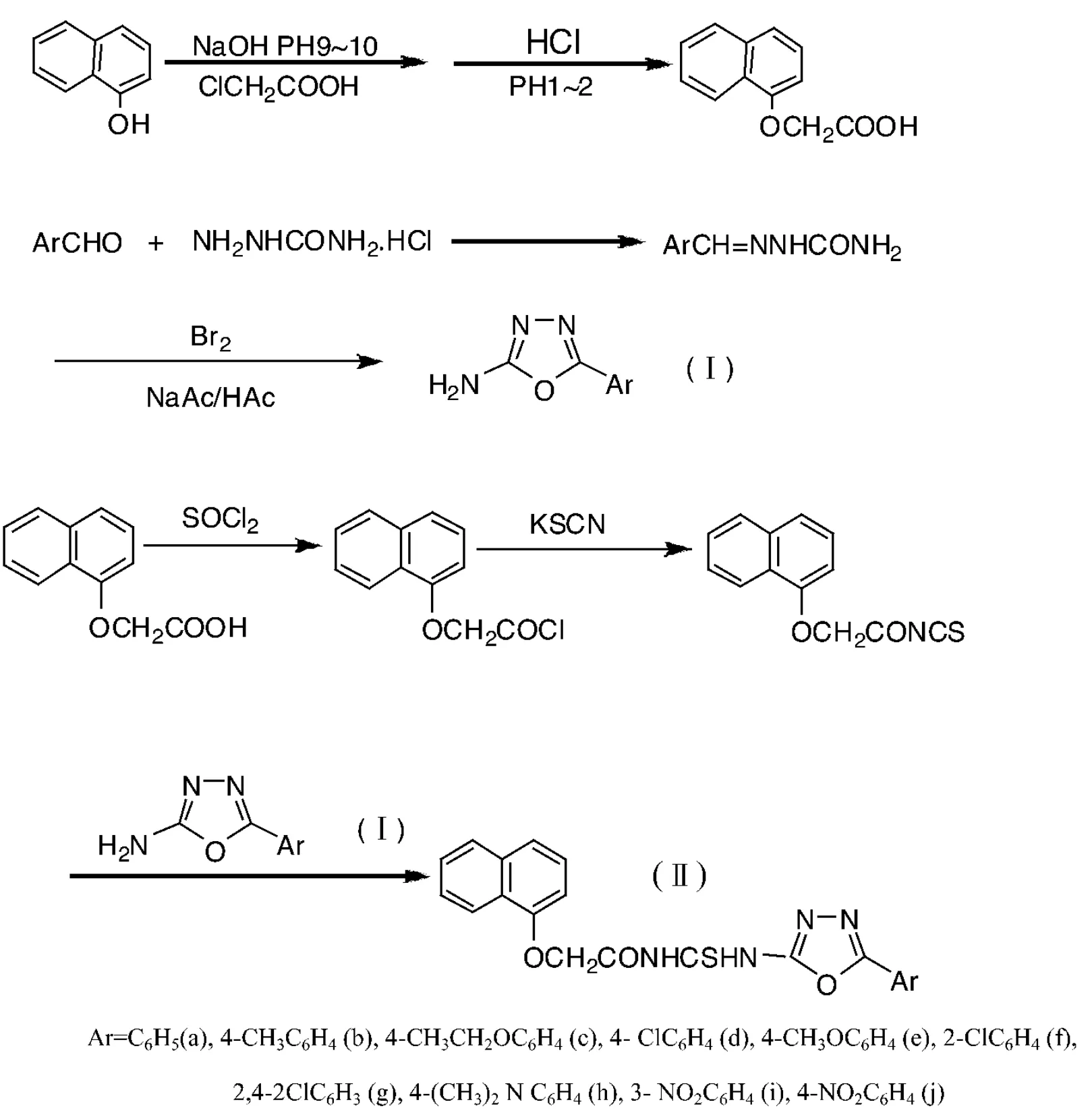
1 实验部分
1.1 仪器和试剂 PE-983红外光谱仪(Perkin-Elemer公司);400型400MHz核磁共振仪(Varian Mercury公司,TMS为内标);Perkin-ElemerCHN2400元素分析仪;X4型熔点测定仪(温度计未校正,北京第三光学仪器厂);HP-5988A质谱仪(惠普公司)。试剂均为市售分析纯和化学纯。
1.2 α-萘氧乙酸的合成 合成方法参照文献[8][9]。
1.3 2-氨基-5-芳基-1,3,4-噁二唑(Ⅰ)的合成 合成方法参照文献[10]。
1.4 目标化合物(Ⅱ)的合成 在50mL三颈烧瓶中加入5mmolα-萘氧乙酸,搅拌下加入5mL二氯亚砜,升温至75℃,反应6h。减压蒸出剩余的二氯亚砜,得黄色油状液体。直接向反应瓶中加入6mmol硫氰酸钾(KSCN)的乙腈溶液(约15mL),反应0.5h后过滤,向滤液中加入4mmol化合物(Ⅰ),70℃下反应4~10h。冷却,过滤的固体物质用少量乙酸乙酯和石油醚混合物洗涤,然后用乙醇-DMF重结晶即得目标化合物(Ⅱ)。所得化合物多数为淡黄色或黄色固体。
2 结果与讨论
2.1 产物的结构表征 目标化合物Ⅱa~Ⅱj为淡黄色或黄色固体,不溶于水,微溶于乙醇、丙酮,能溶于DMF、DMSO中,在室温下能稳定存在。其分子式、物理性质、产率及1HMR,IR,MS和元素分析等数据如下:
Ⅱa:C21H16N4O3S,淡黄色固体,产率68.2%,m.p.216~218℃;1HNMR(d6-DMSO,400MHz)δ:12.10(s,1H,NH),6.82~8.31(m,12Ar-H),5.15(s,2H,CH2);IR(KBr)ν:3384(NH),3071(NH),1723(C=O),1608(C=N),1252(C=S);MS(m/z,%):188(5.16),145(100),128(7.22),118(11.29),92(18.52),77(9.18);Elem.Anal.Calcd.:C 62.36,H 3.99,N 13.85;Found:C 62.55,H 3.79,N 13.80。
Ⅱb:C22H18N4O3S,黄色固体,产率62.0%,m.p.209~211℃;1HNMR(d6-DMSO,400MHz)δ:12.04(s,1H,NH),6.85~8.33(m,11Ar-H),5.13(s,2H,CH2),2.38(d,3H,CH3);IR(KBr)ν:3377(NH),3058(NH),1728(C=O),1592(C=N),1238(C=S);MS(m/z,%):202(6.73),159(71.16),128(6.35),118(17.50 ) 91(100 ), 76(14.95 );Elem.Anal.Calcd.:C 63.14,H 4.34,N 13.39;Found:C 63.01,H 4.22,N 13.50。
Ⅱc:C23H20N4O4S,黄色固体,产率53.6%,m.p.169~172℃;1HNMR(d6-DMSO,400MHz)δ:12.08(s,1H,NH),6.86~8.40(m,11Ar-H),5.17(s,2H,CH2),4.10(s,2H,OCH2),1.35(s,3H,CH3);IR(KBr)ν:3390(NH),3064(NH),1726(C=O),1606(C=N),1260(C=S);MS(m/z,%):232(4.40),149(91.09),128(5.69),121(100),119(28.73 ), 93(20.54 ), 76(14.45 );Elem.Anal.Calcd.:C 61.59,H 4.49,N 12.49;Found:C 61.66,H 4.37,N 12.53。
Ⅱd:C21H15ClN4O3S,黄色固体,产率48.3%,m.p.206~208℃;1HMNR(d6-DMSO,400MHz)δ:12.13(s,1H,NH),6.93~8.52(m,11Ar-H),5.14(s,2H,CH2);IR(KBr)ν:3371(NH),3062(NH),1724(C=O),1602(C=N),1266(C=S);MS(m/z,%):303(13.10),198(6.29),145(12.17),127(8.67),121(100 ), 103(34.35 ), 76(43.70 );Elem.Anal.Calcd.:C 57.47,H 3.44,N 12.77;Found:C 57.31,H 3.54,N 12.76。
Ⅱe:C22H18N4O4S,黄色固体,产率57.6%,m.p.195~196℃;1HNMR(d6-DMSO,400MHz)δ:12.06(s,1H,NH),6.80~8.28(m,11Ar-H),5.12(s,2H,CH2),3.82(s,3H,OCH3);IR(KBr)ν:3362(NH),3047(NH),1722(C=O),1610(C=N),1258(C=S);MS(m/z,%):218(15.30),198(8.10),145(19.70),127(3.83),107(100),77(36.95);Elem.Anal.Calcd.:C 60.82,H 4.18,N 12.90;Found:C 60.70,H 4.35,N 12.84。
Ⅱf:C21H15ClN4O3S,黄色固体,产率50.8%,m.p.205~207℃;1HNMR(d6-DMSO,400MHz)δ:12.14(s,1H,NH),7.01~8.45(m,11Ar-H),5.18(s,2H,CH2);IR(KBr)ν:3374(NH),3062(NH),1724(C=O),1587(C=N),1264(C=S);MS(m/z,%):303(16.58),197(5.71),161(89.31),144(23.35),128(5.66),120(100),103(43.47),76(50.16);Elem.Anal.Calcd.:C 57.47,H 3.44,N 12.77;Found:C 57.36,H 3.50,N 12.81。
Ⅱg:C21H14Cl2N4O3S,黄 色 固 体,产 率46.9%,m.p.236~238℃;1HNMR(d6-DMSO,400MHz)δ:12.16(s,1H,NH),7.04~8.52(m,10Ar-H),5.19(s,2H,CH2);IR(KBr)ν:3379(NH),3066(NH),1725(C=O),1596(C= N),1259(C=S);MS(m/z,%):302(7.76),257(4.60),197(5.07),144(17.63),128(7.61),120(100),103(34.58),77(15.40);Elem.Anal.Calcd.:C 53.29,H 2.89,N 11.84;Found:C 53.08,H 2.94,N 11.90。
Ⅱh:C23H21N5O3S,黄色固体,产率61.4%,m.p.219~221℃;1HNMR(d6-DMSO,400MHz)δ:12.09(s,1H,NH),6.88~8.36(m,11Ar-H),5.16(s,2H,CH2),2.78(s,6H,N(CH3)2);IR(KBr)ν:3387(NH),3070(NH),1726(C=O),1602(C=N),1247(C=S);MS(m/z,%):231(5.70),197(4.55),145(19.80),128(7.34),120(100),118(13.04),76(23.22);Elem.Anal.Calcd.:C 61.73, H 4.73, N 15.65; Found: C61.58, H 4.87,N 15.70。
Ⅱi:C21H15N5O5S,黄色固体,产率56.7%,m.p.208~210℃;1HNMR(d6-DMSO,400MHz)δ:12.13(s,1H,NH),6.98~8.39(m,11Ar-H),5.16(s,2H,CH2);IR(KBr)ν:3394(NH),3059(NH),1724(C=O),1614(C=N),1253(C=S);MS(m/z,%):232(7.88),198(3.90),144(22.64),128(9.20),122(100),119(28.25),76(18.32);Elem.Anal.Calcd.:C 56.12,H 3.36,N 15.58;Found:C 56.26,H 3.24,N 15.51。
Ⅱj:C21H15N5O5S,黄色固体,产率54.5%,m.p.202~204℃;1HNMR(d6-DMSO,400MHz)δ:12.14(s,1H,NH),7.01~8.45(m,11Ar-H),5.18(s,2H,CH2);IR(KBr)ν:3391(NH),3060(NH),1729(C=O),1616(C=N),1255(C=S);MS(m/z,%):231(4.10),198(5.43),145(25.66),127(4.36),121(100),119(14.30),76(16.70);Elem.Anal.Calcd.:C 56.12,H 3.36,N 15.58;Found:C 56.02,H 3.47,N 15.59。
在4-硝基苯氧乙酸的合成反应过程中,PH值要始终保持在9~10,否则合成产率不高,容易导致失败。同时,反应完成后,浓盐酸的酸化PH要在1~2为宜。
在4-硝基苯氧乙酰氯合成的过程中一定要保证实验体系无水,且硫氰酸钾(KSCN)与4-氟苯氧乙酰氯的投料摩尔比为1.2:1时有利于反应的进行,可使4-硝基苯氧乙酰氯尽可能的转化成异硫氰酸酯,减少下一步加成反应中副反应的发生,便于(Ⅰ)与目标产物的分离。
2.2 抑菌活性测试 采用平皿生长速率法对6种植物病原菌(棉花枯萎病菌Fusarium oxysporium、水稻纹枯病菌Rhizatonia solani、黄瓜灰霉病菌Botrytis cinereapers、小麦赤霉病菌Gibberella Zeae、苹果轮纹病菌Dochiorella gregaria、玉米小斑病菌Biopolaris mayalis)进行了抑菌活性测试。用含毒培养基培养病菌,以病菌升长速度的快慢来判断药剂的抑菌活性大小,用公式(1)计算抑菌率。

结果(表1)表明:在50mg/L下,有6个化合物对水稻纹枯病菌抑制效果较好,抑制率达50%以上;大部分化合物对黄瓜灰霉病菌和小麦赤霉病菌抑制效果优于对照商品醚菌酯;特别是Ⅱe对苹果轮纹病菌抑制率达91.3%。由抑菌活性结果发现,苯环上含有对甲氧基总体抑菌活性较好。
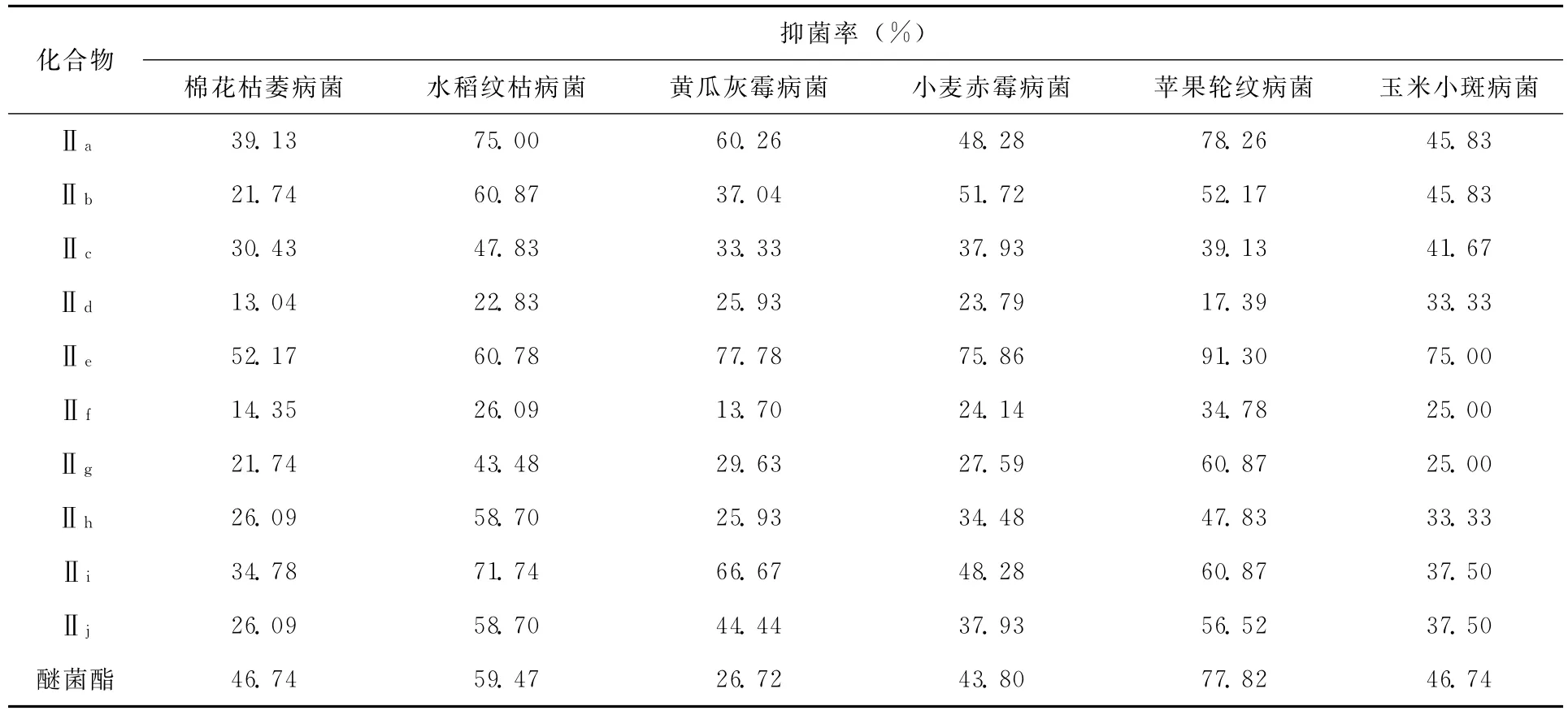
表1 化合物Ⅱ抑菌活性测试 (50mg/L)

