幕上胶质母细胞瘤术后头皮下异位播散转移1例报道*
邹德伟,王俊伟,汪 攀,潘金玉,吴 南
(陆军军医大学附属西南医院神经外科,重庆 400038)
胶质母细胞瘤是恶性程度最高的胶质瘤,一般认为胶质母细胞瘤颅外转移比较少见。现将本科收治的1例幕上胶质母细胞瘤术后转移至皮下的病例,报道如下。
1 病例资料
患者女,24岁,2011年10月22日因发作性意识障碍3次,头痛1月入院,头颅MRI示:右侧顶叶占位,考虑胶质瘤。
第1次手术:2011年10月27日行手术切除肿瘤,术后病理显示:胶质母细胞瘤(WHO Ⅳ级),GFAP(+),Ki67 5%,S-100(+),Olig2散在(+),MGMT散在(+),Vim(+),EMA(-)。术后放疗30次,采用尼莫司汀125 mg化疗4次。

A:第1次手术前;B:第1次手术后3个月;C:第1次手术后2年零4个月
图1第1次手术头颅MRI图像
第2次手术:2015年7月患者出现头痛呕吐,左侧肢体无力,头颅MRI示右侧顶叶胶质瘤复发,于2015年8月12日再次手术治疗,术后病理示:胶质母细胞瘤(WHO Ⅳ级),GFAP(+),CK(-),Ki67 20%,S-100(+),Olig2(+),MGMT(+),Vim(+),EMA(+),CD34(+)。术后给予替莫唑胺化疗15个疗程。
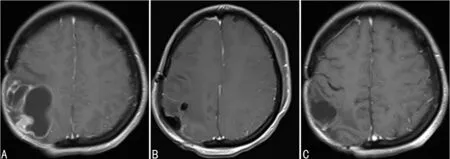
A:第2次手术前;B:第2次手术后第2天;C:第2次手术后4个月
图2第2次手术头颅MRI图像
第3次手术:2016年11月患者再次出现头痛左侧肢体无力,头颅MRI示:右侧顶叶囊实性占位,考虑肿瘤复发,于2016年12月16日行第3次手术,术后病理结果显示:间变型室管膜瘤(WHO Ⅲ级),GFAP(+),CK(-),Ki67 12%,S-100(+),Vim(+),EMA(+),IDH1(-),NeuN(-),Nestin(+)。术后继续给予替莫唑胺化疗7个疗程。

A:第3次手术前;B:第3次手术后第3天;C:第3次手术后3个月
图3第3次手术头颅MRI图像
第4次手术:2017年9月患者再次出现头痛,左侧肢体无力,头颅MRI示:右侧顶叶、右侧脑室后角病变,考虑肿瘤复发,于2017年9月15日行第4次手术治疗,术后病理示:高级别源性胶质瘤(WHO Ⅲ级),GFAP(+),Olig-2(-),NeuN(-),CK(-),Ki67 10%,S-100(+),P53弱(+),EMA(-),IDH1(-),Nestin(+),分子检测:BrAF基因突变,IDH野生型,未检测到TERT基因启动子突变。术后继续给予替莫唑胺化疗8个疗程。

A、B、C:第4次手术前;D、E:第4次手术后第6天;F:第4次手术后3个月
图4第4次手术头颅MRI图像
第5次手术:2017年12月底患者右侧顶部切口旁,头皮下颅骨外出现一包块,质韧,不可活动,该包块在随后4个月内逐渐增大,于2018年4月28日行第5次手术切除皮下包块,术后病理示:间变型多形性黄色星型细胞瘤(WHO Ⅲ级)-BrAF-V600E基因突变,GFAP(-),P53(-),Nestin(++),Olig-2(+),NeuN(+),CK(-),Ki67 20%,CD68(-),CD34(-),S-100(++),Vim(+),EMA(±),分子检测BrAF-V600E基因突变。术后继续予替莫唑胺化疗3个疗程至今。
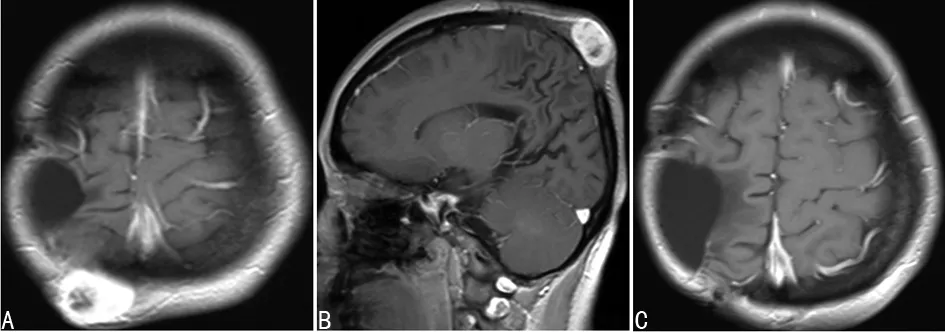
A、B:第5次手术前;C:第5次手术后2个月
图5第5次手术头颅MRI图像
2 讨 论
胶质细胞瘤是中枢神经系统最常见的、预后较差的原发性恶性肿瘤,对于胶质瘤的治疗仍是以手术为主,辅以放疗、化疗以及分子生物学治疗等。由于胶质细胞瘤呈浸润性生长,脑胶质瘤瘤周水肿带均有肿瘤细胞浸润[1],手术难以做到全切,因此胶质瘤术后复发概率很高。肿瘤病理分级越高,恶性程度也越高,术后复发的时间间隔也越短,预后也越差。该例患者第1次手术病理结果为胶质母细胞瘤(WHO Ⅳ级),术后多次复发,且复发时间间隔逐渐缩短。
复发的胶质瘤手术后再复发概率高、间隔时间短,手术可能损害患者的重要功能区,造成患者生存质量低下,因此胶质瘤术后复发是否再次手术治疗尚有争议[2]。近年来随着显微外科技术的提高,更多的学者主张对于复发胶质瘤以手术为主联合放化疗及分子生物学治疗,可以提高患者生存质量、延长生存期[3]。该例患者年龄较小,患者及家属依从性较好,肿瘤多次复发后均采取以手术为主的治疗方案,取得了较好的效果,延长了患者的生存期。
2/3的胶质母细胞瘤复发位于原发肿瘤边缘2 cm内[4],其余小部分复发肿瘤远离原发部位,极少数会出现向颅外转移。近年来胶质母细胞瘤中枢神经系统外转移的报道逐渐增多,但其具体转移机制仍不能明确。文献报道的转移病例中绝大多数为手术后患者,所以认为外科手术可能会增加胶质母细胞瘤转移的风险[5]。胶质瘤手术,尤其是深部胶质瘤手术,为保护正常脑组织,常需要对肿瘤进行分块切除,这可能会增加人为种植和播散转移的机会,术中进入脑室系统可能会使肿瘤细胞随脑脊液播散转移。有文献报道临近脑脊液通路上胶质瘤通过脑脊液播散的概率更高[6],NARAYAN等[7]曾报道胶质瘤术后行脑室腹腔分流导致胶质瘤腹腔转移的病例。另外,胶质母细胞瘤本身和针对肿瘤的放化疗可能导致血脑屏障的破坏,也可能为胶质瘤发生转移提供有利条件。本文中所报道患者肿瘤多次复发并行多次手术,其中肿瘤侵犯脑室系统,手术中脑室系统开放,并形成皮下积液,考虑头皮下播散肿瘤经脑脊液种植和播散可能性大。
对于胶质母细胞瘤的患者应增加复查频率,术后每3个月复查1次头颅增强MRI,出现神经系统症状时应及时检查 MRI,肿瘤复发或播散后,如早期发现可再次手术治疗,最大可能的延长患者生存期。肿瘤组织转移和播散可能是通过多种途径进行的,应尽可能避免手术因素造成肿瘤转移和播散。手术时应尽可能完整切除肿瘤,注意保护脑室系统,手术结束前对术区加强冲洗,减少肿瘤颅外转移的可能性。

