乙酸乙酯-乙腈-1-丁基-3-甲基咪唑磷酸二丁酯盐物系等压气液相平衡数据的测定及关联
张志刚,张德彪,李文秀,杨 茹,杨树元,张亲亲
(1.沈阳化工大学 化学工程学院,辽宁 沈阳 110142;2.内蒙古科右前旗乌兰河自然保护区管委会,内蒙古 科右前旗 137400)
乙酸乙酯和乙腈在一些制药和化学生产过程中会共存[1-3],两者在常压下即可形成共沸点,常规的精馏方法很难实现二者的有效分离。萃取精馏是特殊精馏的一种,并且是工业中最 常采用的一种分离方式,它结合了溶剂萃取和蒸馏的优点。萃取精馏过程中夹带剂的选取是极其重要的[4]。离子液体作为一种绿色的夹带剂已受到学者的广泛关注[5-7]。迪建东[8]以正己烷为夹带剂,利用间歇共沸精馏的方法分离乙酸乙酯和乙腈。马文婵等[9]以水为夹带剂分离乙酸乙酯和乙腈,但存在夹带剂分离回收困难等问题。Li等[10-12]探究了离子液体1-乙基-3-甲基咪唑三氟甲磺酸盐([EMIM][OTf])、1-丁基-3-甲基咪唑三氟甲磺酸盐([BMIM][OTf])、1-辛基-3-甲基咪唑六氟磷酸盐([OMIM][PF6])和1-丁基-3-甲基咪唑六氟磷酸盐对乙酸乙酯和乙腈二元物系的作用。Zhu等[13]探究了离子液体1-乙基-3-甲基咪唑双三氟甲基磺酰亚胺盐,1-己基-3-甲基咪唑双三氟甲基磺酰亚胺盐对乙酸乙酯和乙腈二元物系的作用。对比实验结果表明,几种离子液体作用效果相当,且都能在离子液体浓度较低的情况下将共沸点完全消除。
本工作在101.3 kPa下,对乙酸乙酯-乙腈-1-丁基-3-甲基咪唑磷酸二丁酯盐([BMIM][DBP])三元物系的等压气液相平衡数据进行测定,并与Aspen软件中NRTL模型进行关联,探讨了[BMIM]·[DBP]等多种离子液体对乙酸乙酯-乙腈二元物系的气液相平衡的影响。
1 实验部分
1.1 主要试剂
乙酸乙酯、乙腈:分析纯,中国国药集团有限公司;离子液体[BMIM][DBP]:纯度不少于98%(w),实验室自制,按照专利[14]报道的方法合成,采用卡尔费休滴定法测定离子液体中水含量为 447×10-6。
1.2 仪器和测定方法
采用改进的北洋化工实验设备公司CE-2型平衡釜测定气液相平衡数据[15]。试样均通过重量分析,天平精度0.000 1 g。将配置好的乙酸乙酯与一定量的离子液体共50 mL混合溶液加入到平衡釜中,然后分次加入乙腈与等量离子液体的混合溶液。应用精确校准过的水银温度计对气液相平衡温度进行 测量,其标准不确定度为0.01 K。每一次加热沸腾后温度保持30 min,温度不变则可认为已达到气液相平衡状态,记录平衡温度,然后用微量进样器分别从气相和液相采样口进行采样分析。
采用Agilent公司GC7890A型气相色谱仪分析试样组成,TCD检测,温度为473 K,载气为氢气,流量为45 mL/min,DB-WAXETR型毛细管柱(30 m×0.32 mm×1 μm),柱温340 K,气化室温度453 K。
2 结果与讨论
2.1 实验装置可靠性检验
实验测定的乙酸乙酯-乙腈的二元气液相平衡数据见表1。

表1 在101.3 kPa下乙酸乙酯(1)-乙腈(2)二元等压气液相平衡数据Table 1 Isobaric vapor-liquid equilibrium(VLE) data for the binary system of ethyl acetate(1) + acetonitrile(2) at 101.3 kPa
将实验数据与文献[3]对比,结果见图1。由图1可知,实验数据与文献数据吻合较好,表明本工作所使用的设备和方法是可靠的。

图1 在101.3 kPa下乙酸乙酯(1)-乙腈(2)二元物系的气液相平衡曲线Fig.1 x1-y1 diagram for the binary system of ethyl acetate(1) +acetonitrile(2) at 101.3 kPa.
采用Herington积分法[16]来验证实验测定的二元数据的热力学一致性,结果见图2。

图2 热力学一致性检验Fig.2 Thermodynamic consistency test.
由图2可知,实验所测得的乙酸乙酯和乙腈二元数据满足热力学一致性检验(|D-J|=0.435<10)。
2.2 三元气液相平衡数据
实验测定了乙酸乙酯(1)-乙腈(2)-[BMIM]·[DBP](3)三元等压气液相平衡数据,结果见表2。
2.3 模型关联
采用Aspen软件中NRTL模型关联二元和三元气液相平衡数据,NRTL模型对含有离子液体系统的数据关联有良好的适用性[17]。相关非随机性因素和二元能量参数见表3。

表2 101.3 kPa下乙酸乙酯(1)-乙腈(2)-[BMIM][DBP](3)三元等压气液相平衡数据Table 2 Isobaric VLE data for the ternary system of ethyl acetate(1) + acetonitrile(2) + 1-butyl-3-methylimidazolium dibutylphosphate([BMIM][DBP])(3) at 101.3 kPa

表3 相关非随机性因素和二元能量参数Table 3 Related non-random factors and binary energy parameters
2.4 [BMIM][DBP]对气液相平衡的影响
图3为101.3 kPa下乙酸乙酯(1)-乙腈(2)-[BMIM][DBP](3)三元等压气液相平衡曲线。由图3可知,离子液体[BMIM][DBP]的加入对乙酸乙酯表现出了很明显的盐析效应,使乙酸乙酯在气相中的含量增加,当离子液体摩尔分数达到0.05 时可完全消除共沸。

图 3 101.3 kPa下乙酸乙酯(1)-乙腈(2)-[BMIM][DBP](3)三元等压气液相平衡曲线Fig.3 Isobaric VLE diagram for the ternary system of ethyl acetate(1) +acetonitrile(2) +[BMIM][DBP](3) at 101.3 kPa.
图4为101.3 kPa下离子液体[BMIM][DBP](3)对乙酸乙酯(1)-乙腈(2)相对挥发度的影响。由图4可知,离子液体[BMIM][DBP]的加入可显著提高乙酸乙酯对乙腈的相对挥发度,且离子液体含量越高效果越明显。
2.5 离子液体性能对比
图5为x3= 0.1时不同离子液体(3)对乙酸乙酯(1)-乙腈(2)气液相平衡的影响。由图5可知,四种离子液体对于乙酸乙酯-乙腈共沸体系分离效果相当,都能打破共沸现象。然而从经济效益上对比发现,磷酸酯盐离子液体([BMIM][DBP])与六氟磷酸盐离子液体离子液体([OMIM][PF6])相对于三氟甲磺酸盐离子液体([EMIM][OTf])具有显著的优势,而从离子液体合成角度来看,离子液体[OMIM][PF6]相比于[BMIM][DBP]的制备周期长,合成过程复杂,更为重要的是离子液体[OMIM][PF6]中含有氟原子会产生HF气体,从而对环境有负面影响[18]。综上所述,离子液体[BMIM][DBP]最适合作为分离乙酸乙酯-乙腈共沸体系的夹带剂。
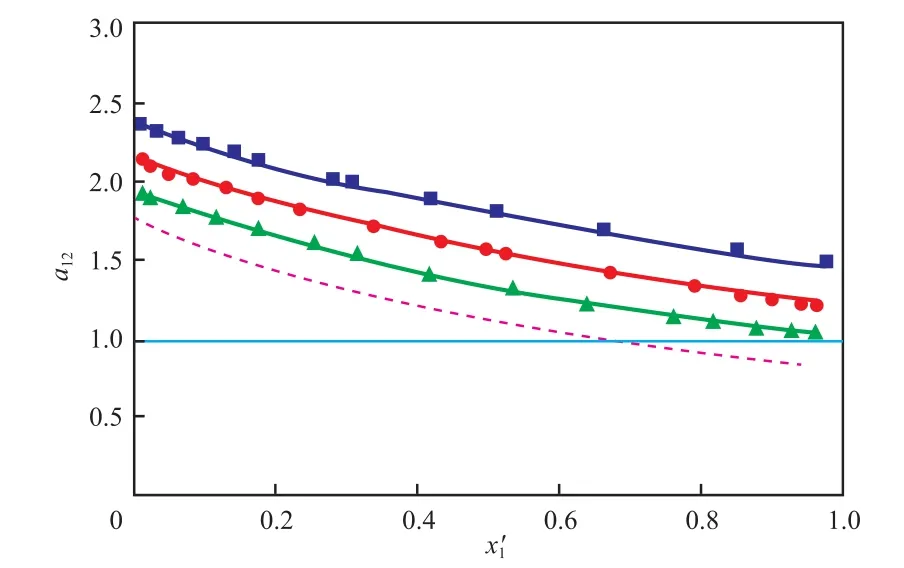
图4 101.3 kPa下离子液体[BMIM][DBP](3)对乙酸乙酯(1)-乙腈(2)相对挥发度的影响Fig.4 Effect of [BMIM][DBP] on the relative volatility of ethyl acetate(1) and acetonitrile(2) at 101.3 kPa.

图5 x3 = 0.1时不同离子液体(3)对乙酸乙酯(1)-乙腈(2)气液相平衡的影响Fig.5 Comparison of the effects of different ionic liquids(3) on the isobaric vapor-liquid equilibrium of ethyl acetate(1)-acetonitrile(2)system at x3=0.1.
3 结论
1)在101.3 kPa下,测定了乙酸乙酯-乙腈二元和乙酸乙酯-乙腈-[BMIM][DBP]三元气液相平衡数据。[BMIM][DBP]能够明显提高乙酸乙酯对乙腈的相对挥发度,且当其摩尔分数达到0.05时就能够彻底使共沸现象消失。
2)采用NRTL模型关联实验所得的气液相平衡数据,回归结果与实验数据具有很好的一致性。
3)[BMIM][DBP]更适合作为分离乙酸乙酯-乙腈体系的夹带剂。

