视黄醇X受体小分子配体衍生物对宫颈癌细胞周期及细胞凋亡的影响
张小丽,涂许煌,谢国斌,蒋福全,张晓坤
(厦门大学药学院,福建厦门361102)
核受体(nuclear receptors)是广泛分布在真核生物体内的一大类蛋白转录因子超家族[1].根据其天然配体的不同,核受体主要分为三大类:类固醇激素受体、非类固醇激素受体和孤儿核受体[2].视黄醇X受体(RXR)是非类固醇激素受体家族的一员,属于配体依赖型转录因子.RXR在核受体中具有重要且独特的作用,许多其他核受体通过与RXR形成二聚体来发挥生理功能[3].RXR在机体内具有广泛的生物学作用,与配体结合后被激活、识别并与DNA上特定的应答元件结合,调控靶基因转录,参与调节机体的生长发育、新陈代谢、免疫、细胞增殖、分化等多种生理病理学过程[4];其表达、定位或功能异常均会导致严重的人类疾病,如生殖系统疾病、代谢性疾病、神经退行性疾病、肿瘤等[5],而RXR的小分子配体能够通过调控其功能而治疗疾病[6].因此,RXR是药物开发的重要靶点.
生物体内细胞周期分为G0/G1、S、G2和M期,其调控是决定细胞命运如增殖、生长、分化等一系列生物学过程的基本机制.细胞周期受到许多监管机制的严格调控,有多个基因和蛋白参与,形成复杂的正、负反馈调控的分子信号系统,周期蛋白依赖性蛋白激酶(CDK)及其负调控因子在细胞周期调控中发挥重要作用[7].肿瘤的发生发展与肿瘤细胞周期的异常调控有关[8].很多临床常用的抗肿瘤药物如氟尿嘧啶、甲氨蝶呤、依托泊苷、长春新碱等,通过诱导肿瘤细胞周期阻滞进而诱导肿瘤细胞凋亡[9].许多新型靶向抗肿瘤药物也是作用于肿瘤细胞增殖周期,通过靶向细胞周期的关键蛋白发挥抗肿瘤效应[10-11].因此,细胞周期阻滞类化合物在抗肿瘤药物开发中具有重要意义.
已有研究发现RXRα可参与调节细胞周期相关蛋白的表达,进而调控细胞增殖[12].本实验室前期报道了一种RXRα的小分子配体XS-23,该化合物可结合于RXRα表面的共调节因子结合位点(图1),通过抑制肿瘤细胞中tRXRα(RXRα的N端截短片段)/PI3K/Akt 生存通路的激活,诱导多种肿瘤细胞凋亡[13].为进一步开发XS-23,本实验室对XS-23进行结构改造和优化,合成了一系列衍生物,初期检测衍生物的生物活性时发现部分衍生物能够明显影响细胞周期,这可能是RXRα新的作用机制.本研究以人宫颈癌HeLa细胞为模型,对XS-23部分衍生物(图2)进行细胞周期活性筛选,以期从中筛选出作用于细胞周期进而诱导HeLa细胞凋亡的化合物.
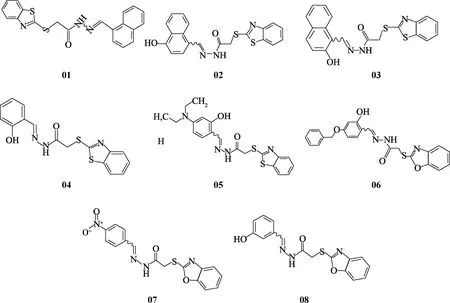
图2 XS-23衍生物的结构Fig.2 Chemical structures of XS-23 derivatives

图1 XS-23与RXRα结合模式的分子对接Fig.1 Proposed binding mode of XS-23 with RXRα by molecular docking
1 材料与方法
1.1 材 料
1.1.1 细胞株
人宫颈癌HeLa细胞来源于ATCC(American Type Culture Collection).
1.1.2 药品与试剂
供筛选的化合物(纯度>98%)由厦门大学药学院药物化学实验室合成提供;聚腺苷二磷酸核糖聚合酶(poly ADP-ribose polymerase,PARP)、细胞M期周期蛋白Cyclin B1(D5C10)、p21 WAF1/CIP1 (12D1)抗体购自CST公司;β-actin抗体购自Sigma公司;RXRα(D-20)抗体购自Santa Cruz公司;偶联辣根过氧化物酶的山羊抗鼠、山羊抗兔二抗购自Millipore公司;脂质体2000购自Thermo公司;MEM/EBSS培养基、胎牛血清购自Gibco公司;含100 U/mL链霉素和青霉素的双抗母液购自Hyclone公司;增强型化学发光(ECL)底物购自APG Bio公司;BCA蛋白分析试剂盒购自Pierce公司;4′,6-二脒基-2-苯基吲哚(4′,6-diamidino-2-phenylindole dihydrochloride,DAPI)购自Roche公司;Annexin V-FITC/碘化丙啶(PI)凋亡检测试剂盒购自BD Biosciences公司.
1.1.3 仪器设备
3111型CO2细胞培养箱、Multiskan FC型酶标仪购自Thermo公司;5424型低温离心机、5424R型常温离心机、A00-1-1102型流式细胞仪购自Beckman公司;MK2000-2型干式恒温器购自杭州奥盛仪器有限公司;PowerPac200电泳仪购自Bio-Rad公司.
1.2 方 法
1.2.1 细胞培养
HeLa细胞用含10%(体积分数)胎牛血清,含100 U/L链霉素和青霉素的MEM/EBSS培养基于37 ℃、5%(体积分数)CO2培养箱中培养,取对数生长期的细胞进行实验.
1.2.2 细胞转染siRNA
当细胞密度达满盘的70%左右时,转染前用不含血清、不含双抗的新鲜MEM/EBSS培养基为细胞换液,在2 mL离心管中分别用适量的培养基稀释双链siRNA、siControl(20 μmol/L)和脂质体2000,5 min后混合siRNA和脂质体溶液(siRNA和脂质体2000的体积比为2∶1),室温放置20 min,使siRNA-脂质体复合物形成,混匀后逐滴加入细胞培养液,4 h后更换新鲜的完全培养基,干扰48~72 h后收集样品.
1.2.3 蛋白免疫印迹(Western blotting,WB)分析
化合物处理后收集的细胞用磷酸盐缓冲液(PBS)洗2次,细胞培养板置于冰上,加蛋白裂解液(50 mmol/L Tris-HCl(pH 7.4)、150 mmol/L NaCl、5 mmol/L乙二胺四乙酸、1%(体积分数)NP-40、0.005 g/mL脱氧胆酸钠、0.001 g/mL十二烷基磺酸钠(SDS),含蛋白酶抑制剂混合物和磷酸化酶抑制剂),收集细胞于1.5 mL离心管中,冰上裂解30 min;4 ℃、12 000 r/min离心10 min,取上清;用酶标仪于560 nm下测定蛋白浓度后,吸取上清加入5×SDS loading buffer,之后置于干式恒温器中,100 ℃沸水浴5 min,常温10 000 r/min离心30 s后上样,或置于-20 ℃冻存备用.用12%(质量分数,下同)的SDS变性聚丙烯酰胺凝胶进行电泳分离蛋白(分离PARP及其切割蛋白用8%),90 V转膜1.5 h;用TBST(10 mmol/L Tris-HCl(pH 8.0),150 mmol/L NaCl,0.05%(体积 分数)Tween 20)配制5%(质量分数)脱脂牛奶,封闭1 h;一抗(1∶1 000稀释)4 ℃孵育过夜(大于8 h),用TBST洗3次,每次10 min;二抗室温孵育1 h,用TBST洗3次,每次10 min;加ECL底物,暗室中胶片曝光、显色.
1.2.4 细胞周期分析
胰酶消化后收集细胞,2 000 r/min离心3 min,弃去培养液;PBS洗2次,2 000 r/min离心3 min,弃去PBS,加入70%(体积分数)冷乙醇4 ℃固定过夜;2 000 r/min 离心5 min,弃去固定液,用PBS洗1次,2 000 r/min 离心5 min,弃去PBS,加入400~500 μL DAPI染色液(1 μg/mL),常温染色10 min;200目以上的筛网过滤,转至流式检测管,用流式细胞仪PB450通道收集细胞,检测细胞周期.
1.2.5 Annexin V-FITC/PI检测细胞凋亡率
胰酶消化后收集细胞,4 ℃、2 000 r/min离心3 min,弃去培养液;用预冷的PBS洗2次,2 000 r/min离心3 min,弃去PBS;用1×binding buffer 500 μL重悬细胞,加入5 μL Annexin V-FITC,混匀,室温(25 ℃)下避光孵育10 min;再加5 μL PI,混匀,室温下避光孵育5 min;流式细胞仪检测,1 h内完成.
1.2.6 统计学分析
使用SPSS 23.0软件进行统计分析,计量数据以平均值±标准差表示,两两比较采用t-检验,p<0.05为差异显著.
2 结果与分析
2.1 化合物活性筛选
对XS-23衍生物(01~08)的活性进行初步筛选.用10 μmol/L化合物分别处理细胞6 h,通过WB检测HeLa细胞中p21 WAF1/CIP1(细胞周期G1期检验点蛋白/CDK抑制蛋白,下文简称p21)和Cyclin B1的表达水平,分析化合物对细胞周期的影响.结果显示,与对照二甲基亚砜(DMSO)相比,化合物05和06可以引起p21表达上调和Cyclin B1表达下调,而其余化合物无明显影响(图3),说明化合物05和06可能具有阻滞肿瘤细胞周期的活性.
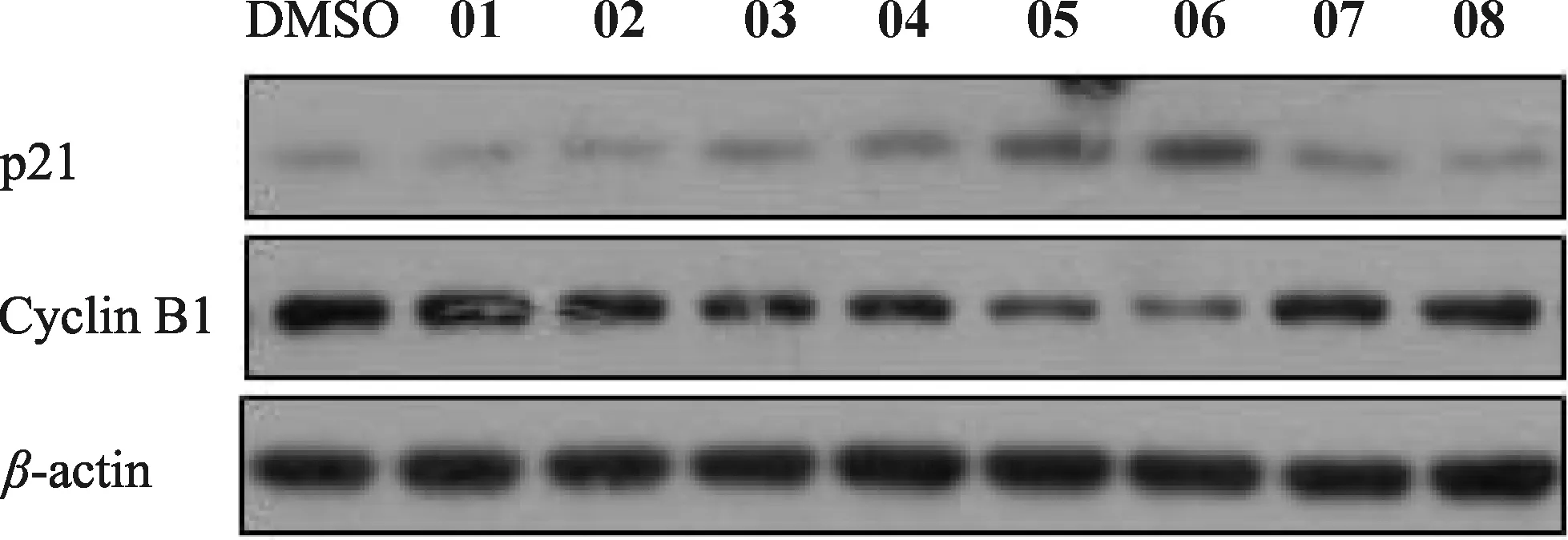
图3 XS -23衍生物的初步筛选Fig.3 Preliminary screening of XS -23 derivatives
2.2 化合物05和06导致人宫颈癌HeLa细胞周期阻滞于G0/G1期
为了进一步检测化合物05和06对HeLa细胞周期的影响,采用流式细胞术检测细胞周期的变化.结果显示:与DMSO相比,用化合物05和06(10 μmol/L,6 h)处理后G0/G1期细胞比例显著上升(p<0.05),同时G2/M期细胞比例显著下降(p<0.05)(表1,图4),说明化合物05和06可以造成HeLa细胞周期阻滞于G0/G1期,且效果明显.

图4 化合物05和06对HeLa细胞周期的阻滞作用Fig.4 Cell cycle arresting effect on HeLa cells by compounds 05 and 06

处理G0/G1SG2/MDMSO69.37±0.458.33±0.1422.04±0.460582.69±0.32*7.89±0.499.30±0.46*0681.02±0.80*8.19±0.4810.38±0.32*
注:*与对照(DMSO)比较,p<0.05,下同.
2.3 化合物05和06对细胞周期阻滞作用的RXRα依赖性
如图5所示:化合物05和06作用于HeLa细胞后,WB检测结果显示p21表达水平显著上调(p<0.05);而用siRNA瞬时干扰RXRα的表达后,化合物05和06引起p21表达水平上调的作用减弱,与DMSO相比无显著差异(p>0.05),说明化合物05和06对细胞周期的阻滞作用在一定程度上依赖于RXRα.
2.4 化合物05和06诱导HeLa细胞凋亡
为了进一步探讨化合物05和06是否具有诱导HeLa细胞凋亡的作用,应用Annexin V-FITC/PI检测凋亡细胞,并应用WB检测PARP蛋白切割情况(PARP切割蛋白出现则表示细胞开始凋亡).不同浓度(10和20 μmol/L)的化合物作用于HeLa细胞24 h后,流式细胞仪检测结果显示:化合物05和06均可导致HeLa细胞凋亡,且随化合物浓度增加,凋亡细胞数目逐渐升高(图6);10 μmol/L化合物05、20 μmol/L化合物05、10 μmol/L化合物06和20 μmol/L化合物06处理下,细胞凋亡率依次为(16.59±1.84)%,(21.20±2.06)%,(13.31±0.89)%和(16.73±0.69)%,与DMSO组(3.15±0.31)%相比均有显著性差异(p<0.05).WB检测结果显示,化合物05和06均可造成HeLa细胞中PARP蛋白切割,且切割效率存在浓度依赖性(图7).上述结果说明化合物05和06具有诱导HeLa细胞凋亡的作用.
2.5 化合物05和06诱导HeLa细胞凋亡作用的RXRα依赖性
siRNA瞬时干扰实验结果显示:与对照(DMSO)相比,干扰RXRα表达后,化合物05和06引起的PARP切割蛋白水平均有所下降(图8),说明化合物05和06诱导HeLa细胞凋亡的作用在一定程度上依赖于RXRα.
2.6 计算机模拟化合物05和06与RXRα的可能结合位点

图5 化合物05和06的细胞周期阻滞作用对RXRα的依赖性Fig.5 RXRα-dependent cell cycle arresting effect of compounds 05 and 06
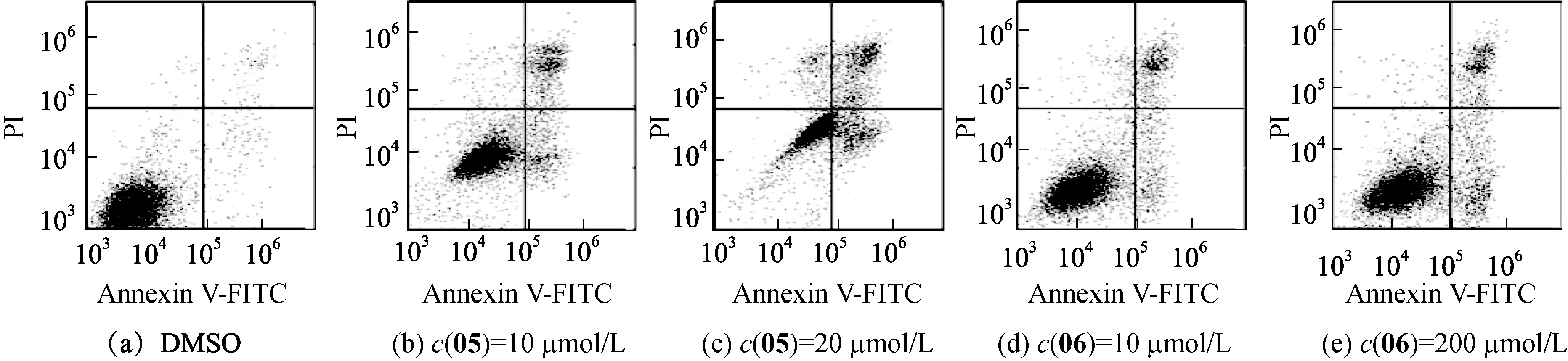
图6 Annexin V-FITC/PI检测凋亡细胞Fig.6 The detection of apoptosis by Annexin V-FITC/PI
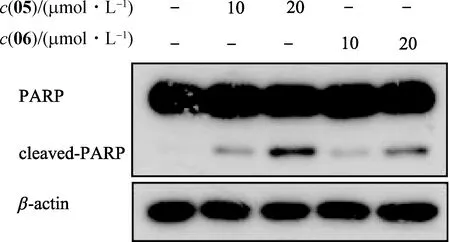
图7 WB检测PARP切割蛋白Fig.7 Detection of cleaved-PARP by WB
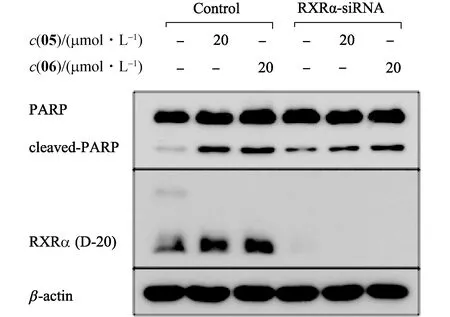
图8 化合物05和06诱导HeLa细胞凋亡作用对RXRα的依赖性Fig.8 RXRα-dependent apoptosis effect of compounds 05 and 06
XS-23结合于RXRα表面的共调节因子结合位点,而非传统配体所结合的配体结合口袋(ligand binding pocket, LBP),其中位于RXRα配体结合区域表面的V298位点对XS-23的结合至关重要[13].为验证化合物05和06是否具有与XS-23相似的RXRα结合模式,使用计算机模拟对化合物05和06与RXRα结构(PDB:3FUG)进行分子对接.结果显示:化合物05和06均可能与RXRα蛋白的helix12、helix3、helix4形成的表面区域结合;其中,位点E453和V298对2个化合物与RXRα的结合均至关重要;此外,L301对化合物05与RXRα的结合也很重要(图9).计算机模拟结果说明,化合物05和06可能具有与XS-23相似的RXRα结合模式,但具体的结合位点可能存在差异.
3 讨 论
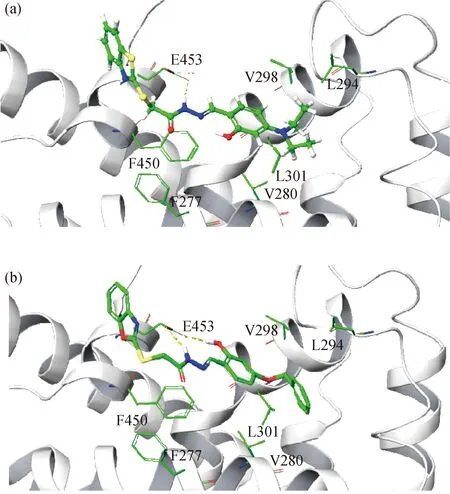
图9 计算机模拟化合物05 (a)和06 (b)与RXRα表面的结合位点Fig.9 Compounds 05 (a) and 06 (b) binding sites to RXRα surface by computer modeling
宫颈癌是威胁女性健康最常见的恶性肿瘤之一.在我国,宫颈癌的发病率位居女性恶性肿瘤第二位,是15~44岁女性中第三大高发癌症[14].宫颈癌也是世界范围内的女性高发恶性肿瘤,死亡率在所有癌症中居第四位[15].目前,治疗宫颈癌的主要手段是手术和放疗.化学药物主要使用顺铂,联合放疗用于晚期宫颈癌的治疗,但多伴有较大的毒副作用,临床上尚缺乏其他安全有效的治疗宫颈癌的化学药物[16].因此,研发治疗宫颈癌的安全有效的新型药物是近些年来国内外科研机构和制药企业重点关注的领域之一.
抗肿瘤药物开发的指导思想之一是直接杀伤癌细胞或是抑制肿瘤细胞的生长,而细胞增殖周期与细胞的生长直接相关.p21是CIP家族的一员,属于抑癌因子p53的下游CDK的负调节因子,与CDK复合物结合并抑制CDK复合物的功能,阻滞细胞周期,是细胞G0/G1期检验点的关键负调节因子[17].有研究显示p21可通过p53非依赖途径发挥作用,而RXRα参与调控p21的表达[18].在本研究对RXRα的小分子配体XS-23衍生物的筛选中发现,化合物05和06能够上调HeLa细胞中p21的表达水平,阻滞HeLa细胞周期于G0/G1期,最终诱导HeLa细胞凋亡,且具有一定的RXRα依赖性.实验结果显示化合物05和06可能通过靶向RXRα调控 p21 的功能进而影响细胞周期.此外,分子对接模拟化合物05和06与RXRα的结合可看出化合物05和06可能具有与XS-23相似的RXRα结合模式,即与RXRα表面结合,但具体的结合位点可能不同,还需进一步的实验验证.
近年来,靶点药物开发成为各国药企开发创新药物的重点.靶向细胞周期调节蛋白以及选择性地阻断肿瘤细胞增殖周期是近年来靶向抗肿瘤药开发的热点之一[19].在精准医疗时代,肿瘤的新药研发也取得了重大进展与突破,由传统的大量化合物的盲目筛选转为基于潜在有效成分或化学基团的细胞分子筛选:首先筛选找到有活性的化合物,再有针对性地进行优化,缩短了筛选周期.本研究在前期已发现的能够诱导肿瘤细胞凋亡的RXRα小分子配体XS-23基础上,基于结构多样性对其结构进行改造和优化,发现了2个能够阻滞细胞周期诱导HeLa细胞凋亡的XS-23衍生物,为该类周期阻滞类化合物的进一步优化提供了参考依据,也为进一步研究RXRα在细胞周期中的功能以及开发新型靶点抗肿瘤药物提供了方向和思路.

