MSCT在肾动静脉畸形诊断中的应用价值
陈亮, 孟红秀, 冯艳, 毛锡金, 殷志杰, 刘泉源, 董立杰, 张贝贝
肾动静脉畸形(renal arteriovenous malformations,rAVM)大多为先天性疾病,少部分因外伤所致,比较少见。常规影像学检查是诊断rAVM的主要方法,超声、MRI、DSA及CT可为其诊断提供重要信息,其中DSA既可确诊又可治疗,是其最主要的诊断方法。有关肾动静脉畸形的CT表现,国内外文献均少有报道。本文回顾性分析14例肾动静脉畸形患者的MSCT表现,旨在探讨MSCT对肾动静脉畸形的诊断价值。
材料与方法
1.病例资料
收集本院2008年5月-2017年9月经MSCT诊断为肾动静脉畸形的患者14例,其中男4例,女10例,年龄12~58岁。14例患者临床均怀疑为肾血管性疾病,主要症状包括间断性无痛血尿、腰部隐痛等。实验室检查仅2例患者血尿素氮(blood urea nitro-gen,BUN)轻度升高。入院时肉眼血尿8例,镜下血尿2例。14例患者中12例行肾动脉介入治疗,2例行手术治疗后确诊。

表1 患者一般信息及病灶相关情况
注:GS=金标准(gold standard);D1=医师1诊断结果;D2=医师2诊断结果;LS=病灶大小(lesion size);RAB=所属肾动脉分支(renal artery branch);DMA=畸形动脉直径(diameter of malformed artery);DMV=畸形静脉直径(diameter of malformed vein)。
2.检查方法
采用GE 64层螺旋CT(LightSpeed VCT)、西门子双源螺旋CT行MSCT检查,层厚、层间距均为5 mm,螺距0.984,管电压120 kV,自动管电流。所有患者均行平扫、增强三期扫描,增强扫描经肘正中静脉团注对比剂碘帕醇(370 mg I/mL),流率3.5 mL/s,剂量:成人100 mL;儿童2 mL/kg,最高不超40 mL。注射对比剂后25 s开始皮质期扫描,60 s开始髓质期扫描,5 min开始排泄期扫描。
3.图像后处理及分析
扫描所获原始数据,以0.625 mm层厚进行薄层重建,由3位副主任医师以上职称的诊断医师(简称“医师”)采用GE AW4.4工作站进行后处理,并对后处理图像进行观察、分析。其中2位医师首先利用MSCT图像对患者进行双盲诊断,计算2位医师对本病的诊断符合率。第3位医师知晓手术及DSA结果,在前2位医师首次诊断后,向其公布DSA及手术结果,并对所有患者进行回顾性分析,测量病灶大小、畸形动脉及静脉的直径(取3位医师测量的平均值作为最终值),评估局部皮质灌注、肾盂肾盏受压情况。后处理技术主要包括最大密度投影(maximum intensity projection,MIP )、多平面重组(multi-planar reformation,MPR)和容积再现(volume rendering,VR)等,观察分析内容主要是不同后处理技术对病变征象的显示能力。
4.统计学分析
使用SPSS 13.0软件进行统计学分析。医师之间的一致性分析采用Cohen's Kappa检验,Kappa值<0.51为不一致,0.51~0.80为一致,>0.80为显著一致。
结 果
1.医师间的一致性分析及诊断符合率
采用Cohen's Kappa检验对2位医师进行一致性分析,Kappa值为0.759,表明2位医师间具有一致性。医师1的诊断符合率为85.71%(12/14),医师2的诊断符合率为78.57%(11/14,表1)。
2.病变情况
14例患者中,病变位于肾皮髓质交界处8例,血管畸形均较小;4例畸形较大,大部分畸形血管位于肾轮廓外,少部分畸形血管位于皮髓质内;另外2例为肾动静脉畸形合并肾下极血管平滑肌脂肪瘤。
3.MSCT表现
CT平扫显示14例患者中8例病灶较小(表1),最大直径<5 cm,病灶呈等密度,肾形态无明显异常;4例病灶较大,最大直径>5 cm,病灶呈稍高密度影,病变大部分突出于肾轮廓外;2例合并血管平滑肌脂肪瘤,脂肪成分呈脂性低密度,血管成分呈稍高密度。14例增强扫描病变各期均明显强化,强化方式与血管相似,以皮质期病变显示最清楚。皮质期畸形血管强化程度高于髓质但稍低于皮质,畸形动脉均可显示,畸形静脉部分显示;髓质期畸形动脉强化程度减弱,开始变淡,畸形引流静脉强化程度增强,逐渐显示清晰;排泄期病变开始近似于平扫或呈稍高密度,肾盂肾盏显示良好,8例病灶较小者肾盂肾盏无明显受压改变,其余病灶较大者邻近肾盂肾盏不同程度受压。
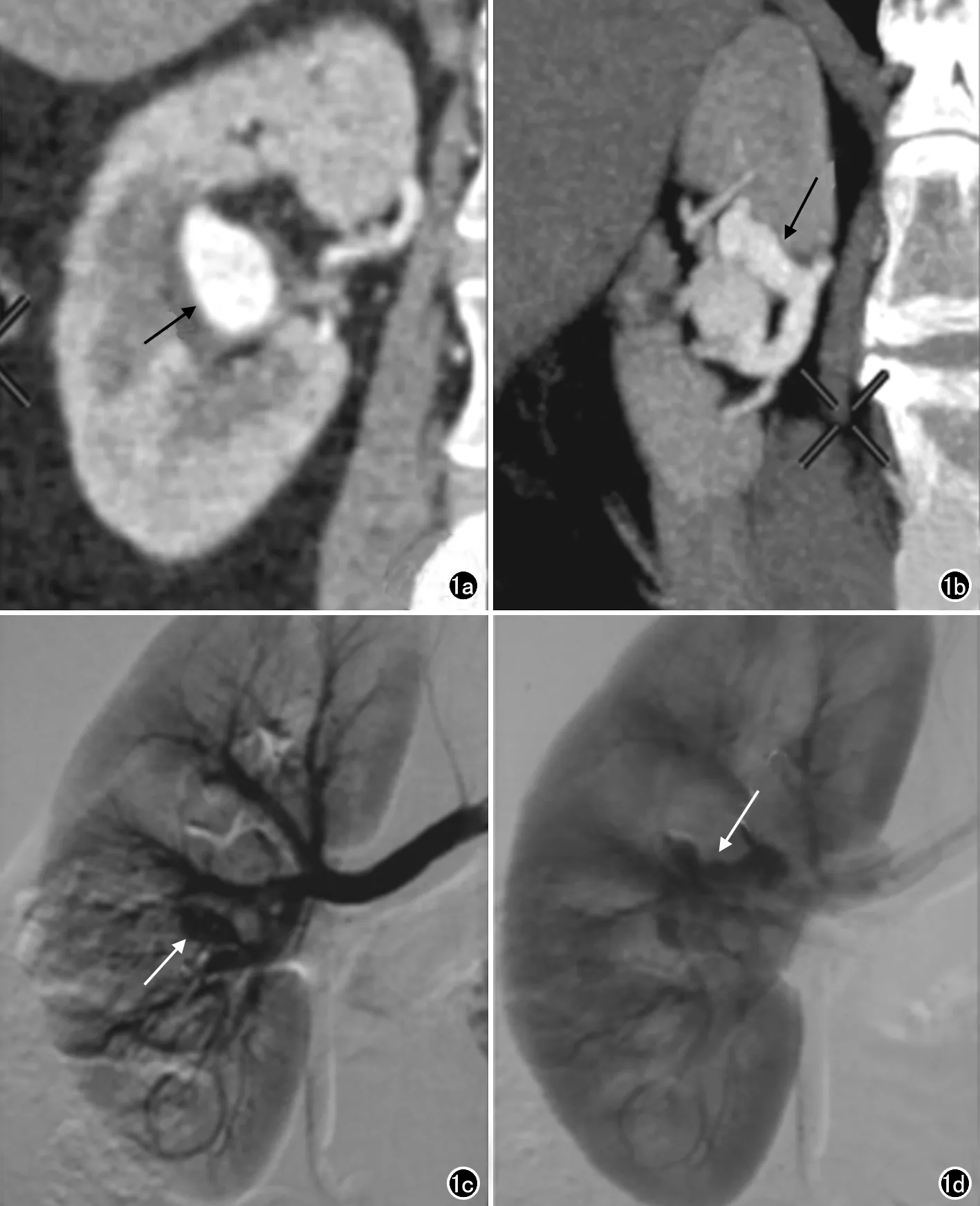
图1 肾动静脉畸形患者,女,65岁,因肉眼血尿1周入院,MSCT对畸形血管团的畸形动脉、静脉的显示与DSA有很好的一致性。a) 皮质期冠状面图像可清晰显示畸形血管团呈动脉瘤样扩张(箭),并可见邻近外侧皮质变薄;b)髓质期MIP图像可清晰显示畸形血管团的粗大引流静脉(箭); c) DSA动脉像显示畸形血管团呈动脉瘤样扩张(箭),供血动脉为后段分支; d) DSA静脉像示迂曲粗大引流静脉(箭)。
4例病灶较大者畸形血管可突出于肾轮廓外,横轴面图像即可显示畸形血管团;8例病灶较小者畸形血管常位于肾皮髓质交界处,横轴面图像仅能显示团块状或条状明显异常强化影,不能区分血管;而后处理技术中的MPR(图1a)及MIP(图1b)图像,皮质期均能清晰显示畸形动脉,并可追踪畸形动脉的供血动脉,对显示病变具有明显优势;VR图像对较大畸形可直观显示其畸形血管的立体走向,但不能显示小病变。皮质期对畸形动脉显示效果最佳同时可明确显示局部肾实质灌注情况;髓质期显示畸形静脉效果最佳;排泄期可显示肾盂肾盏充盈及是否受压情况。MSCT图像同时可以显示伴随征象,如肾积水、肾血肿等。
4.随访结果
12例患者行肾动脉介入治疗时DSA图像均可清晰显示畸形动静脉,MSCT对畸形动静脉的显示与DSA有很好的一致性(图1),同时行供血动脉的栓塞治疗。2例患者手术切除病变,术中可见粗大畸形动脉及引流静脉。
讨 论
1.临床与病理
rAVM大多为先天性疾病,比较少见,可分为静脉曲张型和动脉瘤型两种类型,两者均以女性多见,前者多见于年轻患者,后者多见于老年患者;极少数可继发于肾活组织穿刺或手术后[1];临床上本病可引起血尿及肾肿块[2],少部分可导致难治性高血压[3]。
rAVM的畸形血管常位于肾盂黏膜下固有层内,表现为肾段或肾叶间动静脉间的异常连接,局部异常血管扩张扭曲呈团状、丛状或串珠状,肾静脉压力的增加导致血管破裂,可反复引起血尿[4,5]。rAVM常局限在肾的某一段,这也是选择性肾动脉栓塞可治疗本病的基础[6,7]。
2.rAVM的MSCT影像表现及特征
病灶密度及对肾形态的影响:CT平扫时rAVM病灶多呈等密度,伴发出血时呈高密度,出血量大时肾盂内可见血凝块;病灶较小时肾脏形态多无改变,病灶较大时可使肾变形、肾盂肾盏受压等。本组病例中病灶最大直径<5 cm且位置深在时多不引起肾形态的改变,而对于直径>5 cm且位于肾表面时多引起肾形态改变;部分患者可伴轻度肾积水。
CT增强各期对畸形血管团的显示:增强扫描皮质期病灶呈明显均匀强化,与血管强化相似,呈团块状、条状等,此期对病灶供血动脉及畸形动脉的显示具有明显优势,本组病例中病变可发生于肾脏的各个肾段,病灶较小时多位于一个肾段,病灶较大时可跨肾段分布,但供血动脉只起源于一个肾动脉分支或其亚段;同时CT可测量畸形动脉的最大直径,畸形动脉的直径多大于供血动脉分支亚段的3~10倍;增强扫描髓质期病灶强化程度减弱,此期可明确显示畸形静脉及其引流方向;本研究结果显示畸形静脉的直径可大于或小于畸形动脉,这与其他部位AVM的畸形静脉直径一般大于畸形动脉的情况稍有差异,因此在判断病灶供血动脉时需仔细辨认;增强扫描排泄期病灶随延迟时间的不同可呈稍高密度或等密度,此期可评估肾盂肾盏受压情况;本组病例显示病灶直径小于5 cm的小病灶,一般不引起肾盂肾盏受压;而随着病灶增大,肾盂肾盏受压的概率增高,但两者并不呈正比,这还和病灶的位置有一定关系。MPR可多方位观察病灶,MPR联合MIP找到畸形动脉和/或畸形静脉即可确诊。本组病例中,皮质期MPR联合MIP图像均可清晰显示畸形血管团,从而诊断本病。
3.rAVM的鉴别诊断
rAVM需与肾假性动脉瘤、肾癌及肾感染性疾病等相鉴别:①肾假性动脉瘤多发生于肾外伤后,CT增强扫描可见与相应动脉相通的类圆形或梭形对比剂充盈,无引流静脉,其各期强化程度与血管一致;当动脉瘤较小时与rAVM鉴别困难,DSA对两者的鉴别具有重要意义;本组病例中1位患者病灶总体略呈球形,而畸形动脉与静脉的最大直径相近,两位医师均误诊为动脉瘤。②肾癌平扫多呈低密度,增强扫描明显强化但不均匀,可有坏死,并有明显的占位效应。③肾感染性疾病如肾脓肿早期病灶亦可明显强化,但其强化不均匀并以边缘强化为主;本组病例中有2例病灶很小,皮质期强化呈条状,2位医师均误诊为感染性疾病。
4.rAVM漏诊、误诊原因分析及处理对策
CT检查时易漏诊、误诊rAVM,本研究结果显示,两位医师在双盲的情况下首次诊断,诊断符合率分别为85.71%(12/14)、78.57%(11/14),稍高于文献报道,而且两位医师的诊断符合率相差较大,可能与病例数较少有关。造成CT检查易漏诊、误诊rAVM的原因有多种,其中最重要的一点,Honda等[8]认为与扫描方案及对比剂注射有很大关系。分析本组病例的扫描方案,笔者认为以下几点有利于病灶的显示:① MSCT薄层扫描或厚层扫描薄层重建有利于小病灶的检出。②增强扫描对比剂注射需采用高压注射器,注射流率应≥3.5 mL/s,快速团注对比剂有利于肾段动脉及其分支和病灶畸形血管的显示。③MSCT皮质期扫描时机是显示病变的关键,扫描时间应控制在注射对比剂后25 s,早于普通增强扫描的皮质期扫描时间(30 s)。普通增强扫描的皮质期肾皮质强化明显,很容易掩盖位于皮髓质交界的小病灶;而对比剂注射后25 s扫描,肾动脉及其分支显示良好,肾皮质强化还未达到高峰,密度相对较低,易于显示AVM。④图像后处理技术方面,笔者认为MPR和MIP是关键,不但可以清晰显示畸形血管团,还可以任意层面显示病灶,有利于追踪AVM的供血动脉,这对后续治疗具有指导意义;VR图像由于肾皮质的强化掩盖了畸形血管,不易显示小病变,但对于大病变可以直观观察AVM的立体结构及血管走向。
rAVM的诊断主要依赖影像学检查,如超声、CT、MRI及血管造影等[9]。超声特别是彩色多普勒超声对血流变化敏感,可以发现rAVM所产生的血流动力学变化,但对较小的动静脉畸形不敏感,易漏诊。MRI血管重建技术能显示较大肾动脉分支处的动静脉畸形,但对肾段动脉以下分支发生的病变较难显示[10]。肾动脉造影是诊断先天性肾动静脉畸形的金标准,可以发现很小的病变,能直观和全面地显示动静脉畸形的部位、数目、供血及血流动力学改变等,并且在诊断的同时可进行治疗,是诊治本病的首选方法,但肾动脉造影为有创性检查,且检查费用较高。MSCT采用容积扫描技术,扫描速度快,密度分辨力及空间分辨力高,扫描层厚薄(最薄可达0.625 mm),并配有强大的图像后处理技术,可检出小病灶,多期增强扫描可充分显示畸形动脉、静脉的血管团,同时可较准确地评估病灶周围肾实质灌注和肾盂肾盏受压情况,与DSA相比无创、经济,是筛查本病的有效检查方法。
综上所述,MSCT及其图像后处理技术可显示rAVM的畸形血管团,对本病具有很高的诊断价值,并可追踪供血动脉,有利于临床治疗方案的制定,同时MSCT经济、无创,可作为筛查本病的首选方法。

