响应面法优化野生紫苏籽油提取工艺及其抗氧化活性
曹小燕,杨海涛
(1.陕西理工大学陕西省催化基础与应用重点实验室,陕西 汉中 723000;2.陕西理工大学 化学与环境科学学院,陕西 汉中 723000)
紫苏(PerillafrutescensL.)又称为红苏、白苏、苏麻等,是一种常用的药食两用植物[1]。紫苏全身是宝,其叶、茎、根和籽均可入药,具有抗菌、抗炎、抗过敏、预防癌症、降血脂和血压、保护肝脾等功效[2]。近年来,由于其独特的活性组分和广阔的应用范围越来越受到人们的关注。紫苏籽为紫苏成熟的果实,具有行气和胃、解表散寒、治疗妊娠反应和胎动不安等功效。紫苏籽含有40%~50%的油脂,不饱和脂肪酸含量达90%以上,其中α-亚麻酸含量占55%~65%[3]。紫苏籽油还富含黄酮、多酚、微量元素、甾醇和VE等活性成分,具有抗氧化、抗炎、抗衰老、抗癌和预防老年痴呆等功效[4]。近年来,随着人们对紫苏籽油营养保健功效认识的不断深入,紫苏籽油作为一种重要的油料作物已引起国内外学者的广泛关注,如谢慧等[5]采用改良索式抽提法优化了紫苏籽油的提取工艺;宋曙辉等[6]采用微波辅助法优化了紫苏籽油的最优工艺;胡颖等[7]采用超临界 CO2结合夹带剂乙酸乙酯优化提取了紫苏籽油的提取工艺,其得油率为36.7%。程雪等[8]采用热处理辅助水酶法得到紫苏籽油的提取率为59.02%。由此可见,紫苏籽油作为一种新型营养保健食用油,不同的提取方法对其得油率和油品也有很大的影响。
目前,从原料中提取油的方法有机械压榨法、化学萃取法、索氏提取法、超临界CO2萃取法、水酶法和超声波辅助提取法等[9-12]。其中超声波辅助提取法相较于机械压榨法和超临界CO2萃取来说仪器操作简单;相较于化学萃取法来说不仅减少了浸出时间和杂质的浸出,而且提高了出油品质;与水酶法比较,操作易于控制。由此可知,超声波辅助法低成本、低耗能,且利于大规模生产。近几年,油脂是否具有抗氧化作用也受到了广泛的关注,研究表明较多的油脂对自由基均具有较好的清除作用[13]。因此,本研究采用响应面分析法优化了紫苏籽油的提取工艺,并评价了紫苏籽油的理化性质和自由基清除活性,为紫苏籽油的产业化开发提供一定的理论依据。
1 仪器、材料与方法
1.1 仪器与材料
EL104型电子分析天平;722G型可见分光光度计;SB-4200DTD型超声波清洗机;JXL-2S-6A型数显恒温水浴锅;101A-1型电热鼓风干燥箱;800型离心机;CL-2型恒温加热磁力搅拌器。
紫苏籽:采集于陕西省勉县,分别进行晾干、除杂、50 ℃烘干、粉碎、过80目筛后贮藏在干燥容器中备用。石油醚(AR):60~90 ℃;其他试剂:均为国产分析纯。
1.2 试验方法
1.2.1 超声辅助提取紫苏籽油
准确称取一定量的处理好备用的紫苏籽粉于烧瓶中,依据一定的料液比加入石油醚,在一定的超声功率、提取温度和提取时间下,进行提取、收集提取液、旋转浓缩回收溶剂,得到紫苏籽毛油,于60 ℃电热鼓风干燥箱中干燥至恒重,称重。其提取率计算公式如下:
紫苏籽油提取率(%)=(提取后紫苏籽油的质量/提取前紫苏籽的质量)×100。
1.2.2 单因素试验
基础提取条件:超声功率400 W,提取时间30 min,超声温度60 ℃,料液比1∶10。在该基础条件下适当调整后进行不同的提取溶剂(异丙醇、石油醚、正己烷、乙醇、乙酸乙酯)、超声功率(200,250,300,350,400 W)、提取时间(10,20,30,40,50 min)、超声温度(30,40,50,60,70 ℃)、料液比(1∶2,1∶5,1∶10,1∶15,1∶20)的单因素试验,以紫苏籽油提取率为考察指标,优选各单因素的最优取值范围。
1.2.3 响应面试验
以紫苏籽油提取率为考察指标,根据Box-Behnken中心组合试验设计的原理,设计响应面分析试验[14],优化超声辅助提取紫苏籽油的提取工艺。
1.2.4 紫苏籽油理化指标的测定[15]
水分及挥发物按照GB 5009.236-2016测定;相对密度按照GB/T 5518-2008测定;皂化值按照GB/T 5534-2008测定;碘值按照GB/T 5532-2008测定;酸值按照GB 5009.229-2016测定;过氧化值按照GB 5009.227-2016测定;折光率按照GB/T 5527-2010测定。
1.2.5 抗氧化活性的测定
对O2-·的清除能力:依据邻苯三酚自氧化法[16];对NaNO2的清除:依据盐酸萘乙二胺法[17];还原能力的测定:采用铁氰化钾还原法[18]。
2 结果与分析
2.1 单因素试验对紫苏籽油提取率的影响
以紫苏籽油收率为评价对象,对可能影响得率的提取溶剂、超声功率、超声温度、提取时间和料液比进行了试验筛选,结果见图1~图5。

图1 提取溶剂对紫苏籽油提取率的影响

图2 超声功率对紫苏籽油提取率的影响

图3 提取温度对紫苏籽油提取率的影响

图4 提取时间对紫苏籽油提取率的影响
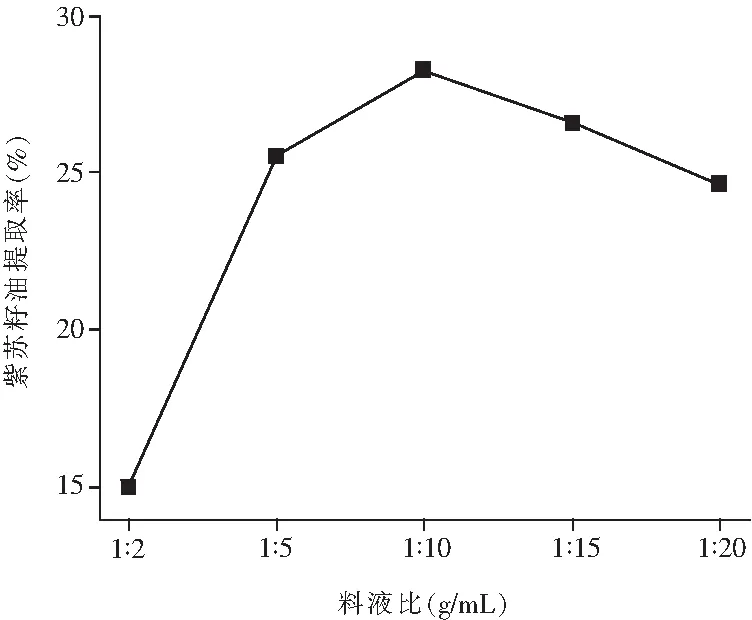
图5 料液比对紫苏籽油提取率的影响
由图1可知,5种提取溶剂对紫苏籽油提取率的差异影响较大,其中石油醚和正己烷的紫苏籽油产率接近且最大,所得油脂颜色淡黄,透明度高。乙酸乙酯、异丙醇、无水乙醇的提取率依次降低,且乙酸乙酯和异丙醇提取的油脂呈黄绿色,略有浑浊。故后续试验选择石油醚(60~90 ℃)为提取溶剂。
由图2可知,当超声功率在200~250 W时,紫苏籽油的提取率随超声功率的增加而增加;250~300 W之间时,紫苏籽油的提取率随超声功率的增加而增加最快;300~350 W时,紫苏籽油的提取率随超声功率的增加而逐渐降低;350~400 W之间时,虽然紫苏籽油的提取率随超声功率的增加而有所增加,但是增加的幅度明显小于200~300 W时的增加幅度。结合超声波的机械效应与热效应,高功率条件下有可能引起油脂中活性成分的降解等原因,故选择超声功率300 W为宜。
由图3可知,随着温度的升高,紫苏籽油的提取率逐渐增加,60 ℃时达到最大值;60 ℃以后紫苏籽油的提取率下降程度非常明显。可能是由于超声温度过高,溶剂挥发过快,使得浸出过程中无法保持稳定的状态,导致提取率降低,故选择超声温度40 ℃为宜。
由图4可知,随着提取时间的延长,紫苏籽油的提取率呈现先增加后降低的趋势,40 min后下降趋势趋于平缓。可能是由于超声处理的时间过长,产生的空化作用或机械效应使紫苏籽油中的不饱和脂肪酸发生了裂解,从而使得紫苏籽油的提取率下降,故在实际生产过程中,超声时间应在30 min为宜。
由图5可知,在1∶2~1∶5时,紫苏籽油的提取率随料液比的增大而增加最快;1∶10时提取率达到最大值;随后紫苏籽油的提取率有所下降。由此可见,提取溶剂用量增加,可使较多的紫苏籽油溶于溶剂中,也可能导致产物中的杂质增多,促使提取率降低,故料液比选择1∶5~1∶15之间较合适。
2.2 响应面分析试验
2.2.1 响应面分析试验设计与结果
依据单因素试验结果,设计4因素3水平的响应面法优化试验,考察超声功率、超声温度、提取时间和料液比对紫苏籽油提取率的影响,优化其提取工艺。响应面分析试验的因素与水平见表1;响应面分析试验的结果见表2,其中1~24为分析试验,25~27为零点试验。

表1 响应面分析因素与水平
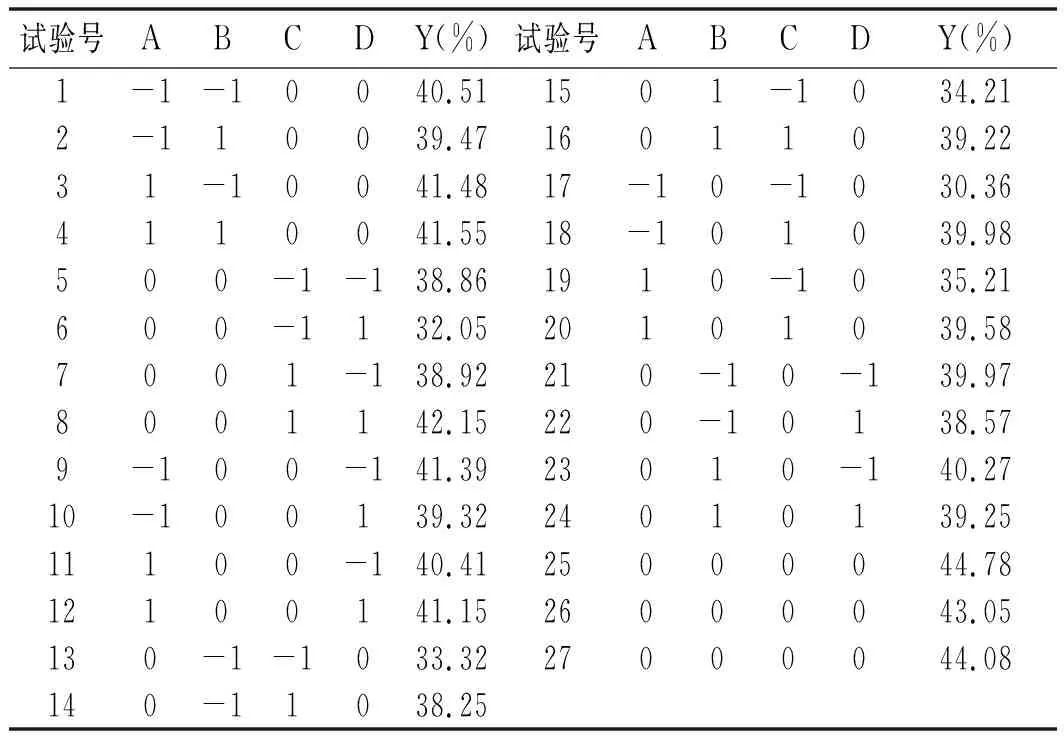
表2 响应面分析试验的设计及结果
2.2.2 响应面试验方差分析
运用Design-Expert 8.0统计学软件,对表2中的试验数据进行二次多项式回归拟合,得到Y与A,B,C,D的二次回归方程为:Y=-46.015833+0.829583A+1.678667B+2.531000C+0.192633D-0.017167A2+0.002775AB-0.022592B2-0.026250AC+0.000400BC-0.210167C2+0.001405AD+0.000190BD+0.010040CD-0.000592D2。
紫苏籽油提取率回归模型的方差分析结果见表3。
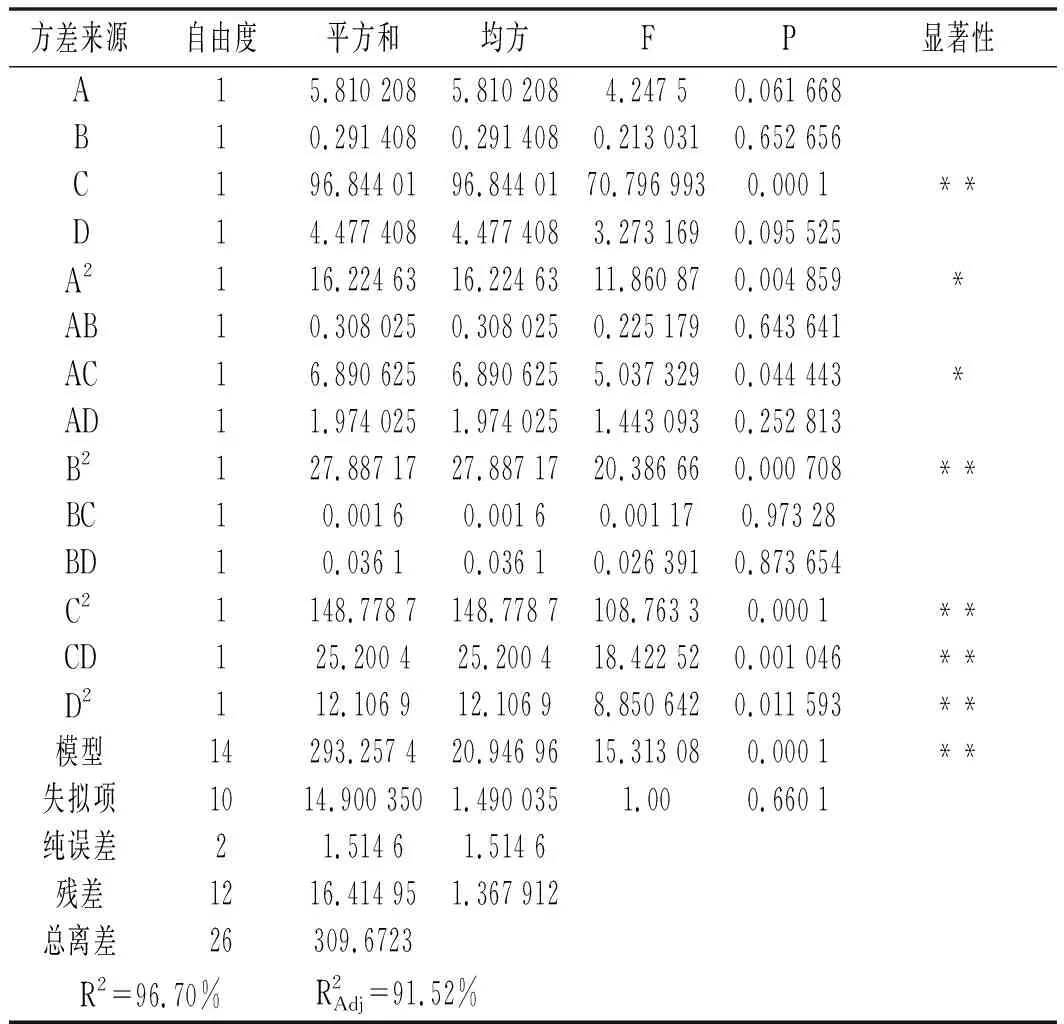
表3 回归方程的方差分析结果
注:“*”表示差异性显著,P<0.05;“**”表示差异性极显著,P<0.01。

2.2.3 确立最佳的提取条件与验证
通过分析响应面试验模型,得到紫苏籽油提取率的预测值为44.52%,即超声时间为40.44 min,温度为31.14 ℃,料液比为1∶11.34 (g/mL),超声功率为302.4 W。为了便于实际操作,设定超声时间为40 min,温度为31 ℃,料液比为1∶11 (g/mL),超声功率为300 W, 进行3次平行试验,得到紫苏籽油的平均提取率为44.31%,与理论预测值的误差为0.47%。因此,本响应面试验模型与实际情况拟合度良好,优化结果可靠,该工艺参数具有较高的稳定性与实际应用价值。
2.2.4 紫苏籽油理化指标的测定
在最佳工艺条件下得到淡黄色、澄清透明的紫苏籽油,具有紫苏特有的气味,加热无沉淀生成。苏籽油的理化性质测定结果见表4。
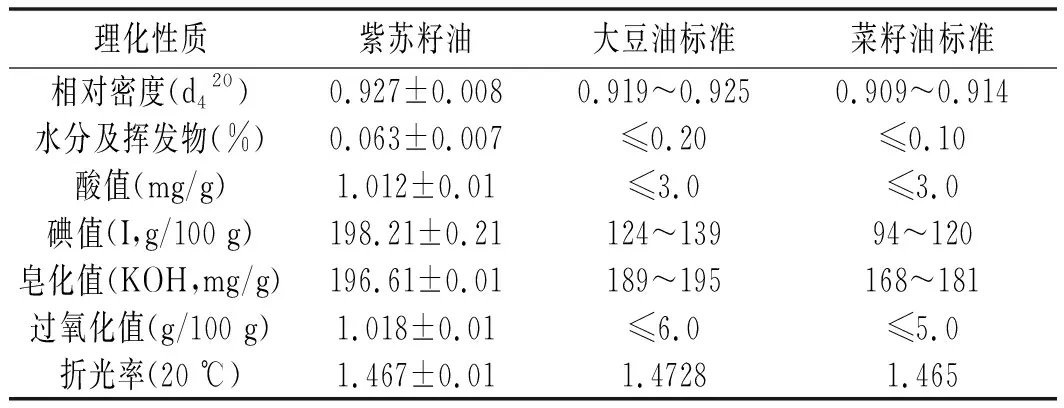
表4 紫苏籽油的理化性质
由表4可知,其相对密度较大,说明其不饱和程度较高;油中水分及挥发物的含量较低,易于长期稳定保存;酸值和过氧化值接近于1,符合国家食用油的标准,表明其具有较好的抗氧化性能;碘值较高,表明其含有较高的不饱和脂肪酸,油品质较好;皂化值高于常见植物油的标准,进一步说明其不饱和脂肪酸含量高;折光率也高于一般的油脂。野生紫苏籽油的酸值、碘值、皂化值和过氧化值均达到了国家食用植物油的标准,是一种理想的保健用油。
2.3 紫苏籽油的抗氧化活性
2.3.1 对超氧阴离子自由基(O2-·)的清除能力
O2-·可以在生物体内发生脂质过氧化或生成其他的氧自由基,引起机体损伤性疾病。
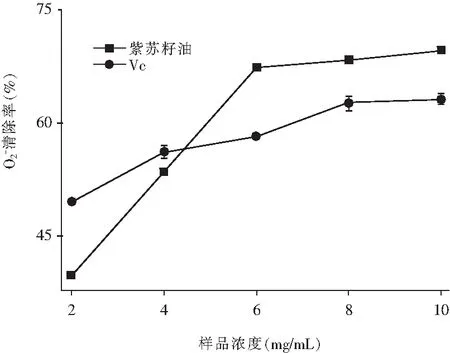
图6 对亚硝酸盐清除活性
由图6可知,紫苏籽油的质量浓度小于6 mg/mL时,紫苏籽油对超氧阴离子自由基的清除率小于Vc,由于紫苏籽油中的活性成分较多,低浓度条件下其自由基清除活性较弱;当质量浓度大于等于6 mg/mL时,紫苏籽油对超氧阴离子自由基的清除率明显高于Vc,且存在明显的量效关系,可能是紫苏籽油中的活性成分存在协同清除自由基的性能。故紫苏籽油对超氧阴离子自由基具有较强的清除作用,其清除IC50值为2.49 mg/mL。
2.3.2 对亚硝酸盐(NaNO2)的清除能力
依据重氮偶合比色法,在酸性环境中亚硝酸盐与对氨基苯磺酸发生重氮化反应,再与盐酸萘乙二胺试剂发生偶联反应,生成的紫红色偶氮化合物于540 nm处的吸光度值增强。
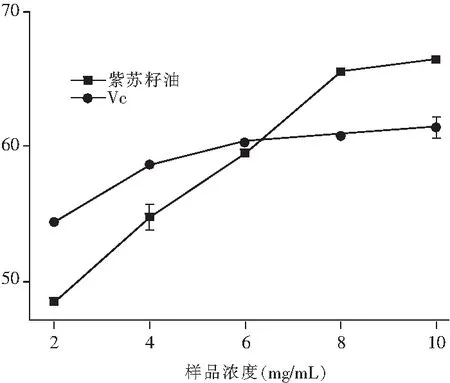
图7 对亚硝酸盐清除活性
由图7可知,在低质量浓度条件下,紫苏籽油对亚硝基的清除能力明显低于Vc,其清除效率增长较快且存在明显的量效关系,而Vc的清除效率增长平缓。紫苏籽油对亚硝基的清除IC50值为2.51 mg/mL,表明相同浓度下紫苏籽油对亚硝酸盐的清除速率优于Vc溶液。
2.3.3 还原能力的测定
利用紫苏籽油被铁氰化钾氧化来表征其还原力。还原力越强表示其给电子能力越强,其自由基清除活性也相对较强,因此常应用还原能力表征其抗氧化活性的强弱。

图8 还原能力的测定
由图8可知,20~80 g/mL时紫苏籽油的还原能力呈现明显的上升趋势,80~140 g/mL时,还原能力上升平缓,但总体趋势优于同浓度条件下Vc溶液的还原能力。由此可见,紫苏籽油的还原能力较为显著,同时佐证了紫苏籽油具有较强的自由基清除活性及抗氧化能力。
3 结论
在单因素试验的基础上,经过响应面试验优化了超声辅助提取紫苏籽油的提取工艺,在最佳的提取工艺参数为超声功率300 W、超声时间40 min、温度31 ℃、料液比1∶11 (g/mL)的条件下,紫苏籽油的提取率为44.31%,与理论预测值的误差为0.47%,表明该工艺条件稳定,切实可行。
紫苏籽油的理化性质研究发现,紫苏籽油为澄清、透明的淡黄色液体,加热无沉淀生成;相对密度(d420)0.927±0.008;酸值(1.012±0.01) mg/g;碘值(I)(198.21±0.21) g/100 g;皂化值(196.61±0.01) KOH mg/g;过氧化值(1.018±0.01) g/100 g。其酸值、碘值、皂化值和过氧化值均达到了国家食用植物油的标准,是一种理想的保健用油。
自由基清除活性研究表明,当浓度10 mg/mL时,紫苏籽油对超氧阴离子自由基和亚硝酸盐的清除率分别高达69.61%和66.46%,其清除IC50值分别为2.49,2.51 mg/mL;在浓度为0.14 mg/mL时,紫苏籽油的还原能力为0.671,高于同浓度条件下Vc的自由基清除活性和还原能力。故紫苏籽油具有良好的抗氧化能力,本研究为其进一步的工业开发与利用提供了一定的试验依据。

