均匀设计法优化红枣红色素的提取及其稳定性研究
罗璇,李婵娟,田喆
(武汉设计工程学院 食品与生物科技学院,武汉 430205)
红枣红色素是一种天然生物色素,不仅安全无毒、色泽自然,可作为保健食品和化妆品等领域重要的添加剂,而且含有较高的营养价值和药用价值。研究表明:红枣红色素对某些氧化剂和还原剂均有良好的稳定作用,是一种理想的食品添加剂与药用原料[1,2]。均匀实验设计是基于不需考虑“整齐可比”,而让实验点在实验的范围内可充分考虑“均匀分散”的一种稳健设计,所以,最大的特点是可节省大量的实验工作量,避免偶然性误差,尤其是在实验因素的水平较多时,其优势更加明显[3,4]。
采用均匀设计法对红枣红色素的提取优化和用正交实验对红枣红色素的稳定性做系统研究国内尚未见报道,本文在前人实验基础上借鉴其他色素的粗提取优化和稳定性研究方法,设计完善的实验方案,对红枣红色素的提取优化和稳定性进行了更深入的研究,为保存天然色素提供了依据。
1 材料与方法
1.1 材料
1.1.1 实验原料与辅料
红枣:市售,干红枣,购于中百超市,产地浙江金华。
1.1.2 试剂
石油醚、乙醚酮:分析纯,天津市凯通化学试剂有限公司;L-抗坏血酸:化学纯,武汉市华顺生物技术有限公司;NaOH、HCl、乙酸乙酯、双氧水:分析纯,国药集团化学试剂有限公司。
1.1.3 仪器
752B型紫外可见分光光度计 天津市普瑞斯仪器有限公司;TG-16WS台式高速离心机 长沙湘智离心机仪器有限公司; HH-S2/HH-6数显恒温水浴锅 金坛市医疗仪器厂/国华电器有限公司;OH6-907385-Ⅲ电热恒温鼓风干燥箱 上海新苗医疗器械制造有限公司; SZ-93自动双重纯水蒸馏器 上海亚荣生化仪器厂; JA2003B电子天平 上海越平科学仪器有限公司。
1.2 方法
1.2.1 原料的预处理
选择饱满、完整的红枣去核,在60 ℃电热鼓风干燥箱中烘干后粉碎,过60目筛,标号,放在干燥器中储存备用。
1.2.2 红枣红色素提取率的计算[5-7]
在最佳的提取条件组合下,多次提取一定量的红枣红色素,直到最后一次提取液呈无色(吸光度<0.01),分别收集各次的色素提取液并测定其体积(Vi)和吸光度(Ai)计算出提取级数。
提取率(%)=(Ai×Vi/A1×V1+ …+An×Vn)×100%(i=1…n)。
式中:Ai为提取色素溶液的吸光值;Vi为提取色素溶液的体积(mL)。
1.2.3 红枣红色素提取单因素实验条件
将红枣粉溶于一定浓度的NaOH溶液,于50 ℃水浴中密闭恒温浸提2 h。速冷后,以4000 r/min离心20 min。吸取1 mL色素溶液,稀释25倍,在波长为330 nm处测吸光度值。单因素实验因素水平条件见表1。

表1 溶剂提取单因素实验因素水平Table 1 Factors and levels of single-factor experiment
1.2.4 均匀设计实验方法
本均匀设计实验的目的是确定红枣红色素的最优因素组合水平。确定NaOH为提取剂,考察提取剂的浓度(x1)、料液比(x2)、提取时间(x3) 、提取温度(x4) 4个因素,每个因素取值范围为t个水平(t为实验次数),4个因素的一次项及二次项各有4项,4项因素间的两两交互作用设有6项,共14项,实验数不能小于14,本实验选用U17(178)表。本实验为4因素,这4个因素安排在均匀表的1,5,7,8列,去掉U17(178)的最后一行,实验方案见表2和表3,最后各管取1 mL于25 mL的比色管中,测量吸光度。
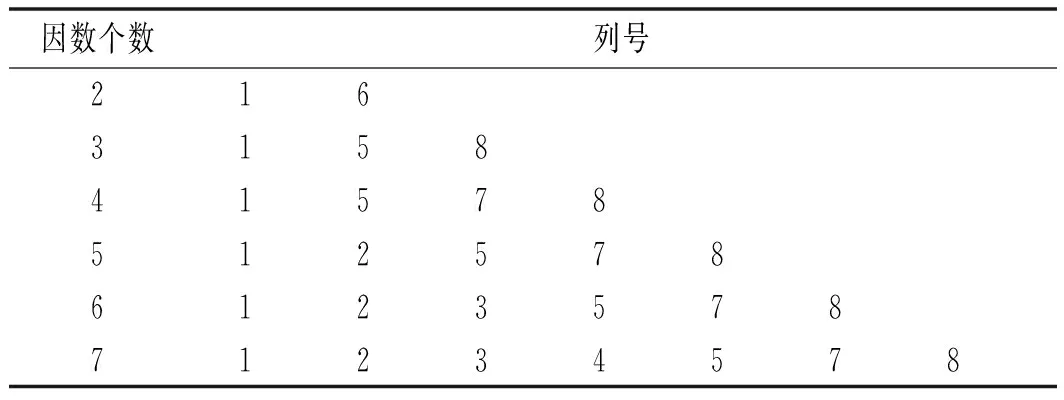
表2 U17(178)均匀设计使用表Table 2 Uniform design table of U17(178)

表3 均匀表U17(178)Table 3 Uniform table of U17(178)
1.2.5 红枣红色素稳定性单因素实验
光因素稳定性:称取1 g红枣粉,在NaOH提取液为0.2 mol/L,料液比为1∶20 (g/mL),温度为50 ℃条件下提取1 h,离心后得到红枣红色素粗提液,然后取红枣红色素粗提液3份,每份6 mL,每份吸取1 mL分装不同的试管中,然后加3 mL蒸馏水稀释,分别置于室内避光处、室内散射光处、室外日光下,定时取样测其吸光度。
热因素稳定性:取红枣红色素粗提液3份,每份6 mL,加入2 mL缓冲溶液,吸取1 mL,然后加3 mL蒸馏水稀释,置于0,25,40,80,90,100 ℃保温1,2,3,4,5 h,取样冷却后测其吸光度。
氧化剂因素稳定性:选用双氧水作为氧化剂。双氧水原溶液(30%)稀释成0.6%和1.2%的溶液,吸取2 mL加入6 mL红枣红色素溶液中,置于室温下避光1,2,3天,稀释3倍,在330 nm的波长下测定吸光度值。
防腐剂因素稳定性:选用抗坏血酸作为防腐剂,配制成0.1%和1%的抗坏血酸后,吸取2 mL加入6 mL红枣红色素溶液中,置于室温下避光1,2,3,4,5,6天,稀释适当的倍数,用同浓度的抗坏血酸钠溶液做参比,在330 nm的波长下测定吸光度值。
1.2.6 红枣红色素稳定性正交实验
稳定性影响因素光、热和抗坏血酸分别用A,B,C表示,采用3因素3水平正交实验。根据9个组合条件进行实验,并依次记录实验的吸光度,见表4。

表4 红枣红色素稳定性正交表Table 4 Orthogonal table of stability of red pigment from red jujube
2 结果与分析
2.1 提取剂的选择

表5 不同提取剂的提取效果Table 5 The extraction effect of different extraction agents
注:此次实验中氢氧化钠、盐酸的浓度均为0.2 mol/L。

图1 不同提取剂的提取效果Fig.1 The extraction effect of different extraction agents
由表5可知,无水乙醇提取为浅黄色,说明红枣红色素微溶于酒精;乙醚、乙酸乙酯、石油醚几乎无色,说明红枣红色素难溶于这3个有机溶剂,由图1可知,红枣红色素不溶于石油醚,红枣红色素在蒸馏水中溶解度较大,而盐酸对红枣红色素的溶解度比蒸馏水大,因此,可以得出盐酸有助于红枣红色素的浸出。NaOH(0.2 mol/L)提取的颜色为红褐色,与红枣的颜色相近,结合图1各种提取剂的提取效果图,得出在本实验中所选的提取剂中氢氧化钠提取效果最好,所以,本实验提取剂采用氢氧化钠溶液作为枣粉的红色素提取溶剂。
2.2 色素提取单因素实验结果
红枣红色素的提取是一个复杂的过程,主要的影响因素有提取溶剂的种类和浓度、料液比、提取温度和时间等。为了减少后续主参数试验和结果分析的工作量,本研究首先分别进行了相关单因素实验, 获得了红枣红色素提取液吸光度最高和提取效果最好的提取溶剂为0.2 mol/L的NaOH溶液,料液比为1∶20 (g/mL),提取时间为5 h,提取温度为80 ℃。

图2 提取剂的浓度对红枣红色素提取的影响Fig.2 The effect of concentration of extractant on the extraction of red pigment from red jujube

图3 料液比对红枣红色素提取的影响Fig.3 The effect of solid-liquid ratio on the extraction of red pigment from red jujube

图4 提取时间对红枣红色素提取的影响Fig.4 The effect of extraction time on the extraction of red pigment from red jujube

图5 提取温度对红枣红色素提取的影响Fig.5 The effect of extraction temperature on the extraction of red pigment from red jujube
2.3 优因素水平组合的确定
采用均匀设计实验得到的实验结果见表6。

表6 均匀设计法结果Table 6 Results of uniform design method
首先建立一次回归方程,利用SAS软件对表6中的实验结果进行拟合,运行结果得出R2达到0.9937,说明了x可以解释y的程度达到了99.37%,解释了绝大部分信息,说明模型正确。从总体的P值都远小于0.05,可知模型是显著的。由各变量的P值可以得出在0.05的水平下x1,x2,x3,x4非常显著,显著结果见表7。从而得到以吸光度为因变量,以NaOH的浓度、料液比、提取温度、提取时间4个因素为自变量的回归方程:y=11.71465284+21.11564674x1-0.48066931x2-0.08376224x3+0.44222659x4。
根据回归方程系数的绝对值,得到影响红枣红色素提取因素的效应是x1>x2>x4>x3,由此可以说明NaOH的浓度对红枣红色素的提取影响最大,其次是料液比,提取温度在50~90 ℃范围内影响最小。此外,对表7建立一次回归方程,由于未通过检验,再次补做赘述。

表7 均匀设计法一次回归模型方差数据分析结果Table 7 Analysis results of variance data of a regression model of uniform design method
对表7的数据进行极差分析,绘出实验因素与指标值的关系曲线,见图6。
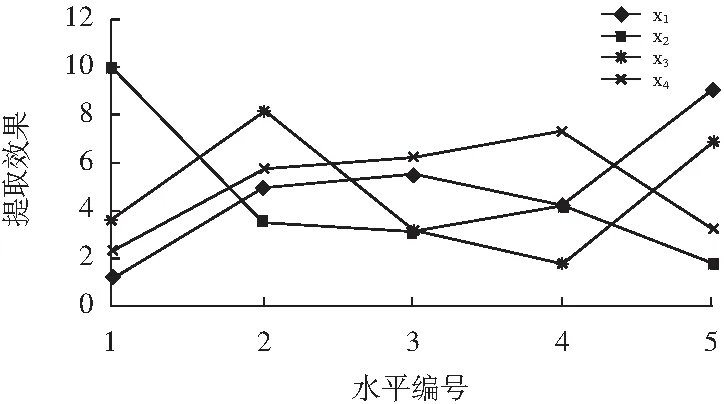
图6 因素水平与提取效果趋势Fig.6 Factors,levels and extraction effect trends
由图6可知,红枣红色素提取优化因素组合为X15X24X32X44(其中,下标中的首数字表示因素,第2个数字表示该因素中的水平编码),即NaOH的浓度为0.5 mol/L,料液比为1∶25 (g/mL),温度为60 ℃,提取时间为5 h。根据提取率计算公式得出:提取级数为3级,提取率为93.11%。
2.4 稳定性单因素实验结果
2.4.1 光照对红枣红色素稳定性的影响

图7 光照对红枣红色素的稳定性的影响Fig.7 Effect of illumination on the stability of red jujube red pigment
由图7可知,随着光照时间的延长,红枣色素的吸光值有所下降,但是下降不是很明显,所以,红枣色素对于光具有一定的稳定性。
2.4.2 氧化剂对红枣红色素稳定性的影响
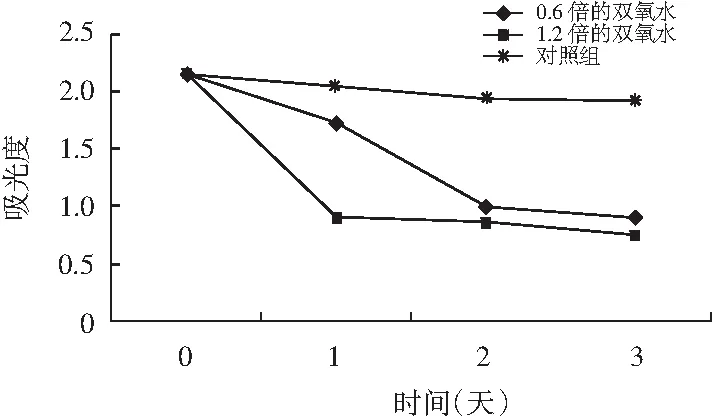
图8 氧化剂双氧水对红枣红色素稳定性的影响Fig.8 Effect of oxidant hydrogen peroxide on thestability of red jujube red pigment
由图8可知,氧化剂对红枣红色素的影响非常大。肉眼观察也非常明显,在很短的时间就将红枣红色素氧化成无色。并且氧化剂的浓度增加,氧化速度明显增加。因此,红枣红色素的抗氧化性比较差,保存的时候应防止氧化。
2.4.3 温度对红枣红色素稳定性的影响

图9 温度对红枣红色素稳定性的影响Fig.9 Effect of temperature on the stability of red jujube red pigment
由图9可知,红枣红色素随温度的上升略有增加,颜色略有加深,但增加不大。温度对红枣红色素的影响较小。
2.4.4 抗坏血酸对红枣红色素稳定性的影响

图10 抗坏血酸对红枣红色素稳定性的影响Fig.10 Effect of ascorbic acid on the stability of red jujube red pigment
由图10可知,抗坏血酸对红枣红色素提取液稳定性有显著的影响,但抗坏血酸的浓度对稳定性的变化不大,在保存红枣红色素的过程中应避免接触抗氧化剂抗坏血酸。
2.5 红枣红色素稳定性影响优化的正交实验结果
根据红枣红色素稳定性单因素实验,得出双氧水对红枣红色素具有氧化性,为了得到红枣红色素在室温附近的最佳保存条件,对因素光、热、防腐剂抗坏血酸的量这3个因素进行正交实验,见表8。

表8 红枣红色素稳定性影响优化的正交实验结果Table 8 Effect of red jujube pigment stability on optimization of orthogonal experiments
注:A 表示光照,B 表示温度,C表示抗坏血酸。
由表8可知,抗坏血酸的极值R最大,热的极值R最小;各因素对红枣红色素稳定性的影响大小为抗坏血酸>光>温度,3个因素的优水平组合是A1B1C1,即:光为阴暗避光处,热为40 ℃,不需要添加抗氧化剂抗坏血酸。
3 结论
在红枣红色素提取的均匀设计实验中,对实验数据建立一次回归方程,通过SAS软件得出Y=11.71465284+21.11594674X1-0.4806693X2-0.0837622X3+0.44222659X4,R2=0.9937,各变量的P值亦通过检验,说明模型正确,结果表明:影响红枣红色素提取效果的诸因素的主次顺序为提取剂浓度>提取料液比>提取时间>提取温度,且提取剂浓度、提取的料液比、提取时间都是影响红枣红色素提取的显著因素。红枣红色素提取的优因素水平组合为NaOH的浓度为0.5 mol/L,料液比为1∶25 (g/mL),温度为60 ℃,提取时间为5 h。提取级数为3级,最高提取率为93.11%。红枣红色素提取条件模型的拟合度高。
红枣红色素的稳定性研究表明:光、温度、抗坏血酸量3个因素对红枣红色素稳定性的影响大小为抗坏血酸>光>热量。40 ℃阴暗避光处,无抗坏血酸的环境是红枣红色素最佳稳定贮存条件。

