激光诱导空泡在生物医学中的应用
周启光, 程 静, 郑璐璐, 张大伟
(上海理工大学 光电信息与计算机工程学院, 上海 200093)
引 言
随着社会经济的快速发展,人民素质的普遍提高,身处和谐社会的人们对自身健康的重视程度也越来越高。因此,研究人员对生物医学领域的研究也越来越深入,生物医学在所有学科中的地位也越来越重要。在生物医学领域中,主要研究对象就是细胞,但细胞的尺寸只有微米级,对单一细胞的操作工具比较少,因此,研究人员想到利用激光诱导空泡产生的冲击波来作为对单一细胞操作的“工具”。激光诱导空泡的方法的优点是:(1) 精度高,激光诱导空泡的尺寸在微米级,与细胞尺寸相当;(2) 非侵入式,可以用于密闭且透明的微流腔内,甚至是活体组织表面及浅层。
近年来,随着微流控这一新兴研究领域的逐渐升温,激光脉冲诱发气泡空化作为一种新的微流体驱动机制应运而生。它在高阻尼的环境中为高速微流体驱动提供高能量密度,高能量转换,高度局部化和大的机械力。能量通过自由空间光学传播传递,不需要任何物理电气或机械互连,这大大降低了器件制造的复杂性。它还融合了图像处理等领域,具有集成光学扫描仪和透镜的并行驱动的潜力。
高功率激光束(功率密度约108W/cm2以上)在液体介质中有一个脉冲周期左右的能量沉积后,则液态物质的特性、状态发生变化,例如:宏观上激光与液态物质相互作用区域发生温升、介质膨胀、汽化、空泡形成等物理现象;微观上电子空穴出现激发跃迁、分子离解和原子电离等物理现象。激光击穿液体介质的一个重要现象是冲击波辐射,其生成的原因是,当激光功率密度超过液体的击穿阈值后,在聚焦区域形成高温高压的等离子体,该等离子体吸收后续激光能量对外膨胀,就会压缩周围液体。在等离子体前方产生一系列压缩波的叠加,从而产生间断面很陡的冲击波波阵面。
1 激光诱导空泡现象用于细胞穿孔
将外源分子递送到哺乳动物细胞中是基因转染和一些特定类型疾病治疗处理的基础。此外,靶向特定单细胞分子递送的能力在生物医学领域的许多研究中是很重要的,例如干细胞研究[1],单细胞分析[2]和其他需要在原位诱导单细胞修饰的研究性实验。广泛使用的分子递送方法有基于病毒或化学的转染[3-4]和使用脉冲电场的电穿孔,这些技术在细胞膜中产生孔,并且这些孔适用于将分子转移到大群细胞中[5-6]。
飞秒激光也已用于细胞穿孔,例如,使用飞秒激光穿孔的转染效率对于干细胞系可以达到80%[7],而对于中国仓鼠卵巢(CHO)细胞可以达到90%[8],还可以实现在穿孔中的高空间精度,分辨率小于单个细胞的尺寸。飞秒激光需要精确地聚焦在上部细胞膜表面上[9],在焦平面中的3 μm的偏差(这可能是由于单元高度的变化引起)可导致大于50%的蚀刻效率的降低。
美国夏威夷大学的研究人员将激光诱导空化现象应用到微流控上,利用气泡产生的冲击波的剪切力使细胞膜切开一个小口(尺寸在30 nm),从而使药物通入到细胞内。他们所使用的激光器是最大功率为800 mW(Laserlands,980MD-0.8W-BL)的980 nm二极管激光器;微流控芯片的结构是吸光基底,由涂覆有厚度为200 nm的铟锡氧化物(ITO)层的1 mm厚的载玻片组成,顶部覆盖有1 μm厚的非晶硅(α-silicon)层,来自激光器的大部分入射光(70%)在吸收性基材的ITO和α-硅层中被吸收并转化成热,在基材上产生蒸气微泡。如图1所示:通过基底的光学加热在靶细胞附近产生微米级气泡(图1(a));气泡迅速膨胀,引起围绕气泡的微流动和相应的剪切应力,剪切应力可以通过由微泡表面上的温度梯度产生的热毛细作用力而增大(图1(b));细胞上的剪切应力还可以在膜中产生纳米级孔,增强膜的通透性,并且对细胞的不利影响很小,气泡的大小在不停地振荡,细胞膜变得对分子是可渗透的(图1(c));当激光消失后,穿孔也立即停止并且细胞膜快速复原(图1(d))。由于激光诱导产生的气泡存在的时间在几十微秒到几百微秒量级,所以细胞膜受到气泡冲击波的作用时间短,细胞的活力不会受到气泡产生的冲击波的影响。从他们实验的结果中可以看到,气泡最佳的位置是离细胞5 μm范围内,穿孔效率可以达到95%,且细胞活性达到97%[10]。
这个实验的创新点是:(1) 将激光击穿液体形成空泡现象与微腔室结合,对细胞进行穿孔操作;(2) 利用激光击穿液体空泡的剪切力,使细胞壁破裂,从而进行物质交换;(3) 使用微秒激光器,作用时间短,从而细胞膜还可以恢复,使细胞保持活性。
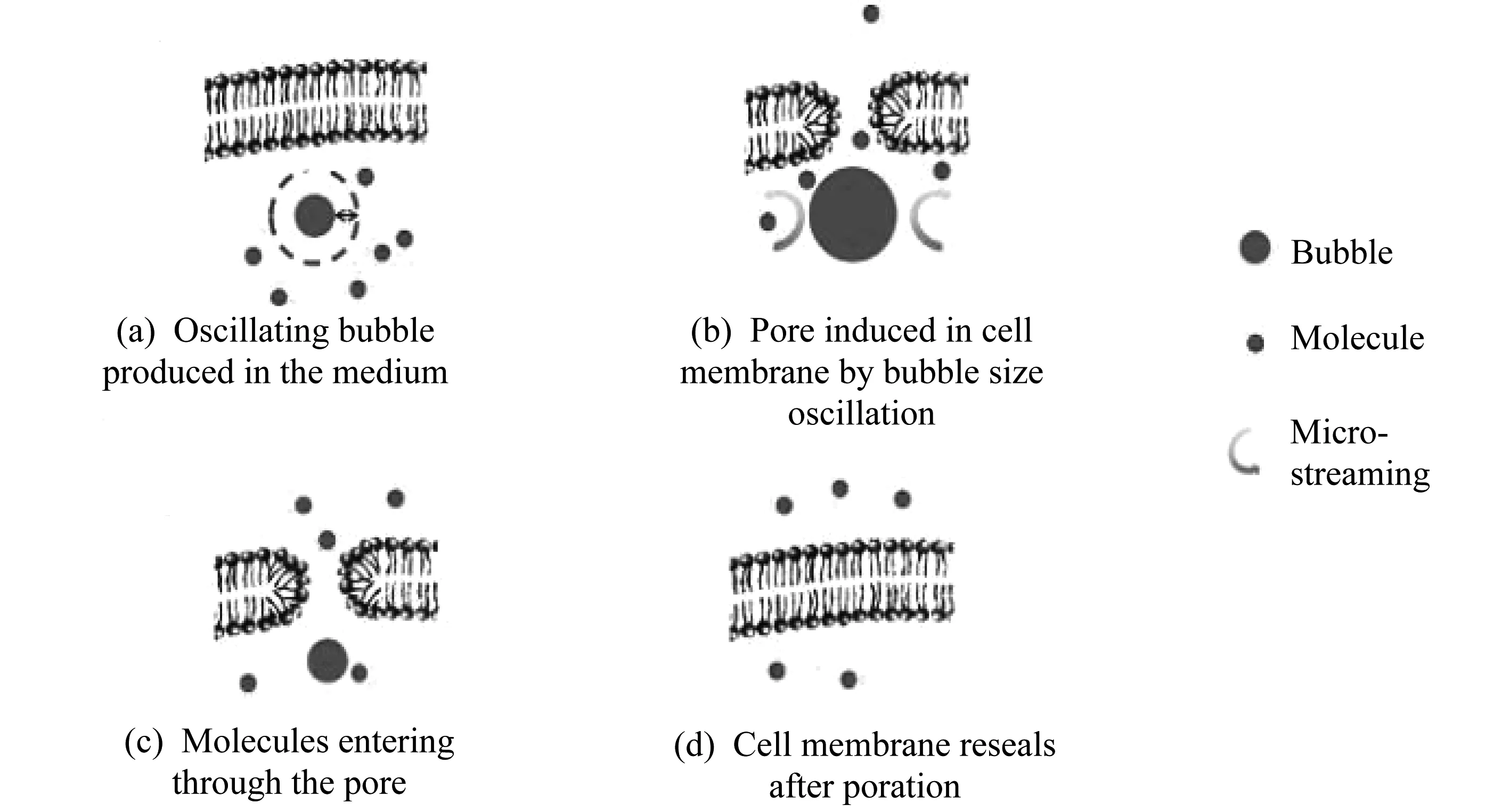
图1 激光诱导细胞穿孔的原理图Fig.1 Laser induced cell perforation
2 激光诱导空泡现象用于细胞检测
红细胞的弹性特性可作为几种疾病的检测指标[11-12],例如,恶性疟原虫加强感染的红细胞,即感染的细胞具有更高的弹性模量,并且在比未感染的细胞更短的时间内恢复它们的形状。红细胞弹性的变化也是身体识别需要从流通中除去的老化红细胞的一种自然方式[13],研究人员已经证明了几种衡量红细胞机械性能的方法,其中有微量吸管[14]、扭转微磁珠[15]、原子力显微镜[16]、剪切流[17]、光学镊子[18-19]和光学担架[20]等方法。
新加坡南洋理工大学研究人员将激光诱导空化现象应用到微腔内,利用气泡冲击波的冲击力对红细胞产生应力形变,再通过观测细胞恢复所需的时间,从而算出不同红细胞的细胞膜硬度,如图2所示,进而通过这种方法对红细胞的细胞膜硬度进行测定,来判断红细胞是否受到病毒感染[21]。他们所使用的激光器是倍频Nd:YAG激光器,在532 nm处产生持续时间为6 ns的单个激光脉冲,微流控芯片结构由两个显微镜盖滑块(尺寸22 mm×40 mm)制成,并用15 μm高的扁平铝箔间隔隔开。总之,新方法的优点是,只需要利用一束脉冲激光就可同时探测多个单元且周转时间少于1 s。技术的处理被大大简化,因为没有外部探针需要连接到细胞(如对于光学镊子和磁性微珠技术),或者单个细胞需要精确地与交叉的一对光纤对准(如光学担架的技术)。与现有技术方法相比,这种简化允许在相对短的时间内获得大量的统计数据。

图2 红细胞气蚀实验Fig.2 The experiment of red blood cells during the cavitation event
此外,该方法中的所有步骤(例如,探测、图像采集和分析以及样品分类)都可以集成到实验室自动化的芯片平台中,用于测试大量细胞群体的机械性能。将来,这种方法还可以应用于研究溶液中其他种类的细胞,例如探测良性和恶性白细胞之间机械性能的差异。
3 激光诱导空泡现象与微流控的结合用于细胞筛选
将微型流体装置用于生物细胞操作,再搭配微型计算机实现自动化的系统具有很大的应用前景。因为这种计算机控制的自动化微型流体装置可以降低试剂成本和反应时间,改进了小型化系统中质量和传热控制[22-26]。微流体的机制包括:通过膜阀实现的气动泵送[27],通过电动力学机制的电渗[28]、介电泳[29]以及光学力[30]、光热[31]和压电致动器[32]等。
加州大学洛杉矶分校研究人员利用高度聚焦的激光束可以在几纳秒内以高达100 m/s的快速膨胀速度和几十MPa的内部压力引发蒸汽气泡,并且这种快速响应和较强的冲击力所引起的激光触发空化气泡可以强烈扰乱通道附近流动的流体。他们采用脉冲持续时间为15 ns的Nd:YAG激光器,其倍频波长为532 nm,能量为108 μJ,聚焦在50 μm宽的微流体通道的中间。该团队利用这个现象做了3种新颖的应用,分别是高速微流体开关,超高速微液滴生成装置和荧光细胞筛选器[33],其中:高速微流体开关可以在2 μs内变形20 μm的距离,这是到目前为止,已经证实的最快的微流体驱动;超高速微液滴生成装置,能够根据需要产生均匀的油浸水滴,尺寸范围为1~150 pL,速度每秒能达到1万滴;荧光细胞筛选器是利用了脉冲激光触发荧光激活微流体开关的原理。
图3为荧光细胞筛选器的实验原理图,该设备由具有两个出口的收集和废弃物的主微通道(或样品通道)组成,使用惯性流体动力学聚焦,待筛选的细胞流向废弃物通道。当荧光细胞流过Y结的顶部时被检测,同时将通过高数值孔径的物镜聚焦的激光脉冲触发到与主通道平行运行的脉冲通道,聚焦的激光脉冲引起随后的气蚀气泡。当气泡膨胀时,周围的液体被推开并通过喷嘴开口挤入主通道,并将荧光细胞挤进收集通道中。这个实验还可以通过优化微流腔的体积和待测细胞液的浓度等参数来分析筛选的效率。

图3 荧光细胞筛选器的实验原理图Fig.3 The schematic diagram of fluorescence cell filter experimental
4 激光诱导空泡现象用于眼科手术
由于激光能量很高,超短激光脉冲的紧密聚焦导致聚焦处发生非线性吸收过程[34-36],利用光破坏的基本物理作用将其应用于生物组织的剥离。因此,眼科手术一般用飞秒激光器,由于激光作用在眼球的时间短,对组织其他部分影响小。将单个超短激光脉冲聚焦到透明生物组织的水性介质后的基本相互作用原理已被广泛研究[37-40]。
德国汉诺威生物医学光学系的Nadine Tinne博士等,用飞秒激光器发射出两个不同时间间隔和聚焦位置的脉冲激光,研究这两个激光诱导气泡的相互作用影响[41]。他们用中心波长1 040 nm、脉冲宽度389 fs、重复频率100 kHz的IMRA America Inc.(Ann Abor,USA)的飞秒激光系统,通过扫描高重复率飞秒激光器的组织切割实验发现,这可能会导致空化气泡和后续激光脉冲在聚焦处发生空间和时间上的重叠,两个气泡的重叠会导致出现喷射流(如图4所示),这会对其他组织造成影响。这项研究表明,为了提高光致破坏效率或轴向精度并减少不必要的副作用,必须避免高重叠,才可以确保微创手术的准确性。在眼科手术中,激光能量应该接近略高于击穿阈值来解剖组织。现有的实验都是在猪的眼球玻璃体上进行,实际人眼的情况会更加复杂。
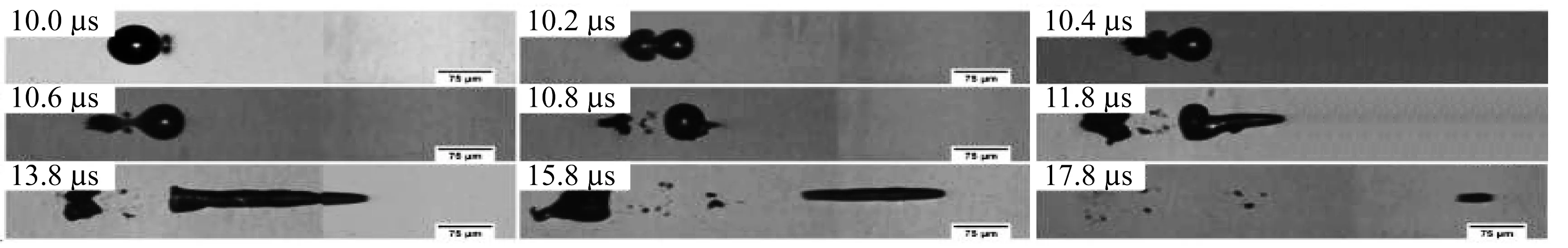
图4 两个腔相互作用的气泡动力学形成射流(71.8 μm的焦距分离和激光脉冲能量是击穿阈值的10.7倍)Fig.4 Bubble-kinetic jet formation with two cavities interacting(the focal length separation for 71.8 μm and the laser pulse energy is 10.7 times the breakdown threshold)
此类实验对激光的焦点要求很高,误差不能超过1 μm,因此,可以考虑使用自带会聚镜头的光纤激光器来侵入到样品,这样可以排除样品内部自聚焦等影响,使实验结果具有更高的可信度。
5 总结与展望
本文介绍了激光诱导空泡的神奇现象,正所谓量变产生质变,即当单脉冲激光的能量密度达到某介质的击穿阈值[42-45]的时候,就会产生一些非线性效应,如多光子电离机制[46-49]和雪崩电离机制,进而产生等离子体[50],并伴随等离子体闪光现象。等离子体通过逆韧致机制和共振机制继续吸收激光能量[51],进而产生空化气泡现象,并伴随冲击波的形成[52-55]。冲击波的产生是激光切割的副产品,冲击波将会对待切割组织的其他部位产生不利的影响,还会有射流的形成。未来在激光微创手术的研究中,应考虑如何避免伴随激光诱导气泡形成的冲击波,或者考虑如何降低冲击波带来的不利影响。生物组织内部结构复杂,既有似水流体,又有组织结构固体,因此,激光导入生物组织内部会有一些自聚焦和散射的不利于激光传播的影响。这方面可以考虑借鉴光学相干断层扫描技术(optical coherence tomography,OCT)的做法,预埋一根光纤就可以将激光安全地导入生物组织内部。还有在等离子体运动的控制上,可以考虑加上一定的磁场来控制等离子体的运动,从而降低对组织其他部位的不利影响。这种非侵入式的医学治疗手段,可以大大缓解病人的伤痛,降低手术带来的副作用,使病人更容易接受。非侵入式医疗技术在未来的临床手术中的地位将越来越高,成为主流医疗技术。
在微流控领域,我们可以利用激光诱导气泡产生的局部巨大能量来做成一些微小器件,从而对单细胞进行有效的操作,例如,检测单细胞的健康情况、筛选单细胞以及分子注入单细胞等操作。我们可以看到,激光诱导空泡现象对生物医学的发展已经提供了不少帮助,产生了一些积极影响,未来还会跟计算机领域有所合作,从而代替实验员的手来实现自动化操作,使一些需要细微操作的实验更容易实现,并且使实验结果的可信度大大提高。

