Fenton氧化法分解水中硝酸异丙酯
陈永康,安振涛,陈明华,张 力
Fenton氧化法分解水中硝酸异丙酯
陈永康1,安振涛1,陈明华2,张 力1
(1.陆军工程大学石家庄校区,河北 石家庄,050003;2. 特种勤务研究所,河北 石家庄,050003)
采用Fenton试剂氧化法对水中硝酸异丙酯进行处理,通过正交试验研究了各个工艺参数对反应的影响,以及间接碘量法对硝酸异丙酯含量进行测定。结果表明:当反应条件为0.4mol/L H2O2、60mmol/L FeSO4、pH值6,温度80℃时,硝酸异丙酯的去除率可达到86%;H2O2浓度、FeSO4浓度、pH值、温度各因素对反应效果的影响依次减弱。对氧化反应进行了动力学计算,发现反应遵从一级反应动力学,优方案的速率常数为0.023min-1。
硝酸异丙酯;Fenton试剂;无害化处理
硝酸异丙酯是一种硝酸酯类物质,在国防建设中发挥着重要作用[1]。据统计,配用硝酸异丙酯的某型火箭,现在已经到达并超过可靠储存寿命末期,必须及时进行报废处理。当前正在采用的硝酸异丙酯处理方法主要是烧毁或者自然挥发,这两种处理方法都存在着环境污染、危险性较大、资源浪费等问题[2-3]。而目前还没有针对硝酸异丙酯的安全无污染的销毁处理方法。硝酸异丙酯与普通酯类不同,其氧化性很强。目前有关于利用Fenton试剂处理硝化甘油和二缩三乙二醇二硝酸酯的研究,已取得了较好的效果[4-5]。本研究针对硝酸异丙酯的特性,采用Fenton试剂氧化的化学方法对水中硝酸异丙酯进行处理,最终实现硝酸异丙酯安全绿色的分解处理。
1 试验
1.1 试验原理
Fenton试剂为Fe2+/H2O2溶液[6],H2O2在Fe2+的催化下生成氧化能力很强的·OH自由基,同时·OH自由基还具有很高的电负性,具有很强的加成反应特征[7],因此普通氧化剂难以氧化的水中有机物,利用Fenton试剂都可以达到良好的效果。
本文选用Fenton试剂来氧化水中的硝酸异丙酯,使之分解。而后采用间接碘量法来测定剩余硝酸异丙酯的含量,以确定硝酸异丙酯的去除率。
目前水中的硝酸异丙酯还没有相应的测定方法,一般硝酸酯的含量可通过比色法[1]来测定。具体方法是硝酸酯在浓硫酸作用下与硫酸亚铁铵作用,生成紫红色络合物,硝酸酯含量越高,溶液颜色越深,通过分光光度计测试溶液光度来测定硝酸酯的含量。而试验证明,加入硝酸异丙酯后没有紫红色络合物生成,因此该方法不适用于硝酸异丙酯。
本文通过间接碘量法测定水中硝酸异丙酯含量,其反应机理如下:
C3H7NO3+ 3K2Cr2O7+ 12H2SO4
→ 3K2SO4+ 3Cr2(SO4)3+ 3CO2+ HNO3+ 15H2O
7H2SO4+ K2Cr2O7+ 6KI
→Cr2(SO4)3+ 4K2SO4+ 7H2O +3I2
I2+ 2Na2S2O3→ 2NaI + Na2S4O6
1.2 试验仪器及试剂
仪器:pH计、恒温水浴锅、滴定管、天平等。
试剂:分析纯的30%过氧化氢、七水硫酸亚铁、硝酸异丙酯、重铬酸钾、碘化钾、硫代硫酸钠、80%浓硫酸、0.5%可溶性淀粉指示剂等。
1.3 试验方法
配制150mL硝酸异丙酯水溶液,硝酸异丙酯质量分数为0.4%。用硫酸调节pH值(氧化体系的初始pH值是Fenton试剂氧化的重要条件),而后升温至相应温度,加入硫酸亚铁,搅拌后,加入过氧化氢。在反应20min、40min、60min、80min、8h时各取20mL样品,用间接碘量法测定硝酸异丙酯含量,从而得到硝酸异丙酯的去除率。间接碘量法的具体方法是:量取20mL反应后的硝酸异丙酯溶液,倒入锥形瓶内,用天平称得溶液质量。取重铬酸钾加入到锥形瓶内,摇匀后倒入硫酸,摇晃锥形瓶,加入碘化钾,摇匀后用配制好的硫代硫酸钠溶液进行滴定。接近终点时,加入2~3mL淀粉指示剂,继续小心滴定至溶液变色为终点,记下硫代硫酸钠溶液消耗的毫升数。其中称取(量取)的重铬酸钾、碘化钾、硫酸均为过量10%左右,以保证能够完全反应。用于间接碘量法滴定的硫代硫酸钠溶液,经标定浓度为0.182 5mol/L。
硝酸异丙酯在溶液中的质量分数为:
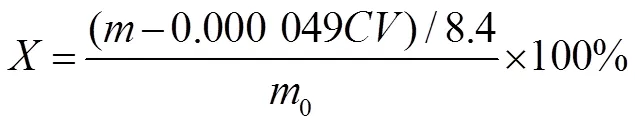
式(1)中:为加入的重铬酸钾质量,kg;为滴定消耗的硫代硫酸钠溶液体积,L;为硫代硫酸钠标准溶液的浓度,mol/L;0为待测溶液质量,kg。利用正交试验来综合考量试剂用量、pH值、反应温度等工艺参数对氧化反应的影响。其中,由于硝酸异丙酯沸点与水接近,容易挥发,因此将反应温度控制在80℃以下。表1为相关因素及水平。据此设计4因素5水平的正交试验。
表1 相关因素及水平
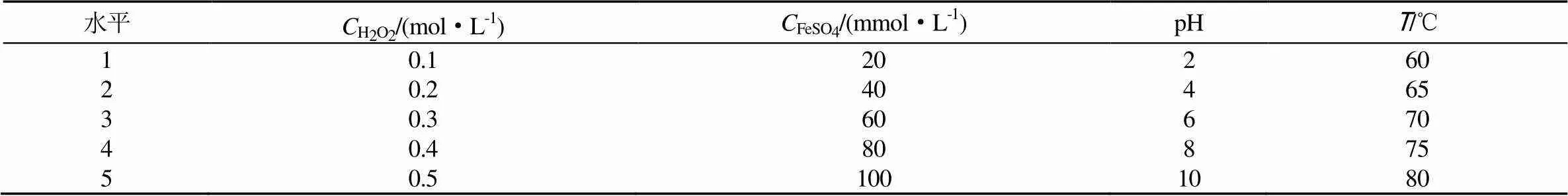
Tab.1 Factors and levels of experiments
2 结果与讨论
2.1 正交试验结果及分析
正交试验表和硝酸异丙酯最终的去除率如表2所示。
表2 正交试验数据
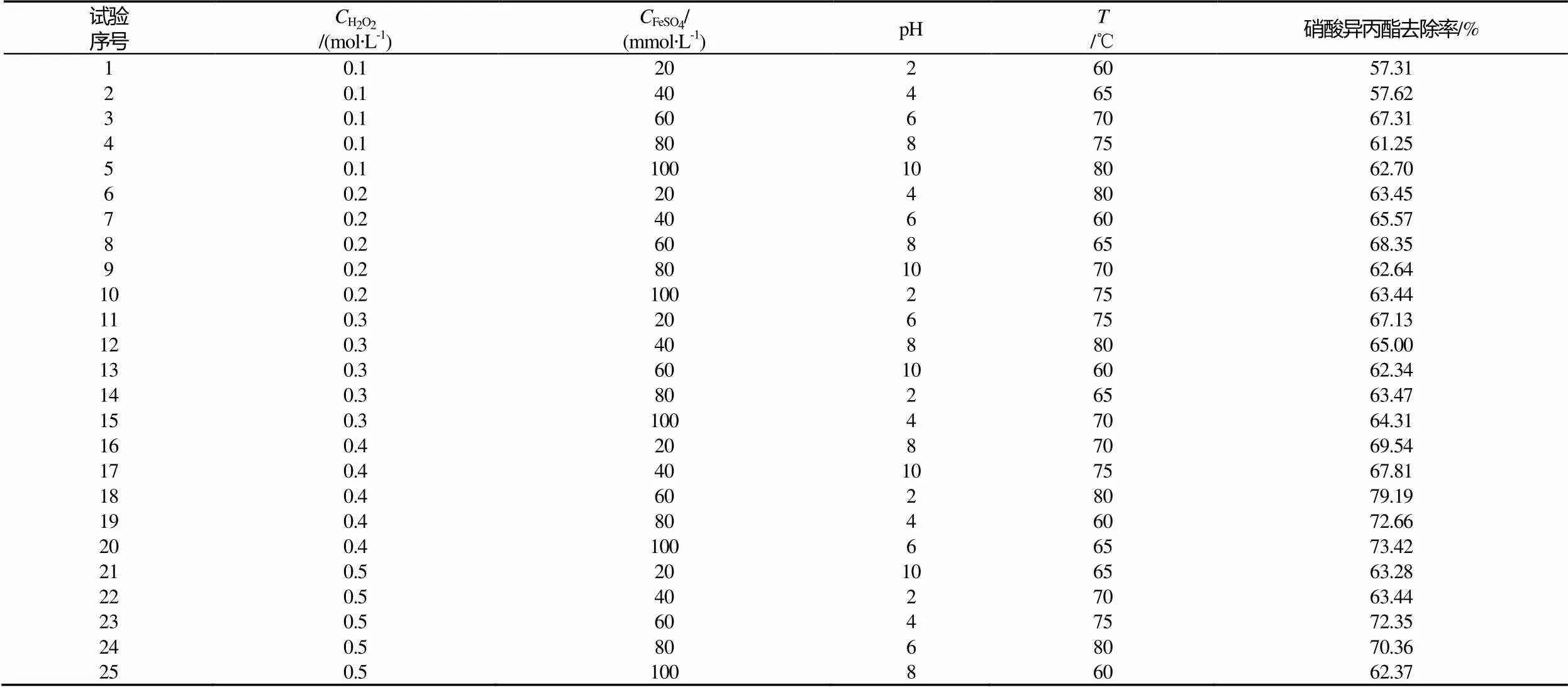
Tab.2 Orthogonal experiments data
对表2的正交试验数据进行极差分析,结果如表3所示,方差分析结果如表4所示。
表3 正交试验的极差分析
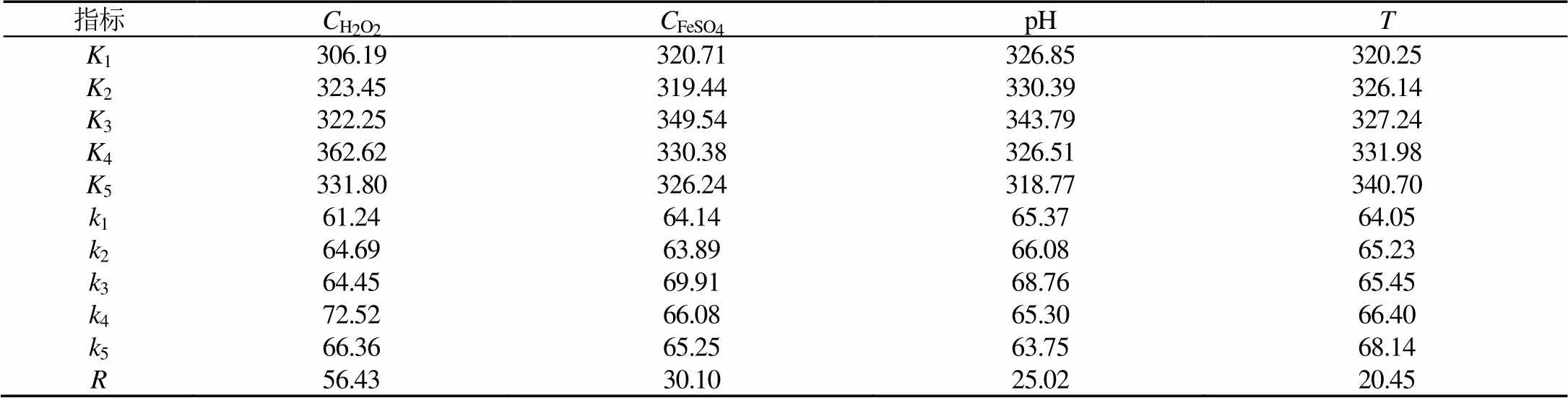
Tab.3 Range analysis of orthogonal experiments
注:K为任一因素水平号为时,所对应的的试验结果之和;k表示任一因素水平为的试验结果的算术平均值;为极差。
表4 正交试验的方差分析
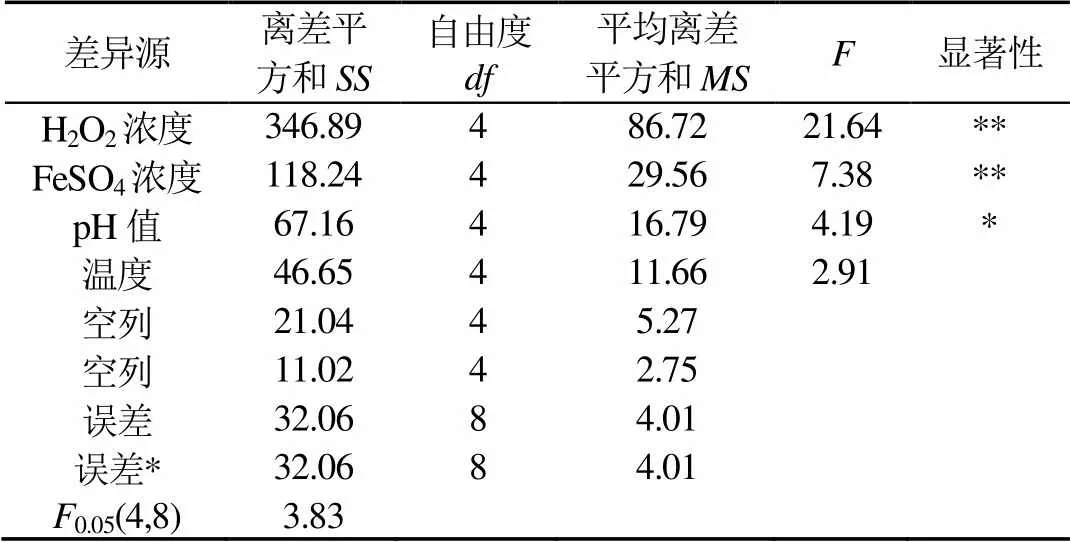
Tab.4 Variance analysis of orthogonal experiments
由表3比较极差可知,各因素的主次顺序为H2O2浓度,FeSO4浓度,pH值,温度。通过比较值的大小可得到试验的最优方案:H2O2浓度为0.4mol/L,FeSO4浓度为60mmol/L,pH值为6,温度为80℃。根据最优方案进行硝酸异丙酯的去能分解试验,其去除率可达到86%。由表4可以发现H2O2浓度、FeSO4浓度和pH值因素对试验结果影响显著,但温度因素对结果没有显著影响,一是由于温度的升高主要是提高了氧化反应的反应速率,对最终硝酸异丙酯的去除率影响相对较小;二是温度因素的水平为60~80℃,所选范围并不大,导致检验结果不显著。
2.2 工艺参数对试验效果的影响
根据正交试验数据,做4个因素对硝酸异丙酯去除率的影响趋势图,如图1所示。由图1(a)可知,随着H2O2浓度的逐渐增大,硝酸异丙酯的去除率呈现先增大后减小的趋势,当H2O2浓度为0.4mol/L时,硝酸异丙酯的去除效果最好。在低浓度情况下,随着H2O2浓度的逐渐增大,生成的自由基不断增多,促进了氧化反应的进行,硝酸异丙酯的去除率逐渐增大。当浓度过高时,在反应初期,H2O2就将Fe2+氧化为Fe3+,抑制了催化反应的进行。同时也有研究认为[8]:当H2O2浓度相对较低时,·OH主要与被氧化物反应,副反应较少,而当H2O2浓度过高后,发生副反应HO· + H2O2→ H2O· + H2O和HO·+ H2O·→ H2O + O2,消耗H2O2和·OH,导致氧化的效果下降。
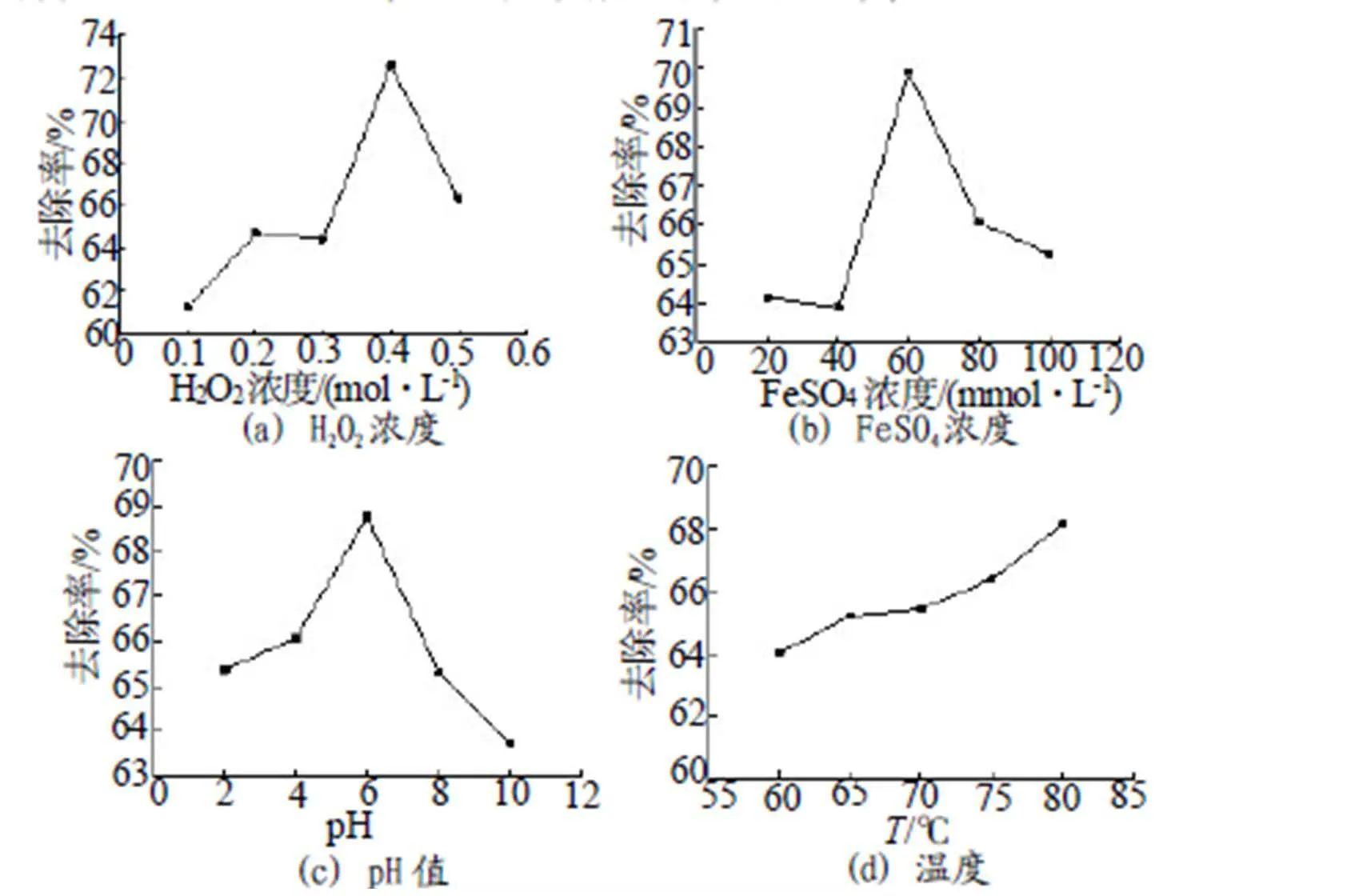
图1 4因素对去除率的影响趋势图
从图1(b)可以发现,硝酸异丙酯的去除率呈现先增大后减小的趋势,当FeSO4浓度为60mmol/L时,硝酸异丙酯的去除效果最好。这是由于当FeSO4浓度较低时,其浓度的不断增加促进了催化反应的进行,使得·OH的浓度升高,导致硝酸异丙酯的去除率升高。而当FeSO4浓度过高时,过量的Fe2+被氧化成Fe3+,消耗了·OH;同时当Fe2+浓度过高时,还会发生以下副反应[9]:
Fe2++ ·OH + 2H2O → H++ Fe(OH)3↓
2H2O + 2Fe3++ 3H2O2→6H++ 2H2FeO4
2H2FeO4+ 3H2O2→ 2H2O + 3O2+ 2Fe(OH)3↓
从图1(c)可知当pH=6时,去除率最高,当pH值继续增大,硝酸异丙酯去除率又开始降低。这是由于当溶液pH值过低时,Fe3+还原成Fe2+的反应被抑制,导致·OH自由基的生成受阻。而当溶液pH值过高,呈中性或碱性时,会抑制自由基的生成,同时Fe2+与氢氧根生成氢氧化物形成沉淀,导致·OH自由基的生成受阻,从而抑制了催化反应。
由图1(d)可知,尽管显著性检验表明温度因素对试验效果的影响并不明显,但随着温度的逐渐升高,硝酸异丙酯的去除率还是呈上升趋势。这是因为温度的升高有利于硝酸异丙酯氧化反应的加速进行,但Fenton试剂氧化反应是一个复杂的反应体系,其中包含了许多副反应[10],温度的升高同时也会加速副反应以及逆反应的进行,因此在本文所选的60~80℃温度范围内,硝酸异丙酯的去除率变化并不太明显。
2.3 氧化反应的动力学研究
试验在反应的20min、40min、60min、80min时各取20mL样品,用间接碘量法测定硝酸异丙酯含量,监测硝酸异丙酯的去除率变化情况,以此确定反应时间,并进行动力学研究。根据不同时间的含量测定结果,发现硝酸异丙酯的氧化去能反应在80min时基本达到终点。而后对优方案的酯含量测定数据进行动力学计算,首先确定反应级数,根据零级、一级、二级以及三级反应的动力学方程[10],以时间为横轴,分别以C,-In(C/0),-(l/0-l/C)为纵轴,作拟合曲线,计算线性相关系数。其中0为硝酸异丙酯的初始浓度,C为反应时间后硝酸异丙酯的残留浓度。结果如图2所示。从图2中可知,相关性最好的是按一级动力学方程的拟合结果,相关系数为0.998 2。因此判定Fenton氧化硝酸异丙酯的反应遵从一级化学反应动力学。其动力学方程为C=0exp(-),根据拟合曲线的斜率,可知速率常数=0.023min-1。
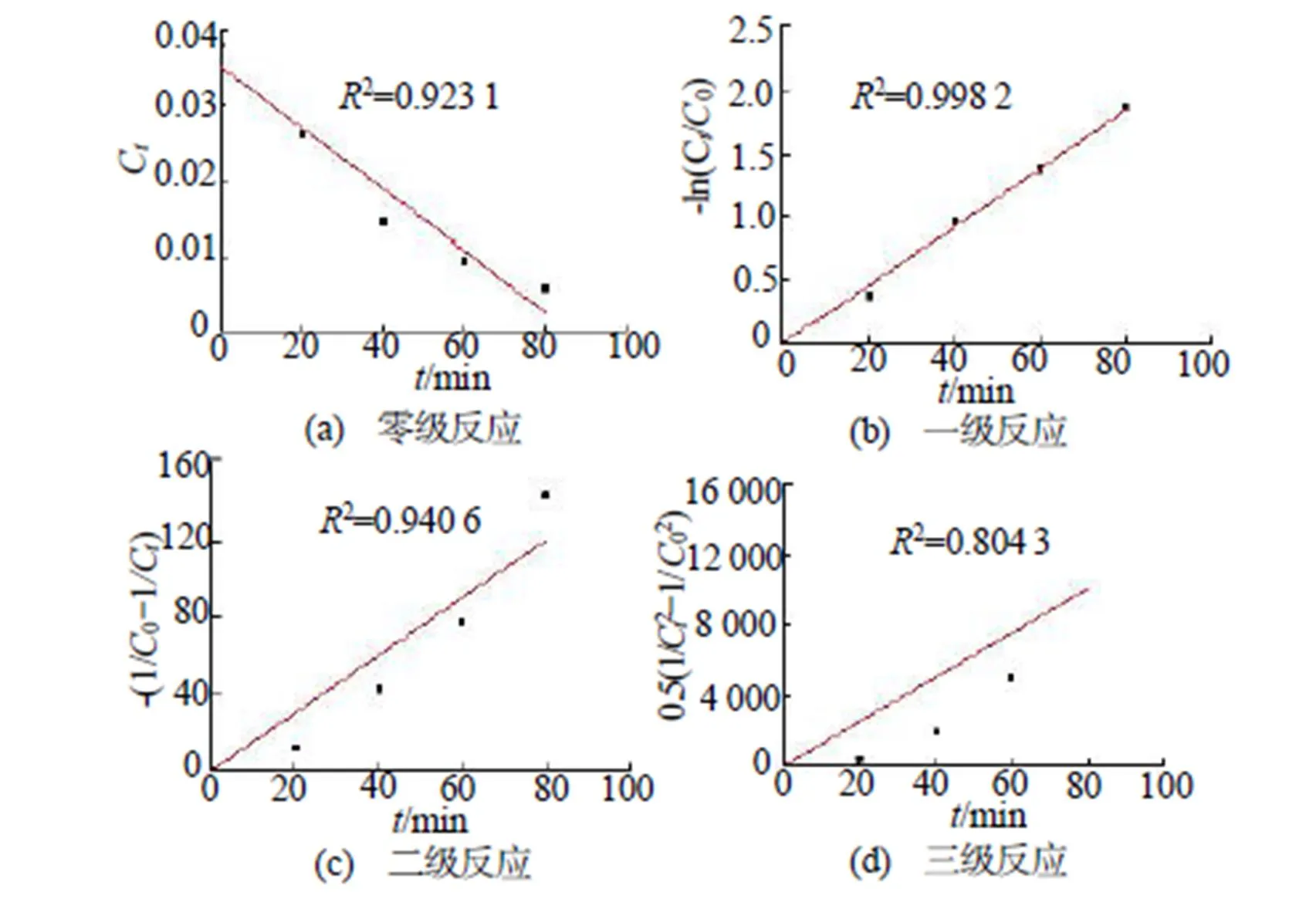
图2 动力学曲线拟合
3 结论
本文采用Fenton试剂氧化法对水中硝酸异丙酯进行处理,得到以下结论:(1)采用间接碘量法测定硝酸异丙酯含量,确定了水中硝酸异丙酯含量测定的新方法。(2)当反应条件范围为H2O2浓度0.35~0.45 mol/L,FeSO4浓度50~70mmol/L,pH值4~6,温度70~80℃,硝酸异丙酯的去除效果较好。经正交试验,确定优方案为H2O2浓度0.4mol/L,FeSO4浓度60mmol /L,pH值6,温度80℃。此时硝酸异丙酯的去除率可达到86%。各因素对反应效果影响的主次顺序为H2O2浓度、FeSO4浓度、pH值、温度。(3)Fenton氧化硝酸异丙酯的反应遵从一级化学反应动力学,优方案的速率常数=0.023min-1。
本文针对水中硝酸异丙酯的含量测定方法和去能处理方法将会为今后硝酸异丙酯的去能分解提供重要的理论依据和指导。
[1] 曾秀琳.硝酸酯热安定性的理论与试验研究[D].南京:南京理工大学, 2007.
[2] Chen W S, Chiang W C, Lai C C. Recovery of nitrotoluenes in wastewater by solvent extraction[J]. Journal of hazardous materials, 2009, 145(1-2): 23-29.
[3] Machacek Oldrich, Eck Gary R. Development of new high energy blasting products using demilitarized ammonium picrate:US, 6214140[P]. 1999-09-22.
[4] 刘亮,张银玲,王中合,等. Fenton法分解NG/TEGDN废水研究[J].固体火箭技术, 2014, 37(4):396-400.
[5] 李峰,张小军,樊娟.含混合硝酸酯废水处理工艺研究[C]//中国宇航协会固体火箭推进第22届年会论文集,2005.
[6] Kym B Arcuri, Duane A Goetsch, Steve J Schmit, et al. Recovery of TNT and RDX from bulk composition B explosive: US, 7423187B1[P]. 2008-09-09.
[7] 胡树枝,刘登里.还原-氧化-石灰法处理氯代硝基苯废水的研究[J].山西化工, 2010, 30(4): 57-60.
[8] Kavitha V, Palanivelu K. Degradation of nitrophenols by fenton and photo-fenton processes[J].Journal of Photo- chemistry and Photobiology A: Chemistry, 2005, 170(l): 83-95.
[9] B Muthukumari, K Selvam, I Muthuve, et al. Photoassisted hetero-Fenton mineralisation of azo dyes by Fe(II)-Al2O3catalyst[J]. Chemical Engineering Journal, 2009, 153(3): 9-15.
[10] Ting, W P, M C Lu, Y H Huang. Kinetics of 2, 6-dimethyla- niline degradation by electro-Fenton process[J]. Journal of Hazardous Materials, 2009, 161(2-3):1 484-1 490.
Treatment of Isopropyl Nitrate in Water by Fenton Reagent Oxidation Method
CHEN Yong-kang1,AN Zhen-tao1,CHEN Ming-hua2,ZHANG Li1
(1.Army Engineering University Shijiazhuang Campus, Shijiazhuang, 050003;2.Ordnance Technology Research Institute, Shijiazhuang, 050003)
Isopropyl nitrate in water was treated by Fenton reagent oxidation method. Orthogonal experiments were used to study the effects of various process parameters on the reaction, and indirect iodometric titration method was used to determine the isopropyl nitrate content. The results show that isopropyl nitrate removal rate can reach 86%, when the reaction conditions are H2O2concentration at 0.4mol/L, FeSO4concentration at 60mmol/L, pH at 6, temperature at 80℃. The effects of H2O2concentration, FeSO4concentration, pH and temperature on the reaction decrease in turn. The oxidation reaction is found to follow the first order kinetics, the rate constant of the optimal conditions is 0.023min-1.
Isopropyl nitrate;Fenton reagent;Innocent treatment
1003-1480(2018)03-0043-04
TQ560.79
A
10.3969/j.issn.1003-1480.2018.03.011
2018-03-16
陈永康(1991 -),男,博士研究生,主要从事弹药保障与安全技术研究。

