鱼明胶/海藻酸钠复合凝胶特性研究
刘凤华, 刘佳林, 陈 浩, 王 煚, 杨梦煊, 姚 瑶
(山东大学(威海)海洋学院,山东威海264209)
凝胶是一种高分子聚合物[1],在特定条件下,体系中的高分子链相互交联形成三维网络结构,在溶剂内溶胀而不溶解。水凝胶具有一定流体性质、黏弹性和良好的生物相容性,故而被广泛应用于医药、食品等行业[2-3]。而在实际生产中,水凝胶多是以天然多糖为原料制备的单网络凝胶,其性能往往不能满足产品需要[4]。随着水凝胶应用范围的不断扩大,各种复配胶的性能及作用机理成了国内外的研究热点[5]。近几年,国内研究的主要是多糖复合凝胶,对蛋白质与多糖的复配则鲜有报道[6]。
蛋白与多糖是食品体系中最常见的高聚物,对构建食品的微结构也起着重要作用,但二者的共混体系热力学不相容[7-9]。已有研究表明,通过共混、交联制备互穿网络聚合物的方法能改善材料性能[10]。因此,研究蛋白与多糖的复配及凝胶性质,有望获得高品质的凝胶产品[11-12]。
鱼明胶是从鱼皮、鱼骨和鱼鳞等部位提取出来的胶原经过进一步水解获得的多肽。安全无毒并且具有许多优良性质的鱼明胶已作为海洋资源开发利用的典范,成为食品加工领域中的重要新材料[13]。海藻酸钠是从褐藻中获取的一种多糖,因其分子链中存在大量亲水性基团(—COOH和—OH)而具有很好的生物相容性[14]。鱼明胶和海藻酸钠单独在食品中的应用国内外都有较深入的研究[15-18],但二者单一网络凝胶各自的力学性能较差,限制了它们的进一步应用,而有关二者在适宜的条件下能否交联形成双网络凝胶的报道也很少[19]。有鉴于此,文章在优化鱼明胶单一网络凝胶的研究基础上,添加海藻酸钠,制备二者双网络凝胶,并对其凝胶特性进行研究,以期得到性质更为优良的凝胶产品。
1 材料与方法
1.1 材料与试剂
250 BL-60鱼明胶,嘉吉亚太食品系统(北京)有限公司;海藻酸钠(食品级),郑州食全食美商贸有限公司;氯化钠(分析纯),天津市瑞金特化学品有限公司;硅油(分析纯),莱阳经济技术开发区精细化工厂。
1.2 仪器与设备
YP601N型电子天平(准确度等级(Ⅲ)),上海精密科学仪器有限公司;CP224C型电子天平(准确度等级(Ⅰ)),奥豪斯仪器(上海)有限公司;RHKT/C型磁力搅拌器,IKA Works Guangzhou;EMS-12型磁力搅拌器,天津欧诺仪器仪表股份有限公司;B-260型恒温水浴锅,上海亚荣生化仪器厂;DHG-9140A型电热恒温鼓风干燥箱,上海精宏实验设备有限公司;NR110型精密色差仪,深圳市三恩驰科技有限公司;Hakke Mars 3型流变仪,德国Hakke公司。
1.3 实验方法
1.3.1 凝胶制备
1.3.1.1 鱼明胶单网络凝胶制备
预实验制备鱼明胶凝胶时,发现质量浓度在0.05 g/mL以下的鱼明胶凝胶成型性差甚至无法形成凝胶,因此实验将鱼明胶用蒸馏水配制成0.06、0.07、0.08、0.09、0.10 g/mL 5 个梯度的溶液,磁力搅拌1 h使其充分溶解,后放置于4℃冰箱冷藏24 h,待充分水化。将水化后的鱼明胶置于60℃的B-260型恒温水浴锅中加热30 min,然后称取50 g该溶液倒入9 cm×9 cm塑料培养皿中,室温静置存放20 min后,4℃冷藏24 h使其充分形成凝胶。用模具取2 cm×2 cm×3 cm圆柱体凝胶,测定各项指标。
1.3.1.2 鱼明胶/海藻酸钠复合凝胶制备
将0.08 g/mL鱼明胶与不同质量浓度海藻酸钠复合,制备复合凝胶。称取一定质量鱼明胶和海藻酸钠粉末,用蒸馏水配制成溶液(见表1),磁力搅拌1 h后,放入4℃冰箱冷藏24 h以保证鱼明胶、海藻酸钠充分水化。后续方法同1.3.1.1所述。
1.3.2 感官评定
对制备好的凝胶,先观察其颜色、透明度和成型性;再用手适度按压,判断凝胶的硬度、质地等特征。
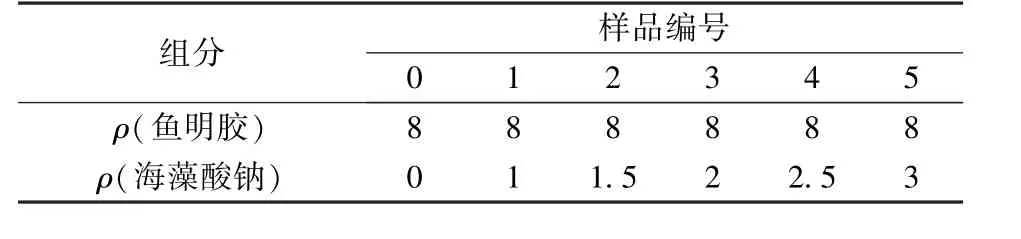
表1 不同质量浓度复合凝胶样品组成Tab.1 Samples with different mass concentration 10-2 g/mL
1.3.3 凝胶色度测定
用NR110型精密色差仪测定凝胶色度,并用白板校准。L*表示照度即明亮指数(L*=0表示黑色,L*=100表示白色),a*表示红绿值(+a方向是红色方向,-a方向为绿色方向),b*表示黄蓝值(+b方向是黄色方向,-b方向是蓝色方向)。
1.3.4 流变性质测定
采用Hakke Mars3型流变仪测定样品流体力学性质。选择型号为P35TiL的转子和35 mm的平行板测量系统,平行板间距1 mm,频率1 Hz,应变0.5%。用移液枪取1 mL样品于流变仪样品台上,用硅油密封缝隙防止水分蒸发,平衡5 min。以5℃/min升温速率将样液从室温连续加热至60℃,平衡10 min后再以5℃/min速度冷却至10℃。记录整个过程中贮能模量G′和损耗模量G″的变化,其中G′越大,弹性越大,G″越大,黏性越大。加热-冷却循环之后,在10℃下对凝胶进行频率扫描(0.1~100 Hz),记录扫描过程中G′和G″的变化。
2 结果与分析
2.1 感官评价结果
随着鱼明胶质量浓度增加,凝胶颜色由无色透明逐渐呈现出淡鹅黄色,但透过凝胶观察纸上字迹,可以发现0.06~0.10 g/mL鱼明胶凝胶均具有良好的透明度,且成型效果良好(见图1)。
0.08 g/mL鱼明胶添加了不同质量浓度海藻酸钠制成的复合凝胶,选取了单一鱼明胶凝胶作为对照,结果见图2。发现随着海藻酸钠加入量增加,凝胶质地更加坚挺,但亮度和透明度略有下降。
鱼明胶单一凝胶的感官特征见表2。随着鱼明胶质量浓度增加,凝胶的颜色略有加深,质地更加坚挺,不易碎,韧性提高,成型性变好且均具有极高的透明度。鱼明胶与海藻酸钠复合凝胶的外观特征见表3。随着海藻酸钠加入量增加,凝胶的颜色略有加深,硬度增加,成型性得到显著改善。相比0.08 g/mL鱼明胶单一凝胶,复合凝胶的透明度略有下降但弹性明显提高。

图1 不同质量浓度鱼明胶凝胶样品Fig.1 Different mass concentration samples of fish gelatin

图2 不同质量浓度复合凝胶样品Fig.2 Different mass concentration samples of composite gelation

表2 不同质量浓度鱼明胶凝胶的感官评定Tab.2 Sensory evaluation of different mass concentration fish gelatin
2.2 色泽比较结果
2.2.1 鱼明胶质量浓度对单网络凝胶色泽的影响
鱼明胶凝胶的色度值L*、a*、b*和ΔE值随鱼明胶质量浓度变化见图3,其中 ΔE=[(ΔL*)2+(Δa*)2+(Δb*)2],并以0.08 g/mL鱼明胶凝胶作为对照,图中小写字母不同代表差异显著。
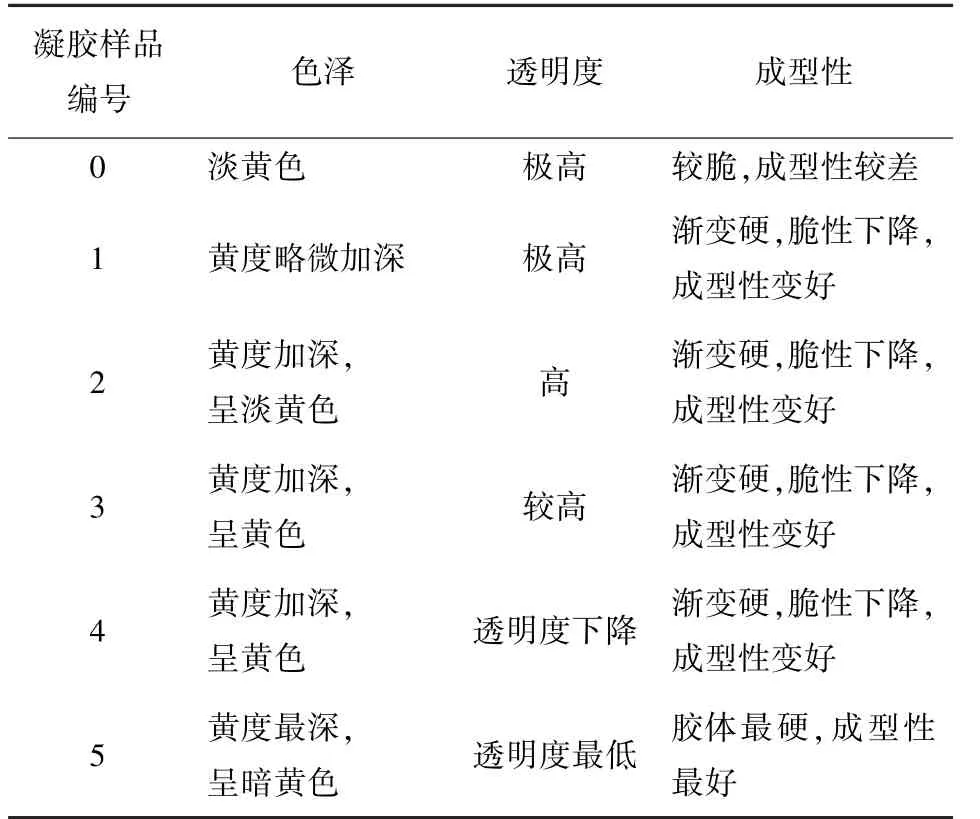
表3 不同质量浓度复合凝胶的感官评定Tab.3 Sensory evaluation of different mass concentration composite gelation
由图3可知,随着鱼明胶质量浓度增加,L*值从57.22降至54.26,亮度下降,a*和b*逐渐升高,ΔE值均小于6.5,即肉眼不能分辨凝胶色彩的差异。L*值可表征凝胶聚集物颗粒的数量和空隙的大小,间接表征凝胶网络的交联程度;一般而言,随机微粒聚合成的凝胶透光性差,有序结构状凝胶透光性好[20]。由此推断,鱼明胶质量浓度增加使凝胶聚集物颗粒数量增加,凝胶网络交联程度变大,凝胶的浊度变高,透光度变低,透过凝胶到达白色背景再反射回来的光线变弱,即明亮指数下降。虽然鱼明胶质量浓度增加使亮度变小,但是凝胶的整体色泽较均一,仍具有良好的视觉效果。
2.2.2 海藻酸钠质量浓度对复合凝胶色泽的影响
不同质量浓度复合凝胶色度值结果见图4,样品编号见表1,以0.08 g/mL单一鱼明胶凝胶为对照。随着海藻酸钠质量浓度提高,复合凝胶的L*持续下降,由1号样品的57.65,降低至5号样品的51.47,说明海藻酸钠的添加降低了复合凝胶的亮度。推测原因可能是多糖对于蛋白质凝胶有空间占位效应[21],添加海藻酸钠后,凝胶网络空间变得致密,不利于光线透过,使复合凝胶的明亮指数下降。各样品间a*值和b*值均有显著差异,且随着海藻酸钠质量浓度提高,逐渐升高。由图4d可知,复合凝胶的色度值较单一鱼明胶凝胶而言均表现出显著差异,海藻酸钠加入量为0.03 g/mL时,ΔE值高达8.92,说明样品间出现了肉眼可见的差别。

图3 不同质量浓度鱼明胶凝胶色度值Fig.3 Chromatic values of different mass concentration fish gelatin
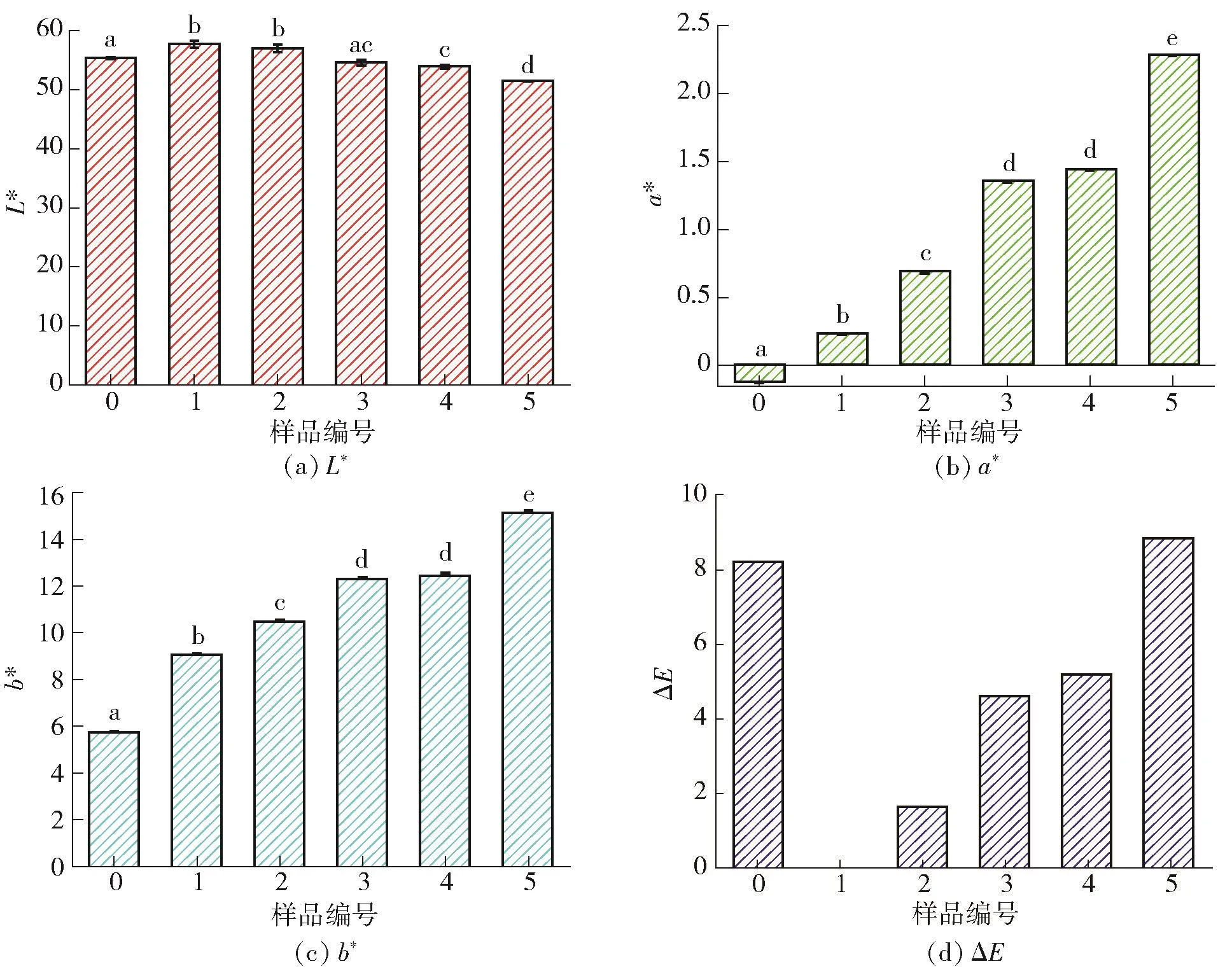
图4 不同质量浓度复合凝胶色度值Fig.4 Chromatic values of different mass concentration composite gelation
2.3 凝胶的流变性质分析
2.3.1 海藻酸钠对鱼明胶热诱导凝胶过程的影响
0.10 g/mL鱼明胶单一凝胶在升温过程中贮能模量G′及损耗模量G″的变化曲线见图5。由图5可知,升温过程中凝胶的G′和G″均降低,但G′的下降幅度较大;当温度升至接近40℃时,G″开始大于G′,说明体系开始由以弹性为主的凝胶状态向以黏性为主的溶胶状态转变,凝胶熔化。加热过程中G″和G′交汇点的温度即为熔化点[22-23]。其他质量浓度鱼明胶升温过程呈现相同趋势即交点。由此可知鱼明胶凝胶具有热可逆性,其黏弹性与温度有关,溶胶-凝胶态转折点在40℃左右。
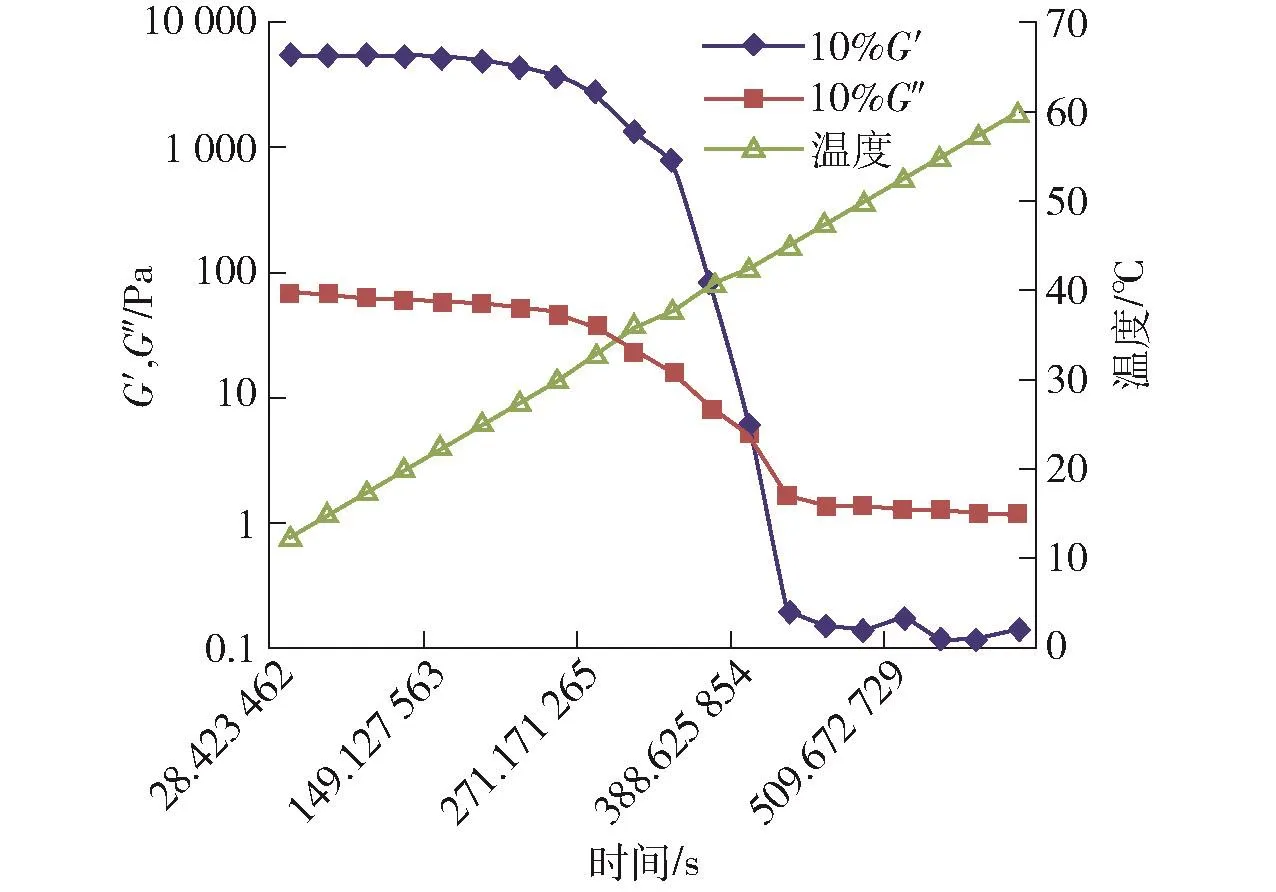
图5 0.10 g/mL鱼明胶凝胶的G′及G″在加热凝胶过程中的变化Fig.5 Changes of G′and G″of 0.10 g/mL fish gelatinduring heat-induced gelation
1号复合凝胶的贮能模量G′及损耗模量G″在加热过程中的变化曲线见图6。与图5呈现大致相同的趋势,由此可推断,该复合凝胶亦具有热可逆性;其他复合凝胶也呈现出相同趋势。
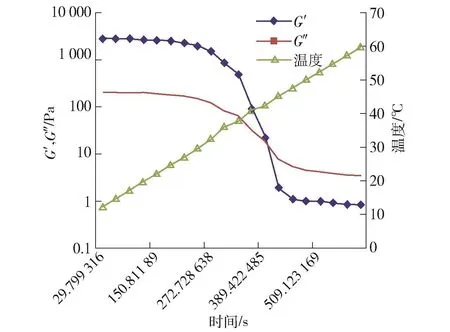
图6 1号复合凝胶G′及G″在加热凝胶过程中的变化Fig.6 Changes of G′and G″of No.1 composite gelation during heat-induced gelation
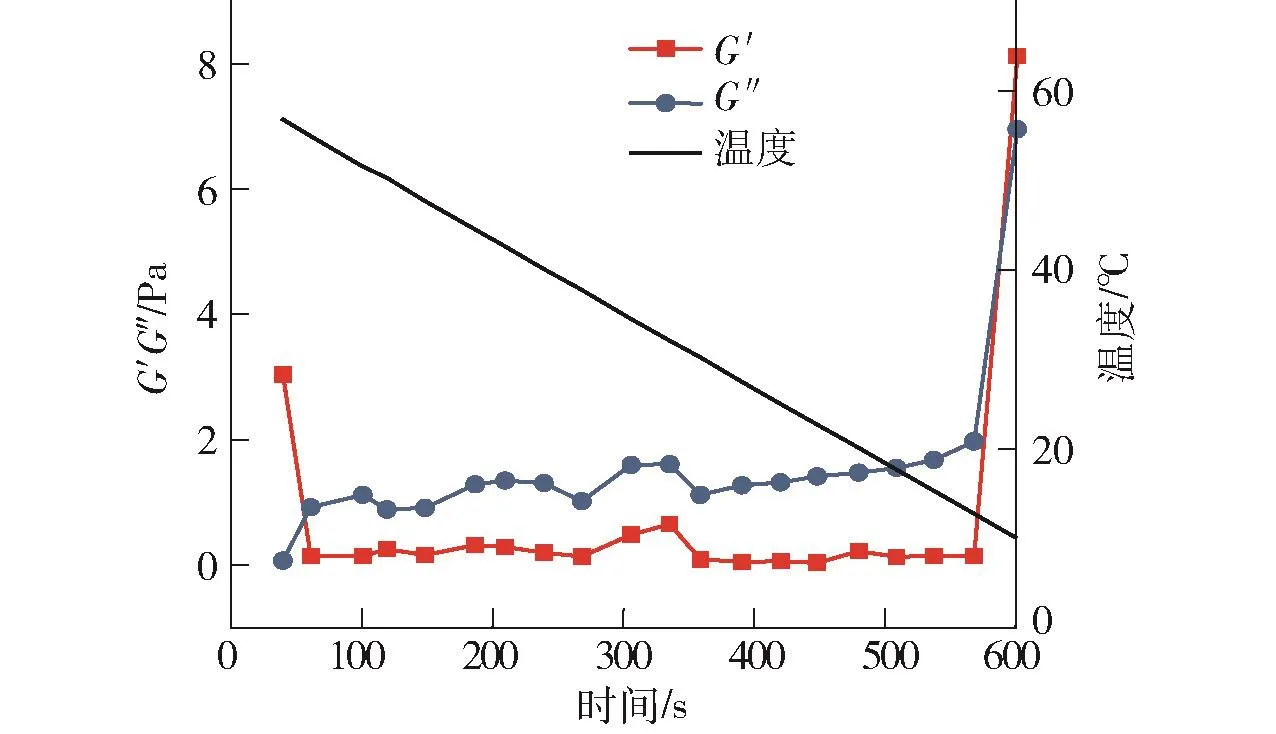
图7 0.10 g/mL鱼明胶凝胶降温过程中G′及G″的变化Fig.7 Changes of G′and G″of 0.10 g/mL fish gelatin in process of cooling

图8 1号复合凝胶在降温过程中G′及G″的变化Fig.8 Changes of G′and G″of No.1 composite gelation in process of cooling
0.10 g/mL鱼明胶单一凝胶和1号复合凝胶降温过程中贮能模量G′及损耗模量G″变化曲线见图7、图8。从图7可以看出,降温过程中单一凝胶的G′和G″逐渐增大,当温度降至10℃左右时,G′和G″均急剧上升且G′的上升幅度大于G″。此时,G′开始大于G″,说明体系中的弹性成分增加,体系开始发生胶凝。分析图8可知,复合凝胶也发生类似变化,但图中G′和G″的图线相互靠近并未相交,依据现实成胶结果推测海藻酸钠的加入提高了鱼明胶的热稳定性,延长了成胶时间,所成凝胶网络结构更加细致均一,与之前研究结果一致[24]。
2.3.2 海藻酸钠对鱼明胶热凝胶动态黏弹性的影响
不同质量浓度鱼明胶凝胶在10℃下储能模量G′及损耗模量G″随频率的变化曲线见图9。由图9可知,单一凝胶样品的G′均远远大于G″,而且随着鱼明胶质量浓度增加,G′和G″逐渐增大,这说明鱼明胶凝胶体系以弹性为主,呈胶凝状态且随着鱼明胶质量浓度增加,凝胶弹性增大,网络结构逐渐改善,即0.10 g/mL的鱼明胶凝胶网络质地结构最好,这与感官评价结果相一致。随着频率增加,G′和G″均增大,可知鱼明胶凝胶是介于固体与液体之间的黏弹体[25]。当频率增至85 Hz左右时,G″急剧上升,G′急剧下降,二者交汇,此时体系弹性下降,黏性上升,这是因为频率升高到一定程度时,分子能量高,形变快,胶体破裂。
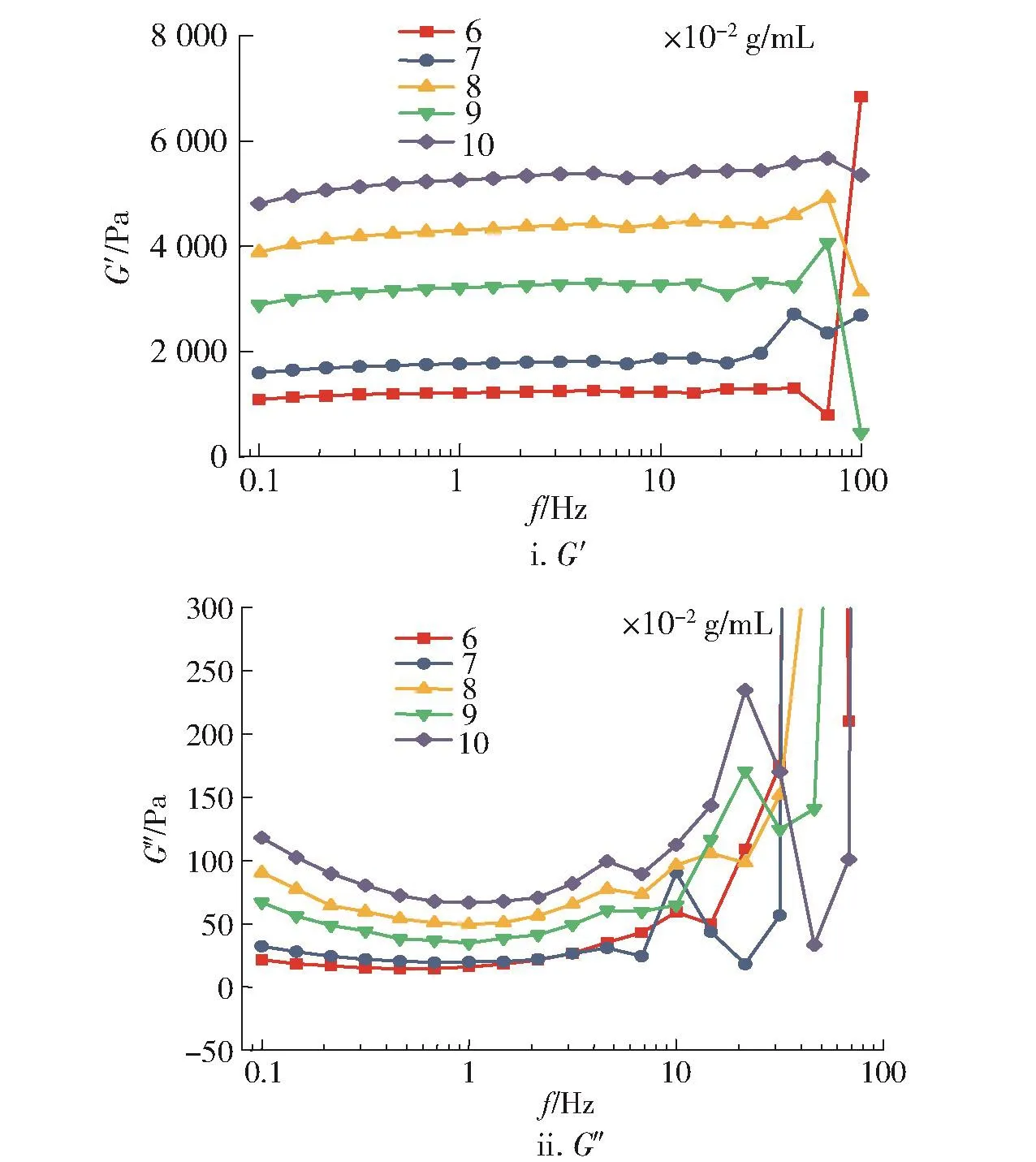
图9 鱼明胶凝胶的G′及G″随频率的变化Fig.9 Changes of G′and G″of fish gelatin with frequency
0、1、5号复合凝胶在10℃下储能模量G′及损耗模量G″随频率的变化曲线见图10。随着海藻酸钠质量浓度升高,G′逐渐减小,G″逐渐增大,说明海藻酸钠的加入使复合凝胶的弹性下降,黏性上升[26]。但是3组体系中的G′均远远大于G″,可见体系仍以弹性为主,呈胶凝状态。G′和G″均随频率增加而增大,说明复合凝胶亦是介于固体与液体之间的黏弹体[25]。当频率增至75 Hz左右时,0.08 g/mL鱼明胶单一凝胶破裂,而复合凝胶的G′和G″均急剧上升,且G′上升幅度较大,说明海藻酸钠的加入能提高复合凝胶的强度。继续增大频率,G″进一步增大,复合凝胶呈现破裂的趋势。
3 结 论
1)鱼明胶单一凝胶和鱼明胶/海藻酸钠复合凝胶的表观特征、色差、流变性质均与鱼明胶以及海藻酸钠的质量浓度呈现出密切依存关系。
2)鱼明胶单一凝胶是一种颜色微黄,外观形态良好,透明度高的凝胶。随着鱼明胶质量浓度增大,凝胶的弹性提高,机械强度增大,网络结构更优且硬度增加,成型性变好。相对于单一凝胶,复合凝胶的凝胶强度显著提高,且随着海藻酸钠质量浓度增加,凝胶成型性显著改善。
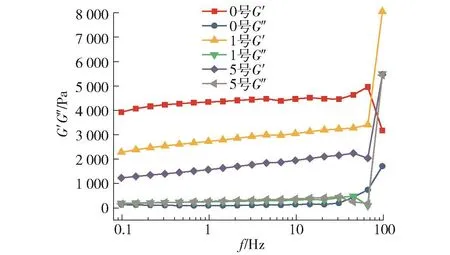
图 10 0、1、5 号复合凝胶的 G′及 G″随频率的变化Fig.10 Changes of G′and G″of No.0,No.1,No.5 composite gelation with frequency
3)鱼明胶单一凝胶和鱼明胶/海藻酸钠复合凝胶均属于热可逆凝胶,且胶凝点在40℃左右。
4)探讨了鱼明胶单一凝胶和鱼明胶/海藻酸钠复合凝胶的各项凝胶特性,具体的分子内及分子间相互作用机理有待进一步研究。

