头孢曲松引起成年患者药物性肝脏损害分析
李晓烨, 张均睿, 吴 薇
复旦大学附属中山医院药剂科,上海 200032
头孢曲松是目前广泛应用的三代、长效类广谱抗生素,临床主要应用于革兰阳性菌和革兰阴性菌感染[1]。头孢曲松可腹泻、粒细胞缺乏等,发生率约为2%[2]。研究[3-5]认为,抗生素是非对乙酰氨基酚类药物中引起肝脏损害比例最高的药物,其中以阿莫西林克拉维酸钾及抗结核类药物(异烟肼和利福平等)为主。目前,关于头孢类药物尤其是头孢曲松引起的药物性肝脏损害(drug-induced liver injury, DILI)少有报道,且头孢曲松相关的DILI未引起临床重视。DILI的危险因素主要包括给药剂量、药物亲脂性及基础肝代谢水平等[3]。因此,本研究对应用头孢曲松过程中发生的肝脏损害进行危险因素分析,以期为临床提供参考。
1 资料与方法
1.1 一般资料 选择2015年1月至2016年12月于复旦大学附属中山医院使用头孢曲松注射液的成年患者384例。其中,男性251例,女性133例;年龄28~87岁,平均(60.0±16.2)岁;体质量45~103 kg,平均(63.2±9.8)kg。入选标准:(1)年龄≥18岁;(2)连续使用头孢曲松注射液3 d以上;(3)尿路、胆道、腹腔、盆腔以及心内膜、脑膜感染等。排除标准:(1)年龄<18岁;(2)住院期间3 d内停止或者更换头孢曲松;(3)使用头孢曲松前后未行肝功能检查。本研究经医院伦理委员会审核批准,患者知情同意并签署知情同意书。
1.2 分 组 依据头孢曲松使用剂量,将384例患者分为低剂量(≤2 g/d)组和高剂量(>2 g/d)组,分别为318例、66例。当诊断为感染性脑膜炎或心内膜炎时,推荐使用剂量为4 g/d,对存在严重肝功能不全的患者,需调整药物治疗剂量。384例患者使用头孢曲松3~19 d,平均(6.1±3.7)d。
1.3 评价指标 通过医院信息管理系统收集患者资料。其中,基本信息包括姓名、性别、年龄、身高、体质量、入院时间和出院时间。临床资料包括感染诊断(如严重脓毒症及感染性休克等)、感染部位及其他合并症(包括肝硬化、胆囊炎、肝炎、恶性肿瘤、高血压病、高脂血症、糖尿病以及慢性肾功能不全等)。临床化验指标包括:(1)用药前后肝功能指标,如丙氨酸氨基转移酶(alanine aminotransferase, ALT)、天冬氨酸氨基转移酶(aspartate aminotransferase, AST)、碱性磷酸酶(alkaline phosphatase, ALP)和总胆红素(total bilirubin, TB),其正常值上限分别为40 U/L、35 U/L、125 U/L和20.4 μmol/L;(2)肾功能指标,如血清肌酐(Scr)、尿酸(UA)及肾小球滤过率(GFR)。合并用药包括:质子泵抑制剂(proton pump inhibitors, PPIs)、非甾体抗炎药(non-steroid anti-inflammatory drugs, NSAIDs)、降糖药物、降压药物、降脂药物以及其他抗生素(包括大环内酯、克林霉素及抗结核类药物)。
1.4 肝功能评价方法 参照目前国际DILI指南[6],满足下列任何1项可定义为DILI:(1)≥5倍ALT的正常值上限(upper limits of normal, ULN);(2)≥2倍ALP的ULN;(3)≥3倍ALT的ULN并伴有≥2倍ALP的ULN。对于在应用头孢曲松前已合并肝功能不全的患者,入院时其肝功能指标已经高于ULN,应用R值,即ALT活性[ALT/ALT(ULN)]和ALP活性[ALP/ALP(ULN)]的比值,评估其入院时的肝功能异常水平。结果判读:(1)R≥5为肝细胞性损伤;(2) 2 次级评价指标包括接受头孢曲松治疗期间导致的轻度肝脏损害,参照目前的国际医学组织标准委员会(Council for International Organizations of Medical Sciences, CIOMS)制定的DILI分类鉴别诊断标准,满足其中任何1项即可定义为轻度DILI:(1)≥2倍ALT的ULN;(2)AST、ALP或者TB中的任何1项超过2倍的ULN[7]。 2.1 低剂量组与高剂量组肝功能损害比较 结果(表1)显示:384例患者中,12例(3.1%)在使用头孢曲松期间发生DILI,其中高剂量组发生率高于低剂量组(13.6%vs0.9%;OR=16.58,95%CI 4.35~63.11,P<0.001);44例(11.4%)发生轻度肝脏损害,其中高剂量组发生率高于低剂量组(25.8%vs8.5%;OR=3.74,95%CI 1.90~7.37,P<0.001)。 2.2 头孢曲松相关性肝脏损害单因素分析 结果(表2)显示:384例患者中12例发生DILI,临床应用高剂量(>2 g/d)头孢曲松增加DILI发生的风险(OR=16.58,95%CI 4.36~63.11,P<0.001)。 表1 低剂量组和高剂量组基线比较 n(%), HIV:人类免疫缺陷病毒;ICU:重症监护室;CNS:中枢神经系统;PPIs:质子泵抑制剂;NSAIDs:非甾体抗炎药物;AST:天冬氨酸转氨酶;ALT:丙氨酸转氨酶;ALP:碱性磷酸酶;TB:总胆红素;DILI:药物性肝脏损害 表2 肝损害组和肝未损害组相关危险因素比较 n(%), HIV:人类免疫缺陷病毒;ICU:重症监护室;CNS:中枢神经系统;PPIs:质子泵抑制剂;NSAIDs:非甾体抗炎药物;AST:天冬氨酸转氨酶;ALT:丙氨酸转氨酶;ALP:碱性磷酸酶;TB:总胆红素 头孢曲松主要通过肝脏代谢,随着剂量的增加,其导致肝脏损害的比例增加。头孢曲松导致肝脏损害的系统临床研究相对较少,此类不良反应多见于病例报道。研究[8]发现,对于接受高剂量头孢曲松治疗(4 g/d)的患者较低剂量治疗(2 g/d)患者易发生DILI,且前者轻度肝功能异常的发生率较高。本研究中,高剂量组13.6%的患者发生了DILI,高于低剂量组,与文献[8]报道结果基本一致。 成年患者使用头孢曲松注射液的过程中,常出现多种不良反应,主要包括:胃肠道不适、胰腺炎、头孢曲松钠-钙沉淀、变态反应、白细胞和中性粒细胞计数下降及肝酶升高[2]。研究[9]显示,头孢曲松可导致肝酶升高(包括ALT、AST、ALP、TB),发生率为3.3%。然而,头孢曲松使用剂量与肝脏损害的临床联系目前尚无定论。一项评估氨苄西林联合头孢曲松治疗粪肠球菌感染心内膜炎有效性和不良反应的前瞻性研究[10]显示,其中氨苄西林联合头孢曲松(4 g/d)组主要不良反应为潮红、低热(0.6%)及白细胞减少(0.6%),而未发生DILI。一项纳入471例使用头孢曲松注射液患者的回顾性研究[8]中,有3.2%的患者发生了DILI。本研究结果与之相似。但本研究没有明确感染病原菌及具体感染部位,同时患者合并各种病症,这些因素都会影响肝功能指标;单因素分析结果显示高剂量的头孢曲松(>2 g/d)是导致肝脏损害的危险因素之一。研究[11]显示,随着口服药物使用剂量的增加,DILI的发生增加,进而导致肝脏衰竭甚至患者死亡。研究[12]发现,在头孢曲松每日剂量超过100 mg时,其较高的亲脂性可导致DILI发生率升高。 综上所述,本研究结果显示,高剂量头孢曲松是导致DILI的危险因素之一。因此,在患者应用高剂量头孢曲松过程中,应密切关注患者肝功能指标的变化。本研究的不足之处为:混杂因素较多;在病例的选择上存在偏倚性;纳入样本量不足,缺乏随访数据;评估肝脏损害指标主要采用肝酶的变化,未能排除患者基础肝功能水平。今后将通过排除上述影响因素、增加样本量等验证头孢曲松对肝功能的影响。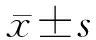
2 结 果
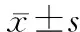
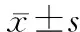
3 讨 论

