昆仑雪菊不同溶剂萃取物抗氧化活性研究
邵冬冬,陈千,李赫宇,肖文平,3,*
(1.黄冈师范学院化学化工学院,催化材料与制备湖北省重点实验室,湖北黄冈438000;2.天津益倍生物科技集团,天津300457;3.湖北中医药大学药学院,湖北武汉430065)
昆仑雪菊是维吾尔族人民传统的养生保健的天然植物,当地人称其为“古丽恰尔”。由于其生长环境较少污染,富含多种对人体有益的成分,故现今已逐渐作为一种茶饮普及开来。雪菊,学名两色金鸡菊(Coreopsis Tinctoria)蛇目菊,为菊科金鸡菊属(Coreopsis)多年生草本植物,在我国新疆尤其是和田地区、云南部分地区有一定规模栽培。目前雪菊的提取方法主要有水提法,醇提法,醇水混合提取,微波及超声波提取及超临界二氧化碳提取等。其主要的化学成分有酮、有机酸、萜烯、多糖等,迄今已报导的雪菊活性主要包括抗炎、降脂、降压、降糖、抗凝血、抗氧化、抗病毒等[1-9]。国内外很多学者研究雪菊,但大部分是关于含量测定和生物活性的,而关于雪菊粗提物的分离和雪菊中化合物的结构研究报道较少[10-21]。
抗氧化物质与人们的生产和生活密不可分,疾病治疗、食品加工、生活用品中都可能会用到。研究来源无害、不造成环境污染的天然抗氧化物质—植物源抗氧化剂成为了近年来食品界研究的热点。雪菊作为一种新型的植物抗氧化剂原料越来越受到重视,由于其产量在新疆地区丰富,在该地区分布广泛,其挥发油、有机酸和黄酮产量丰富,具有抑菌和抗氧化、促生长等作用而成为需要大力开发的资源[6]。
1 材料与方法
1.1 试剂与仪器
昆仑雪菊:江西致和堂中药饮片有限公司。
所有试剂均为市售分析纯。
UV-3802型紫外可见分光光度计:尤尼柯仪器有限公司;RE-52AA旋转蒸发器:上海亚荣生化仪器厂;DG-120型四两装中药材粉碎机:浙江省瑞安市春海药材器械厂。
1.2 石油醚部位、氯仿部位、乙酸乙酯部位、正丁醇部位的制备
参考文献方法[22],取雪菊30 g,粉粹至10目左右,每次加入75%的乙醇400 mL[9],90℃加热回流提取3次,回流时间分别是1 h、1 h、40 min。放冷,合并3次提取液进行减压抽滤,滤液通过旋转蒸发仪浓缩至无醇味。浓缩液分别用与其体积比为1∶1的石油醚、氯仿、乙酸乙酯、正丁醇萃取,分别回收至干燥,得到石油醚部位76.9 mg、氯仿部位677.2 mg、乙酸乙酯部位498.4 mg、正丁醇部位 2 747.3 mg。
1.3 抗氧化活性的测定[23]
1.3.1 不同溶剂提取物对DPPH自由基清除率
将1.2中得到的石油醚部位用75%的乙醇溶解,定容至50 mL的容量瓶中,用移液枪取5mL上述溶液,用75%的乙醇定容至10 mL,此为待测液。称取5 mg DPPH,用75%的乙醇溶液定容至250 mL容量瓶中,避光备用。将2 mL待测液及2 mL DPPH溶液置于一具塞试管中,摇匀,放置30 min,以75%乙醇加DPPH溶液为空白,以待测液加75%乙醇为对照,于517 nm处测定吸光度,并以下式计算清除率。
以同样的方法测定氯仿部位、乙酸乙酯部位和正丁醇部位的清除率。另取70 mgVC加75%的乙醇定容至50 mL,用移液枪取上述溶液5 mL,用75%的乙醇定容至10 mL,测定清除率。
1.3.2 雪菊各提取部位清除·OH的能力的测定
分别取1.2中的提取物25 mg,用乙醇定容至25 mL。在10mL试管中分别加入6mmol/L的FeSO4溶液1 mL,分别加入上述溶液1.0 mL,再加6 mmol/L的H2O2溶液1.0 mL,摇匀,放置10 min,再加入6 mmol/L的水杨酸溶液3 mL,摇匀,37℃恒温反应30 min,于510 nm处测吸光度,空白试剂代替样品为空白组,以空白试剂代替水杨酸为对照组,VC为阳性对照,每个样品重复3次,取平均值。按以下公式计算各提取部位的清除率。
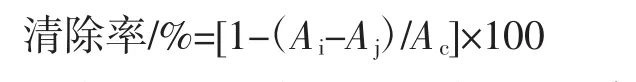
式中:Ac为空白组吸光度;Ai为待测样品的吸光度;Aj为对照组吸光度。
1.3.3 总还原能力的测定
采用铁离子还原能力测定法测定1.2中各种提取物的总还原能力。分别取1.2中的提取物25 mg,用乙醇定容至25 mL,用移液枪取10 mL上述溶液,用乙醇定容至25 mL。分别取1 mL上述溶液,分别依次加入pH6.6的磷酸盐缓冲液2.5 mL(0.2 mol/L)和1%的铁氰化钾溶液2.5 mL,混匀,于50℃恒温反应20 min,急速冷却后,加2.5 mL 10%的三氯乙酸,混匀后6 000 r/min离心10 min,取上清液2.5 mL,分别加蒸馏水2.5 mL和0.1%三氯化铁溶液0.5 mL,混匀,静置10 min后,在700 nm测定吸光度。以空白试剂作为阴性对照,以VC溶液为阳性对照,每个样品重复测3次,取平均值。吸光度值越大,表明样品总还原能力越强。
1.4 乙酸乙酯部分的提取分离
结合参考文献[22,24],另取雪菊 235 g,重复 1.2的操作,得到乙酸乙酯部分3.3 g。将乙酸乙酯部分加少量10%乙醇溶解,经过预处理的大孔树脂柱中,依次用10%、20%、30%、40%、50%、60%、70%、80%、90%、100%的乙醇溶液冲洗。流出液点硅胶薄层,如图1,70%乙醇冲洗液斑点清晰可见。70%乙醇部分回收至完全干燥,用少量无水乙醇溶解,加入少量柱层析硅胶,加热,待无水乙醇完全蒸干得到硅胶样品。将样品上入硅胶柱中,依次用氯仿、氯仿∶甲醇(9∶1,体积比)、氯仿∶甲醇(8∶2,体积比)、氯仿∶甲醇(7∶3,体积比)冲洗,流出液分别点硅胶薄层,如图2,氯仿∶甲醇(9∶1,体积比)部分的流[11]出液斑点清晰可见。将氯仿∶甲醇(9∶1,体积比)的部分回收,用丙酮重结晶,抽滤,减压真空(60℃)干燥24 h,得到化合物1。

图1 70%乙醇流出液的硅胶薄层Fig.1 Silica gel thin-layer chromatography of 70%ethanol solution

图2 氯仿∶甲醇(9∶1)流出液硅胶薄层Fig.2 Silica gel thin-layer chromatography of chloroform∶methanol(9 ∶1)solution
2 结果与讨论
2.1 抗氧化活性的结果
2.1.1 DPPH法进行了抗氧化活性的测定
将石油醚部位、氯仿部位、乙酸乙酯部位、正丁醇部位分别用DPPH法进行抗氧化活性的测定,结果显示,正丁醇部位清除率为96.97%,其次是乙酸乙酯部位为93.86%,石油醚部位清除率为87.72%。但若与相同浓度的VC相比,正丁醇部位的抗氧化活性不如VC的抗氧化活性。结果表明,正丁醇提取部位发挥清除DPPH自由基作用的成分较多,且这些成分大部分是极性较大的成分,可能多为黄酮类化合物的苷类物质。
2.1.2 雪菊各提取部位清除·OH的能力
将石油醚部位、氯仿部位、乙酸乙酯部位、正丁醇部位分别用水杨酸法进行清除·OH的测定,结果显示,当所有提取部位浓度为1 mg/mL时,乙酸乙酯部位对羟基的清除能力最强,达到85.96%,其次是正丁醇部位,达到80.23%,石油醚部位对羟基的清除能力最低,只有21.31%。但若与相同浓度的VC相比,清除羟基自由基的能力均小于等于相同浓度VC。结果表明,雪菊各提取部位清除羟基自由基的能力与提取部位的浓度和各提取部位的化学成分相关。雪菊清除羟基自由基的能力可能与黄酮类化合物的苷元相关。
2.1.3 总还原能力的测定
将石油醚部位、氯仿部位、乙酸乙酯部位、正丁醇部位分别用铁离子还原能力法进行总还原能力的测定,结果显示,当所有提取部位浓度为1 mg/mL时,其还原能力由强到弱依次为乙酸乙酯提取部位>正丁醇提取部位>氯仿提取部位>石油醚部位。结果表明,不同溶剂提取部位的总还原能力不同,乙酸乙酯部位最大,可能与其黄酮类成分含量最高有关系。
2.2 化合物1的表征
化合物1的红外光谱如图3所示,3 440 cm-1是-OH伸缩振动吸收峰,1 638 cm-1是苯环上C=C骨架振动的吸收峰,827 cm-1是苯环上C-H面外弯曲振动的吸收峰。

图3 化合物1的红外图谱Fig.3 The IR spectrum of compound 1
化合物2的1HNMR如图4所示,根据文献推断[23],其结构可能为对羟基苯丙烯酸。在化学位移值7.5左右的峰是苯环上的氢,化学位移6.9和7.9的峰分别是碳碳双键上的2个氢,化学位移10.81是-OH的峰,13.00是-COOH的峰。
3 结论
用75%的乙醇加热回流提取法提取昆仑雪菊中的化学成分,有机溶剂分别萃取得到了石油醚部位,氯仿部位,乙酸乙酯部位,正丁醇部位。DPPH法分别测定4个提取部位的抗氧化活性,结果表明,正丁醇部位的抗氧化活性最强,其次是乙酸乙酯部位。用水杨酸法进行了其清除·OH的测定,结果表明,乙酸乙酯部位对羟基自由基清除能力最强。采用铁离子还原能力测定法测定各提取部位的总还原能力,乙酸乙酯部位总还原能力最强。用分别用大孔树脂柱和硅胶柱对乙酸乙酯部位进行了分离,得到化合物1。由红外图谱和1H-NMR进行结构鉴定,结合参考文献[22],得到的化合物1为苯丙烯酸的类似物。

图4 化合物1的1HNMR图谱Fig.4 The1HNMR spectrum of compound 1

