锂离子电池镍基正极材料水溶液体系中氧化铝包覆研究
李伟伟
(新乡学院 化学化工学院,河南 新乡 453003)
锂离子电池作为一种优良的便携式电源,已经广泛进入了人们的生活,但寻找更高能量密度的正极材料仍然是科学家追求的目标[1-2]。现有的锂离子电池正极材料中,LiNiO2具有比容量较高、资源丰富、价格便宜、毒性较低且对环境污染小等优点,已经成为了研究的热点。但镍酸锂的合成较困难,易形成非化学计量化合物,存在耐过充性能和热稳定性能差等问题[3];单纯的LiNiO2在充放电过程中有多次的相变过程,导致电化学性能快速衰减[4];LiNiO2材料表面Li残留较多,pH值较高,容易吸收水,会和空气中的水、CO2发生不可逆的化学反应[5]。
为了提高LiNiO2的稳定性能,很多研究者使用离子掺杂和表面包覆的方法改善其性能[6-9]。掺杂可以抑制锂离子脱嵌/嵌入过程中的相变,提高晶体结构的稳定性;表面包覆可以使正极材料与电解液分开,减少材料与电解液副反应,改善氧化物表面结构,减缓锂电池性能的衰减[10]。研究表明,LiNiO2正极材料,通过Co3+、Al3+的共同掺杂有效抑制了LiNiO2在充放电过程中的相变,得到稳定的层状结构与晶格参数、较低的阳离子混排,使材料具有优越的质量比容量,良好的循环性能以及深度放电的能力[11-12]。
本文采用沉淀法在Co掺杂的镍基正极材料LiNi0.9Co0.1O2表面包覆 Al2O3, 研究表面包覆 Al2O3的作用,为得到高性能的镍基材料提供参考依据。
1 实验
1.1 样品制备
镍基正极材料 LiNi0.9Co0.1O2由河南科隆新能源有限公司提供。首先称取四份20 g LiNi0.9Co0.1O2材料备用。在250 mL的锥形瓶中加入去离子水200 mL,分别按Al2O3的包覆量(质量分数)是0.5%,1.0%,1.5%,2.0% 称量所需 Al(NO3)3·9H2O, 在约800 r/min的搅拌条件下将Al(NO3)3·9H2O加入到锥形瓶中,再加入已经称量好的LiNi0.9Co0.1O2,搅拌30 min左右。然后用氨水调节溶液pH值为6~7,搅拌1 h后过滤,130℃干燥4~5 h。最后将干燥后的样品在550℃热处理4 h,得到Al2O3包覆的样品。未包覆的及 Al2O3包覆量(质量分数)是0.5%,1.0%,1.5%,2.0% 的样品分别记为 0#、1#、 2#、 3#、 4#。
1.2 样品表征
样品的形貌用美国FEI Quanta250FEG SEM观察,元素的含量通过采用美国PE Optima8300 ICPAES进行确定,X射线衍射分析(XRD)采用德国布鲁克公司的D8 Advance型X射线衍射仪,扫描范围15°~70°, 扫描速度2°/min。
1.3 样品电化学性能测试
在室温下,将样品和导电石墨、乙炔黑、聚偏氟乙烯(PVDF) 按质量比90∶2∶2∶6在N-甲基吡咯烷酮(NMP)溶液中充分搅拌混合均匀,然后涂覆在铝箔集流体上。经过110℃干燥10 h后,切成直径为15 mm的圆形极片。最后在充满高纯氩气的手套箱中将正极极片、金属锂负极、隔膜和电解液组装成CR2016型扣式电池。电解液为1 mol/L LiPF6。采用深圳市新威尔电子有限公司生产的电池测试仪进行电性能测试,充放电电压范围为2.75~4.25 V。
2 结果与讨论
2.1 实验现象分析
溶液中的Al3+离子遇到OH-生成白色絮状不容物Al(OH)3,Al(OH)3为两性产物,较高的酸性或碱性都会使Al(OH)3再溶解。已知Al3+在水溶液中完全生成Al(OH)3条件为pH值在6左右。在1#样品的制备过程中,由于Al(NO3)3·9H2O较少,而 LiNi0.9Co0.1O2的 pH 值较高(约 11.42), 加入LiNi0.9Co0.1O2以后溶液的 pH值仍然大于8,导致Al3+不能完全沉淀,因此最终产物上Al2O3的包覆量达不到化学计量比0.5%,所以在随后实验中没有对1#样品进行物理化学性能表征。4#样品制备过程中, 在 LiNi0.9Co0.1O2表面沉淀 Al(OH)3, 过滤并在干燥箱中干燥后,具有一定程度的板结,这可能是较多的Al(OH)3干燥收缩导致。在制作扣式电池的过程中,发现4#样品的电极极片上有许多较硬的白色颗粒,并且在热压以后,铝箔基板上出现许多凸点,如图1所示。

图1 (a)正常电极极片正面;(b)4#样品电极极片正面;(c)正常电极极片反面;(d)4#样品电极极片反面Fig.1 (a)The positive of normal electrode plate;(b)The positive of 4#electrode plate;(c)The back of normal electrode plate;(d)The back of 4#electrode plate
经分析,导致这些凸点出现的原因可能是4#产品中含有Al2O3颗粒;4#样品制备过程中,由于铝含量较多,可能使部分 Al(OH)3没有沉淀在LiNi0.9Co0.1O2表面; 也可能是部分 Al(OH)3在热处理过程中从镍基体剥落,导致Al2O3颗粒没有包覆在镍基体表面,而是和镍基体混合在一起。因此,在随后实验中没有对4#样品进行物理化学性能表征。
取少量的0#、2#、3#样品溶解,然后用ICP方法测四种金属元素的摩尔比,结果如表1所示。
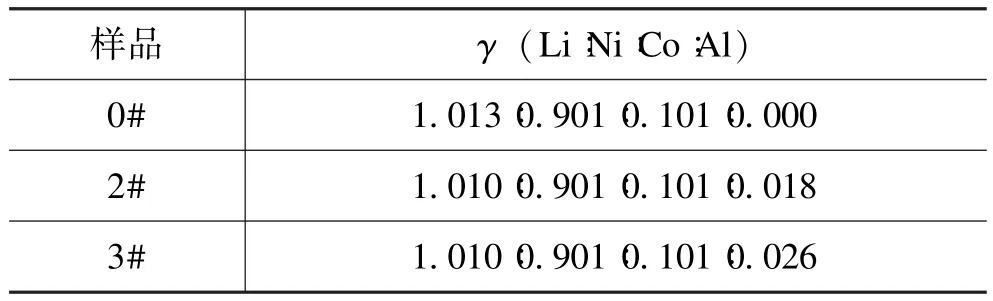
表1 0#、2#、3#样品中四种金属元素的摩尔比Tab.1 The molar ratio of four metal elements of samples 0#,2#,3#
由表1可以看出,所有样品中Ni、Co、Li三种元素的摩尔比接近于理论配比,Li元素的摩尔比大于1, 是因为 LiNi0.9Co0.1O2材料在制备时 Li元素的配比过量;在2#、3#样品中,Al元素的含量与理论配比几乎一致,表明Al3+已完全沉淀。比较发现,2#、3#样品中Li元素的含量略小于0#样品,这可能是在样品的制备过程中,LiNi0.9Co0.1O2材料表面残留Li被溶解所致。
称量2 g 0#、2#、3#样品,加入20 mL去离子水,搅拌10 min后静置,用pH计测溶液的pH值,0#、 2#、 3#样品溶液的pH值分别为11.41,10.72,10.61,由此可见,Al2O3包覆以后能降低镍基材料的pH值,表明材料残留Li显著减少,这可能是在样品的制备过程中,LiNi0.9Co0.1O2材料表面残留Li被溶解,也可能是Al2O3与表面残留的Li反应生成LiAlO2。
2.2 结构、形貌及电化学性能分析
图2是0#、2#、3#样品的XRD谱。由图2可知,所得样品无杂相峰出现,衍射峰位置一致,且具有六方晶系的 ɑ-NaFeO2结构[13-14]。图2中显示,主强峰为(003),次强峰为(104),0#、2#、3#样品的I(003)/I(104)值分别为 1.990,2.201,2.019,三个样品中阳离子混排程度都很小,相对而言2#样品更好一些,表明Al2O3包覆后不仅没有提高阳离子混排程度,而且还能小幅度降低阳离子混排程度;(006)与(102)峰、(108)与(110)峰分裂明显,说明三个样品都具有良好的层状结构。这些都预示着所得材料具有优良的电化学性能。

图2 0#、2#、3#样品的XRD谱Fig.2 The XRD patterns of samples 0#,2#,3#
图3是包覆前后样品的SEM照片。从0#样品照片上可以看出,镍基材料没有包覆之前,一次颗粒团聚体之间的边界清晰可见,大颗粒表面比较洁净。从2#、3#照片上可以看出,镍基材料包覆之后,一次颗粒团聚体之间的边界仍然清晰可见,表明包覆层的厚度比较小;但是2#、3#样品大颗粒表面的洁净程度相对于0#有些差,表明有产物覆盖在镍基材料表面。总体来说,Al2O3包覆对形貌的影响不大,材料仍然保持为球形状态。

图3 0#、2#、3#样品的SEM照片Fig.3 The SEM images of samples 0#,2#,3#
图4是0#、2#、3#样品的电化学性能,测试条件为0.2C、 2.75~4.25 V。 由图4(a) 可以看出,0#样品的首次放电容量约为202.1 mAh/g,首次充电容量约为233.1 mAh/g,库伦效率约为86.7%;2#样品的首次放电容量约为182.1 mAh/g,首次充电容量约为220.0 mAh/g,库伦效率约为82.7%;3#样品的首次放电容量约为166.6 mAh/g,首次充电容量约为208.6 mAh/g,库伦效率约为79.9%。由此可知,Al2O3表面包覆以后,随着包覆量的增多,充放电容量和库伦效率下降得越多,原因可能是Al2O3包覆量较多时生成较多无活性的LiAlO2。

图4 0#、2#、3#样品的电化学性能Fig.4 The electrochemical properties of samples 0#,2#,3#
由图4(b)可以看出,在0.2 C放电倍率下,经过50次循环后,0#、2#、3#三个样品的放电容量分别为 145.6,146.3,130.6 mAh/g, 容量保持初始放电容量的73.7%,81.4%,77.4%。 由此可知,Al2O3表面包覆以后,循环性能提高,Al2O3的包覆量(质量分数)为1.0%时比包覆量(质量分数)为1.5%时的循环性能好,原因可能是表面包覆后,正极活性材料与电解液分开,减少材料与电解液副反应,改善氧化物表面结构,减缓锂电池性能的衰减;但是如果包覆量太多,可能导致无活性界面层太厚,不利于Li+的迁移,使循环性能下降。
3 结论
水溶液体系中, 在 LiNi0.9Co0.1O2表面包覆了Al2O3。Al2O3包覆后,形貌基本无变化,具有良好的层状结构,能小幅度降低阳离子混排程度;在0.2 C、 2.75~4.25 V 测试条件下,Al2O3包覆后,容量和库伦效率下降,循环性能提高,50次循环后,质量分数1.0%Al2O3包覆量的产物容量大于未包覆的产物。

