基于8-羟基久洛尼定的荧光探针用于谷胱甘肽的特异性检测研究
王 超, 闫钰佳,2, 张诣为, 武雨珽, 代方方
(1.陕西科技大学 化学与化工学院, 陕西 西安 710021; 2.西北大学 化工学院, 陕西 西安 710069)
0 引言
还原型谷胱甘肽(GSH)是一种广泛存在于各种生物细胞内的含有巯基的三肽,这一特异结构使其成为体内重要的抗氧化剂和自由基清除剂[1].可以保护蛋白质等分子中的巯基,抑制自由基对各种生物大分子的侵袭和生物膜的损伤;与进入人体的有毒化合物、重金属离子或致癌物质等相结合,并促进其排出体外,起到中和解毒的作用[2].鉴于GSH在细胞中的重要作用,如何快速、高效、特异性的检测GSH非常重要.目前,常用的GSH检测方法有分光光度法、碘量法、高效液相色谱法、酶循环法和纸层析法等.但是这些方法往往存在特异性不够好,操作过程复杂,无法在细胞内实时、原位检测GSH等缺点[3].
荧光探针作为一种新型的检测工具,经过不断地发展,已经被广泛应用于各种物质的特异性检测.它具有操作简便、灵敏度高、选择性好以及非生物破坏性等优点,尤其可用于活细胞、组织甚至动物体内原位检测各种物质的动态变化过程,所以该方法对于疾病诊断与相关研究等具有重要的应用价值[4-6].目前用于检测GSH的荧光探针反应机理主要基于分子中硫醇结构与探针间的特异性反应[7-11].例如,利用GSH分子中巯基的亲核性或还原性,使得荧光探针分子中部分化学键断裂,改变荧光探针的光谱性质,实现GSH荧光检测[7].
本论文以8-羟基久洛尼定为基本骨架,利用其刚性平面结构增强香豆素母体的平面性,进而实现荧光探针波长的红移.同时,在香豆素母体3,4位分别引入醛基和氯原子作为GSH氨基和巯基的识别位点,最终获得高特异性的GSH荧光探针,并进一步通过光谱分析评价该荧光探针用于GSH比率响应、定量检测的可行性.
1 实验部分
1.1 试剂与仪器
(1)主要试剂:丙二酸、苯酚、三氯氧磷、间氨基苯酚、1-溴-3-氯丙烷、甲苯、碳酸氢钠、DMF、无水硫酸镁、乙酸乙酯、二氯甲烷、甲醇、石油醚、KH2PO4、Na2HPO4·12H2O、氯化钠、氯化钾、谷胱甘肽、L-半胱氨酸、二甲基亚砜、氘代氯仿,均为分析纯.
(2)主要仪器:RE-52系列旋转蒸发仪(上海亚荣生化仪器厂);SHB-Ⅲ型循环水多用真空泵(郑州长城科工贸有限公司);Lumina荧光分光光度计(赛默飞世尔科技有限公司);400 MHz核磁共振波谱仪(bruker公司);PHS-3E型pH计(上海仪电科学仪器股份有限公司).
1.2 探针的合成
目标探针分子的合成路线如图1所示.经过四步合成得到,具体步骤如下.
1.2.1丙二酸二苯酯(1)的合成
参考Liu等[12]报道的方法,将三氯氧磷(4.7 mL,50.3 mmol)加入茄形瓶中,在冰水浴条件下,将丙二酸(4.49 g,43.3 mmol)和苯酚(8.15 g,86.6 mmol)缓慢的滴加到三氯氧磷中.在油浴115 ℃下回流反应1.5 h,直到无氯化氢气体冒出.反应结束后,将上层黄色油状液体倒入75 mL的水中,然后用150 mL乙酸乙酯萃取3次,无水硫酸镁干燥,抽滤,旋蒸除去溶剂,得到黄色油状产品10.32 g,产率94%,产物纯度高,未经进一步纯化直接用于下一步反应.
1.2.28-羟基久洛尼定(2)的合成
参考Liu等[13]报道的方法,将间氨基苯酚(8.73 g,80 mmol)溶于DMF(40 mL)中,再加入1-溴-3-氯丙烷(50.4 g,320 mmol),最后加入碳酸氢钠(26.88 g,320 mmol).加热60 ℃,回流反应15 h后,再升高温度到90 ℃,回流9 h.反应结束后,加入150 mL的乙酸乙酯萃取,300 mL水洗三次,无水硫酸镁干燥,抽滤,旋蒸除去溶剂,得到黑色胶状液体.硅胶柱色谱分离,展开剂为石油醚∶乙酸乙酯=10∶1.得到白色固体产物3.4 g,产率23%.化合物结构经核磁共振氢谱表征.
1H NMR(400 MHz,CDCl3)δ:6.66 (d,J=8.0 Hz,1H),6.06(d,J=8.0 Hz,1H),4.43(s,1H),3.10(dd,J=11.0,4.5 Hz,4H),2.68(dt,J=14.9,6.6 Hz,4H),2.03~1.91 (m,4H) ppm.
1.2.39-羟基香豆素6H(3)的合成
参考Chen等[14]报道的方法,将8-羟基久洛尼定(0.5 g,2.64 mmol)、丙二酸二苯酯(0.56 g,2.15 mmol)、甲苯(4 mL)加入茄形瓶中.在115 ℃下回流反应6 h.反应结束后,将上层墨绿色液体倒掉.下层沉淀物加入石油醚洗涤,干燥后得到产物0.41 g,产率62%.
1.2.4探针的合成
参考Zhang等[15]报道的方法,将9-羟基香豆素6H(3)(0.32 g,1.25 mmol)溶于DMF(3.9 mL)中,记为①,将DMF(1 mL)和三氯氧磷(0.7 mL)混合,加热50 ℃,磁力搅拌30 min,记为②,将①缓慢的滴加到②中,升温到60 ℃反应6 h.反应结束后,取7 mL冰水,将反应物倒入,产物析出,抽滤,干燥,得到砖红色固体.硅胶柱色谱分离,展开剂二氯甲烷∶甲醇=20∶1.得到固体产品0.165 g,产率43%.化合物结构经核磁共振氢谱表征.
1H NMR (400 MHz,CDCl3)δ:10.27(s,1H),7.43(s,1H),3.38(dd,J=11.9,6.8 Hz,4H),2.86(t,J=6.4 Hz,2H),2.79(t,J=6.2 Hz,2H),2.03~1.93(m,4H)ppm.

图1 探针的合成路线
1.3 光谱测试
探针母液的配制:准确称量探针的质量,将其溶于DMSO中,配制成浓度为5 mmol/L的母液备用.检测物母液的配制:准确称量GSH和L-半胱氨酸(Cys)的质量,将GSH和Cys分别溶于PBS缓冲液中,配制成浓度为10 mmol/L的母液备用.工作液的配制:将母液用含有10%二甲基亚砜的PBS稀释到一定的倍数,得到所需工作液的浓度,探针为10μmol/L.按实验浓度分别将GSH和Cys加入探针溶液中,进行光谱测试.
2 结果与讨论
2.1 探针的光谱性质与GSH的响应
通过核磁共振氢谱表征,确定探针结构正确,分别测定其激发和发射光谱如图2(a)所示.激发波长峰值为466 nm,发射波长峰值为516 nm.
在探针中加入GSH后其光谱性质如图 2(b)所示.与图 2(a)相比,其激发和发射光谱均发生了变化,激发光谱波长发生红移.荧光光谱也呈现显著地红移现象,在516 nm处的发射峰消失,在561 nm处出现新的发射峰.探针和GSH反应,应该生成了共轭程度更高的物质,从而使其激发和发射光谱均发生红移.
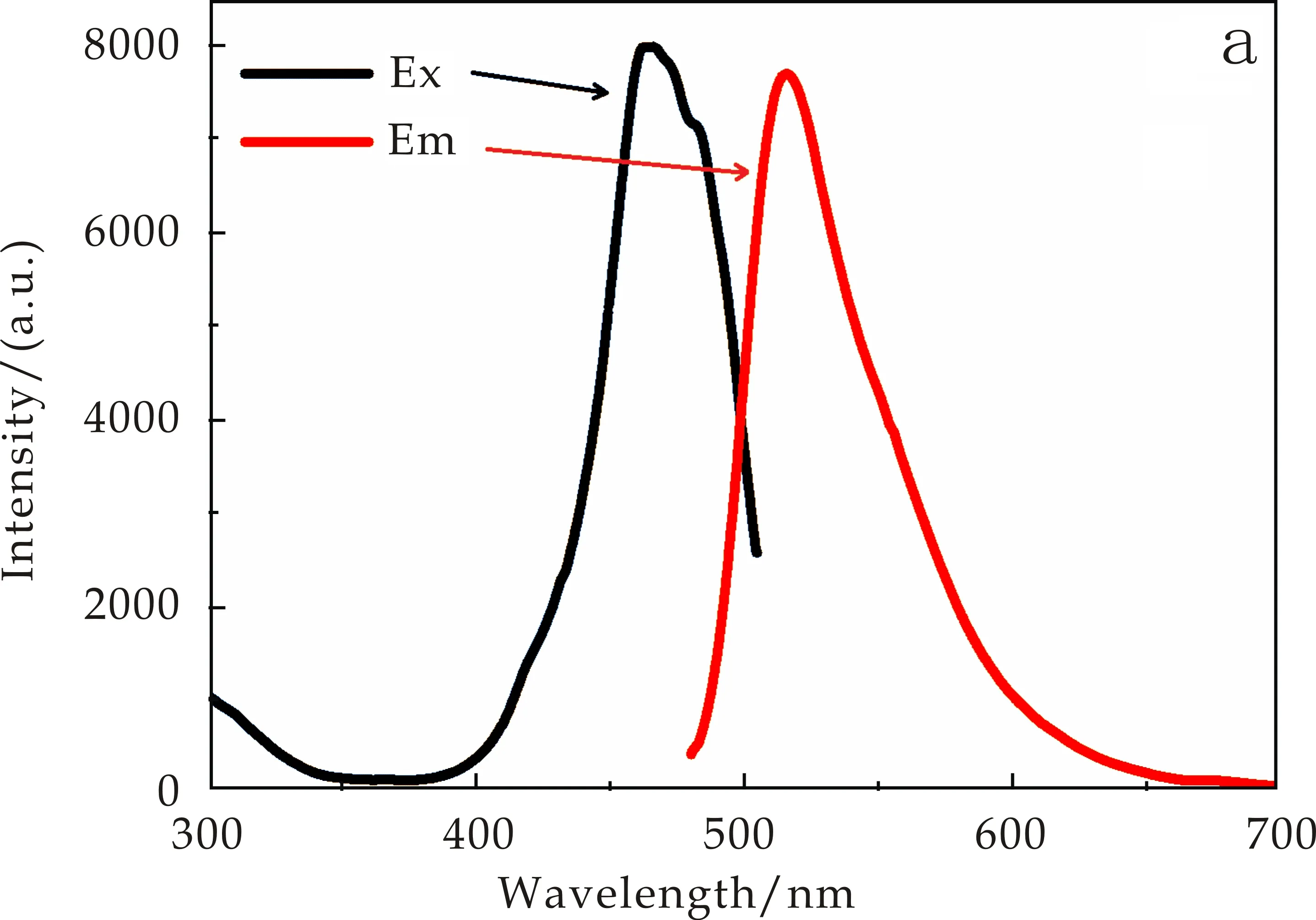
(a)探针(10 μmol/L)

(b)探针(10 μmol/L)加入50 μmol/L GSH图2 探针加入GSH前后的激发、发射光谱
2.2 探针对GSH响应的选择性
当GSH荧光探针在检测应用时,易受到Cys等巯基化合物的干扰,为评价探针对于GSH响应的选择性,选用和GSH具有相似结构的Cys作为对比.在使用380 nm的光激发时,探针对于GSH和Cys的荧光响应如图3(a)所示.由图可知,探针及其与GSH反应后荧光较弱,而探针与Cys反应后荧光较强,峰值为515 nm.在使用470 nm光激发时,探针对于GSH和Cys的荧光响应如图3(b)所示.与探针相比,探针与GSH和Cys反应后,荧光强度均减弱.其中,与GSH反应后荧光峰值发生显著红移,与Cys反应后荧光峰值发生微弱蓝移.同时,可见光下和在紫外光下的荧光图像如图3(c)~(e)所示,三者之间荧光颜色有显著差异.综上,探针可以较好地实现GSH与Cys的选择性检测.
2.3 探针与GSH和Cys反应机理推测
参考文献报道的机理[11],推测探针和GSH及Cys的作用机理如图4所示.当探针和GSH反应时,巯基对氯原子进行取代,由于空间位阻效应,其分子内氨基不会对巯基发生进一步取代,而是与醛基反应生成希夫碱结构,并进一步形成分子内氢键,会使其共轭程度增强,其激发和发射波长均会发生红移.而探针与Cys反应时,与GSH反应类似,巯基会对氯原子进行取代,但是由于Cys分子较小所受空间位阻小,其分子内氨基会进一步对巯基发生取代,因而影响了探针的共轭结构,使其激发和发射波长都发生蓝移.

(a)380 nm波长激发的荧光光谱

(b)470 nm波长激发的荧光光谱

(c)可见光下荧光图像

(d)紫外灯254 nm下荧光图像

(e)紫外灯365 nm下荧光图像图3 探针对于GSH和Cys的荧光响应
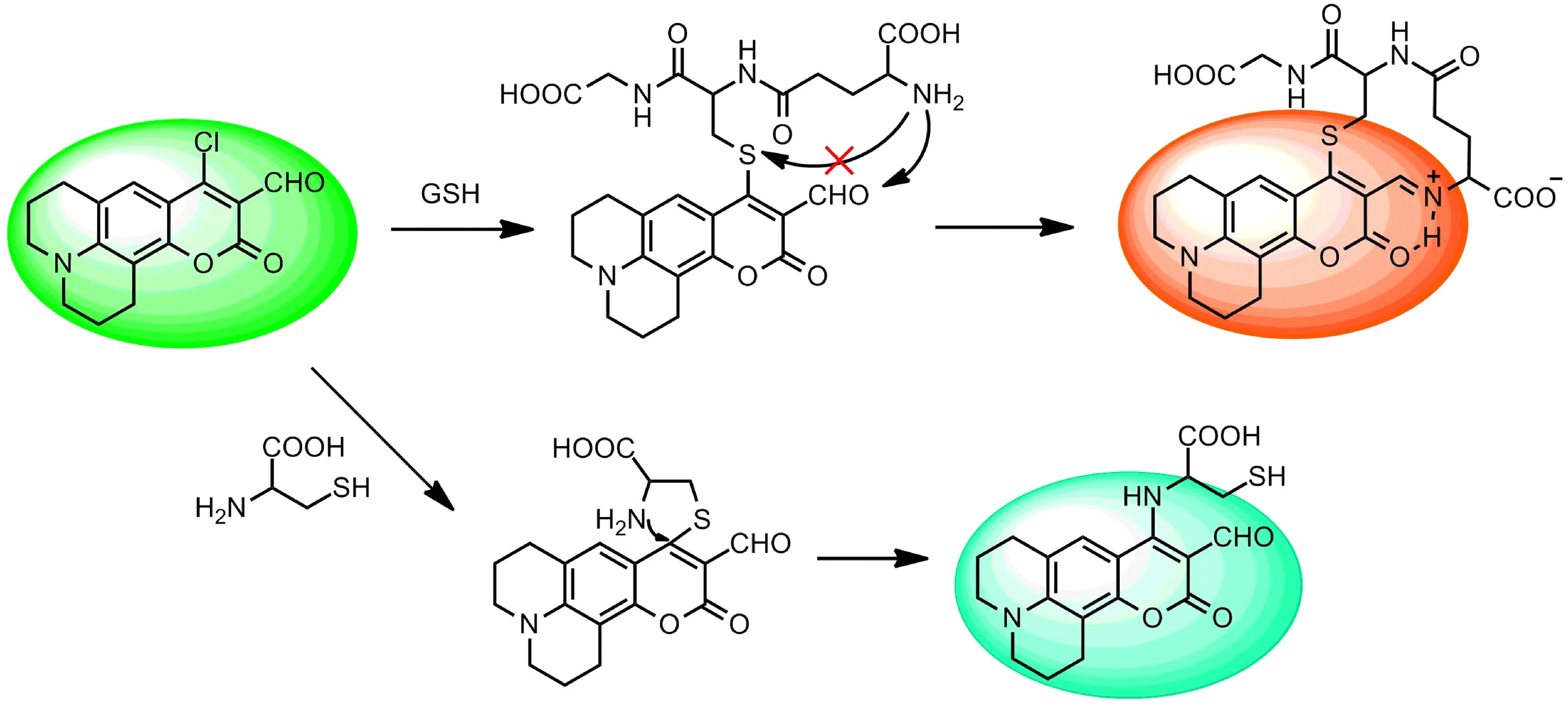
图4 探针与GSH、Cys的反应机理
2.4 探针对GSH的响应过程分析
为了进一步评价探针对GSH的检测能力,进行了探针的响应过程分析.在10 μmol/L探针中加入50 μmol/L的GSH后,在不同时间点测定反应体系的荧光光谱.
如图5(a)所示,当470 nm光激发时,随着时间的延续,探针在516 nm处的发射峰逐渐降低,表明探针逐渐发生反应被消耗.其在516 nm处的荧光强度随时间的变化关系如图5(a)插图所示,在250 min后,荧光强度基本趋于不变,说明反应基本完全,经拟合表明该反应过程符合二级反应特征.
如图5(b)所示,当540 nm光激发时,随着时间的延续,561 nm处出现显著的荧光峰,且强度逐渐增大,表明探针与GSH逐渐反应生成新的化合物.561 nm处的荧光强度随时间的变化关系如图5(b)插图所示,表明新化合物的生成过程同样符合二级反应特征.

(a)470 nm波长光激发

(b)540 nm波长光激发图5 探针加入GSH后在不同波长光激发时的荧光变化过程
2.5 探针对不同浓度GSH的响应分析
为评价探针用于GSH定量检测的可行性,固定探针浓度,分析了探针对不同浓度GSH响应的荧光光谱,如图6所示.为更好地展示探针比率响应的性能,选择510 nm光作为激发光源.由图6可知,随着GSH浓度的升高,522 nm处的荧光峰逐渐降低,而561 nm处的荧光峰逐渐升高,呈现典型的比率响应特征.对两处荧光峰强度比率拟合分析,结果如图6插图所示,呈现良好的线性关系.因此,根据荧光比率关系可实现GSH浓度的定量检测.

图6 探针与不同浓度的GSH(0.1、0.5、1、 2、4、10、 20、40和100 μmol/L)反应后的荧光光谱(插图为I 561 nm/I 522 nm比率与GSH浓度关系)
3 结论
本文以8-羟基久洛尼定为基本骨架,合成了一例基于香豆素的GSH荧光探针.结果表明,该探针对GSH具有较高的选择性,对GSH响应后,探针在516 nm处的荧光逐渐减弱,561 nm处荧光逐渐增强,呈现典型的比率型响应特征.该探针对不同浓度GSH的荧光响应呈现较好的线性关系,表明该探针可以实现GSH的特异性和定量检测.

