替格瑞洛与氯吡格雷用于急性冠状动脉综合征合并糖尿病行经皮冠状动脉介入治疗患者的疗效和安全性比较的系统评价
李君霞,焦雪峰,罗 琳
(河南省胸科医院药剂科,河南 郑州 450000)
急性冠状动脉综合征(acute coronary syndrome,ACS)是一组以冠状动脉粥样硬化斑块糜烂或破裂,继发完全或不完全闭塞性血栓形成,从而导致病变血管出现不同程度的阻塞为病理基础的临床综合征,包括ST段抬高型心肌梗死、非ST段抬高型心肌梗死和不稳定性心绞痛[1]。经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)具有血管再通率高、出血风险低和预后好等优点,目前已被广泛用于ACS的治疗。PCI术前和术后至少12个月患者需使用抗血小板药防止血栓(包括支架内血栓)形成[2],目前临床上氯吡格雷联合阿司匹林双重抗血小板治疗是治疗ACS的金标准。但有研究结果表明,合并糖尿病的ACS患者的血小板反应性升高,其发生氯吡格雷抵抗的概率增加,从而大幅度增加了不良心血管事件的发生风险[3-5]。替格瑞洛是一种新型P2Y12受体拮抗剂,与氯吡格雷相比,其抗血小板作用更快速、强效和稳定[6]。目前,已有多个随机对照试验(randomized controlled trial,RCT)比较了替格瑞洛与氯吡格雷用于ACS合并糖尿病行PCI术患者的疗性和安全性,但其结论却不一致[7-16]。此外,单个研究的样本量往往较小,其研究结论具有一定的局限性。因此,本研究采用文献荟萃分析(Meta分析)方法,系统评价了替格瑞洛与氯吡格雷用于ACS合并糖尿病行PCI术患者的疗效和安全性,以期为临床用药提供参考。
1 资料与方法
1.1 纳入与排除标准
1.1.1研究类型:比较替格瑞洛与氯吡格雷用于ACS合并糖尿病行PCI术患者的疗效和安全性的RCT,无论是否采用盲法。
1.1.2研究对象:患者诊断为ACS合并糖尿病且行PCI术,其诊断标准参考国内外相关指南,主要根据患者症状、体征、心电图、血糖和血心肌坏死标志物等确诊;研究对象不受种族、性别、血糖控制情况和疾病分型的限制。
1.1.3干预措施:观察组采用替格瑞洛治疗,对照组采用氯吡格雷治疗;两组的其他基础治疗措施一致。
1.1.4结局指标:ADP抑制率;血小板聚集率;主要不良心血管事件(major adverse cardiovascular events,MACE);不良反应。
1.1.5排除标准:仅有摘要而无法获取全文的文献;无法提取数据且联系作者未回复的文献;重复发表的文献;非中、英文文献。
1.2 检索策略
计算机检索PubMed、The Cochrance Library、EMbase、维普数据库(VIP)、中国知网(CNKI)和万方数据库(WanFang DATA)等,收集替格瑞洛与氯吡格雷分别治疗ACS合并糖尿病行PCI术患者的RCT,检索时限为建库至2017年10月28日。同时,进一步追溯纳入研究的参考文献,以补充获取相关文献。英文检索词包括“Clopidogrel*”“Iscover”“Plavix”“SC 25989C”“SC 25990C”“SR 25989”“SR26334”“PCR 4099”“PCR-4099”“2-(2-chlorophenyl)-2-(6,7-dihydro-4H-thieno(3,2-c)pyridin-5-yl)acetic acid”“methyl(o-chlorophenyl)-6,7-dihydrothieno(3,2-c)pyridine-5(4H)acetate polystyrene sulfonate”“Ticagrelor*”“Brilinta”“Brilique”“AZD 6140”“AZD6140”“AZD-6140”“AR-C124910XX”“3-(7-((2-(3,4-difluorophenyl)cyclopropyl)amino)-5-(propylthio)-3H-(1-3)-triazolo(4,5-d)pyrimidin-3-yl)-5-(2-hydroxyethoxy)cyclopentane-1,2-diol”“Diabetes*”“Diabetic*”“Prediabetic State”“Scleredema Adultorum”“Glycosylation End Products”“Advanced”“Glucose Intolerance”及“Gastroparesis”等;中文检索词包括“替格瑞洛”“氯吡格雷”及“糖尿病”等。如遇到缺乏资料或试验报告不详细的情况,则通过邮件或电话与作者联系以尽量获取。
1.3 文献筛选与资料提取
2名评价员分别按照纳入和排除标准独立筛选文献、提取相应的资料。遇到分歧时由2名评价员讨论解决,若仍无法解决则交给第三方判断和裁定。文献筛选过程:首先阅读文题和摘要进行初筛,对于初筛符合标准的文献则通过进一步阅读全文以判断是否可以纳入。提取的资料主要包括:纳入研究的基本信息,包括题目、发表时间、发表国家及第一作者等;研究对象的基线特征,包括病例数、年龄及性别等;研究采用的方法,包括研究的类型、干预措施等;本研究关注的结局指标及相应的结果测量数据。
1.4 纳入文献的质量评价
参照原国家食品药品监督管理总局药品评价中心颁布的《药品文献评价指导原则》,依据证据金字塔分级标准(新九级证据)[17]对纳入的文献分级,具体分级方法为:Ⅰ级,系统评价和Meta分析;Ⅱ级,RCT;Ⅲ级,队列研究;Ⅳ级,病例对照研究;Ⅴ级,病例系列;Ⅵ级,病案报道;Ⅶ级,专家的观点、评论和意见;Ⅷ级,动物实验;Ⅸ级,体外实验。
1.5 统计学方法
采用RevMan 5.3软件进行操作。计数资料选用RR作为效应指标,计量资料选用MD作为效应指标,各效应量均用点估计值和95%CI表示。纳入研究间的异质性采用χ2检验分析(检验水准为α=0.1),并结合I2值进行定量判断研究间异质性的大小。若各研究结果间无统计学异质性,选择固定效应模型进行Meta分析;若各研究结果间有统计学异质性,首先分析异质性来源,在排除明确的临床异质性后,选择随机效应模型进行Meta分析,明确的临床异质性则采用敏感性分析或亚组分析处理或只对结果进行描述性分析。当纳入文献≥10篇时,采用倒漏斗图分析和判断发表偏倚。
2 结果
2.1 纳入文献的基本特征与质量评价
初检共获得436篇相关文献,经过逐层筛选,最终纳入10篇文献[7-16],文献筛选流程见图1。纳入文献的基本特征与质量评价结果见表1,按照证据金字塔分级标准分级,10篇文献均为Ⅱ级证据。
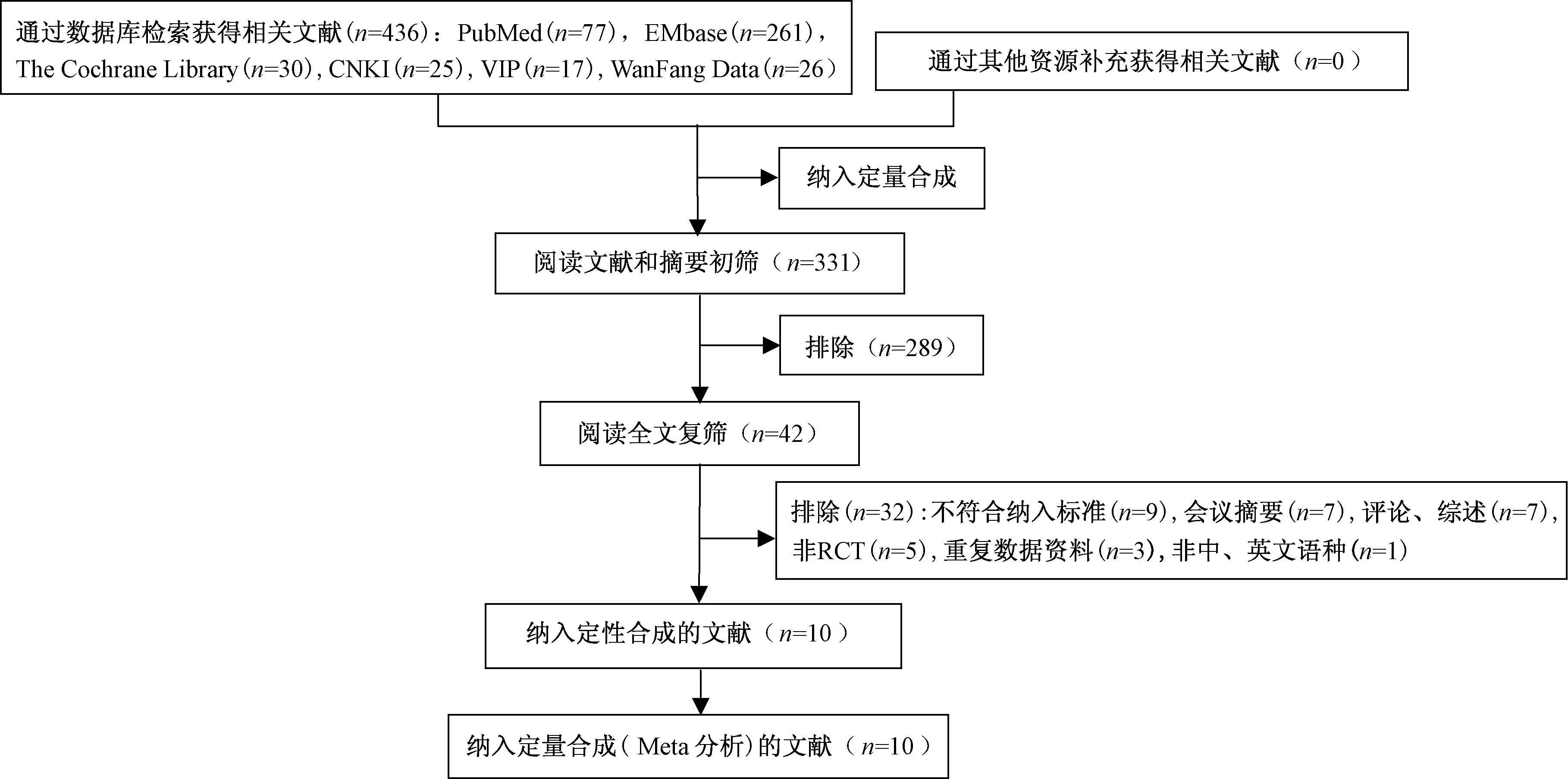
图1 文献筛选流程及结果Fig 1 Process and results of literature screening
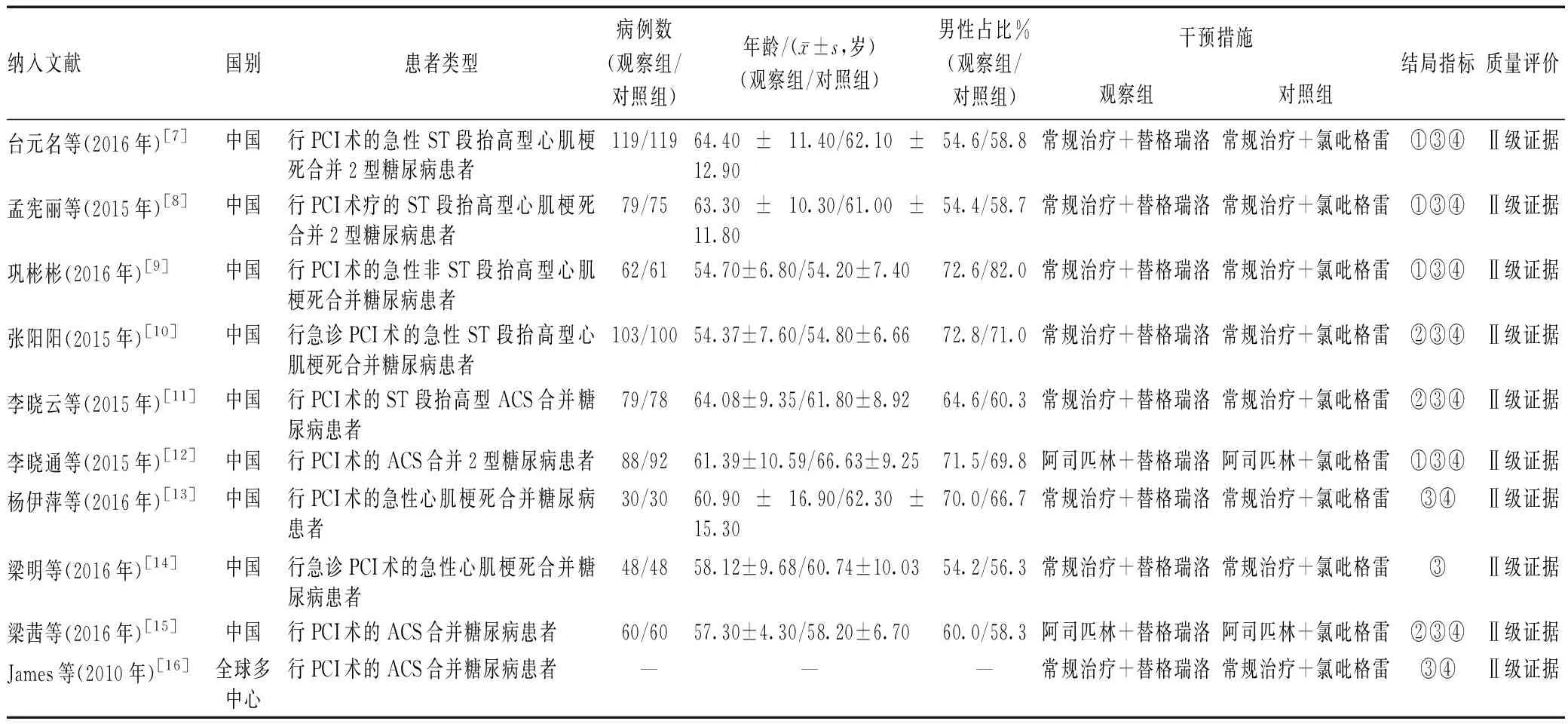
纳入文献国别患者类型病例数(观察组/对照组)年龄/(x±s,岁)(观察组/对照组)男性占比%(观察组/对照组)干预措施观察组对照组结局指标质量评价台元名等(2016年)[7]中国行PCI术的急性ST段抬高型心肌梗死合并2型糖尿病患者119/11964.40±11.40/62.10±12.9054.6/58.8常规治疗+替格瑞洛常规治疗+氯吡格雷①③④Ⅱ级证据孟宪丽等(2015年)[8]中国行PCI术疗的ST段抬高型心肌梗死合并2型糖尿病患者79/7563.30±10.30/61.00±11.8054.4/58.7常规治疗+替格瑞洛常规治疗+氯吡格雷①③④Ⅱ级证据巩彬彬(2016年)[9]中国行PCI术的急性非ST段抬高型心肌梗死合并糖尿病患者62/6154.70±6.80/54.20±7.4072.6/82.0常规治疗+替格瑞洛常规治疗+氯吡格雷①③④Ⅱ级证据张阳阳(2015年)[10]中国行急诊PCI术的急性ST段抬高型心肌梗死合并糖尿病患者103/10054.37±7.60/54.80±6.6672.8/71.0常规治疗+替格瑞洛常规治疗+氯吡格雷②③④Ⅱ级证据李晓云等(2015年)[11]中国行PCI术的ST 段抬高型ACS合并糖尿病患者79/7864.08±9.35/61.80±8.9264.6/60.3常规治疗+替格瑞洛常规治疗+氯吡格雷②③④Ⅱ级证据李晓通等(2015年)[12]中国行PCI术的ACS合并2型糖尿病患者88/9261.39±10.59/66.63±9.2571.5/69.8阿司匹林+替格瑞洛阿司匹林+氯吡格雷①③④Ⅱ级证据杨伊萍等(2016年)[13]中国行PCI术的急性心肌梗死合并糖尿病患者30/3060.90±16.90/62.30±15.3070.0/66.7常规治疗+替格瑞洛常规治疗+氯吡格雷③④Ⅱ级证据梁明等(2016年)[14]中国行急诊PCI术的急性心肌梗死合并糖尿病患者48/4858.12±9.68/60.74±10.0354.2/56.3常规治疗+替格瑞洛常规治疗+氯吡格雷③Ⅱ级证据梁茜等(2016年)[15]中国行PCI术的ACS合并糖尿病患者60/6057.30±4.30/58.20±6.7060.0/58.3阿司匹林+替格瑞洛阿司匹林+氯吡格雷②③④Ⅱ级证据James等(2010年)[16]全球多中心行PCI术的ACS合并糖尿病患者———常规治疗+替格瑞洛常规治疗+氯吡格雷③④Ⅱ级证据
注:①ADP抑制率;②血小板聚集率;③MACE;④不良反应;“—”表示无法提取数据
Note:①ADP inhibition rate;②platelet aggregation rate;③MACE;④adverse reactions;“—” indicates that data cannot be extracted
2.2 Meta分析结果
2.2.1ADP抑制率:4篇文献[7-9,12]比较了ADP抑制率,各研究间存在统计学异质性(P<0.000 1,I2=88%),在排除明确的临床异质性后,选择随机效应模型进行Meta分析。结果显示,观察组患者的ADP抑制率明显高于对照组,差异有统计学意义(MD=19.74,95%CI=12.38~27.11,P<0.000 01),见图2。敏感性分析中,分别剔除纳入的4项研究,合并效应量均仍有统计学意义且森林图结果的方向均未改变。
2.2.2血小板聚集率:3篇文献[10,11,15]比较了血小板聚集率,各研究间同质性较好(P=0.14,I2=49%),选择固定效应模型进行Meta分析。结果显示,观察组患者的血小板聚集率明显低于对照组,差异有统计学意义(MD=-2.99,95%CI=-3.78~-2.19,P<0.000 01),见图3。
2.2.3MACE:6篇文献[7-10,13,15]比较了MACE总体发生率,固定效应模型的Meta分析结果显示,观察组患者的MACE总体发生率明显低于对照组,差异有统计学意义(RR=0.53,95%CI=0.36~0.77,P<0.001);5篇文献[9,10,13-15]比较了心源性死亡发生率,固定效应模型的Meta分析结果显示,两组患者心源性死亡发生率的差异无统计学意义(RR=0.41,95%CI=0.12~1.36,P=0.15);7篇文献[9-12,14-16]比较了心肌梗死发生率,固定效应模型的Meta分析结果显示,两组患者心肌梗死发生率的差异无统计学意义(RR=0.89,95%CI=0.74~1.08,P=0.23);5篇文献[9-12,15]比较了心绞痛发生率,固定效应模型的Meta分析结果显示,观察组患者的心绞痛发生率明显低于对照组,差异有统计学意义(RR=0.29,95%CI=0.15~0.56,P=0.000 2);8篇文献[7-8,11-16]比较了支架内血栓形成发生率,固定效应模型的Meta分析结果显示,观察组患者的支架内血栓形成发生率明显低于对照组,差异有统计学意义(RR=0.53,95%CI=0.33~0.85,P=0.008);2篇文献[7-8]比较了支架内再狭窄发生率,固定效应模型的Meta分析结果显示,观察组患者的支架内再狭窄发生率明显低于对照组,差异有统计学意义(RR=0.50,95%CI=0.32~0.78,P=0.002);3篇文献[11-13]比较了心力衰竭发生率,固定效应模型的Meta分析结果显示,两组患者心力衰竭发生率的差异无统计学意义(RR=0.39,95%CI=0.09~1.71,P=0.21),见表2。
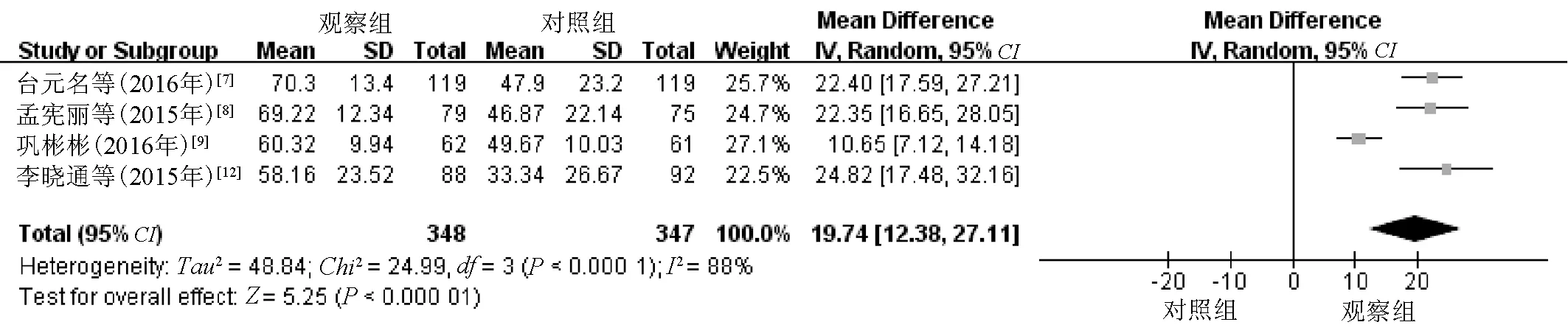
图2 两组患者ADP抑制率比较的Meta分析森林图Fig 2 Forest plot of Meta analysis on comparison of ADP inhibition rates between two groups

图3 两组患者血小板聚集率比较的Meta分析森林图Fig 3 Forest plot of Meta analysis on comparison of platelet aggregation rates between two groups

表2 两组患者MACE发生率比较的Meta分析Tab 2 Meta analysis on comparison of incidences of MACE between two groups
2.2.4不良反应:4篇文献[11-13,15]比较了总不良反应发生率,固定效应模型的Meta分析结果显示,观察组患者总不良反应发生率高于对照组,差异有统计学意义(RR=1.56,95%CI=1.01~2.41,P=0.05);9篇文献[7-13,15-16]比较了出血发生率,固定效应模型的Meta分析结果显示,两组患者出血发生率的差异无统计学意义(RR=1.03,95%CI=0.90~1.18,P=0.66);7篇文献[7-9,11-13,15]比较了呼吸困难发生率,固定效应模型的Meta分析结果显示,观察组患者的呼吸困难发生率明显高于对照组,差异有统计学意义(RR=3.95,95%CI=2.19~7.13,P<0.000 01);2篇文献[11, 13]比较了胃肠道症状发生率,固定效应模型的Meta分析结果显示,两组患者胃肠道症状发生率的差异无统计学意义(RR=0.73,95%CI=0.25~2.12,P=0.56),见表3。

表3 两组患者不良反应发生率比较的Meta分析Tab 3 Meta-analysis on comparison of incidences of adverse drug reactions between two groups
2.3 发表偏倚评估
以上结局指标中的文献数量均<10篇,因此均未能进行倒漏斗图分析。
3 讨论
有效性方面,本次Meta分析结果表明,观察组患者的ADP抑制率高于对照组(P<0.000 01),血小板聚集率、MACE总体发生率、心绞痛发生率、支架内血栓形成发生率和支架内再狭窄发生率均低于对照组(P<0.05),差异均有统计学意义;而两组患者心源性死亡发生率、心肌梗死发生率和心力衰竭发生率的差异均无统计学差异(P>0.05)。以上表明,替格瑞洛用于ACS合并糖尿病行PCI术患者的疗效优于氯吡格雷。合并糖尿病的ACS患者对氯吡格雷抗血小板功能的反应性会下降,文献报道,氯吡格雷抵抗在糖尿病患者中的发生率高达44.1%[18]。分析其原因,可能是由于高血糖会使血小板表面P选择素表达上调,激活蛋白激酶C和血小板表面蛋白糖基化[19],从而使血小板表现为高反应性,更趋于黏附、聚集和激活[5]。此外,氯吡格雷本身是无活性的前体药物,需在体内生物转化为活性代谢物后才能发挥抗血小板作用,从而延长了起效时间;CYP2C19等位基因的携带还会降低前体药物转化为活性代谢物的比例,削弱氯吡格雷的抗血小板聚集作用[20-21]。而替格瑞洛本身为生物活性药物,无需经肝脏代谢即可快速发挥抗血小板作用,其疗效不受CYP2C19基因多态性的影响[22];此外,替格瑞洛不仅可以通过抑制ADP的靶受体P2Y12发挥抗血小板作用[23],还可以抑制红细胞上平衡型核苷转运蛋白1对腺苷的再摄取过程,促进局部腺苷反应,从而发挥额外的抗血小板活化和聚集作用[24]。两者药理作用机制的不同可能是导致其疗效差异的重要原因。
抗血小板药常见的不良反应包括出血(鼻出血、血肿、胃肠道出血、皮下或真皮出血、瘀斑及操作部位出血等)、胃肠道症状(恶心、呕吐、消化不良、腹泻及腹痛等)和呼吸困难等。本次Meta分析结果显示,观察组患者的总不良反应发生率略高于对照组(P=0.05),其中观察组患者的呼吸困难发生率明显高于对照组(P<0.000 01),差异均有统计学意义。以上结果提示,替格瑞洛在临床使用过程中应密切关注其安全性,尤其是呼吸困难的发生情况。近期一项真实世界研究结果表明,使用替格瑞洛的ACS患者因不良反应而中断治疗的发生率高于氯吡格雷[25]。随着对替格瑞洛安全性的质疑越来越多,目前已有学者建议美国食品药品监督管理局复查替格瑞洛PLATO试验的研究数据,进一步审查替格瑞洛临床应用的安全性[26]。
在本研究的各项结局指标中,报告了“ADP抑制率”的研究间存在异质性,且无法消除,但敏感性分析表明其Meta分析结果稳定;报告其他结局指标的研究间同质性均较好,均无需进行敏感性分析。
本次系统评价的局限性包括:(1)语种和地域的影响。本次系统评价的语种仅限定为中、英文,经检索后纳入9篇中文文献、1篇英文文献,且仅有1篇为全球多中心的RCT,其余均为在我国开展的RCT,故本研究结果的外推性受到一定程度的限制;(2)纳入研究的数量相对较少,且部分研究评价的结局指标不全面,故存在发表偏倚的潜在可能。
综上所述,当前证据表明,替格瑞洛用于ACS合并糖尿病行PCI术患者的疗效优于氯吡格雷,但安全性略差。受纳入研究数量和质量的限制,本研究结论尚需在不同地区和国家开展更多大样本、高质量的RCT予以验证。此外,在后续研究中,还需进一步探讨疾病分型、支架类型和血糖控制水平等因素对研究结果的影响,从而为临床决策提供更多证据。

