“球囊挤压”术在冠状动脉慢性完全闭塞病变中应用的可行性和有效性
宗雪梅,孙鸿彬,李兵强
冠状动脉慢性完全闭塞病变(CTO)是冠状动脉(冠脉)病变中较为常见的严重冠脉病变,是冠心病发生发展至终末期的血管病变[1]。经皮冠状动脉介入治疗(PCI)被称为CTO病变“最后的堡垒”,PCI手术时间长,介入治疗难度大。据研究[2,3]报道,CTO患者中有20.7%~43.7%接受PCI血管再通治疗。在CTO病变的PCI血管再通治疗中,导丝不能通过病变头端的纤维帽是CTO病变PCI失败的重要原因之一,尤其对于血管闭塞处存在分支血管的CTO病变,由于导丝容易进入分支增加了正向导丝技术治疗CTO病变的难度。对于这种冠脉闭塞处存在分支的CTO病变的正向技术介入治疗,可以先将指引导丝放置在分支血管内,在分支血管开口处放置合适大小球囊并给于一定压力,挤压CTO病变近端纤维帽使其碎裂,然后再尝试通过闭塞病变行PCI术,我们把这方法称为“球囊挤压”术。本文主要探讨“球囊挤压”技术在CTO中应用的可行性和有效性。
1 资料与方法
1.1 研究对象 收集平顶山市第二人民医院心内科于2013年4月~2017年5月间行PCI的闭塞处存在分支血管的CTO患者41例,其中男性26例,女性15例,年龄41~75(62.8±6.1)岁。入选标准:①冠状动脉造影提示冠状动脉主支血管100%闭塞,闭塞血管远端前向血流TIMI 0级,闭塞血管的直径≥2.25 mm,供血范围较大;②闭塞处存在较大分支血管且分支血管无严重狭窄病变;③CTO患者病史>3个月,闭塞时间根据既往心肌梗死史、临床表现(突发胸痛或胸痛突然加重)及既往冠状动脉CTA、冠状动脉造影(CAG)等。排除标准:①CTO远端血管直径<2 mm;②CTO闭塞病变长且合并严重钙化;③心、肺功能较差的、合并肿瘤等疾病预期寿命小于1年的。所有入选患者均知情同意签字。
1.2 “球囊挤压”术 “球囊挤压”术指先将导丝置于血管闭塞部位分叉处的另一分支血管中,选择合适大小的球囊,球囊直径与分支血管直径比例一般为1:1或1.5:1,一般分支血管存在轻度狭窄病变时按1:1比例选择球囊,血管无病变时按1.5:1比例选择球囊,以保证球囊在不损伤分支的前提下充分挤压斑块使其碎裂。将选择好的球囊的1/2左右置于分支,以6-10 atm扩张球囊以挤压闭塞处斑块纤维帽使其碎裂,减小导丝通过难度,然后撤回导丝至闭塞血管按照常规方法尝试通过闭塞病变完成PCI术。
1.3 研究方法 按随机分组方法随机分为应用“球囊挤压”术的治疗组(19例)和常规技术方法的对照组(22例)。患者术前行ALLEN实验均为阳性,在局麻下穿刺右侧桡动脉,置入6F动脉长鞘,后经鞘管给予硝酸甘油200 ug预防血管痉挛、给予肝素2000 u预防血栓形成。根据病变特点选择合适导管、导丝、球囊行PCI术。对照组按常规治疗方法选择合适导丝直接尝试通过病变斑块纤维帽;治疗组采用“球囊挤压”术,后再尝试导丝通过病变。两组患者通过闭塞病变后行PCI治疗.术前均给于阿司匹林300 mg、氯吡格雷300 mg口服,后阿司匹林100 mg,1/d;氯吡格雷75 mg,1/d,维持至手术日;术中按常规在动脉内注射普通肝素100 U/kg达到肝素化,PCI成功后于静脉应用替罗非班,维持48 h,后按常规继续口服阿司匹林100 mg,1/d;氯吡格雷75 mg,每日1次维持1年,根据患者情况常规给予调脂、降压及其它对症药物应用。随访患者1年内心血管不良事件发生情况。
1.4 比较指标 比较两组患者年龄、性别、合并症、吸烟、左室射血分数、肌酐、稳定型心绞痛、不稳定型心绞痛、陈旧性心肌梗死、既往PCI史、冠脉闭塞时间、CAG特征及J-CTO积分等基线临床资料。比较两组间X线曝光时间、对比剂用量、PCI失败率、手术并发症、1年内心血管主要不良事件(发生心绞痛、心肌梗死等)等有关指标。J-CTO积分指根据既往PCI手术失败史、冠状动脉闭塞的形态、钙化、迂曲及病变长度大于20 mm等指标计算,每项赋值1分。
1.5 统计学方法 采用SPSS 16.0统计软件进行数据统计,计量资料采用均数±标准差(±s)表示,两组间均数的比较采用t检验;计数资料采用例数(构成比)表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者一般临床资料比较 两组患者年龄、男性、合并症、吸烟、左室射血分数(LVEF)、肌酐、稳定型心绞痛、不稳定型心绞痛、陈旧性心肌梗死、既往PCI史等情况比较,差异无统计学意义(P均>0.05)(表1)。
2.2 两组间CAG特征比较 两组患者冠状动脉血管造影特征及积分比较差异均无统计学意义(P均>0.05)(表2)。
2.3 两组间患者手术相关指标比较 两组间X线曝光时间、对比剂用量、PCI失败率比较差异具有统计学意义(P<0.05)。两组间手术并发症、1年内心血管主要不良事件(MACE事件)比较差异无统计学意义(P>0.05),治疗组有2例出现分支血管狭窄加重情况,对照组出现1例分支开口狭窄加重,均给予球囊扩张术后狭窄改善,未行支架干预;治疗组出现再发心绞痛3例,对照组出现再发心绞痛2例,均给予对症药物强化治疗后症状改善(表3)。
3 讨论
CTO病变一直是PCI病变治疗中成功率最低的,研究表明近年来手术器械及技术的不断更新发展提高了PCI病变治疗的成功率,但手术技术挑战仍是成功率偏低的主要原因[4-6]。有研究报道,虽然主要心血管不良事件发生率相似,但经验丰富的中心较经验欠佳的中心CTO病变的PCI成功率有较明显的提高(90.6%vs. 85.6%,P<0.01)[6]。长时间的冠状动脉血管闭塞可导致心肌细胞变性、心室重构、心脏扩大、室壁运动及心功能减退,影响患者预期寿命及生活质量。多项研究表明,开通闭塞血管不仅可为存活心肌供血、改善阶段性室壁运动及左心功能,改善患者预后,且有助于干细胞治疗对心肌损伤区域的定位[7-9]。因此,CTO病变的PCI血管再通越来越受到重视。近年来,双导丝轨道技术、多导丝斑块挤压技术、逆向导丝技术、STAR技术、CART技术等导丝技术的相继应用,在多种器械的配合基础上大大增加了CTO病变手术的成功率[10]。但多种操作技术复杂,对于介入医生需要较长的学习曲线。而且尽管逆向导丝技术提高了CTO病变的治疗成功率,但由于逆向导丝技术对器械及术者要求更高,且X线放射量更大、造影剂量更多,所以正向导丝技术是多数术者的首选。而对于血管闭塞部位存在分支的CTO病变的治疗,正向介入治疗中由于导丝容易进入分支而增加了手术难度,“球囊挤压”术指在导丝进入分支后,在球囊辅助下挤压闭塞部位斑块,使其纤维冒碎裂从而降低导丝进入的难度、节省手术时间。
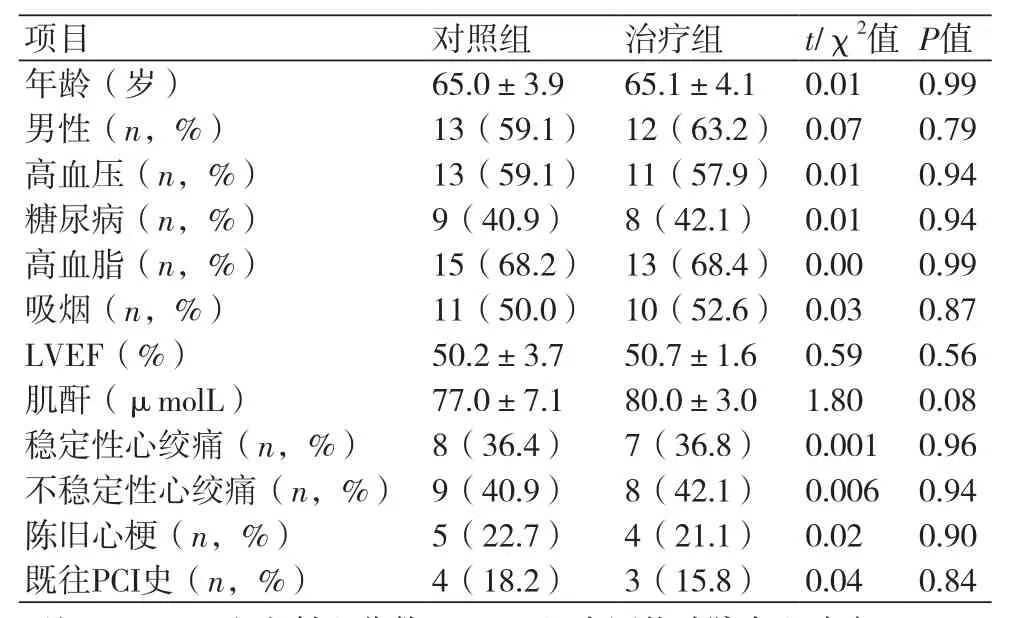
表1 两组患者基线临床资料比较
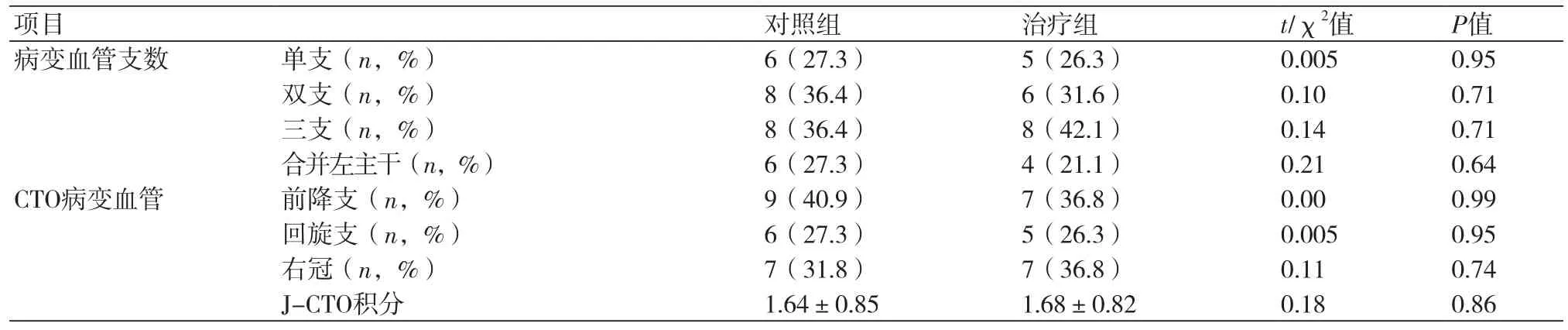
表2 两组间冠脉造影特征比较情况

表3 两组间手术相关情况比较
研究表明,与常规治疗方法比较,使用“球囊挤压”术的治疗组PCI成功率明显高于常规组,而且X线曝光时间较少、造影剂用量较少,差异均具有统计学意义(P<0.05)。在介入过程中,我们常常发现,在主支血管闭塞处存在分支或开口闭塞紧邻另一主支血管时,导丝常常易进入分支或另一主支,这也被认为是CTO病变血管开通的困难因素之一。但对于使用“球囊挤压”术挤压斑块纤维帽时,这种病变特点恰恰提供了解剖基础,成为易化CTO病变治疗的因素。在将导丝置于分支内选择球囊给予一定压力挤压后,撤回球囊及导丝,重新将导丝置于闭塞的主支血管按照常规方法尝试通过闭塞病变完成PCI术。研究表明,使用“球囊挤压”术的治疗组PCI成功率高于常规组(P<0.05),考虑与球囊挤压后使坚硬的斑块纤维冒碎裂减小了导丝通过的难度有关。由于球囊挤压可能产生的分支血管受损、狭窄甚至闭塞等问题是采用此方法可能出现的并发症情况,但本研究结果表明两组患者手术并发症比较差异无统计学意义(P>0.05),1年内随访两组患者心血管不良事件比较差异无统计学意义(P>0.05)。这表明“球囊挤压”术对分支血管并未因球囊的挤压而明星受损,“球囊挤压”术在存在分支血管的CTO病变PCI术中应用是安全的。我们的经验是仔细阅读造影图像,根据分支病变及直径选择合适大小的球囊,在球囊进入分支血管1/2左右后给予低压力扩张,必要时可较高压力再次扩张,球囊扩张速度尽量均匀缓慢,充分扩张挤压后按常规方法行CTO病变的PCI治疗。在球囊扩张挤压过程中如果分支血管受损严重,必要时给予支架置入补救治疗。
对于冠状动脉血管闭塞处存在分支的CTO病变,“球囊挤压”术利用原本增加手术难度的分支血管,将其解剖基础变为易化CTO-PCI治疗的有利因素,降低CTO-PCI治疗的难度、增加手术成功率。“球囊挤压”术只能应用于闭塞处存在分支血管的CTO病变,且有增加分支血管损伤风险,术者需严格阅读造影结果,根据分支情况决定是否采取“球囊挤压”术及准确选择合适球囊,对潜在并发症要有提前准备。CTO病变临床表现多样,但缺乏特异性,临床症状与冠状动脉血管严重程度不完全符合[11]。其PCI治疗情况复杂、治疗难度大、潜在风险高,对于介入医生不管采取何种技术策略,都要充分评估风险、有预案准备,“球囊挤压”术为CTO病变正向介入治疗提供了一种新方法,我们的小样本研究,结果证明该方法可行有效,进一步还需大样本研究。
[1]陈亚磊,贺毅,米宏志,等. 冠状动脉慢性完全闭塞病变开通价值的研究进展[J]. 中国循证心血管医学杂志,2016,11(8):1391-3.
[2]Yang JH,Kim BS,Jang WJ,et al. Optimal Medical Therapy vs Percutaneous Coronary Intervention for Patients With Coronary Chronic Total Occlusion-A Propensity-Matched Analysis[J]. Circ J,2016,80(1):211-7.
[3]Bucciarelli-Ducci C,Auger D,Di Mario C,et al. CMR Guidance for Recanalization of Coronary Chronic Total Occlusion[J]. JACC Cardiovasc Imaging,2016,9(5):547-56.
[4]Sapontis J,Christopoulos G,Grantham JA,et al. Procedural failure of chronic total occlusion percutaneous coronary interve-Ntion: Insights from a multicenter US Registry[J]. Catheterization & Cardiovascular Interventions, 2015,85(7):1115-22.
[5]Amsavelu S,Christakopoulos GE,Karatasakis A,et al. Impact of Crossing Strategy on Intermediate-term Outcomes After Chronic Total Occlusion Percutaneous Coronary Intervention[J]. Canadian Journal of Cardiology, 2016, 32(10):1239.e1-7.
[6]Habara M,Tsuchikane E,Muramatsu T,et al. Comparison of percutaneous coronary intervention for chronic total occlusion outcome according to operator experience from the Japanese retrograde summit registry[J]. Catheterization & Cardiovascular Interve ntions,2016,87(6):1027-35.
[7]Joyal D,Afilalo J,Rinfret S. Effectiveness of recanalization of chronic total occlusions: a systematic review and meta-analysis[J]. Am Heart J,2010,160(1):179-87.
[8]Strauer BE,Brehm M,Zeus T,et al. Repair of infarcted myocardium by aytologous intracoronary mononuclear bone marrow cell transplantation in humans[J]. Circulation,2002,106(15):1913-8.
[9]Kirschbaum SW,Baks T,van den Ent M,et al. Evaluation of left ventricular function three years after percutaneous recanalizat-ion of chronic total occlusions[J]. Am J Cardiol,2008,101(2):179-85.
[10]吴龙梅,李俊峡,田新利,等. 冠状动脉慢性完全闭塞病变介入治疗策略[J]. 中国循证心血管医学杂志,2017,9(4):496-9.
[11]胡云华,熊力. 冠状动脉慢性完全闭塞病变的临床特点分析[J]. 中国循证心血管医学杂志,2014,6(5),620-1.

