MR T2WI信号特征预测HIFU消融治疗子宫腺肌病疗效
刘 畅,陈锦云,*,陈文直,肖智博,杨 超,王 玲,魏 庆
(1.重庆医科大学生物医学工程学院 省部共建国家重点实验室培育基地—重庆市超声医学工程重点实验室 重庆市生物医学工程学重点实验室 重庆市微无创医学协同创新中心,重庆 400016;2.重庆医科大学附属第一医院超声消融治疗中心,3.放射科,重庆 400042)
子宫腺肌病是妇科常见疾病,系子宫内膜腺体和间质侵入子宫肌层所致,临床表现为进行性加重的痛经、月经量增多和不孕等[1],发病率约8.8%~31.0%[2]。子宫腺肌病MR T2WI特征性表现主要包括子宫体积不对称性增大和子宫内点片状高信号(异位子宫内膜组织、内膜囊肿或出血)[3-5]。临床对子宫腺肌病尚缺乏有效的保守治疗手段,目前最有效的方法为子宫切除术。HIFU是近年来迅速发展的一种非侵入性热消融技术,用于治疗子宫腺肌病具有准确性高、疗效确切、不良反应少、重复性好等优点[6-8]。本研究探讨术前MR T2WI信号特征对HIFU消融治疗子宫腺肌病疗效的预测作用。
1 资料与方法
1.1 一般资料 收集2012年1月—2016年12月接受HIFU治疗的子宫腺肌病患者502例,年龄18~53岁,平均(39.3±5.7)岁,体质量指数(body mass index, BMI)为16.56~30.47 kg/m2,平均(22.32±2.85)kg/cm2,临床均表现为不同程度的痛经和/或月经量增多,且均排除合并子宫肌瘤及其他盆腔疾病。所有患者均知晓HIFU治疗风险,并签署知情同意书。
1.2 超声消融 术前完善心电图、血常规、肝肾功能等检查。建立静脉通道,导尿并留置尿管。采用海扶JC型聚焦超声肿瘤治疗系统行HIFU治疗,超声换能器功率0~400 W,频率0.8 MHz,物理学焦域1.5 mm×1.5 mm×10.0 mm,机载显像超声频率3.5 MHz,循环脱气水耦合。嘱患者俯卧,于超声实时引导下进行消融,术中根据患者耐受程度及靶区灰度变化调整治疗方案。
1.3 MR检查 采用GE Signa HD Excite 3.0T MR成像系统,体部环形线圈,分别于HIFU消融术前及术后次日行MR检查。嘱患者仰卧,行轴位、冠状位及矢状位扫描,扫描范围自髂嵴至耻骨联合下缘。扫描序列及参数:①T1W、脂肪抑制T1W序列,TR 502 ms,TE 12 ms,层厚4 mm,层间距1 mm;②T2W、脂肪抑制T2W序列,TR 4 000 ms,TE 98 ms,层厚6 mm,层间距0.875 mm;③增强T1W序列,TR 5.13 ms,TE 2.37 ms,层厚2.5 mm,层间距0.5 mm,对比剂采用钆双胺注射液(欧乃影,0.5 mmol/ml),剂量15~20 ml。

图1 Ⅰ组子宫腺肌病患者矢状位T2WI A.ⅠA亚组,无稍高和极高信号; B.ⅠB亚组,有稍高信号(箭); C.ⅠC亚组,有极高信号(箭)或极高合并稍高信号 图2 Ⅱ组子宫腺肌病患者矢状位T2WI A.ⅡA亚组,无稍高和极高信号; B.ⅡB亚组,有稍高信号(箭); C.ⅡC亚组,有极高信号(箭)或极高合并稍高信号

图3 基于MR T2WI子宫腺肌病病灶体积测量方法 A.矢状位测量病灶长径(平行于子宫内膜的最大径)和前后径(垂直于长径的最大径); B.轴位测量病灶左右径(水平最大径)
1.4 T2WI信号分析及分组 根据MR T2WI信号强度,以正常子宫肌层及宫腔信号为参照,如子宫腺肌病病灶信号低于正常子宫肌层信号为低信号,等于正常子宫肌层信号为等信号,高于正常子宫肌层但低于宫腔信号为稍高信号,等于或高于宫腔信号为极高信号。按照T2WI主要信号特征将患者分为2组,其中Ⅰ组以低信号为主(低信号范围>50%),可有少量等信号;Ⅱ组以等信号为主(等信号范围>50%),可有少量低信号;每组再按照子宫腺肌病病灶内次要信号特征分为A(无稍高和极高信号)、B(有稍高信号)、C(有极高或极高合并稍高信号)亚组,见图1、2。
1.5 超声消融效果评价与治疗参数分析 基于术前MR T2WI测量子宫腺肌病病灶体积(图3),基于术后次日增强T1WI测量无灌注区体积(non-perfused volume, NPV),体积均按照椭圆体公式计算:体积=a×b×c×0.5233,其中a、b、c分别代表长径、前后径及左右径。计算病灶体积消融率(non-perfused volume ratio, NPVR):NPVR=NPV/病灶体积×100%。记录HIFU术中平均功率、辐照时间,计算总消融剂量及能效因子(energy efficiency factor, EEF),即消融单位体积病灶所需超声能量;总消融剂量(kJ)=P×t,EEF(J/mm3)=η×P×t/NPV,其中η为聚焦系数(η=0.7),P为声功率(W),t为辐照时间(s)。
1.6 疼痛及并发症评价 于HIFU消融术中要求患者进行主观疼痛评分:0分为无痛;1~2分为轻度疼痛;3~4分为中度疼痛;5~6分为重度疼痛;7~8分为极重度疼痛;9~10分为难以忍受的剧痛。根据国际介入放射学会(society of interventional radiology, SIR)分类法[9],评价术后并发症。
1.7 统计学分析 采用SPSS 20.0统计分析软件,计量资料以±s表示,2组间比较采用两独立样本t检验;同组内各亚组间比较时,如方差齐则采用单因素方差分析,两两比较采用LSD-t检验,如方差不齐则采用KruskalWallisH检验进行比较,以Bonferroni校正P值后采用Mann-WhitneyU检验进行两两比较。计数资料以百分率表示,采用χ2检验进行比较。P<0.05为差异有统计学意义。
2 结果
502例子宫腺肌病患者中,病变类型为局限型247例、弥漫型255例,其中病灶位于子宫前壁、后壁、侧壁、宫底分别为242例、376例、65例及108例;前、中、后位子宫分别为285例、83例及134例。HIFU消融术前病灶体积15.49~742.68 cm3,平均(145.42±107.61)cm3。Ⅰ组与Ⅱ组间及组内不同亚组间患者年龄、病灶体积、病变类型、子宫及病灶位置差异均无统计学意义(P均>0.05)。见表1。
2.1 超声消融效果 Ⅰ组与Ⅱ组间及组内不同亚组间NPV差异均无统计学意义(P均>0.05)。Ⅰ组与Ⅱ组NPVR差异无统计学意义(LSD-t=-0.504,P=0.612)。Ⅰ组中,ⅠA亚组NPVR高于ⅠB亚组及ⅠC亚组(LSD-t=2.608、3.677,P=0.009、<0.001),ⅠB亚组与ⅠC亚组NPVR差异无统计学意义(LSD-t=-0.852,P=0.395);Ⅱ组中,ⅡA亚组NPVR高于ⅡB亚组及ⅡC亚组(LSD-t=3.255、3.778,P=0.001、<0.001),ⅡB亚组与ⅡC亚组NPVR差异无统计学意义(LSD-t=0.278,P=0.781)。见表2。
2.2 超声消融治疗参数 对502例患者进行HIFU治疗的平均功率、辐照时间、总消融剂量及EEF分别为(391.79±24.08)W、(1 003.44±642.98)s、(394.37±255.80)kJ和(8.94±17.03)J/mm3。Ⅰ组与Ⅱ组间及组内不同亚组间HIFU治疗平均功率差异均无统计学意义(P均>0.05)。Ⅰ组与Ⅱ组辐照时间、总消融剂量和EEF差异无统计学意义(辐照时间:t=-1.716,P=0.087;总消融剂量:t=-1.676,P=0.094;EEF:t=0.044,P=0.965)。Ⅰ组中,ⅠA亚组辐照时间、总消融剂量和EEF均低于ⅠB亚组及ⅠC亚组(辐照时间:LSD-t=2.123、2.717,P=0.035、0.007;总消融剂量:LSD-t=2.117、2.698,P=0.035、0.007;EEF:Z=-3.409、-2.950,P=0.001、0.003),ⅠB亚组与ⅠC亚组辐照时间、总消融剂量和EEF差异均无统计学意义(辐照时间:LSD-t=0.407,P=0.684;总消融剂量:LSD-t=0.394,P=0.694;EEF:Z=-0.378,P=0.705);Ⅱ组中,ⅡA亚组辐照时间、总消融剂量和EEF均低于ⅡB亚组及ⅡC亚组(辐照时间:LSD-t=2.778、4.229,P=0.006、<0.001;总消融剂量:LSD-t=2.843、4.206,P=0.005、<0.001;EEF:Z=-2.678、-3.025,P=0.007、0.002),ⅡB亚组与ⅡC亚组辐照时间、总消融剂量和EEF差异均无统计学意义(辐照时间:LSD-t=1.292,P=0.198;总消融剂量:LSD-t=1.195,P=0.233;EEF:Z=-0.185,P=0.853)。见表3。
2.3 疼痛及并发症 所有患者均耐受治疗,部分患者HIFU术中出现治疗区及骶尾部痛、下肢放射痛等,疼痛评分为0者9例(9/502, 1.79%);1~2分168例(168/502, 33.47%);3~4分264例(264/502,52.59%);5~6分59例(59/502,11.75%);7~8分2例(2/502,0.40%)。术后361例(361/502,71.91%)患者出现疼痛等不适,为SIR A~B级并发症,无SIR C~F级并发症发生。
3 讨论
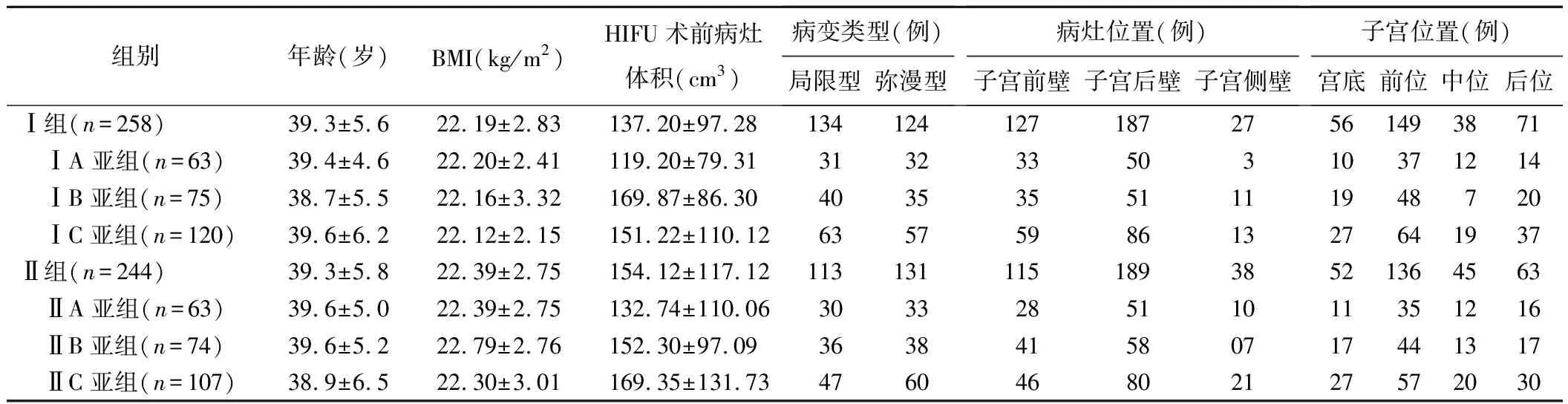
表1 HIFU术前不同MR T2WI信号特征组子宫腺肌病患者及病灶资料
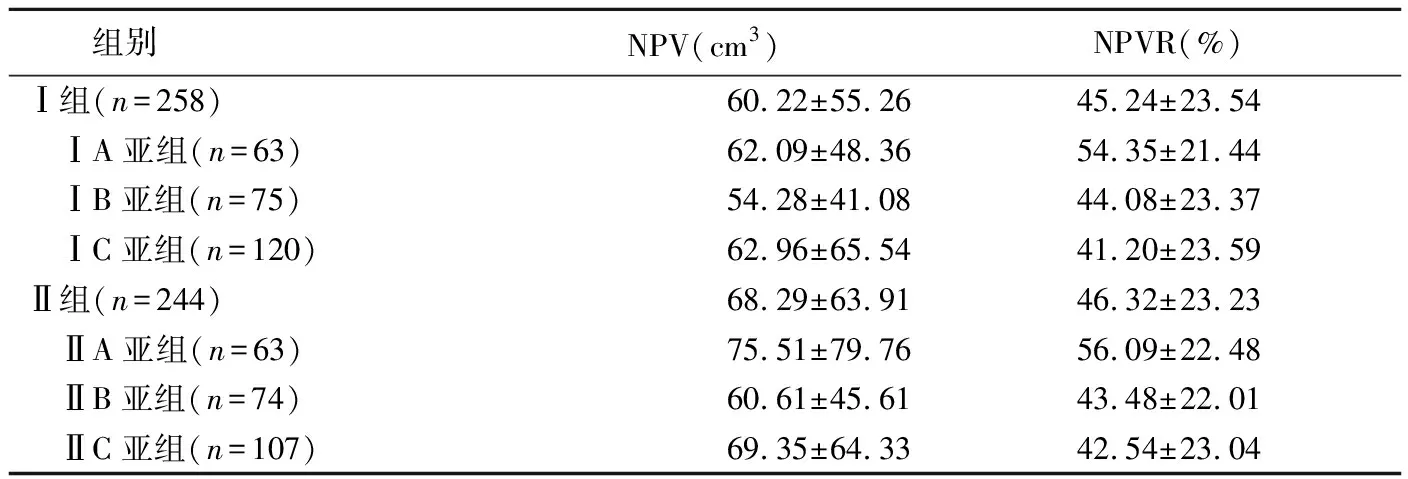
表2 不同MR T2WI信号特征组子宫腺肌病患者HIFU术后NPV及NPVR比较
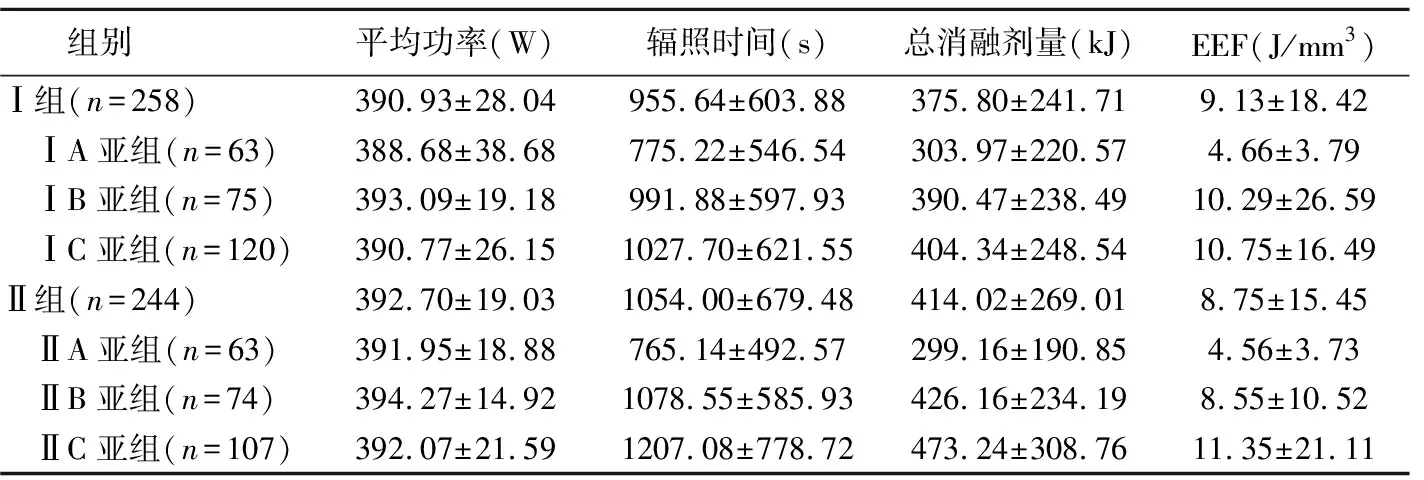
表3 不同MR T2WI信号特征组子宫腺肌病患者HIFU消融平均功率、辐照时间、总消融剂量及EEF比较
MR T2WI能清楚显示子宫腺肌病的部位、范围、异位内膜组织和出血灶。研究[10-12]报道,不同T2WI信号强度的病灶HIFU消融疗效及剂量存在差异,但目前对超声消融子宫腺肌病是否存在规律尚无定论,也无公认的子宫腺肌病MR T2WI信号特征分类方法。本研究对子宫腺肌病MR T2WI信号特征进行分类,探究其对HIFU消融治疗子宫腺肌病疗效的预测作用。
本研究根据子宫腺肌病T2WI信号特征,将患者分为Ⅰ组和Ⅱ组,结果显示2组NPVR及EEF差异均无统计学意义,表明子宫腺肌病以等信号为主或低信号为主对HIFU消融疗效无明显影响,单位体积所需超声消融剂量亦无明显差别,提示MRI表现虽可在一定程度上反映子宫腺肌病病灶的生物学特征[13],但本病组织病理学表现多样,仅根据T2WI等信号或低信号预测消融疗效较为困难。因此,本研究进一步分析HIFU消融治疗子宫腺肌病的疗效是否与T2WI病灶内的点片状高信号有关,这些点片状高信号大部分为异位的子宫内膜组织,异位内膜组织通常会随月经周期改变发生周期性出血,出血时期不同,其T2WI信号强度也会发生改变[14]。本研究将子宫腺肌病病灶内无稍高和极高信号、存在稍高信号、存在极高或极高合并稍高信号者进一步分为A、B、C亚组,结果显示在Ⅰ组及Ⅱ组中,A亚组NPVR均高于B亚组及C亚组,辐照时间、总消融剂量和EEF均低于B亚组及C亚组,而B亚组与C亚组间NPVR、辐照时间、总消融剂量和EEF差异均无统计学意义;表明对MR T2WI病灶内无稍高和极高信号的子宫腺肌病患者更易获得理想的HIFU消融效果,且消融单位体积病灶所需消融剂量更小,而对病灶内有稍高或极高信号者消融难度增加,消融单位体积病灶所需消融剂量也更多;提示子宫腺肌病高信号灶是影响超声消融能量沉积的重要因素,病灶内有无稍高和极高信号可预测子宫腺肌病对HIFU消融的疗效。分析出现上述结果的原因,可能在于子宫腺肌病病灶在月经期间反复出血,引起病灶结构改变,影响其对超声能量的吸收、反射和散射,造成能量损失,减少焦点处能量沉积,相应所需的单位体积病灶超声消融剂量增加,最终导致消融疗效降低。另一方面,影响HIFU消融疗效的因素较多,如不同患者的疼痛阈值、病灶血供、位置、最大径等均可能致使同样的超声能量对不同患者的HIFU消融疗效产生差异[15],尚需进一步观察。
综上所述,MR T2WI信号特征对于HIFU消融子宫腺肌病难易程度和消融效果具有重要预测作用,可为超声消融方案的制定提供依据。
[参考文献]
[1] Zhang X, Yuan H, Deng L, et al. Evaluation of the efficacy of a danazol-loaded intrauterine contraceptive device on adenomyosis in an ICR mouse model. Hum Reprod, 2008,23(9):2024-2030.
[2] Jason M, Dechenne V, Chantraine F, et al. Adenomyosis. Rev Med Liege, 2013,68(4):160-162.
[3] Sudderuddin S, Helbren E, Telesca M, et al. MRI appearances of benign uterine disease. Clin Radiol, 2014,69(11):1095-1104.
[4] 段寿生,邝平定.子宫腺肌症MRI临床表现及诊断价值分析.医学影像学杂志,2016,26(5):943-946.
[5] 侯金文,程华,李传福.子宫腺肌病的MRI表现及其病理学对照研究.中华放射学杂志,2002,36(1):67-71.
[6] 冯玉洁,陈锦云,胡亮,等.弥漫型和局限型子宫腺肌病超声消融安全性对比分析.中国介入影像与治疗学,2016,13(6):342-347.
[7] 陈锦云,陈文直,王智彪,等.子宫腺肌病病变形态对超声消融耐受性及安全性的影响.中国实用妇科与产科杂志,2013,29(12):976-979.
[8] Liu X, Wang W, Wang Y, et al. Clinical predictors of long-term success in ultrasound-guided high-intensity focused ultrasound ablation treatment for adenomyosis. Medicine (Baltimore), 2016,95(3):e2443.
[9] Goldberg SN, Grassi CJ, Cardella JF, et al. Image-guided tumor ablation: Standardization of terminology and reporting criteria. Radiology, 2005,235(3):728-739.
[10] Zhao WP, Chen JY, Zhang L, et al. Feasibility of ultrasound-guided high intensity focused ultrasound ablating uterine fibroids with hyperintense on T2-weighted MR imaging. Eur J Radiol, 2013,82(1):e43-e49.
[11] Funaki K, Fukunishi H, Funaki T, et al. Magnetic resonance-guided focused ultrasound surgery for uterine fibroids: Relationship between the therapeutic effects and signal intensity of preexisting T2-weighted magnetic resonance images. Am J Obstet Gynecol, 2007,196(2):184.e1-e6.
[12] 李非,冉剑波,黄浩然,等.HIFU消融不同T2WI信号子宫肌瘤疗效差异的组织声学性质.中国介入影像与治疗学,2016,13(7):434-436.
[13] Reinho1d C, McCarthy S, Bret PM, et al. Diffuse adenomyosis: Comparison of endovaginal US and MR imaging with histopathologic correlation. Radiology, 1996,199(1):151-158.
[14] 胡春洪,汪文胜,方向明,等.MRI诊断手册.北京:人民军医出版社,2013:6-11.
[15] 李发琪,王智彪,杜永洪,等.高强度聚焦超声“切除”组织的剂量学研究.生物医学工程杂志,2006,23(4):839-843.