烃露点分析在天然气标准气体制备中的应用
邓凡锋, 周 鑫, 董了瑜, 李志昂, 郑力文, 方 正
(中国测试技术研究院, 四川 成都 610021)
1 引 言
天然气来源和组成的不同使其发热量有很大差异,因此天然气以能量计量更能合理反映天然气热能价值[1]。真正直接对天然气进行能量测定的系统还在开发之中,估计近期内难以商品化[2]。目前所采用的能量计量方法均属于间接测定,通过对天然气标气和待测天然气气相色谱分析,进而对待测天然气的组分定值,计算出发热量。目前天然气标气主要依据GB/T 5274—2008 《气体分析校准用混合气体的制备称量法》进行制备,为了保证天然气中的重组分不发生冷凝液化,该方法建议各组分的充装压力不超过组分常温蒸汽压的50%,最好不超过25%,这种计算由于过于保守使得配制压力较低。
本文运用Peng-Robinson物性方程建立计算模型,绘制气液平衡相图。对不同组成的天然气烃露点的变化规律进行求解,通过对相图中烃露点线的分析,可以准确地预测天然气在特定压力和温度条件下组分出现冷凝液化的可能性,提高标气配制的可靠性。
2 模型的建立
2.1 状态方程的选择
维里状态方程和立方型状态方程常用于烃类混合物的物性进行描述和模拟计算。维里状态方程对于极性混合物和高压状态下气液两相的物性缺乏准确性,立方型状态方程则可通过对体积三次幂的解析求根及相关参数的关联,进而对天然气的物性参数进行计算[3]。常见的方程有Redlich-Kwong-Soave(SRK)、Peng-Robinson(PR)、Benedict-Webb-Rubin-Starling(BWRS)、Gaussian(GS)等,但由于PR方程对于烃类物性很好的适应性,且方程的性能稳定、参数少、形式简单、易于计算的收敛、计算精度高,因此本文选择PR方程[4~6]进行计算,其表达式见式(1)~(9)。
(1)
(2)
α0.5=1+(0.376 46+1.542 2ω-
(3)
(4)
(5)
Z3-(1-B)Z2+(A-3B2-2B)Z-
(AB-B2-B3)=0
(6)
(7)
(8)
(9)
式中:p为组分的压强,Pa;R为理想气体常数,8.314 J/(mol·K);V为摩尔体积,m3/mol;Tc为临界温度,K;pc为临界压强,Pa;a,b为与Tc、pc关联的特征参数;ac为与Tc、pc相关的常数;ω为偏心因子;Tr为对比温度;α为与Tr、ω关联的函数;β为与m、T关联的函数;m、n为与ω关联的函数;A为与α、a、p、T、R关联的参数;B为与b、p、T、R关联的参数;Bi为组分i的参数B值;aj为组分j的特征参数a值;Z为压缩因子;xi、yi分别为液相、气相中i组分的摩尔分数;φi为组分i的逸度系数;φl,i、φg,i为液相、气相中i组分的逸度系数。
2.2 物性参数
本文所用组分的主要参数临界温度(Tc)、临界压力(pc)、偏心因子(ω)、沸点(Tb)在文献[7]可查得,具体数据见表1。

表1 天然气组分的物性参数表
2.3 模型计算
本文的气液两相的平衡通过图1所示的迭代计算流程进行求解,具体过程:将表1中的数据代入式(1)~式(5)求解状态方程的系数;将状态方程系数代入式(6)~式(7)计算压缩因子;最后将上述参数代入式(8)计算逸度系数;迭代终止的条件见式(9),即气液两相达到平衡状态,两相的逸度系数近似相等。

图1 模型的计算流程简图
3 结果与讨论
本文选用文献[8~12]中的模拟天然气(simulated nature gas,SNG)SNG-1~SNG-6组分摩尔分数数据(见表2),对模型的可靠性和准确性进行验证,得到的相图见图2。
3.1 模型的可靠性
(1)本文采用的PR方程模拟计算烃露点的方法,与文献中的高压函数方程[8]、PR方程计算方法和冷凝镜面法[9,12]、EOS-CR模型计算法[10]、EOS-EF模型计算法[11]得到的相平衡曲线与文献可以准确地吻合,表明采用PR方程对天然气的相图规律进行计算模拟在理论上是准确可靠的。
(2)为验证理论值在实际标准气体中的可行性,采用称量法[13]分别配制SNG-6组分不同压力条件下的2种标气,配制值-1、配制值-2的配制压力分别为2.9 MPa、8.5 MPa,分析值是以低压气为标准分析高压气得到的值,误差是配制值-2与分析值之间的差值,具体分析结果见表3。由表3结果可知:高压8.5 MPa标气的配制误差可以控制在0.1%以内,在高压条件下天然气保持了气相的单一性,无液相析出,这表明相图的理论计算值可以在实际中得到很好的应用。

表2 研究所用的模拟天然气组分摩尔分数表 (%)

图2 天然气的模拟计算图
3.2 模型的应用
本文以SNG-6为例说明露点线分析在天然气标准气体研制中的应用。
3.2.1 天然气标气配制压强的选择
SNG-6中沸点最低的组分n-C6H14的摩尔分数为0.3%,n-C6H14的饱和蒸气压为17.6 kPa(20 ℃条件下)。根据GB/T 5274—2008中的饱和蒸气压估算法,在20 ℃的条件下此组成天然气最高可以配到5.8 MPa,加之标准气体的配制通常须考虑一定的安全充装系数,如按50%系数计算,SNG-6天然气只能配制到2.9 MPa。但由图2中SNG-6的烃露点线看出,点A(20 ℃,5.8 MPa)处于烃露点线的外侧,表明此时天然气处于气相状态,无冷凝液体析出;考虑到安全充装系数的点B(20 ℃,2.9 MPa)亦处于烃露点线的外侧,说明此时天然气完全以气相状态存在。根据20 ℃条件下甲烷焦汤系数[14]可知在5.8 MPa时,甲烷的焦汤系数在1.7左右,此天然气降至0.3 MPa的使用下限时温降为9.35 ℃左右,对照图2可知此时天然气仍以气相存在。由此证明GB/T 5274—2008的条件限制可以配制出纯气相的天然气标气,但由图2烃露点线可知在固定温度20 ℃条件下,天然气均以气相存在。因此,在此温度条件下该组成的天然气可以配制到更高的压力,从而增加用户的天然气使用寿命和更换周期。
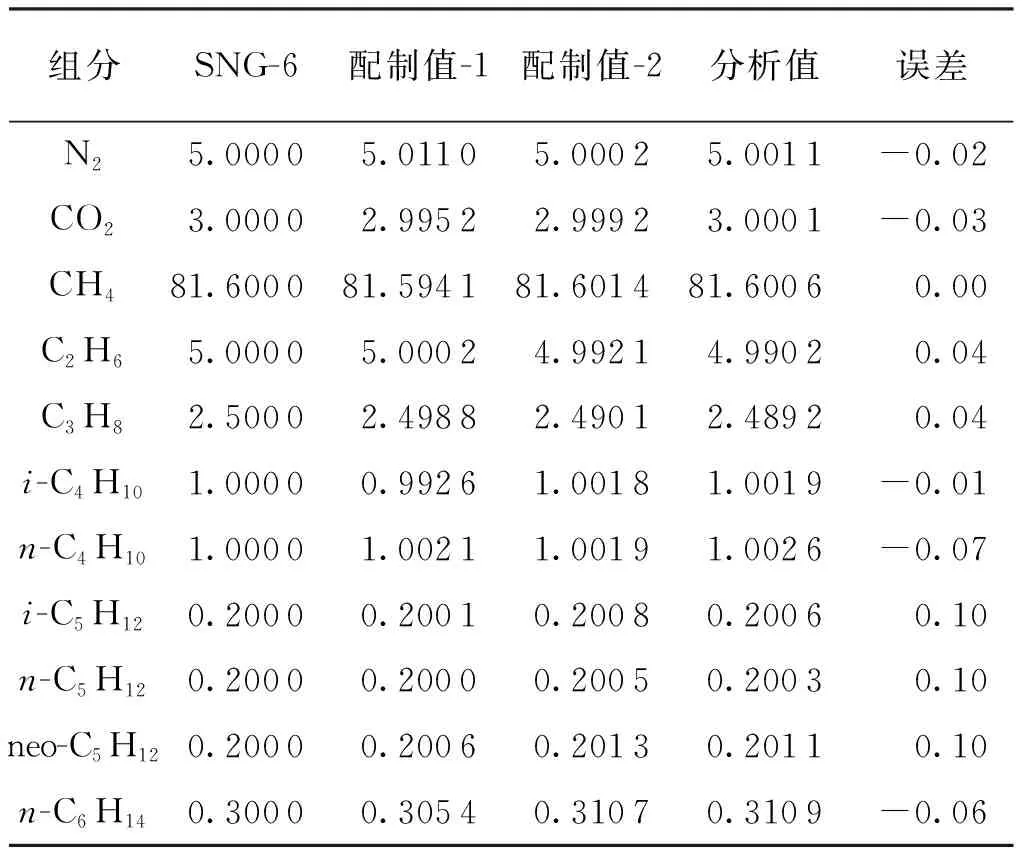
表3 模拟天然气SNG-6摩尔分数分析表 (%)
3.2.2 天然气配制温度的选择
天然气标气在配制和使用过程中还应考虑温度因素,由SNG-6的露点线可知:在0 ℃条件下C、D两点之间的区域已经出现在露点线内部(包含A、B两点对应的压力),表明此时天然气标气已经出现液体凝析,如若用此标气进行分析比对得到的结果就会失真。由图可知在0 ℃条件下,此组成天然气最高可配到2.0 MPa。因此在使用温度条件有波动的地区和季节,露点分析可以提供很好的配制条件,避免凝析液的产生。
4 结 语
天然气的烃露点曲线分析与GB/T 5274—2008 称重法制备气体标准物质中的饱和蒸汽压估算法相比,可以更准确地预测天然气在特定压力和温度条件下组分出现冷凝液化的可能性,提高标气配制和使用的可靠性。
[参考文献]
[1] 王池, 李春辉, 王京安,等.天然气能量计量系统及方法[J].计量学报,2008,29(5):403-406.
[2] 李佳, 孙国华, 王海峰,等.基于氧弹热量计测量天然气发热量标准装置及方法的研究[J].计量学报,2013,34(6):592-596.
[3] 李佩铭, 焦文玲, 管胜强. 天然气液化工艺的相平衡计算[J]. 能源工程,2007,(3): 20-23.
[4] Nasrifar K, Bolland O, Moshfeghian M. Predicting natural gas dew points from 15 equationsof state[J].EnergyFuels, 2005, 19(2):561-572.
[5] Ding Y P, Donald B R. A new two-constant equation of state[J].Industrial&EngineeringChemistryFundamentals,1976,15(1):59-64.
[6] Zheng D Q, Guo T M. Prediction of the Phase Behavior of Gas Condensates Using Patel-Teja Equation of State and Gamma Distribution Function[J].ChineseJournalofChemicalEngineering,1997,5(3):12-19.
[7] 郭天民. 多元气-液平衡和精馏[M]. 北京:石油工业出版社,2002.
[8] Blanco S T, Avila S, Velasco I,etal. Dew points of ternary methane+ethane+butane and quaternary methane+ethane+butane+water mixtures: measurement and correlation [J].FluidPhaseEquilibria, 2000, 171(1-2): 233-242.
[9] Mørch Ø, Nasrifar K, Bolland O,etal. Measurement and modeling of hydrocarbon dew points for five synthetic natural gas mixtures [J].FluidPhaseEquilibria. 2006, 239(2): 138-145.
[10] Avila S, Blanco S T, Velasco I,etal. Thermodynamic Properties of Synthetic Natural Gases. 2. Dew Point Curves of Synthetic Natural Gases and Their Mixtures with Water and Methanol. Measurement and Correlation[J].EnergyFuels, 2002, 16(4): 928-934.
[11] Avila S, Blanco S T, Velasco I,etal. Thermodynamic properties of synthetic natural gases. 4. Dew point curves of synthetic natural gases and their mixtures with water: measurement and correlation [J].FluidPhaseEquilibria, 2002, 202(2): 399-412.
[12] Vasiliki L, Pappa G, Boukouvalas C,etal. Measurement and prediction of dew point curves of natural gas mixtures[J].FluidPhaseEquilibria,2012,334(6):1-9.
[13] 方正, 周鑫, 潘义.氮气中1 μmol·mol-1硫化氢气体标准物质的研制[J]. 化学研究与应用,2014,26(11):1809-1812.
[14] 聂廷哲, 段常贵. 高压天然气绝热节流系数的确定[J]. 煤气与热力,2004,24(2):61-64.

