海南黄芩中黄酮类化合物的分离与鉴定
刘洁,李备,刘春,陈露,梁扬,周玦飞,颜彦,陈赞民
1.海南省药品检验所,海南 海口 570216;2.海南省食品检验检测中心,海南 海口 570311
唇形科(Labiatae)黄芩属(Scutellaria)植物资源十分丰富,全世界共有300余种。该属物种多具有清热燥湿、泻火解毒之功效[1-2]。黄芩属植物具有广泛的药理作用,如抗肿瘤、保肝、抗氧化等活性。现代化学成分研究表明,黄酮和二萜为其主要活性成分[3]。近十几年,有大量研究对从黄芩属植物中所得化学成分的活性进行筛选,发现了许多结构新颖且活性显著的化合物。海南黄芩(S.hainanensis)为唇形科黄芩属植物,分布于海南地区,长于石山上,是海南特有植物,具有清热解毒的功效[4]。迄今,有关海南黄芩化学成分研究的报道较少。在此,我们利用多种提取分离技术研究海南黄芩中的化学成分,并利用波谱学方法对所得化合物的结构进行鉴定,从海南黄芩中得到5种黄酮类化合物。
1 材料与方法
1.1 材料
所用植物于2014年8月采自海南省霸王岭,经鉴定为海南黄芩。
BrukerAVⅢ600型核磁共振仪;RE-52A型旋转蒸发仪(上海亚荣生化仪器厂);SHZ-D(Ⅲ)型循环水真空泵(河南巩义英峪予华仪器厂);超声波清洗仪(昆山市超声仪器有限公司);岛津LC-10AD二元低压半制备液相色谱仪;Agilent半制备色谱柱(Phenyl,2.5mm × 25.0cm,5 μm);岛津20A高效液相色谱仪;薄层色谱预制板、柱色谱硅胶(100~200目,200~300目,青岛海洋化工厂);SephadexLH-20(Healthcare公 司),HICHROM ApolloC18色谱柱(250mm × 4.6mm,5 μm)。
综上,微创低温等离子射频消融术联合低剂量放疗能缩短手术时间,减少并发症,降低复发率,促进患者发声功能恢复,提高术后生活质量,值得应用。
1.2 提取黄酮类化合物
干燥粉碎后的海南黄芩(5kg)用95%乙醇(20L)冷浸24h,然后采用加热回流进行提取。共提取3次,每次2h;减压回收溶剂,直至乙醇味消失;母液加水后,用石油醚萃取,继而采用氯仿萃取,浓缩后得到50g浸膏。
1.3 分离纯化黄酮类化合物
将氯仿萃取物进行硅胶柱色谱分析,用氯仿-丙酮梯度洗脱,合并后得到洗脱物Fr.A、Fr.B和Fr.C。Fr.B用硅胶柱色谱分离后,再进行凝胶柱色谱分离,采用反相高效液相制备色谱进行分离,得到化合物 1(12.0mg)、3(18mg)、5(23.0 mg);Fr.C通过硅胶柱色谱、凝胶柱色谱、反相高效液相制备色谱得化合物2(10mg)、4(9.0mg)。
1.4 测定黄酮类化合物纯度
称取5种化合物各约2mg,精密称定,分别至100mL量瓶中,甲醇溶解并稀释至刻度,即得供试品。
色谱条件:HICHROMApolloC18色谱柱(250 mm × 4.6mm,5μm),流动相A为0.3%磷酸,流动相B为甲醇∶乙腈=2∶3,流动相A∶流动相B=40∶60;流速1.0mL/min,柱温 35℃,进样量 20 μL,检测波长280nm。
1.5 核磁测定方法
采用BrukerAVⅢ600型核磁共振仪,化合物1 溶剂为 CDCl3,化合物 2~5 溶剂为 DMSO-d6,1H-NMR为600MHz,13C-NMR为150MHz。
2 结果
2.1 化合物1结构鉴定
化合物1为无色油状物,HPLC归一化法测得纯度为 98.2%(图 1)。根据其1H-NMR(CDCl3,600 MHz)谱(图2),推断δ:12.20(5-OH),7.31(1H,t,J=8.4Hz,H-4′),6.60(2H,d,J=8.4Hz,H-3′,5′),6.08(1H,s,H-6),6.07(1H,dd,J=13.2,4.8Hz,H-2),3.88(3H,s,-OCH3),3.86(1H,dd,J=17.2,13.2Hz,H-3a),3.81(6H,s,2′,6′-OCH3),3.70(3H,s,-OCH3),2.56(1H,dd,J=17.2,4.8Hz,H-3b)。以上数据与文献[5]报道的 5-羟基-7,8,2′,6′-四甲氧基二氢黄酮基本一致,故确定化合物1为5-羟基-7,8,2′,6′-四甲氧基二氢黄酮。
2.2 化合物2结构鉴定
化合物2呈无色针晶状(甲醇),HPLC归一化法测得纯度为97.5%(图3)。根据其1H-NMR(DMSO-d6,600MHz)谱(图4),推断δ:12.50(1H,s,5-OH),7.86(1H,dd,J=8.4,2.4Hz,H-6′),7.61(1H,t,J=8.4 Hz,H-4′),7.26(1H,d,J=8.4Hz,H-3′),7.18(1H,t,J=8.4Hz,H-5′),6.76(1H,s,H-3),6.20(1H,s,H-8),3.91(3H,s,7-OCH3)。根据其13C-NMR(DMSO-d6,150MHz)谱(图5),推断δ:181.4(C-4),100.1(C-8),105.0(C-10),109.7(C-3),115.0(C-3′),120.4(C-1′),121.3(C-5′),128.7(C-4′),129.4(C-6′),133.6(C-6),150.2(C-7),156.8(C-2,C-2′),158.1(C-5),56.4(7-OCH3)。以上数据与文献[6]报道的5,6,7-三羟基-2′-甲氧基黄酮基本一致,故确定化合物2为5,6,7-三羟基-2′-甲氧基黄酮。
2.3 化合物3结构鉴定
化合物3为无色油状物,HPLC归一化法测得纯度为98.0%(图6)。根据其1H-NMR(DMSO-d6,600 MHz)谱(图7),推断δ:12.50(1H,s,5-OH),7.86(1H,dd,J=8.4,2.4Hz,H-6′),7.61(1H,t,J=8.4Hz,H-4′),7.26(1H,d,J=8.4Hz,H-3′),7.18(1H,t,J=8.4 Hz,H-5′),6.76(1H,s,H-3),6.20(1H,s,H-8),3.91(3H,s,7-OCH3),3.79(3H,s,2′-OCH3)。根据其13CNMR(DMSO-d6,150MHz)谱(图8),推断δ:181.4(C-4),100.1(C-8),105.0(C-10),109.8(C-3),115.0(C-3′),120.2(C-1′),121.3(C-5′),126.7(C-5′),129.4(C-6′),133.5(C-6),150.1(C-7),156.7(C-2,C-2′),158.1(C-5),56.4(7-OCH3),61.2(2′-OCH3)。 以上数据与文献[7]报道的5,2′-二羟基-6,7-二甲氧基黄酮基本一致,故确定化合物3为5,2′-二羟基-6,7-二甲氧基黄酮。
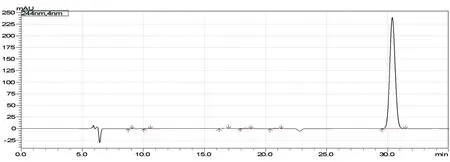
图1化合物1纯度测定液相色谱图
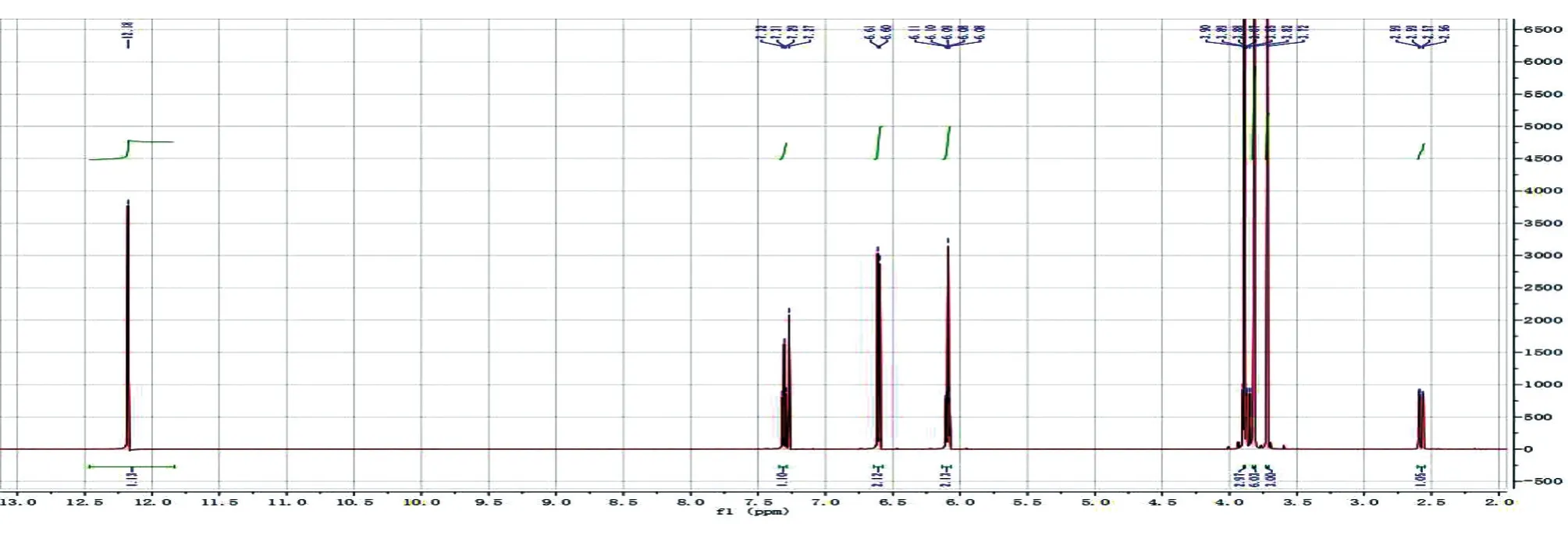
图2化合物1的1H-NMR谱
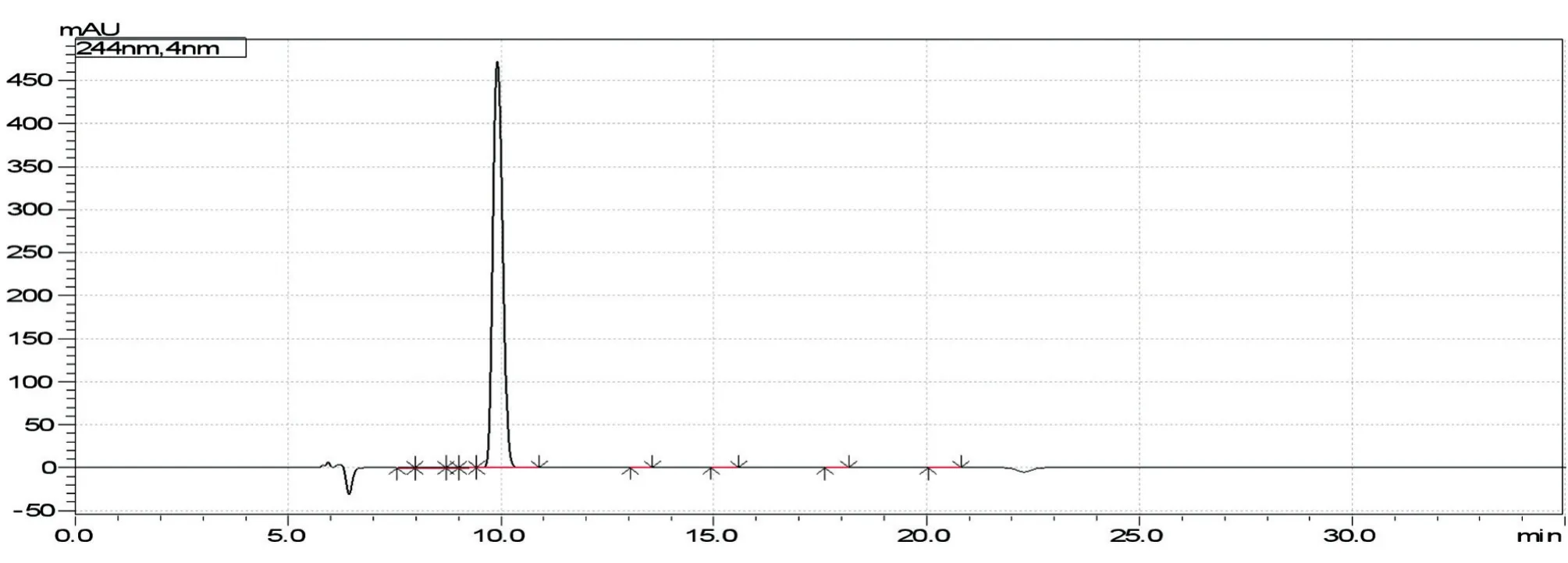
图3 化合物2纯度测定液相色谱图
2.4 化合物4结构鉴定
化合物4为无色油状物,HPLC归一化法测得纯度为 97.1%(图 9)。根据其1H-NMR(600MHz,DMSO-d6)谱(图10),推断δ:13.00(1H,s,5-OH),7.92(2H,t,J=8.4Hz,H-2′,6′),7.52(3H,m,H-3′,4′,5′),6.50(1H,s,H-3),6.24(1H,s,H-8)。以上数据与文献[8]报道的黄芩素基本一致,故确定化合物4为黄芩素。
2.5 化合物5结构鉴定
化合物5呈无色片晶状,HPLC归一化法测得纯度为95.8%(图11)。根据其1H-NMR(DMSO-d6,600 MHz)谱(图12),推断δ:12.50(1H,s,5-OH),8.08(1H,d,J=15.6Hz,H-7),7.61(3H,m,H-3′,4′,5′),6.80(1H,s,H-3),6.29(1H,s,H-8),3.81(3H,s,7-OCH3)。以上数据与文献[9]报道的黄芩素7-甲醚基本一致,故确定化合物5为黄芩素7-甲醚。
图4 化合物2的1H-NMR谱
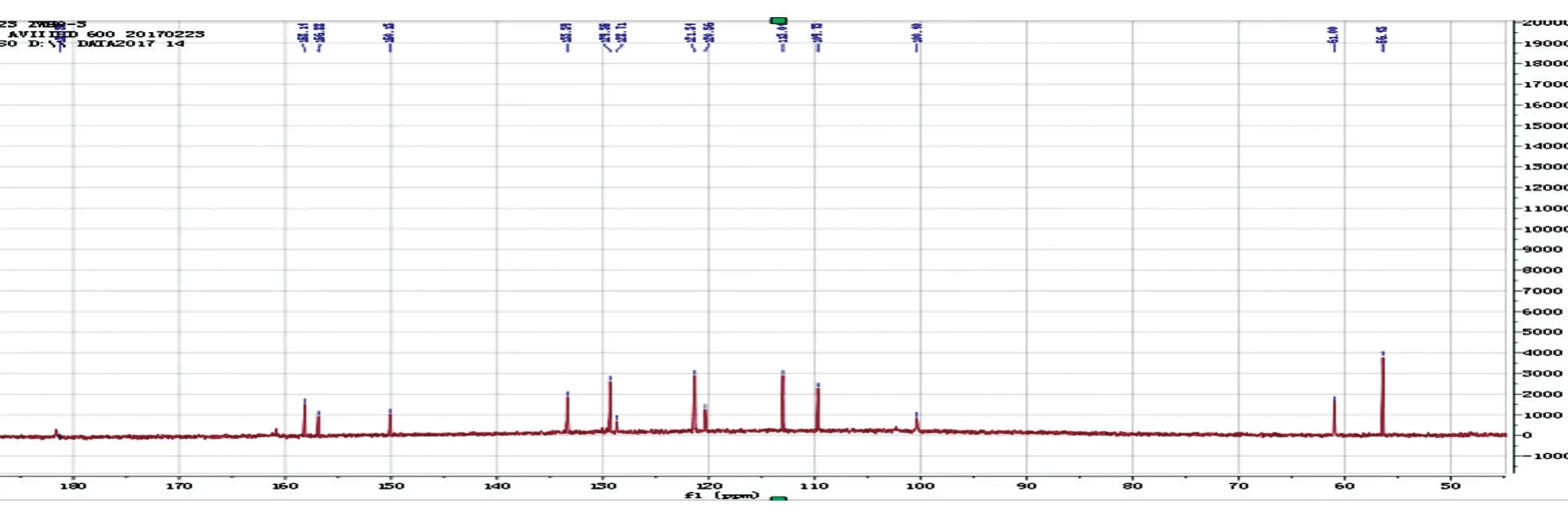
图5 化合物2的13C-NMR谱
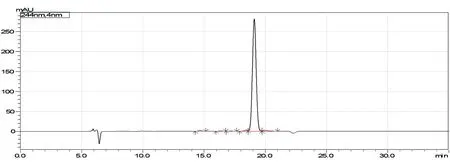
图6 化合物3纯度测定液相色谱图
3 讨论
我们采用多种提取分离技术,并利用波谱学方法对所得结构进行鉴定,首次从海南黄芩中得到5种黄酮类化合物,分别鉴定为5-羟基-7,8,2′,6′-四甲氧基二氢黄酮(为多甲氧基二氢黄酮)、5,6,7-三羟基-2′-甲氧基黄酮、5,6-二羟基-7,2′-二甲氧基黄酮、黄芩素和黄芩素-7甲醚。这些化合物的获得丰富了海南黄芩化学成分组成,为其深入研究与开发提供了科学依据。
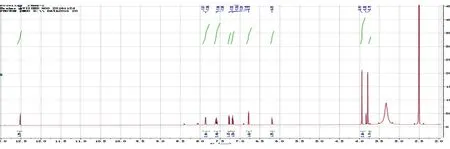
图7 化合物3的1H-NMR谱

图8 化合物3的13C-NMR谱
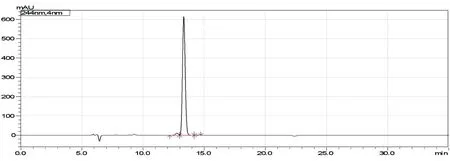
图9 化合物4纯度测定液相色谱图
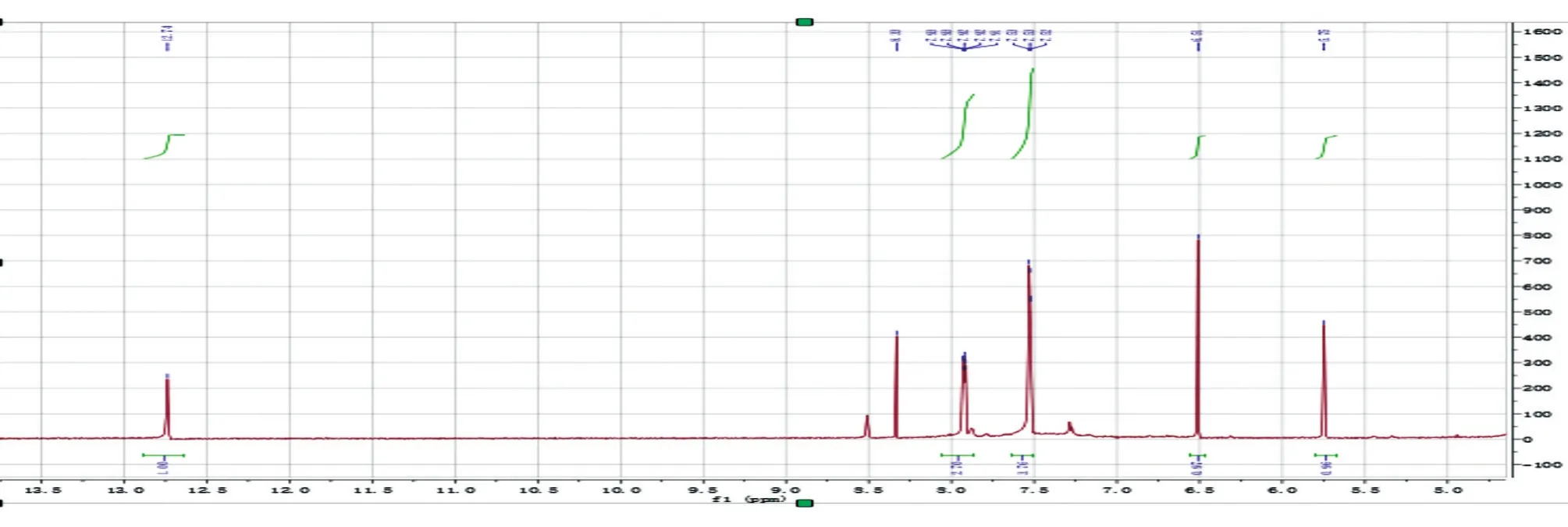
图10 化合物4的1H-NMR谱

图11 化合物5纯度测定液相色谱图

图12 化合物5的1H-NMR谱

