改性锯末对铀的吸附机理研究
宋 勇,吕俊文,张园园,张潮滨,黎炽昊,房 琦
(南华大学环境与安全工程学院,湖南 衡阳 421001 )
核工业铀矿冶经过了50多年的发展,产生了大量的放射性废物,必然会对环境产生严重的影响,造成环境污染。尤其是铀矿的开采与水冶过程中产生的大量铀废石和铀尾矿堆积在地表,极易与水相互作用,产生渗滤液,造成放射性核素的迁移与扩散,威胁着周边居民的健康。据我国核工业30年辐射环境质量评价,铀矿冶系统产生的辐射剂量占总辐射剂量的69%,其中主要是铀矿水冶产生的铀废石和铀尾矿造成的[1-2]。铀废石和铀尾矿对环境的污染主要是其表面氡的析出、含铀粉尘、环境γ辐射以及含放射性核素的渗滤液的排放。对前三种污染可以通过覆盖法得到较好的控制,而渗滤液的排放具有隐蔽性和季节性,很难加以控制[3]。
渗滤液不仅污染土壤、地表水甚至还有污染地下水的可能。对于渗滤液的处理,由尾矿产生的渗滤液,一般的处理方法是在可能有渗滤液流出的地方设置渗滤液收集井,再把渗滤液回用,而由含铀废石产生的渗滤液基本上未对其进行处理。目前,针对含铀废石产生的渗滤液的处理,在渗滤液流经的地方设置可渗透反应墙(PRB)进行拦截处理是一种比较好的方法,该方法已在我国西南某铀矿退役治理中使用[1],很多研究者也认为PRB技术处理含铀废石产生的渗滤液是最具有发展潜力的一种方法[4-5]。PRB技术中吸附材料的选择,是决定该技术处理效果的关键因素,零价铁是目前最常用的渗透反应墙吸附材料,但由于具有成本较高且在环境中不稳定的缺点使其在PRB技术中的应用受到了限制[6]。生物质材料作为渗透反应墙中可供选择的吸附材料之一,具有来源广泛、成本低廉、吸附速度快、吸附量大等特点,曾一度掀起了研究热潮,许多生物质材料如稻草、麦秸和榕树叶[7-8]等都被应用到铀的吸附研究中。
锯末作为常见的生物质材料,其表面含有大量羟基(—OH)、碳氢键(C—H)、碳碳双键(C=C)等基团,吸附的过程中存在离子交换吸附、表面络合吸附等,属于物理和化学的混合吸附类型[9-10]。本文基于锯末的吸附类型对锯末进行改性,通过研究改性锯末对模拟废水中铀(U)的吸附影响因素以及吸附过程中的动力学和热力学行为,分析了改性锯末对铀的吸附机理,探索了改性锯末对铀的最佳吸附条件,以为利用PRB技术处理含铀废水提供新的思路。
1 材料与方法
1. 1 试验材料
试验所用试剂:磷酸、硫酸、尿素、硫酸亚铁铵、三氯化钛、亚硝酸钠、二苯胺磺酸钠、氢氧化钠、碳酸氢钠、碳酸钠、磷酸三钙等。所用试剂均为分析纯。
动力学和热力学试验所用的铀溶液为U3O8配制的标准铀溶液,其余试验所用的铀溶液为我国某矿山铀矿石利用酸法浸出液配制成的模拟含铀废水,其主要成分为U(309.86 mg/L)、Al(203.18 mg/L)、Mn(12.17 mg/L)、Fe( 2.19 mg/L)、Cu(2.06 mg/L)和Zn(4.25 mg/L),pH值为2.83。
1. 2 试验仪器
试验仪器:恒温振荡器(2S-RDD,长沙天恒有限责任公司);电热恒温干燥箱(202-2A,苏州广郡电子科技有限公司);便携式pH测量仪(PHBJ-260,上海精密科学仪器有限公司);电子天平(AL104,长沙百思得电子科技有限公司);台式高速离心机(TG16-W,长沙维尔康湘鹰离心机有限公司)。
1. 3 试验方法
1.3.1 改性锯末的制备
将锯末破碎、洗涤、 烘干,用氯化锌(ZnCl2)溶液作改性剂,称取8 g烘干后的锯末加入质量分数为50%的ZnCl2溶液,搅拌均匀后浸泡24 h;用去离子水将浸泡后的锯末洗涤至中性,抽滤后放入恒温干燥箱中,在45℃下烘干至恒重,干燥后密封保存。采用类似的方法用氢氧化钠(NaOH)、高锰酸钾(KMnO4)、甲醛(CH3OH)、氢氧化钾(KOH)溶液对锯末进行改性。
1.3.2 改性锯末对铀的吸附
量取一定浓度的铀溶液放入一系列250 mL锥形瓶中,分别加入0.5 g 改性好的改性锯末,根据不同的试验目的,选择相应的试验条件,置于200 r/min的恒温振荡器中振荡一定时间,达到吸附平衡后取出5 mL,用离心机在5 000 r/min转速下进行离心分离20 min后,取上清液采用亚钛还原钒酸铵滴定法测定溶液中的铀含量,每组试验重复2次。根据下式计算改性锯末对铀的吸附量(qe) :
qe=(C0-Ce)V/m
(1)
式中:qe为改性锯末的平衡吸附量(mg/g);C0、Ce分别为溶液中铀的初始浓度和吸附平衡后的浓度(mg/L);V为溶液的体积(mL);m为改性锯末的质量(g)。
1. 4 分析方法
溶液中铀含量采用中核天山铀业有限公司的QB/T 73707—2003[11]企业标准中的亚钛还原钒酸铵滴定法测定;溶液中其余重金属元素含量采用7700系列 ICP-MS(Agilent Technologies,Japan)测定。
2 结果与分析
2. 1 不同改性锯末对铀的吸附效果
分别称取0.5 g利用不同改性剂改性后的锯末和0.5 g未改性的锯末放入6个锥形瓶中,在铀溶液体积为50 mL、铀初始浓度为150 mg/L、温度为25℃、接触时间为120 min的条件下进行不同改性锯末对铀的吸附试验,其试验结果见表1。

表1 不同改性锯末对铀的吸附效果Table 1 Effects of different modified materials on the uranium adsorption
由表1可见,未改性的锯末对铀的吸附效果较差,其吸附量仅为1.19 mg/g;氯化锌改性的锯末对铀的吸附效果最好,其吸附量高达8.46 mg/g。分析原因认为:这可能是因为氯化锌能作为电子对的给予体和接受体中心与纤维素复合体的—OH发生作用,导致纤维素分子间的链断裂,使得木纤维素结构发生变化,形成了很多细孔,这种细孔使得改性后锯末的吸附能力大大提高[12]。因此,以下试验均选取氯化锌改性的锯末作为最佳吸附材料,进行改性锯末对铀的吸附机理研究。
2. 2 改性锯末吸附铀的影响因素
2.2.1 溶液pH值对改性锯末吸附铀的影响
在改性锯末的投加量为0.5 g、铀溶液体积为50 mL、铀初始浓度为50 mg/L、温度为25℃、接触时间为120 min的条件下进行试验,探讨了溶液pH值对改性锯末吸附铀的影响,其试验结果见图1。

图1 pH值对改性锯末吸附铀的影响Fig.1 Effects of pH on uranium adsorption by modified sawdust

2.2.2 铀初始浓度对改性锯末吸附铀的影响
在改性锯末的投加量为0.5 g、铀溶液体积为50 mL、溶液pH值为4.5、温度为25℃、接触时间为120 min的条件下进行试验,探讨了铀初始浓度对改性锯末吸附铀的影响,其试验结果见图2。
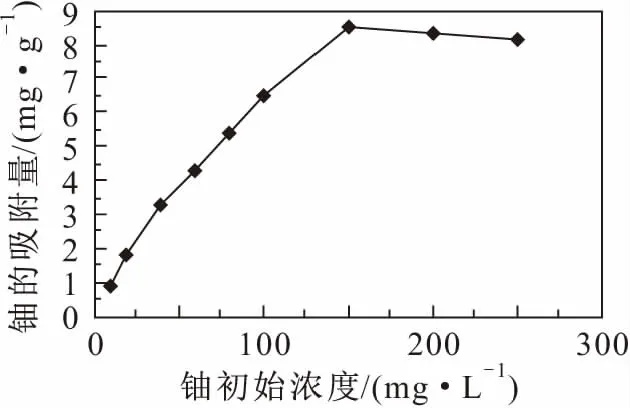
图2 铀初始浓度对改性锯末吸附铀的影响Fig.2 Effects of initial uranium concentration on uranium adsorption by modified sawdust
由图2可见,铀初始浓度小于150 mg/L时,改性锯末对铀的吸附量随铀初始浓度的的升高而增大,对铀的吸附量最大,可达到8.50 mg/g,这是由于铀初始浓度较低时,改性锯末表面的吸附位点相对于溶液中的铀离子是过量的,随着铀初始浓度的增加,溶液中的铀离子可以被大量吸附,改性锯末对铀的吸附量逐渐变大;当铀初始浓度大于150 mg/L时,改性锯末对铀的吸附量逐渐变小。分析原因认为:这可能是由于试验所用的铀溶液为铀浸出液配制成的模拟含铀废水,铀初始浓度越高,废液中Al、Mn、Fe、Cu和Zn等重金属离子的浓度也越高,大量的吸附位点被这些干扰离子占据,导致溶液中铀离子的吸附位点减少,造成改性锯末对铀的吸附量变小。
2.2.3 吸附时间对改性锯末吸附铀的影响
在改性锯末的投加量为0.5 g、铀溶液体积为50 mL、铀初始浓度为120 mg/L、溶液pH值为4.5、温度为25℃的条件下进行试验,探讨了吸附时间对改性锯末吸附铀的影响,其试验结果见图3。

图3 吸附时间对改性锯末吸附铀的影响Fig.3 Effects of contact time on uranium adsorption by modified sawdust
由图3可见,吸附时间对改性锯末吸附铀的效果有较大的影响,达到吸附平衡的时间约为30 min。当吸附时间小于30 min时,改性锯末对铀的吸附量随着吸附时间的增加迅速增大,之后其吸附量基本趋于稳定,达到吸附平衡。分析原因认为:这可能是因为吸附初期,吸附作用主要为溶剂扩散,改性锯末主要以表面孔隙吸附为主,发生瞬间吸附[15-16];随着吸附时间的增加,铀酰离子逐渐占据了改性锯末表面的吸附位点,并与其表面的活性基团相互作用形成络合物,其吸附量也逐渐增加;当吸附时间达到30 min时,溶液中游离态的铀离子与活性吸附位点结合的空间位阻逐渐增大,吸附逐渐达到平衡[17]。
2.2.4 温度对改性锯末吸附铀的影响
在改性锯末的投加量为0.5 g、铀溶液体积为50 mL、铀初始浓度为120 mg/L、溶液pH值为4.5、接触时间为120 min的条件下进行试验,探讨了温度对改性锯末吸附铀的影响,其试验结果见图4。
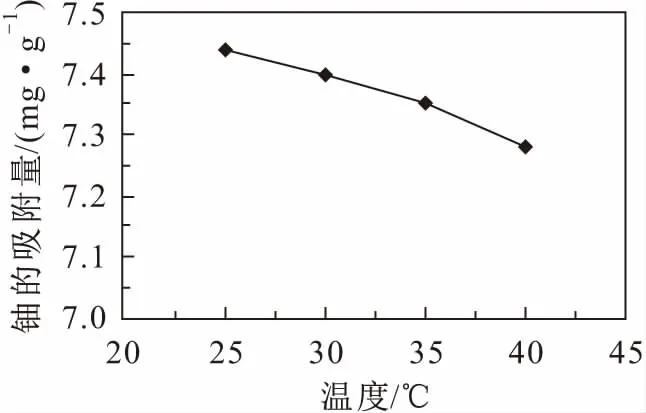
图4 温度对改性锯末吸附铀的影响Fig.4 Effects of temperature on uranium adsorption by modified sawdust
由图4可见,随着温度的升高,改性锯末对铀的吸附量逐渐变小,可见升温不利于改性锯末对铀的吸附。分析原因认为:这可能是由于随着温度的升高,铀在锯末上的脱附作用也随之增强,从而导致改性锯末对铀的吸附量变小。
2. 3 吸附动力学分析
本文采用准一级、准二级和Elovich动力学方程对不同吸附时间下改性锯末对铀的吸附试验数据进行了拟合分析。准一级、准二级动力学方程的表达式[18]如下:
准一级动力学方程:
ln(qe-qt)=lnqe-k1t
(2)
准二级动力学方程:
(3)
式中:qe为平衡吸附量拟合值(mg/g);qt为t时刻的平衡吸附量(mg/g);t为吸附时间(min);k1为准一级吸附速率常数(min-1);k2为准二级吸附速率常数[g/(mg·min)]。
根据公式(2)和(3),分别利用ln(qe-qt)和t/qt对t作图,对改性锯末对铀的吸附试验数据进行了拟合分析,其拟合结果见图5。
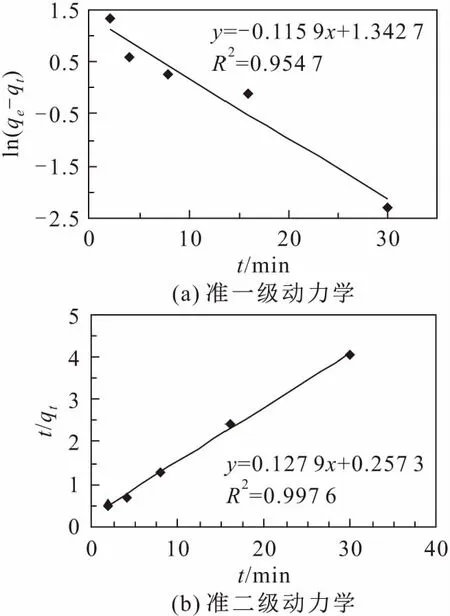
图5 改性锯末吸附铀的准一级、准二级动力学拟合曲线Fig.5 Pseudo-first-order and Pseudo-second-order model of uranium adsorption by modified sawdust
考虑到锯末被氯化锌改性后,纤维素结构被破坏,其对铀的吸附过程可能为复杂的非均相扩散过程,因此本文采用Elovich动力学方程对改性锯末对铀的吸附试验数据进行了拟合分析[19-20],探究改性锯末对铀的吸附机理。Elovich动力学方程的表达式可简化为
qt=(1/βE)ln(αEβE)+(1/βE)lnt
(4)
式中:t为吸附时间(min);qt为t时刻的平衡吸附量(mg/g);αE、βE分别为吸附速率常数和脱附速率常数。
根据公式(4),利用qt对lnt作图,对改性锯末对铀的吸附试验数据进行了拟合分析,其拟合结果见图6。
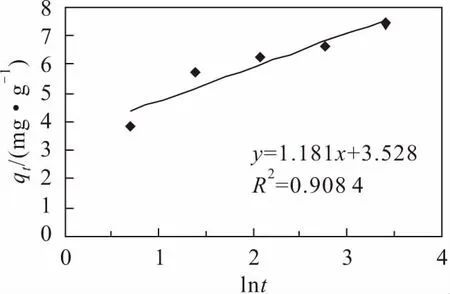
图6 改性锯末吸附铀的Elovich动力学拟合曲线Fig.6 Elovich kinetic curve of uranium adsorption by modified sawdust
由图5和图6可见,在初始铀浓度和温度相同的条件下,准一级、准二级和Elovich动力学方程的拟合相关系数R2分别为0.954 7、0.997 6、0.908 4,准二级动力学方程的拟合相关系数R2大于准一级和Elovich动力学方程的拟合相关系数,说明改性锯末对铀的吸附主要是铀离子与改性锯末表面的官能团反应产生络合物,即发生了化学吸附[21-22]。因此,利用准二级动力学方程能够较好地描述改性锯末对铀的吸附过程。
2. 4 吸附热力学分析
2.4.1 吸附等温线
本文采用Langmuir和Freundlich吸附等温线方程[23-24]对不同铀初始浓度下改性锯末对铀的吸附试验数据进行了拟合分析。吸附等温线方程如下:
Langmuir方程:
(5)
Freundlich方程:
(6)
式中:Ce为吸附平衡时的铀浓度(mg/L);qe为平衡吸附量(mg/g);qmax为相应的最大吸附量(mg/g);kl为Langmuir吸附平衡常数(L/mg);n为与温度、吸附强度有关的无因次常数;kf为Freundlich模型下与吸附容量和吸附强度有关的常数。
根据公式(5)和(6),分别利用Langmuir和Freundlich吸附等温线方程对不同铀初始浓度下改性锯末对铀的吸附试验数据进行了拟合分析,拟合得到的吸附等温线方程的拟合曲线及其相关的拟合参数见图7和表2。
由图7和表2可见,不同温度下Langmuir吸附等温线方程的拟合相关系数R2均大于Freundlich吸附等温线方程的拟合相关系数R2,表明Langmuir吸附等温线方程拟合程度优于Freundlich吸附等温线方程,更适合描述此吸附过程。结合Langmuir吸附等温线方程的假定条件,推测改性锯末对铀的吸附为单层吸附,吸附只发生在锯末表面,且吸附质之间没有相互作用[25]。

图7 改性锯末吸附铀的Langmuir和Freundlich吸附等温线方程拟合曲线Fig.7 Fitting curves of Langmuir and Freundlich isotherm for uranium adsorption by modified sawdust

表2 改性锯末对铀的吸附等温线方程的相关拟合参数Table 2 Langmuir and Freundlich isotherm parameters for uranium adsorption by modified sawdust
2.4.2 吸附热力学参数
吸附热力学参数焓变(△H)和熵变(△S)可通过下面公式计算[26]:
(7)
(8)
式中:Cad为吸附平衡时吸附剂对吸附质的吸附量(mg/g);Ce为吸附平衡时吸附质的浓度(mg/L);kd为表观吸附平衡常数;R为气体常数,取8.314 J/(mol·K);T为热力学温度(K);△H为吸附焓变(kJ/mol)。
根据公式(7)和(8),以lnkd对1/T作图,对改性锯末对铀的吸附试验数据进行了拟合分析,其拟合结果见图8。
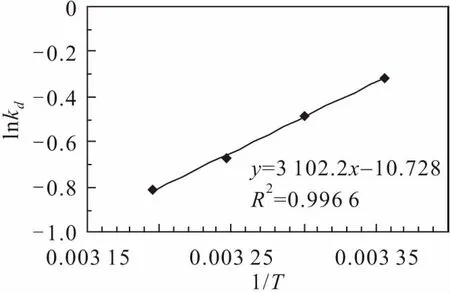
图8 改性锯末吸附铀的lnkd与1/T的关系拟合曲线Fig.8 Fitting curve of the relation between lnkd and 1/T of uranium adsorption by modified sawdust
通过拟合直线的斜率可求出吸附焓变(△H)、吸附熵变(△S),吸附摩尔自由能变△G可由Gibbs自由能方程计算得到,其表达式为[27]
△G=△H-T△S
(9)
式中:△G、△H和△S分别为吸附摩尔自由能变(kJ/mol)、吸附焓变(kJ/mol)和吸附熵变[J/(mol·K)];T为热力学温度(K)。
根据公式(7)、(8)、(9)以及图8的拟合曲线,可计算出热力学参数△H、△G、△S,其计算结果见表3。

表3 改性锯末对铀的吸附热力学参数Table 3 Theromodynamic parameters of the process of uranium adsorption by modified sawdust
由表3可知,吸附焓变△H为负值,说明改性锯末对铀的吸附过程为放热反应;吸附摩尔自由能变△G为负值,说明改性锯末对铀的吸附是自发进行的,且随着温度的升高,△G绝对值降低,说明随着温度的升高,吸附过程自发趋势降低,升温不利于吸附的进行;吸附熵变△S为负值,说明改性锯末对铀的吸附是一个熵减少的过程,达到吸附平衡时吸附质分子的自由度减少。
2. 5 扫描电镜和红外光谱分析
2.5.1 扫描电镜(SEM)分析
本文利用扫描电镜(SEM)观察改性锯末吸附铀前后的表面形貌,改性锯未吸附铀前后的SEM图见图9。

图9 改性锯末吸附铀前后的SEM图Fig.9 SEM of modified sawdust before and after adsorption of uranium
由图9可见,在2 kV电压下,单个团聚清晰可见。改性锯末吸附铀前[见图9(a)、(b)],其表面凹凸不平,含有大量的凸起结构,这些表面凸起大大地增加了改性锯末的表观比表面积,提供了更多的吸附位点,有利于铀酰离子的吸附;改性锯末吸附铀后[见图9(c)、(d)],其表面出现了不规则的团聚体,这些团聚体可能是铀酰离子与改性锯末表面的活性基团作用形成的络合物。
2.5.2 红外光谱(FTIR )分析
本文利用红外光谱(FTIR)分析了改性锯末吸附铀前后分子结构的变化,改性锯末吸附铀前后的FTIR图见图10。
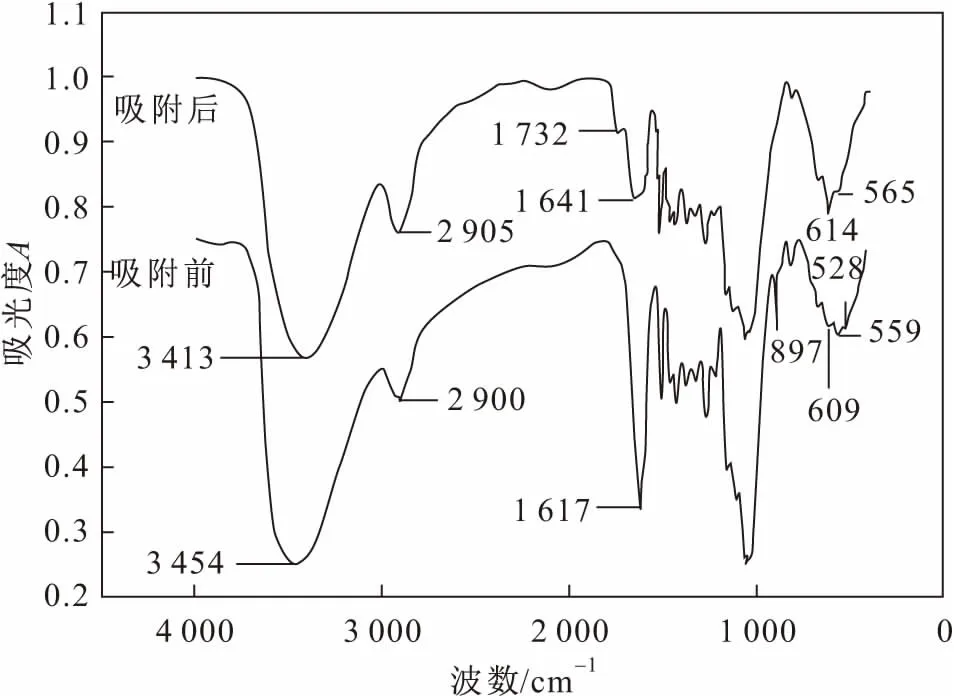
图10 改性锯末吸附铀前后的FTIR图Fig.10 FTIR of modified sawdust before and after adsorption of uranium

综上所述,改性锯末表面参与吸附的基团主要为酰胺基、羟基、酮基和芳烃C—H键等基团,吸附机理中存在表面络合吸附。
3 结 论
(1) 氯化锌改性的锯末对铀的吸附效果最好;溶液pH值对改性锯末吸附铀的效果影响较大,当溶液pH值为4.5时其吸附效果最佳;改性锯末对铀的吸附平衡时间约为30 min。
(2) 动力学分析表明,准二级动力学方程能够较好地描述改性锯末对铀的吸附过程,其相关系数R2为0.997 6,改性锯末对铀的吸附主要是表面络合吸附。
(3) Langmuir吸附等温线方程更适合描述改性锯末对铀的吸附过程,推测改性锯末对铀的吸附为单层吸附,吸附只发生在锯末表面,且吸附质之间没有相互作用。
(4) 热力学分析表明,改性锯末对铀的吸附热力学参数△H=-25.792 kJ/mol、△G=-16.327~-15.851 kJ/mol、△S=-31.760 J/(mol·K)均为负值,说明吸附反应是一个放热自发的过程。
(5) SEM和FTIR分析表明,改性锯末对铀的吸附机理中存在表面络合吸附,参与吸附活动的官能团主要为改性锯末表面的酰胺基、羟基、酮基和芳烃C—H键等基团。
参考文献:
[1] 吕俊文,杨勇,徐乐昌,等.我国西南某铀矿水冶尾矿库的退役治理[J].金属矿山,2007(7):83-86.
[2] 王志章.铀尾矿库的退役环境治理[J].铀矿冶,2003,22(2) :95-99.
[3] 孙占学,刘媛媛,马文洁,等.铀矿区地下水及其生态安全研究进展[J].地学前缘,2014,21(4):158-167.
[4] Bayramoglu G,Celik G,Arica M Y.Studies on accumulation of uranium by fungusLentinussajor-caju[J].JournalofHazardousMaterials,2006,136(2):345-353.
[5] 李乐乐,张卫民.渗透反应墙技术处理铀尾矿库渗漏水的研究现状[J].环境工程,2016,34(1):168-172.
[6] Morrison S J,Metzler D R,Dwyer B P.Removal of As,Mn,Mo,Se,U,V and Zn from groundwater by zero-valent iron in a passive treatment cell:Reaction progress modeling[J].JournalofContaminantHydrology,2002,56 (1/2):99-116.
[7] 冯媛,易发成.稻壳对铀吸附性能的研究[J].原子能科学技术,2011,45(2):161-167.
[8] 夏良树,谭凯旋,王晓,等.铀在榕树叶上的吸附行为及其机理分析[J].原子能科学技术,2010,44(3):278-284.
[9] 王哲,易发成,冯媛.铀在木纤维上的吸附行为及机理分析[J].原子能科学技术,2015,49(2):263-272.
[10]郭秀荣,杜丹丰,马岩.炭化微米木纤维滤芯柴油机排放纳米颗粒吸附特性[J].江苏大学学报,2013,34(1):7-12.
[11]中核天山铀业有限公司企业标准:QB/T 73707—2003[S].
[12]邓先仑.氯化锌法制造活性炭的机理探讨[J].生物质化学工程,1987(1):14-15.
[13]Esposito A,PagnanellI F,Veglio F.pH-related equilibria models for biosorption in single metal systems[J].ChemicalEngineeringScience,2002,57(3):307-313.
[14]Parab H,Joshi S,Shenoy N,et al.Uranium removal from aqueous solution by coir pith:Equilibrium and kinetic studies[J].BioresouceTechnology,2005,96(11):1241-1248.
[15]Khani M H,Keshtk A R ,Ghanndi M,et al.Equilibrium,kinetic and thermodynamic study of the biosorption of uranium onto cystoseria indica algea[J].JournalofHazardousMaterials,2008,150:612-618.
[16]熊骁,王清良,李乾,等.Fe(OH)3胶体对铀的吸附行为[J].原子能科学技术,2016,50(1):39-45.
[17]夏良树,黄欣,曹存存,等.红壤胶体对U(Ⅵ)的吸附性能及机理[J].原子能科学技术,2013,47(10):1692-1699.
[18]Tu Y J,You C F,Chang C K.Kinetics and thermodynamics of adsorption for Cd on green manufactured nano-particles[J].JournalofHazardousMaterials,2012,235/236:116-122.
[19]Samrani A G,Lartiges B S,VilliéRas F.Chemical coagulation of combined sewer overflow:Heavy metal removal and treatment optimization[J].WaterResearch,2008,42(4/5):951-960.
[20]Aroua M K,Leong S P,Teo L Y,et al.Real-time determination of kinetics of adsorption of lead(Ⅱ) onto palm shell-based activated carbon using ion selective electrode[J].BioresourceTechnology,2008,99(13):5786-5792.
[21]Indra D M,Vimal C S,Nitin K A.Removal of orange-G and methyl violet dyes by adsorption onto bagasse fly ash—kinetic study and equilibrium isotherm analyses[J].DyesandPigments,2006,69(3):210-223.
[22]周书葵,曾光明,刘迎九,等.改性羧甲基纤维素对铀吸附机理的试验研究[J].中国环境科学,2011,31(9):1466-1471.
[23]Hameed B H,Din A T M,Ahmad A L.Adsorption of methylene blue onto bamboo-based activated carbon:Kinetics and equilibrium studies[J].JournalofHazardousMaterials,2007,141:819-825.
[24]陈再明,方远,徐义亮,等.水稻秸秆生物炭对重金属Pb2+的吸附作用及影响因素[J].环境科学学报,2012,32(4):769-776.
[25]Demiral H,Demiral I,Tumsek F,et al.Adsorption of chromium(Ⅵ) from aqueous solution by activated carbon derived from olive bagasse and applicability of different adsorption models[J].ChemicalEngineeringJournal,2008,144(2):188-196.
[26]王哲,易发成,冯媛.铀在木纤维上的吸附行为及机理分析[J].原子能科学技术,2015,49(2):263-272.
[27]Mark S,Pinhua R,Irene L.Effects of hardness and alkalinity on the removal of arsenic (V) from humic acid-deficient and humic acid-rich groundwater by zero-valentiron[J].WaterResearch,2009,43(17):4296-4304.
[28]Lin Z Y,Wu J M,Xue R,et al.Spectroscopic characterization of Au3+biosorption by waste biomass ofSaccharomycescerevisiae[J].SpectrochimicaActaPartA:MolecularandBiomolecularSpectroscopy,2005,61(4):761-765.
[29]Das S K,Das A R,Guha A K.A study on adsorption mechanism of mercury onAspergillusversicolorbiomass[J].EnvironmentalScience&Technology,2007,41(24):8281-8287.

