静脉注射环氧合酶-2抑制剂在带状疱疹神经痛患者中的疗效观察
代月娥,文传兵,刘 柳,林 涛,杜 宇(四川省医学科学院·四川省人民医院疼痛科,四川 成都 610072)
带状疱疹神经痛是由水痘带状疱疹病毒(varicella-zostre virus,VZV)感染周围神经导致疼痛的一种神经病理性疼痛综合征。急性带状疱疹感染后持续疼痛时间大于1个月定义为带状疱疹后神经痛(Post-herpetic neuralgia,PHN),是带状疱疹最严重的并发症[1]。老年患者PHN发病率高,是公认的世界级疼痛性疾病。目前研究显示,年龄越大,发病率越高[2]。我国进入老龄化社会,全国60岁以上老年人口已经达到2.3亿,占总人口的16.7%。到2020年,我国人口老龄化水平将达到17.8%。因此,加强急性期带状疱疹神经痛的治疗,降低PHN的发生是目前临床工作的重点[3]。本试验将探讨环氧合酶-2抑制剂帕瑞昔布钠用于急性期带状疱疹神经痛的患者,通过观察试验组和对照组两组患者在不同时点的疼痛评分、疱疹结痂脱落情况和测定不同时点患者血清中炎性反应因子含量,随访观察PHN的发生率,为临床优化治疗方案、降低PHN发生率提供依据。
1 资料与方法
1.1一般资料:本研究经医院伦理委员会批准,所有患者或家属均签署《知情同意书》,选择我院2016年6月~2017年11月疼痛科住院的急性期带状疱疹神经痛患者60例,年龄50~75岁,体重43~80 kg,ASA Ⅰ~Ⅱ级符合带状疱疹神经痛诊断标准纳入本研究。纳入标准:①符合《疼痛诊疗学》中HZ诊断标准[4];②病程小于10 d;③疱疹皮损分布区主要为胸背部、腰腹部等躯干部,均沿相应脊神经走向成簇样分布的红色丘疱疹,伴明显神经痛表现;④疼痛视觉模拟评分(VAS)≥4分;⑤术前检查未见其他神经系统疾病及精神疾病,术前无癫痫发作,偏瘫及失语,无其他系统肿瘤病史,心、肺功能未见明显异常,肝、肾、电解质功能基本正常,血糖、血压控制稳定。病例排除标准:①不符合HZ诊断标准者;②合并其他引起神经痛的潜在疾病,不能明确判断疼痛单纯为带状疱疹引起者;③合并严重的心血管、脑血管、肝、肾、造血系统等原发性疾病或全身衰竭者,恶性肿瘤、精神病患者;④已入组并已完成治疗方案,又接受其他治疗方法的病例或拒绝定期详细评估治疗后情况及随访的患者。
1.2治疗过程:符合本研究纳入标准的HZ住院患者,按照随机数字表法随机分为两组(n=30):试验组(P组)、对照组(C组)。所有患者均经规范化口服药物:按照加巴喷丁用药指南给药,第一晚加巴喷丁给药300 mg,第2天中午、晚上分别口服加巴喷丁300 mg,第3天开始加巴喷丁300 mg,3次/d;3天后根据患者疼痛程度和疼痛频率的变化情况调整加巴喷丁剂量,最大量加至600 mg,3次/d。甲钴胺片500 μg,3次/d;阿米替林12.5 mg,1次/d。P组患者在上诉口服药物基础上给予40 mg帕瑞昔布钠(生产厂家:辉瑞制药有限公司;国药准字J20080045)稀释至5 ml连续静脉注射3 d,对照组给予相等剂量生理盐水5 ml,固定同一名护士进行操作。
1.3观察评价指标:两组患者均在入院当天、静脉滴注帕瑞昔布钠后第1、3、5、8、11天进行疼痛评分、睡眠质量(SIS)评分,观察疱疹结痂日期和脱落时间,同时记录不良反应。疼痛评分采用(visual analogue scale,VAS)作为疼痛程度评价指标。0分为无痛,10分为剧烈疼痛;让患者在描述最剧烈疼痛程度所代表数字上画圈,0代表无痛,1~3代表轻度疼痛(疼痛不影响睡眠),4~6代表中度疼痛(疼痛影响入睡困难),7~10代表重度疼痛(不能入睡或者睡眠中痛醒)。睡眠质量SIS采用类似VAS评分法:0分为不影响睡眠,10分为因疼痛完全无法睡眠。在上诉相同时间点采集患者血清并测量IL-1β、IL-6、TNF-α含量。同时记录所有患者的头晕、头痛、恶心、呕吐、嗜睡、乏力、严重窦性心动过缓(心率<50次/min,需要给予阿托品等药物处理)等不良反应。经治疗疼痛缓解又恢复到治疗前的疼痛程度定为复发,所有患者出院后门诊或电话随访90 d,统计发生PHN的患者例数。以上指标及评分固定一名主治医师进行评定和记录。

2 结果
2.1一般资料比较:在参加此项前瞻性随机对照研究的60例患者中,两组患者在性别比例、年龄、病程、合并症、VAS、SIS评分等方面比较,差异无统计学意义(P>0.05)。见表1。
表1患者的一般资料(n=30)

组别性别(男/女,例)合并症(例)高血压 糖尿病年龄(x±s,岁)病程(x±s,d)体重(x±s,kg)VAS(x±s)SIS(x±s)P组13/17128671±7634±24635±3272±1363±12C组14/16147659±9232±27628±2971±1661±16t值06650732065808210794085208310785P值>005>005>005>005>005>005>005>005
2.2临床疗效比较:两组患者治疗后VAS评分和SIS与治疗前比较降低,差异有统计学意义(P<0.05);与C组比较,P组患者在不同时间点VAS评分、SIS评分下降更为显著,差异有统计学差异(P<0.05),见表2、3。P组患者治疗后各时间点血清中IL-1β、IL-6、TNF-α含量均明显低于C组,差异有统计学意义(P<0.05),见表4。
2.3其他指标和不良反应比较:P组患者在疱疹结痂日期和脱落时间明显早于C组,差异有统计学意义(P<0.05)。 P组随访观察到发生PHN4例,C组随访观察到发生PHN9例, P组患者发生PHN的例数发生率明显低于对照组,差异有统计学意义(P<0.05),见表5。P组观察到头昏8例,恶心、呕吐1例,嗜睡9例。C组观察到头昏10例,恶心、呕吐1例,嗜睡11例,未观察到出血等不良反应,两组不良反应比较,差异无统计学意义(P>0.05)。

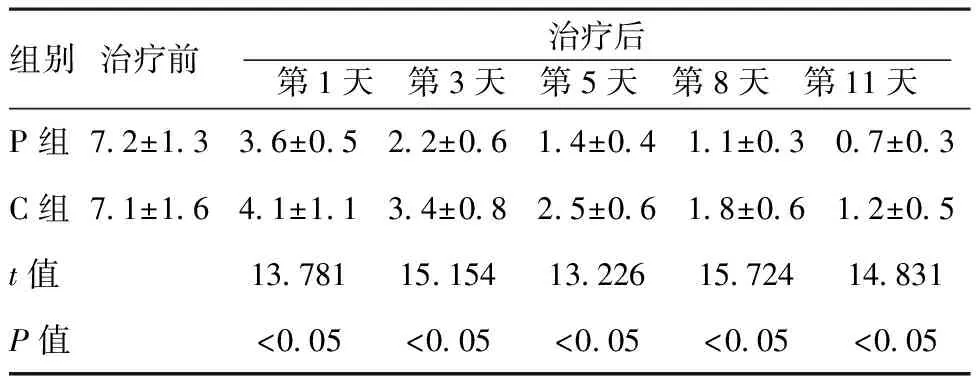
组别治疗前治疗后 第1天 第3天 第5天 第8天 第11天 P组72±1336±0522±0614±0411±0307±03C组71±1641±1134±0825±0618±0612±05t值1378115154132261572414831P值<005<005<005<005<005


组别治疗前治疗后 第1天 第3天 第5天 第8天 第11天 P组63±1236±0522±0614±0411±0307±03C组61±1641±1134±0825±0618±0612±05t值1437215285123611341512572P值<005<005<005<005<005

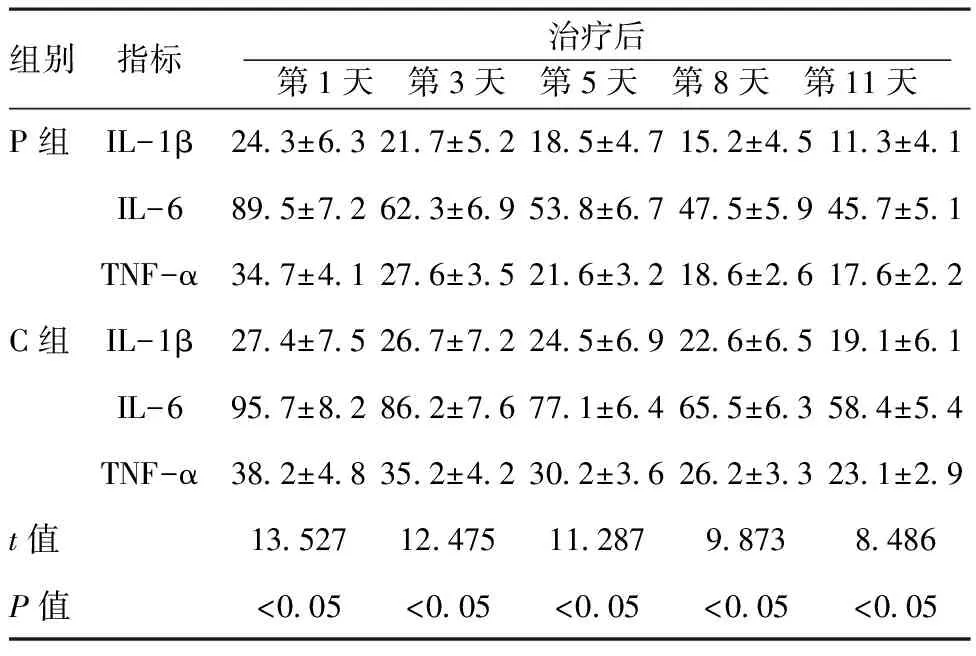
组别指标治疗后 第1天 第3天 第5天 第8天 第11天 P组IL-1β243±63217±52185±47152±45113±41IL-6895±72623±69538±67475±59457±51TNF-α347±41276±35216±32186±26176±22C组IL-1β274±75267±72245±69226±65191±61IL-6957±82862±76771±64655±63584±54TNF-α382±48352±42302±36262±33231±29t值13527124751128798738486P值<005<005<005<005<005
表5两组患者其他指标和不良反应比较
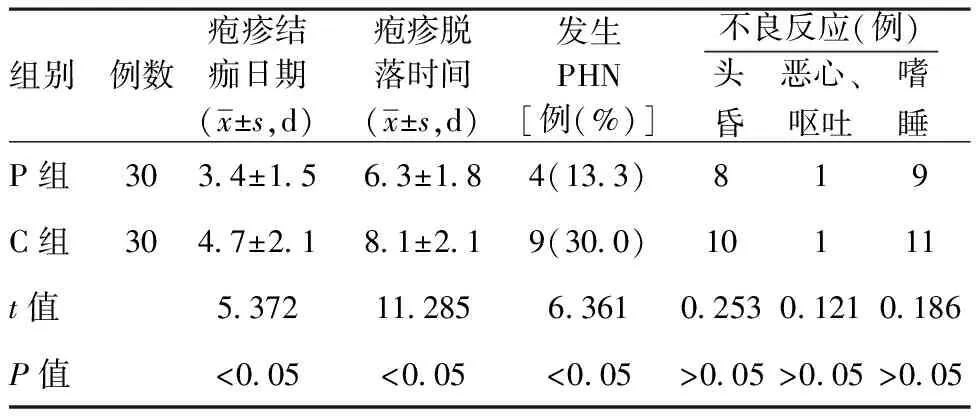
组别例数疱疹结痂日期(x±s,d)疱疹脱落时间(x±s,d)发生PHN[例(%)]不良反应(例)头昏 恶心、呕吐 嗜睡P组3034±1563±184(133)819C组3047±2181±219(300)10111t值5372112856361025301210186P值<005<005<005>005>005>005
3 讨论
带状疱疹后神经痛是皮损愈合后持续性剧烈的、顽固难治的神经病理性疼痛。在带状疱疹急性期尽早进行干预治疗降低PHN的发生是解决问题的根本所在。本试验观察到,在常规口服抗病毒、营养神经的基础上[5],急性期带状疱疹神经痛的患者给予环氧合酶-2抑制剂帕瑞昔布钠40 mg静脉注射,可明显减轻疼痛和改善睡眠质量,降低血清中炎性反应因子的释放,并能降低带状疱疹后神经痛的发生率。
目前,国内外关于带状疱疹所引起的神经痛研究表明,不论是炎性反应性疼痛还是神经病理性疼痛,神经炎性反应是启动和维持慢性疼痛的重要原因[6]。帕瑞昔布钠是一种高选择性的COX-2特异性抑制剂,通过抑制炎性反应因子的释放同时减少前列腺素的生成,提高患者神经疼痛阀值缓解神经疼痛和疼痛过敏[7]。最近几年的一些研究发现帕瑞昔布钠除了具有镇痛作用外,还有一些其他的效应,包括机体神经保护、器官保护以及抗肿瘤作用[8-10]。帕瑞昔布钠可以通过抑制COX-2 的活性以及前列腺素的代谢减少炎性反应因子(IL-1b、IL-6、TNF-α、MIP-2、MIP-1α)的表达。在目前已知的30 多种细胞因子中, IL-1β、IL-6 和TNF-α 则被认为是典型的促炎细胞因子,通过减少这些促炎细胞因子的产生,可以显著减轻中枢神经系统参与调控的一系列疾病的发生[11]。笔者观察到,使用帕瑞昔布钠患者血清中IL-1β、IL-6、TNF-α在使用帕瑞昔布钠后不同时间点其含量均明显低于未使用患者,说明帕瑞昔布钠可明显减轻神经炎性反应;静脉使用帕瑞昔布钠患者疼痛改善优于未使用者,说明帕瑞昔布钠对神经病理性疼痛也有缓解作用,这与既往的研究一致[12]。
疱疹消退时间和脱落时间也是患者愈后的关键因素之一。本研究观察到,带状疱疹发病初期的患者使用帕瑞昔布钠后其疱疹结痂时间和脱落时间明显少于未使用者,说明使用帕瑞昔布钠的患者其炎性反应消退明显加快,神经损伤明显减轻。在随访中发现,使用帕瑞昔布钠的患者发生PHN的发生率也明显低于未使用者。这也说明在发病初期即神经炎症启动初期,使用帕瑞昔布钠早期进行炎性反应干预,神经炎性损伤就会明显减轻,带状疱疹后神经痛的发生率也会明显下降。本试验中帕瑞昔布钠的使用按照该药指南推荐的成人安全剂量和使用周期[13],未观察到有出血、心血管事件等不良反应发生。两组患者头昏、嗜睡、恶心、呕吐等药物不良反应发生率比较,差异无统计学意义(P>0.05)。说明帕瑞昔布钠并不会增加患者的不适与并发症,可安全使用。本试验选择的患者病程均为带状疱疹神经痛的初期,而对病程较长的已发生明显神经炎性损伤的患者并未进行观察和评估。因此,帕瑞昔布钠对已发生神经损伤的这类患者是否仍然有效,需在以后的临床工作中进一步观察。
总之,帕瑞昔布钠是现用于临床的唯一一种注射用高选择性环氧合酶-2抑制剂,在急性期带状疱疹神经痛的患者早期使用,可明显减轻炎性反应,明显缓解患者的疼痛,降低带状疱疹后神经痛的发生。
4 参考文献
[1] Forbes HJ,Thomas SL,Smeeth L,et al.A systematic review and meta-analysis of risk factors for postherpetic neuralgia[J]. Pain,2016,157(1):30.
[2] Johnson RW,Rice AS.Clinical practice.Postherpetic neuralgia[J].N Engl J Med,2014,371(16):1526.
[3] Van Wijck AJ,Wallace M,Mekhail N,et al.Evidence-based interventional pain medicine according to clinical diagnosis.17.Herpes zoster and post-herpetic neuralgia[J].Pain Practice,2011,11(1):88.
[4] 神经病理性疼痛诊疗专家组.神经病理性疼痛诊疗专家共识[J].中国疼痛医学杂志, 2013,19(12):705.
[5] 陈 静.神经阻滞治疗带状疱疹的观察与护理[J].吉林医学,2013,34(14):2816.
[6] 董 东,何小亮,皮肖冰,等.万乃洛韦治疗带状疱疹30例临床疗效评价[J].吉林医学,2017,38(10):1918.
[7] 李秋月,许海玉,杨洪军.促炎因子TNF-α,IL-1β,IL-6在神经病理性疼痛中的研究进展[J].中国中药杂志,2017,42(19):3709.
[8] 曾秋谷,黎达锋,岑相如,等.帕瑞昔布超前镇痛在小儿扁桃体切除术中的应用[J].吉林医学,2017,38(11):2033.
[9] AA Elmawgood,S Rashwan,D Rashwan.Effect of parecoxib on remifentanil induced postoperative shivering [J].Egyptian Journal of Anaesthesia,2014,30(4):399.
[10] 刘少星,谢先丰,曹德钧,等.帕瑞昔布钠预先给药对大鼠局灶脑缺血再灌注血脑屏障通透性的影响[J].昆明医科大学学报,2016,37(8):47.
[11] 王 波,旷 昕,田绍文.帕瑞昔布钠的作用机制及最新进展[J].海南医学,2014,25(23):3496.
[12] H Lenz,J Raeder,T Draegni,et al.Effects of COX inhibition on experimental pain and hyperalgesia during and after remifentanil infusion in humans[J].Pain,2011,152(6):1289.
[13] 崔向丽,赵志刚,陈 丽,等.新型注射用选择性COX-2抑制剂帕瑞昔布钠[J].中国新药杂志,2009,18(14):1283.

