2,4,6-三甲基间苯二腈氧化物的合成及固化性能分析
王晓川,舒远杰,卢先明,刘 宁,莫洪昌,徐明辉
(西安近代化学研究所,陕西 西安 710065)
引 言
腈氧化物(RCNO)是一类-CNO直接与分子上的碳原子相连的能量丰富的有机化合物[1-2],其结构与起爆药雷酸汞Hg(CNO)2类似,也可视为雷酸(HCNO)的衍生物[3]。脂肪族的腈氧化物不稳定,容易二聚形成氧化呋咱[4-7]。因此,小分子的腈氧化物和聚合的腈氧化物都可看作是潜在的含能材料。
添加空间位阻基团有利于腈氧化物的稳定,有空间位阻的芳香族腈氧化物在室温下可以稳定存在[8]。因为腈氧化物可以和不饱和化学键发生1,3-偶极环加成反应生成五元环[9],所以含有两个腈氧基团的稳定的腈氧化物可以作为室温固化剂,交联液体橡胶或其他含有不饱和健的高分子[10]。
由于稳定的腈氧化物不易制备,以前的研究多集中于制备出腈氧化物前驱体,使用时即时生成腈氧化物。如B. S. Huffman等[11]以异氰酸酯和烷基硝酸酯反应制备出的腈氧化物前驱体,需要在加热条件下分解生成腈氧化物,交联聚异戊二烯橡胶。樊亚勤等[12]制备的腈氧化物前驱体,使用时需要加入三乙胺,反应生成的铵盐会残留于体系中,影响固化物的性能。
本研究以均三甲苯为原料,经溴甲基化反应、氧化反应、缩合反应、脱氢氧化反应等合成了含能固化剂2,4,6-三甲基间苯二腈氧化物,并对其结构进行了表征,优化了合成工艺,用DSC法分析了其热性能,并初步评估了其与液体聚丁二烯的固化。
1 实 验
1.1 试剂与仪器
1,3,5-三甲苯,化学纯,成都市科龙化工试剂厂;氢氧化钾、盐酸羟胺、氢氧化钠、次氯酸钠溶液、多聚甲醛,均为分析纯,成都市科龙化工试剂厂;冰乙酸、乙醇、碳酸钠,均为分析纯,西安化学试剂厂;异丙醇、二氯甲烷,均为分析纯,广东光华科技股份有限公司;溴化氢的乙酸溶液(质量分数33%),萨恩化学技术(上海)有限公司;2-硝基丙烷(质量分数96%),上海麦克林生化有限公司;聚丁二烯(Mn≈3000),化学纯,Sigma-Aldrich试剂公司。
NEXUS 870型傅里叶变换红外光谱仪,美国Nicolet公司;AV 500型(500MHz)超导核磁共振仪,瑞士Bruker公司;Vario ELⅢ型自动微量有机元素分析仪,德国Elementar公司。
1.2 目标化合物的合成
1.2.1 合成路线
以均三甲苯为原料,经溴甲基化、氧化、缩合、脱氢氧化4步反应合成2,4,6-三甲基间苯二腈氧化物,具体合成路线如下:

1.2.2 2,4,6-三甲基间二溴甲基苯的合成
向配有磁力搅拌的250mL反应瓶中加入均三甲苯12.0g(100mmol)、多聚甲醛6.0g(200mmol)、50mL醋酸,混合均匀后,再快速加入40mL溴化氢的乙酸溶液(质量分数33%),在 80℃下反应8h,再向反应瓶加入100mL蒸馏水,产品析出,过滤、干燥,得三甲基间二溴甲基苯24.3g, 产率80% 。
IR (KBr) ,ν(cm-1):2976, 1201, 866.1H NMR (500MHz, CDCl3),δ6.89(s, 1H), 4.56(s, 4H), 2.43(s, 3H), 2.37(s, 6H);13C NMR(125MHz, CDCl3),δ138.1, 137.2, 132.6, 130.7, 29.8, 19.5, 14.7。 元素分析(C11H14Br2,%):实测值,C 43.15,H 4.47;计算值,C 43.17, H 4.61。
1.2.3 2,4,6-三甲基间苯二甲醛的合成
在氮气保护下,向配有磁力搅拌的500mL反应瓶中加入300mL异丙醇、氢氧化钾6.9g(123mmol)和2-硝基丙烷10.92g(123mmol),搅拌数分钟后,再加入三甲基间二溴甲基苯15.6g(51mmol),搅拌至反应完成(TLC检测),除去反应体系中的溶剂,加入100mL蒸馏水,产品析出,过滤、干燥,得三甲基间二苯甲醛7.9g, 产率90%。
IR (KBr),ν(cm-1):2961, 1697, 870.1H NMR(500MHz, CDCl3),δ10.62(s, 2H),7.00(s, 1H), 2.79(s, 3H), 2.57(s, 6H);13C NMR(125MHz, CDCl3),δ193.4, 145.0, 142.9, 133.2,132.6, 20.9, 15.3。 元素分析(C11H12O2,%):实测值,C 75.25,H 6.89; 计算值,C 74.98,H 6.86。
1.2.4 2,4,6-三甲基间苯二甲醛肟的合成
向配有磁力搅拌的250mL反应瓶中加入3g(17mmol)三甲基间二苯甲醛和69mL乙醇,加热至50℃,然后向反应瓶中先加入盐酸羟胺4.76g(68mmol),搅拌变澄清后,再加入氢氧化钠2.8g(70mmol),升温至回流,搅拌反应4h后,除去溶剂,再加入20mL水,过滤、干燥,得三甲基间二苯甲醛肟2.86g,产率80%。
IR (KBr) ,ν(cm-1):3317, 2961, 1626, 886.1H NMR(500MHz, CD3OD),δ8.29(s, 2H), 6.93(s, 1H), 4.84(s, 2H), 2.28(s, 6H), 2.21(s, 3H);13C NMR(125MHz, CD3OD),δ148.5, 137.4, 136.0, 129.9, 128.9, 19.5, 16.6。元素分析(C11H14N2O2,%):实测值,C 64.10,H 6.83,N 12.95;计算值,C 64.06,H 6.84,N 13.58。
1.2.5 2,4,6-三甲基间苯二腈氧化物的合成
将制备好的三甲基间苯二甲醛肟700mg(3.4mmol)溶于20mL二氯甲烷中,冰水浴冷却至0℃,缓慢滴加次氯酸钠溶液(质量分数10%)28g(43mmol),滴加约30min,滴加完成后在0℃下搅拌反应30min,升温至25℃继续反应1h,反应结束后,分离出有机层,用二氯甲烷萃取水相,合并所有有机相,蒸去溶剂得到三甲基间苯二腈氧化物500mg,产率73%。
IR (KBr) ,ν(cm-1): 2985, 2296, 1324, 892.1H NMR(500MHz, CDCl3),δ7.06(s, 1H), 2.60(s, 3H), 2.46(s, 6H);13C NMR(125MHz, CDCl3),δ145.0, 144.3, 129.6, 113.5, 21.2, 20.3。元素分析(C11H10N2O2,%):实测值,C 63.32,H 5.04,N 12.06;计算值,C 65.34,H 4.98,N 13.85。
2 结果与讨论
2.1 合成反应机理分析
2.1.1 溴甲基化的反应历程
在酸性条件下,氢离子与甲醛发生亲电加成反应生成羟甲基碳正离子,羟甲基碳正离子再与均三甲苯发生亲电取代反应生成苄醇类中间体,最后HBr再与中间体作用生成2,4,6-三甲基间二溴甲基苯(该溴甲基化反应,通过简单的调整反应温度,可以精确控制引入溴甲基的数目)。反应历程如下:

2.1.2 伯溴代烃被2-硝基丙烷氧化的反应历程

2.2 2,4,6-三甲基间苯二腈氧化物合成反应条件
2.2.1 反应时间的影响
在合成2,4,6-三甲基间苯二甲醛的过程中,考察了在三甲基间二溴甲基苯为51mmol,氢氧化钾为123mmol,2-硝基丙烷为123mmol,反应温度为室温(25℃)时,反应时间对产率的影响,结果见表1。

表1 反应时间对醛产率的影响Table 1 Effect of reaction time on the yield of aldehyde
由表1可知,从反应时间为1d起,随着反应时间的延长,产率增加,当反应时间为3d时,产率达最大,为90%,然后随着反应时间的增加,产率缓慢下降。时间过长,副反应增加,从而使产率降低。因此,最佳反应时间为3d。
2.2.2 碱种类的影响
在合成2,4,6-三甲基间苯二甲醛肟的过程中,考察了在三甲基间苯三醛为17mmol,盐酸羟胺为68mmol,碱用量为70mmol,反应温度为乙醇回流时,不同碱种类对产率的影响。
以NaCO3、NaOH和KOH为催化剂时,产率分别为50%、80%和80%,NaOH和KOH为催化剂时,产率最高,说明NaCO3碱性太弱,不利于反应完全。因此,考虑到价格因素,选择NaOH作为催化剂。
2.2.3 NaClO摩尔量的影响
在合成2,4,6-三甲基间苯二腈氧化物的过程中,考察了在三甲基间苯三醛肟为3.4mmol,二氯甲烷为20mL,反应温度为室温(25℃)时,不同NaClO摩尔量对产率的影响,结果见表2。
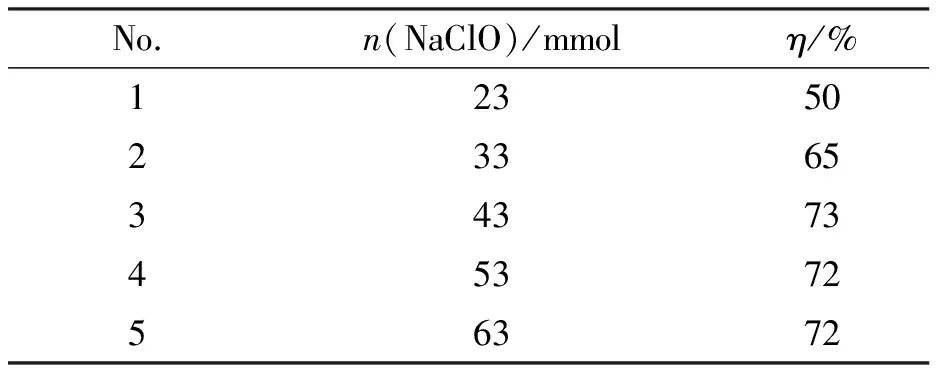
表2 NaClO摩尔量对腈氧化物产率的影响Table 2 Effect of molar amount of NaClO on the yield of nitrile oxide
由表2可知,随着NaClO摩尔量的增加,产率不断增加,但当摩尔量超过43mmol后,产率不再增加。因此,从经济效率考虑,43mmol为反应所需NaClO的最佳摩尔量。
2.3 2,4,6-三甲基间苯二腈氧化物的热分析
用DSC法对2,4,6-三甲基间苯二腈氧化物的热分解性能进行了研究,初始加热温度为26℃,加热速率为10℃/min,DSC曲线见图1。

图1 2,4,6-三甲基间苯二腈氧化物的DSC曲线Fig.1 DSC curve of 2,4,6-Trimethylisophthtalodinitrile oxide
从图1可以看出,2,4,6-三甲基间苯二腈氧化物相对比较稳定,100℃才开时分解,经过133.4℃的强放热峰,到160℃该放热峰分解完全,在296℃第二个峰达到最大值。第一个放热峰为腈氧基团的放热峰,放热比较集中,第二个放热峰为苯环的放热峰,破坏苯环需要较高的温度。
2.4 2,4,6-三甲基间苯二腈氧化物的固化能力评估
使用液体聚丁二烯初步评估2,4,6-三甲基间苯二腈氧化物的室温固化能力。将1.44g 2,4,6-三甲基间苯二腈氧化物、12g液体聚丁二烯和10mL二氯甲烷混合均匀,真空脱气后,在25℃下固化3d,得到的弹性体如图2所示。不同固化体系的固化温度见表3。

图2 2,4,6-三甲基间苯二腈氧化物固化的弹性体Fig.2 Elastomer of 2,4,6-trimethylisophthtalodinitrile oxide

表3 不同固化体系的固化温度Table 3 Curing temperature of different curing systerms
注:t为固化体系的固化温度。
从表3可以看出,以甲苯二异氰酸酯(TDI)与端羟基聚丁二烯(HTPB)组成的异氰酸酯固化剂体系,固化温度为60℃;以丁二酸二丙炔醇酯(BPS)与叠氮聚醚(GAP)组成的聚三唑固化体系,固化温度为65℃;而以2,4,6-三甲基间苯二腈氧化物(TINO)与液体聚丁二烯(PB)组成的聚异噁唑啉固化体系,固化温度仅为25℃。
3 结 论
(1)以均三甲苯为原料,经溴甲基化反应、氧化反应、缩合反应、脱氢氧化反应等成功合成了含能固化剂2,4,6-三甲基间苯二腈氧化物,总收率42.0%。
(2)2,4,6-三甲基间苯二腈氧化物的合成工艺中各步反应的最佳工艺条件为:氧化反应的反应时间为3d、缩合反应的催化剂为NaOH、脱氢氧化反应NaClO摩尔量为43mmol,产率最高,为73%。
(3)对2,4,6-三甲基间苯二腈氧化物固化液体聚丁二烯橡胶形成弹性体的研究结果表明,25℃下固化3d,即可实现液体聚丁二烯橡胶的固化。
参考文献:
[1] 王晓川,舒远杰,卢先明,等. 1,3-偶极环加成反应在固化含能黏合剂中的应用[J]. 化学推进剂与高分子材料,2017, 15(4): 32-37.
WANG Xiao-chuan, SHU Yuan-jie, LU Xian-ming, et al. Application of 1,3-dipolar cycloaddiyion reaction in curing energetic binders[J]. Chemical Propellants and Polymeric Materials, 2017, 15(4): 32-37.
[2] Kumar K A, Govindaraju M, Jayaroopa P, et al. Nitrile oxides: a key intermediate in organic synthesis [J]. International Journal of Pharmaceutical Chemical and Biological Sciences, 2012, 3(1): 91-101.
[3] Beck W, Evers J, Göbel M, et al. The crystal and molecular structure of mercury fulminate (knallquecksilber) [J]. Zeitschrift Für Anorganische Und Allgemeine Chemie, 2007, 633 (9) :1417-1422.
[4] 李亚南, 舒远杰, 张志忠. 氧化氰二聚成环:对称氧化呋咱衍生物制备的重要途径[J]. 含能材料, 2009, 17(6): 740-744.
LI Ya-nan, SHU Yuan-jie, ZHANG Zhi-zhong. Dimerization reaction of cyanide oxide: important route for synthesis of furoxan derivatives[J]. Chinese Journal of Energetic Materials, 2009, 17(6): 740-744.
[5] Grundmann C, Dean J M.Nitrile oxides.V.stable aromatic nitrile oxides[J]. Journal of Organic Chemistry, 1965, 30 (8) :2809-2812.
[6] 吴敏杰,李祥志,毕福强,等. 4,5-二氧代氰基咪唑盐酸盐的合成与表征[J]. 火炸药学报, 2017, 40(3): 41-46.
WU Min-jie, LI Xiang-zhi, BI Fu-qiang, et al. Synthesis and characterization of 1H-imidazolium-4,5- dinitrile dioxides hydrochloride[J]. Chinese Journal of Explosives & Propellants (Huozhayao Xuebao), 2017, 40(3): 41-46.
[7] 薛云娜,杨建明,李春迎,等. 3,4-二苯基氧化呋咱的高效合成[J]. 火炸药学报, 2010, 33(1): 34-37.
XUE Yun-na, YANG Jian-ming, LI Chun-ying, et al. Synthesis of 3,4-diphenylfuroxan with high efficiency[J]. Chinese Journal of Explosives & Propellants(Huozhayao Xuebao), 2010, 33(1): 34-37.
[8] Singh I, Zarafshani Z, Lutz J-F, et al. Metal-free “click”chemistry: efficient polymer modification via 1,3-dipolar cycloaddition of nitrile oxides and alkynes[J]. Macromolecules, 2009, 42(15): 5411-5413.
[9] Grundmann C, Dean J. Stable aromatic nitrile oxides[J]. Angewandte Chemie International Edition, 1964, 3 (8): 585-586.
[10] Tsyganov D V, Yakubov A P, Belenkii L I, et al. Synthesis and properties of stable aromatic bis(nitrile oxides) [J]. Russian Chemical Bulletin, 1991, 40(6): 1238-1243.
[11] Huffman B S, Schultz R A, Schlom P J. Novel reagents for heat -activated polymer crosslinking[J]. Polymer Bulletin, 2001, 47: 159-160.
[12] 樊亚勤,向尧,雷永林,等. 对苯二腈氧化物的合成及其室温固化性能[J]. 精细化工,2017, 34(9): 1063-1069.
FAN Ya-qin, XIANG Yao, LEI Yong-lin, et al. Synthesis of terephthalonnitrile oxide and its curing properties at room temperature[J]. Fine Chemicals, 2017, 34(9): 1063-1069.
[13] 吴兴宇,崔庆忠,徐军. HTPB/TDI粘结体系的固化反应动力学[J]. 含能材料, 2016, 24(11): 1097-1101.
WU Xing-yu, CUI Qing-jun, XU Jun. Curing reaction kinetics of HTPB/TDI bonding system[J]. Chinese Journal of Energetic Materials, 2016, 24(11): 1097-1101.
[14] Thomas K, Werner K, Siegfried E, et al. Isocyanate-free curing of glycidyl azide polymer (GAP) with bis-propargyl-succinate(Ⅱ)[J]. Propellants, Explosives, Pyrotechnics, 2009, 34:210-217.

