人工颈椎间盘假体体外功能试验方法及评价策略
张家振 翟豹 闵玥 刘斌
人工颈椎间盘置换术恢复了颈椎的高度和生理曲度,保留了相邻椎体节段的运动功能,减少了相邻节段的应力水平,有利于防止术后邻近节段发生退变。人工颈椎间盘假体设计理念的关键,在于切除椎间盘后假体能够合理分布椎体各部位所承受的载荷,尽可能地模仿人体正常椎间盘的生物力学及运动功能[1]。根据假体的结构外形,可将假体分为球窝假体(Ball and socket)、硬终板-硬髓核假体(Hard plates/hard core)、硬终板-软髓核假体(Hard plates/soft core)等类型。 许多研究报道了人工颈椎间盘置换术的相关并发症。Sekhon等[2]报道了人工颈椎间盘置换术后出现吞咽困难、假体半脱位等情况。Archibeck等[3]研究了关节面磨损产生的磨屑与假体周围骨质溶解的相关性。另有研究报道了金属骨科植入物与过敏反应(如皮炎、荨麻疹、血管炎),以及可能的无菌性松动和骨质溶解之间的潜在关联[4-5]。
人工颈椎间盘假体的相关风险,包括组件的早期或晚期松动、组件拆卸分离、髓核脱位或半脱位、终板的弯曲破坏、假体的移位或错位、假体尺寸不匹配、上下终板的沉陷、髓核(高分子材料)的蠕变、磨屑引起的组织反应等。椎体之间的正常运动发生在“瞬时旋转中心”附近,旋转中心的位置是变化的,但是通常位于下椎体上部的后半部分。椎体间运动不是纯粹的旋转,同时还伴有一定程度的水平移动。因此,有些人工颈椎间盘假体在保证旋转运动的同时,也允许其进行水平运动。此外,假体的初始稳定性取决于假体与椎体的固方式,假体与椎体的界面具有足够的结合强度,促进骨长入以保证传递相邻节段的作用力,初始稳定性和长期稳定性可以避免假体发生半脱位、脱位、沉陷、移位等风险,应当在产品设计过程中充分考虑、验证和确认这些因素[6]。
目前,国内应用的人工颈椎间盘假体主要是进口产品,国产同类产品大多处于研发生产过程中。通过介绍人工颈椎间盘假体的沉陷、蠕变、推出、半脱位试验,以及动静态压缩、剪切试验、磨损试验等体外功能评价方法,可评价产品临床使用的安全性和有效性。本文分析比较了5种不同设计的人工颈椎间盘假体体外功能性试验的FDA公开数据,探讨人工椎间盘假体体外评价试验的可接受依据,为国产同类产品的研发提供参考(表1)。
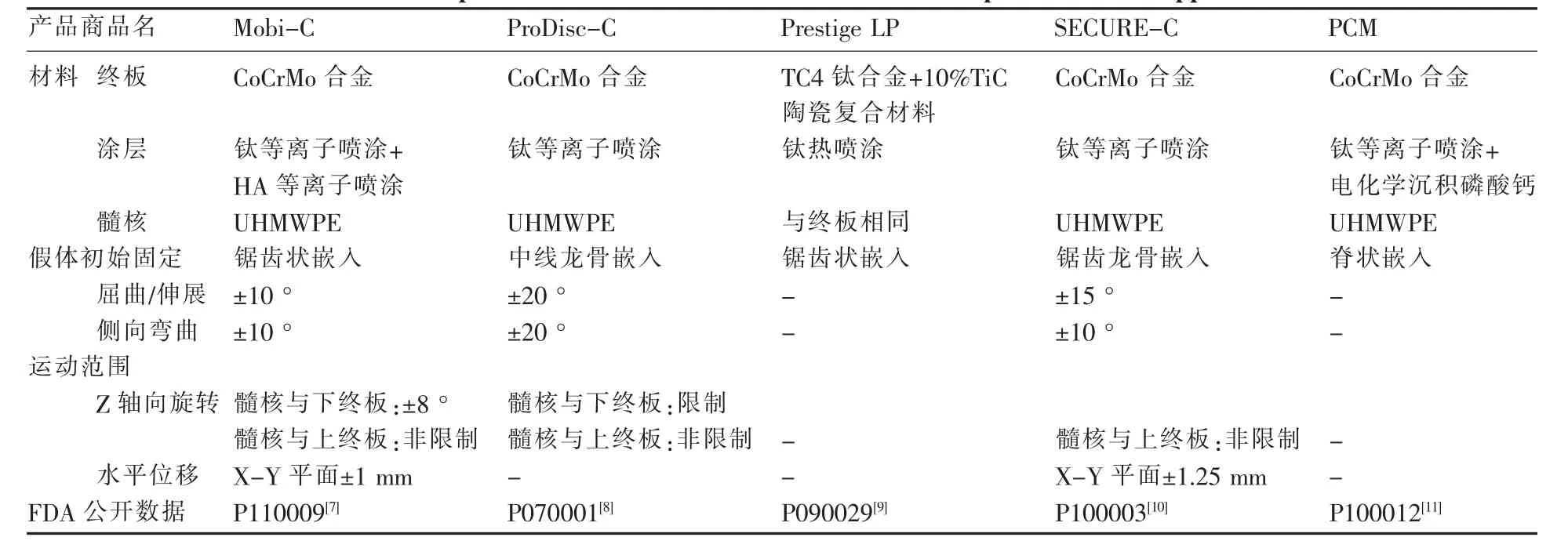
表1 FDA批准上市的5种人工颈椎间盘假体产品信息Table 1 Five product informations of artificial cervical disc prosthesis FDA approved
1 静、动态压缩和剪切测试
静态和动态压缩和剪切试验按照ASTM F2346[12]进行,旨在评价不同材料和结构设计的人工颈椎间盘假体承受载荷的能力,对不同设计的颈椎间盘假体的静态和动态力学性能进行量化对比(图1)。静态轴向压缩和剪切试验是将人工颈椎间盘样品放在不锈钢试验块上通过位移控制加载(加载速率不大于25 mm/min),记录相应的载荷和位移曲线。动态试验通过载荷控制的方式对椎间盘假体施加动态轴向和剪切载荷F,载荷比R=10,直至样品发生结构性功能失效,或达到1千万次载荷循环未发生功能失效。对于任何机械损伤(如表面磨损、裂纹萌生、裂纹扩展等)都应该在1千万次循环结束时记录下来。

图1 人工颈椎间盘假体的静动态压缩和剪切测试示意图Fig.1 Static and dynamic compression and shear test of artificial cervical disc prosthesis
基于FDA的公开数据,已上市的5种人工颈椎间盘假体的动态压缩和剪切试验的1千万次疲劳试验最低载荷分别为150 N和106 N。人体颈椎间盘生物力学研究表明,人体颈椎间盘所能承受的最大轴向载荷和剪切载荷分别为74 N和20 N[13-14]。Anderson等[15]的研究表明,颈椎节段在日常活动中承受的压缩载荷为70~150 N,这意味着在典型日常运动中,颈椎经受的最大压缩载荷为150 N。与颈椎生物力学数据对比,5种假体在150 N压缩载荷下可以经受的1千万次轴向压缩疲劳试验,体外动态剪切疲劳施加载荷(106 N)远高于人体颈椎所受剪切力。
阿里低下头,仿佛是想了一想,说:“哦。”然后怏怏地跟着罗爹爹朝外走。走了几步,又回过头望望,自语道:“姆妈还在睡。”
当人处于直立位时,人体椎间盘所承载的力远大于椎间盘上方身体部位的重量,还承载躯干受到的压缩载荷和扭矩。在屈曲/伸展和侧向弯曲的生理运动时,椎间盘的某些部分会产生拉应力。躯干相对于骨盆的轴向旋转时会承受扭矩,导致椎间盘承受剪切力。此外,在涉及动态负载(如跳跃和创伤)的活动中,椎间盘上的实际负载要高得多,可能高达静态位置负载的两倍。通过静态和动态压缩和剪切试验可知,5种假体的力学性能超过日常活动下颈椎负载,有些产品结构设计具有两倍以上的安全系数(表2)。
2 蠕变测试
根据人工颈椎间盘负载的持续时间,可将假体受力分为短期高载荷(如挺举)和长期低载荷(日常活动)。对于高分子材料制造的人工颈椎间盘假体髓核,由于高分子材料具有黏弹性,椎间盘高度的保持与假体所承受的载荷持续时间有关。随着施加载荷持续时间的延长,高分子材料会发生蠕变和应力松弛,导致人工颈椎间盘高度的丢失,也可能造成上下终板边缘的撞击。因此,需要评价人工颈椎间盘假体材料和结构设计的抗蠕变性能。
人工颈椎间盘假体的蠕变测试旨在评价极端荷载下假体耐受长期变形的能力。选择最差情况解剖剪切角和弯曲角,将假体组件置于固定装置里,在37℃下模拟体液中,按不同载荷水平施加动态轴向压缩蠕变荷载,施加不同动态荷载时,在施加一个荷载之后,立即施加一个较低的静态缓解荷载。评价在每个蠕变载荷结束时的最大位移和缓解期结束时的残余变形。3种已上市假体蠕变测试结果显示,在远高于人体颈椎椎间盘承载持续超过24 h条件下,假体表现出良好的抗蠕变变形能力(表3)。
3 推出试验
人工颈椎间盘假体推出试验用于测试超高分子量聚乙烯髓核与下终板锁扣固定的强度,或上下终板在聚氨酯泡沫模拟骨上的固定强度和初始稳定性,从而评估在植入人工颈椎间盘假体后,髓核或假体在剪切力作用下从椎间盘脱出的风险。
人工颈椎间盘假体髓核推出试验,是根据锁扣设计,将超高分子量聚乙烯髓核安装在下终板上,终板固定在试验装置上,由于髓核最可能从前方脱出,对髓核施加恒定速度的颈椎前向剪切力,直至髓核被推出或破坏。假体推出试验是将假体放置在聚氨酯泡沫模拟骨上,施加恒定轴向载荷,同时施加恒定速度侧向剪切力,直至假体移动超过设定位移或初始固定失效。5种不同产品结构设计的假体和髓核推出力测试结果显示,假体的推出力最低为(127.4±3.2)N,髓核的推出力最低为(351.8±10.2)N。推出力越大,说明假体初始稳定性越好,髓核固定越牢固。通过与人体颈椎间盘所承受的剪切力20 N相比,上述5种假体设计均可以获得较好的初始稳定性(表 4、5)。
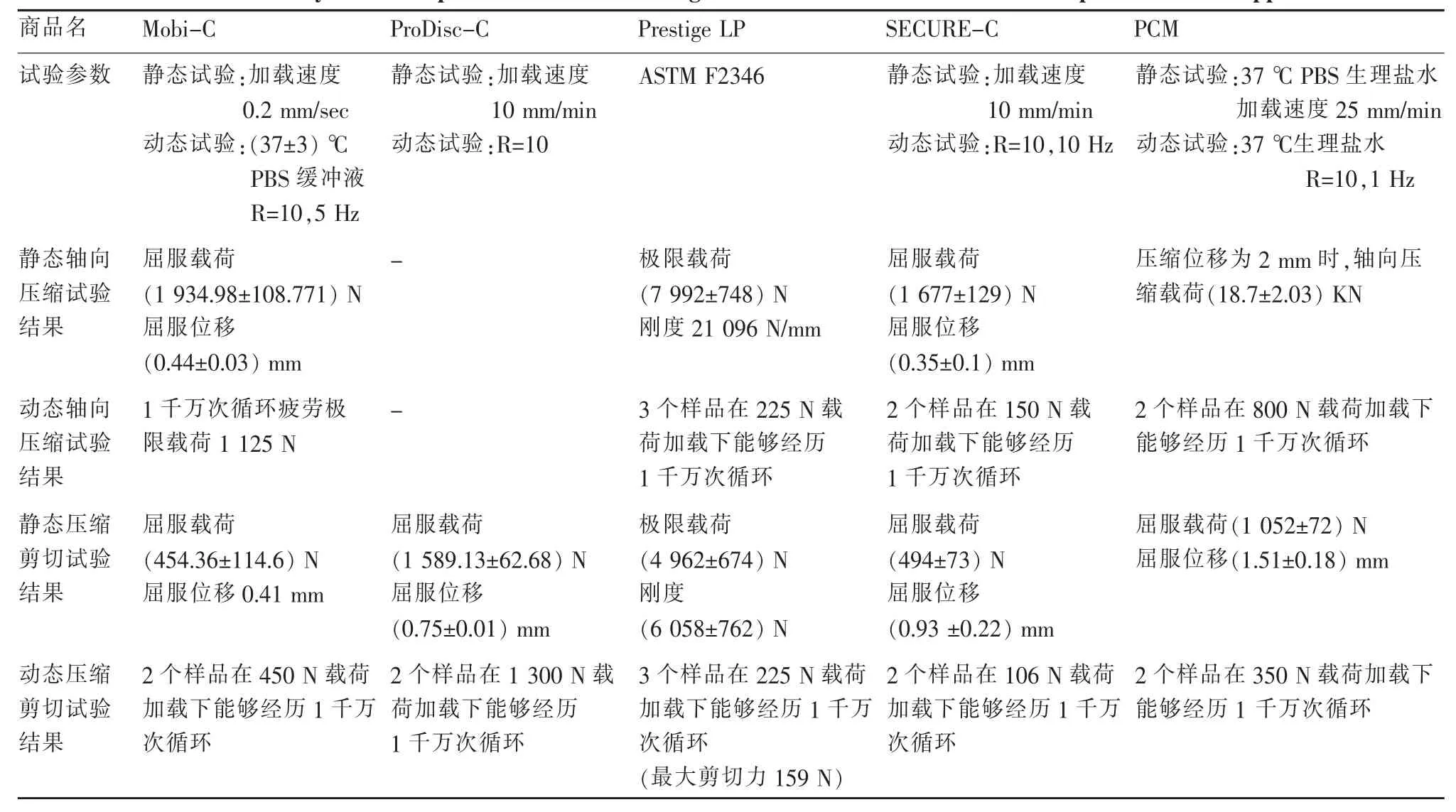
表2 FDA批准上市的5种人工颈椎间盘假体的静态和动态压缩和剪切试验结果[7-11]Table 2 Static and dynamic compression and shear testing results of five artificial cervical disc prosthesis FDA approved[7-11]

表3 FDA批准上市的3种人工颈椎间盘假体的蠕变试验结果[7-11]Table 3 Creep testing results of three artificial cervical disc prosthesis FDA approved[7-11]

表4 FDA批准上市的5种人工颈椎间盘假体推出试验结果[7-11]Table 4 Static expulsion testing(full device)results of five artificial cervical disc prosthesis FDA approved[7-11]

表5 FDA批准上市的4种人工颈椎间盘假体髓核推出试验结果[7-11]Table 5 Static expulsion testing(insert only)results of four artificial cervical disc prosthesis FDA approved[7-11]
4 沉陷试验
上下终板的沉陷是人工颈椎间盘假体一种潜在的临床失效模式。人工颈椎间盘假体沉陷试验的目的,是通过施加恒定速度轴向载荷,在标准化的聚氨酯泡沫模拟骨上将不同设计的椎间融合器的沉陷特性进行量化,可用于对比不同假体设计所导致的沉陷特性的差异(图2)。比较相同沉陷位移对应的轴向载荷或相同轴向载荷对应的沉陷位移,沉陷量一定时轴向载荷越大,或者轴向载荷一定时沉陷量越小,说明所设计的假体发生沉陷失效的风险越低(表6)。
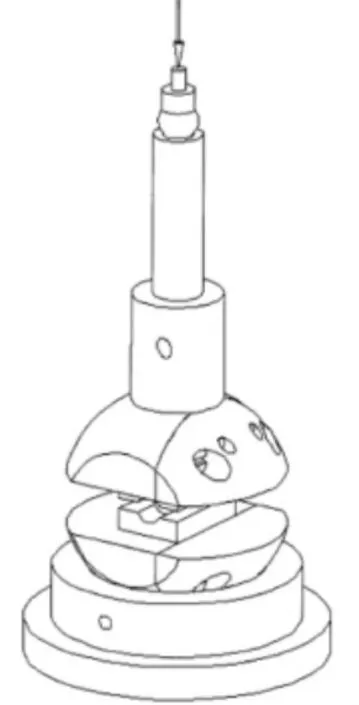
图2 人工颈椎间盘假体的沉陷试验示意图Fig.2 Subsidence testing of artificial cervical disc prosthesis
5 半脱位测试
半脱位测试是指将终板固定在夹具上,施加恒定轴向载荷,模拟头部重量对假体产生的压缩载荷,以恒定加载速度在上终板后侧施加向前的剪切力,直到假体完全分离或失效。4种不同结构设计的假体半脱位测试显示均超过人颈椎间盘所能承受的最大剪切载荷20 N[13-14]。Panjabi等[16]报告颈椎横截面上的总位移为(3.5±0.3)mm,其中前向位移1.9 mm,向后位移1.6 mm。在未发生后部构造(脊柱关节、韧带、肌腱)重度损伤时是不可能发生这种程度的前向移位的(表7)。
6 磨损测试
为比较不同材料、尺寸和外形的人工颈椎间盘假体的磨损性能,ASTM和ISO均制定了人工椎间盘假体磨损测试标准[17-18]。磨损测试通过对假体施加轴向压缩载荷,同时控制围绕三个坐标轴旋转的角度运动。坐标原点位于假体的几何中心或旋转中心,Z轴平行于轴向载荷方向,X轴指向椎体前后方向,Y轴指向椎体内外侧方向。假体的三个运动包括屈曲/伸展(围绕Y轴在矢状面内旋转),侧向弯曲(围绕X轴在冠状面内旋转)和轴向旋转(围绕Z轴在横截面内旋转)。轴向载荷和运动的范围显示,载荷和运动以正弦曲线方式施加。磨损试验总循环周期为1千万次,通过测试各个间隔样品的重量损失评估人工颈椎间盘假体的耐磨损性能(图3,表8)。
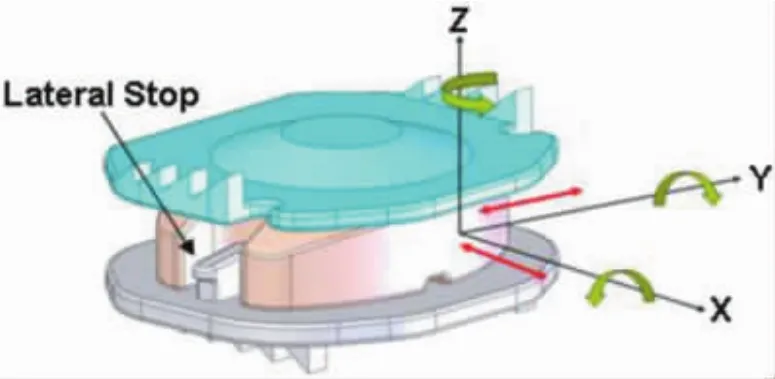
图3 人工颈椎间盘假体载荷和运动示意图Fig.3 Load and motion of artificial cervical disc prosthesis
人工颈椎间盘假体关节面的磨损产生磨屑,会进入假体周围间隙,被局部细胞吞噬后能激发细胞释放细胞间介质因子及产生组织细胞代谢副产物而激活局部破骨细胞,促进假体周围骨吸收,造成骨质溶解,最终引起假体的无菌性松动。金属-金属关节面假体会产生金属离子,可能造成周围组织炎症反应。目前所开展的相关研究还未确定统一的磨损率和磨屑的可接受依据,通常通过与已上市产品进行体外磨损试验对比分析,预测新研发产品的临床安全性和有效性(表9)。
此外,在磨损试验中,通过将假体置于过度倾斜的中立位置,并在测试之前将样品压缩变形以模拟上下终板边缘撞击的情况,可以评估人工椎间盘假体可能存在的上下终板边缘撞击的风险。Mobi-C假体经过1百万次撞击试验后,上终板的磨损率为(0.23±0.20)mg/million cycles,下终板的磨损率为(0.87±1.1) mg/million cycles[7]。

表6 FDA批准上市的4种人工颈椎间盘假体沉陷试验结果[7-11]Table 6 Subsidence testing results of four artificial cervical disc prosthesis FDA approved[7-11]

表7 FDA批准上市的4种人工颈椎间盘假体半脱位试验结果[7-11]Table 7 Subluxation testing results of four artificial cervical disc prosthesis FDA approved[7-11]

表8 人工颈椎间盘假体ASTM和ISO磨损测试标准试验参数对比Table 8 Comparison of ASTM and ISO weartestin gstandard of Artificial Cervical Disc Prosthesis

表9 FDA批准上市的5种人工颈椎间盘假体磨损试验结果[7-11]Table 9 Wear testing results of five artificial cervical disc prosthesis FDA approved[7-11]
7 结论
通过介绍人工颈椎间盘假体的体外功能评价方法,基于FDA已上市的5种人工颈椎间盘假体数据,总结了该类产品体外评价策略。随着国内人工颈椎间盘置换术的发展,国内企业对人工颈椎间盘假体的研发与临床应用将不断加快。基于FDA已上市产品的公开数据,借鉴国外产品标准和研究成果,探讨人工颈椎间盘假体科学合理的体外功能试验方法和可接受依据,可为国产同类产品的研发提供参考。

