金纳米簇荧光探针对盐酸小檗碱测定研究
李志英, 刘 倩, 葛 超, 张海容
(1.忻州师范学院化学系 山西忻州 634000;2.忻州师范学院生化分析技术研究所,山西忻州 034000)
金纳米簇(AuNCs)由于尺寸小、生物相溶性好、光学稳定性好、无毒等优点而得到广泛应用。而AuNCs作为荧光探针展现出的独特光学特性,使其在生物检测和医学诊断中表现出了很好的前景[1]。
小檗碱是黄连、黄柏等中药中含量最多的生物碱。研究表明其具有局部麻醉、抗心律失常、治疗原发性高血压,对痢疾杆菌、链球菌等有较强的抑制作用,并有增强白血球吞噬作用,临床主要用于肠道感染,有较强的体内外抗肿瘤活性[2]。而盐酸小檗碱含量测定是衡量黄连质量的重要指标,其测定方法主要有高效液相色谱法[3 - 5]、薄层色谱法[6 - 7]、双波长扫描法[8]、SDS法[9]、毛细管区带电泳[10]等。本实验经吐温20增敏的金纳米簇(AuNCs)具有很高的稳定性和优良的光学性能,盐酸小檗碱与AuNCs作用使AuNCs团聚,荧光强度降低,据此,建立了AuNCs荧光探针测定盐酸小檗碱的新方法。方法简便、准确、快速,重复性好。
1 实验部分
1.1 仪器、试剂与材料
F-4600荧光光度计(日本,日立公司);Tecnai G2F205-TWIN透射电子显微镜(美国,FEI公司);FTIR8400傅立叶变换-红外光谱仪(日本,岛津公司)。
HAuCl4·4H2O (国药集团化学试剂有限公司);2-巯基苯并噻唑(天津市光复精细化工研究所) ;盐酸小檗碱(Be -H,国药集团化学试剂有限公司)。实验用水为二次蒸馏水。
盐酸小檗碱片(东北制药集团沈阳第一制药有限公司);黄连、黄柏均购自于山西省忻州市五台山大药房。
1.2 实验方法
1.2.1AuNCs的合成分别准确吸取15 mL 0.4 g·L-1的HAuCl4溶液,20 mL 1.0×10-3mol·L-1的D -甘露糖溶液,10 mL 1.0×10-2mol·L-1的2-巯基苯并噻唑溶液,置于100 mL的锥形瓶中,摇匀。将锥形瓶放入数控超声波清洗器中,设置温度为40 ℃、水位高为80 cm、功率为8 0Hz、超声50 min,即制得AuNCs。
1.2.2盐酸小檗碱(Be-H)的测定精确吸取0.5 mL AuNCs溶液,1 mL吐温20溶液,2 mL pH=7的乙酸缓冲溶液,加入不同浓度的Be-H溶液于10 mL的比色管中,用二次蒸馏水定容,在激发波长和发射波长为346/532 nm处测定荧光强度F。计算:ΔF=F0-F,其中F0为未加Be-H时体系的荧光强度。
2 结果与讨论
2.1 AuNCs的透射电镜和红外光谱表征
由图1透射电镜(TEM)图可以看出,制备的AuNCs为比较规则的球形,直径为1.7~1.9 nm。由图2红外(IR)光谱图可知:D -甘露糖在2 950 cm-1的O-H 伸缩振动吸收峰向高波数方向移动;1 760 cm-1为C=O的伸缩振动吸收峰,690 cm-1为C-H的峰,D -甘露糖分子和AuNCs均含有两种类型的羧基,但AuNCs均减弱。

图1 AuNCs的透射电镜(TEM)图Fig.1 TEM image of AuNCs

图2 AuNCs和原料的红外(IR)光谱图Fig.2 IR spectra of AuNCs and ram material
2.2 AuNCs和实验体系的荧光光谱
分别配制1.0×10-3mol·L-12-巯基苯并噻唑溶液,1.0×10-4mol·L-1D -甘露糖溶液,一定浓度AuNCs溶液,1.0×10-5mol·L-1的Be-H溶液,在室温下放置20 min后,在激发波长为346 nm,发射波长为532 nm下测量各自的荧光强度。从图3曲线1可知,2-巯基苯并噻唑发射波长441 nm,曲线2说明D -甘露糖没有荧光,由曲线3可知AuNCs发射波长为532 nm,说明原料对AuNCs的荧光没有影响。图4曲线1为AuNCs,曲线2为AuNCs-Be -H的体系,说明Be -H可使AuNCs荧光猝灭,曲线3说明Be -H在532 nm处没有荧光。

图3 AuNCs体系的荧光光谱图Fig.3 The fluorescence spectra of AuNCs system

图4 测定体系的荧光光谱Fig.4 The fluorescence spectra of measurement system
2.3 反应机理
通过D -甘露糖还原法制备的AuNCs其溶液在532 nm波长处有荧光,粒子外层被过量的D -甘露糖所包围而显一定负电性,稳定剂2-巯基苯并噻唑通过Au-S键而使粒子也带上负电,它容易和正电荷物质发生静电作用,使AuNCs粒径变大,随着粒径的增大,AuNCs荧光强度也随之降低。由于电性关系,Be -H与AuNCs作用,导致AuNCs荧光强度降低。据此,可以实现对Be -H的测定。

图5 AuNCs和盐酸小檗碱的作用机理Fig.5 The mechanism of interaction between AuNCs and the berberine hydrochloride
2.4 AuNCs对Be -H的选择性
为了确认AuNCs对Be -H的选择性,对Be -H及其它一系列有机物及中药中常见物质的干扰进行测定。由图6可知,在1.0 ×10-6mol·L-1相同浓度下,Be -H可以跟AuNDs作用,使其荧光猝灭。F/F0值的巨大差异表明了AuNCs对Be -H的良好选择性。
2.5 表面活性剂的种类及用量的选择
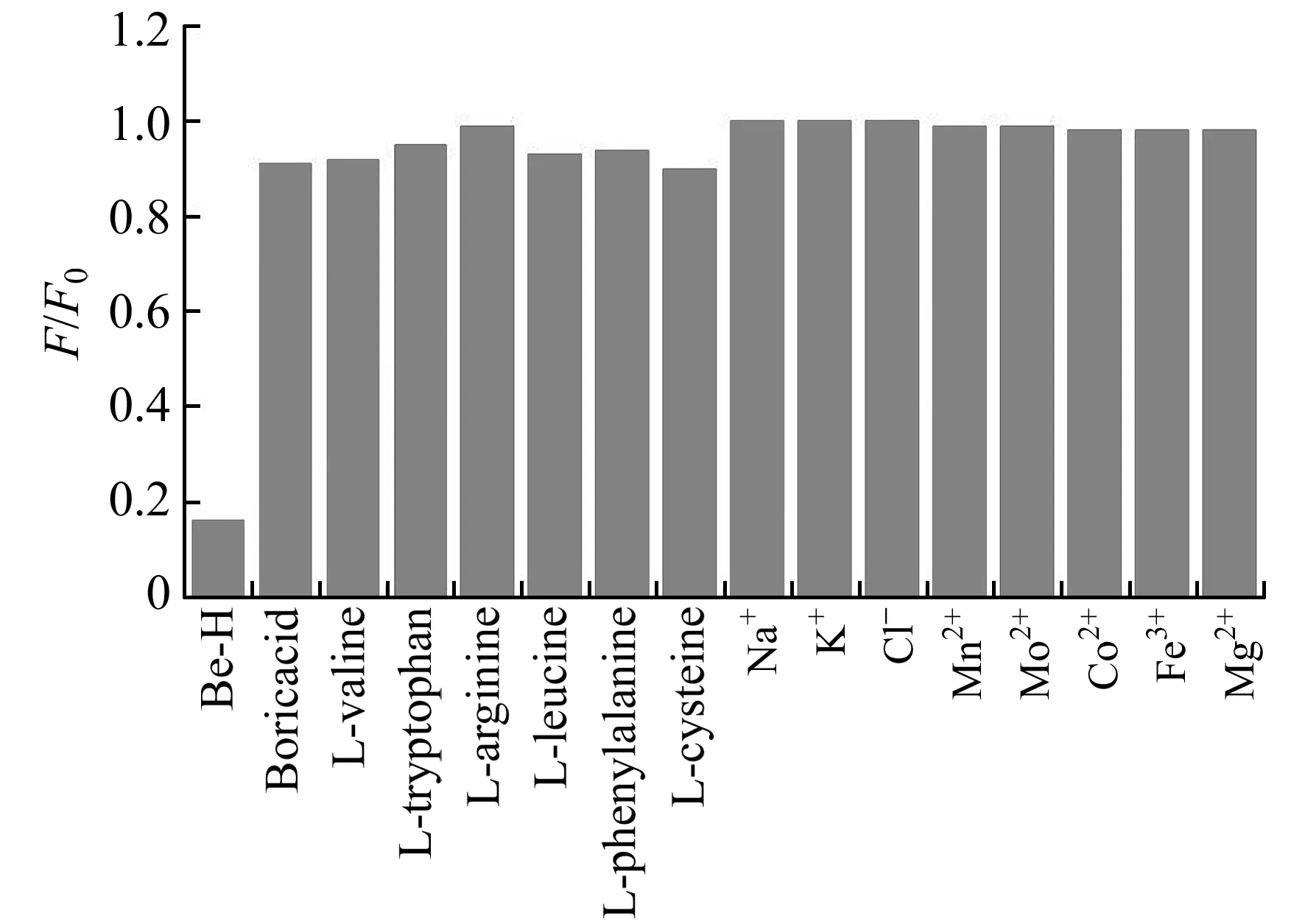
图6 AuNCs对不同物质的响应Fig.6 Response of AuNCs to different compounds
根据实验方法,分别试验了表面活性剂CTMAB、OP乳化剂、吐温80、吐温60、吐温20、SDS表面活性剂对AuNCs荧光强度的影响。结果表明吐温20的增敏效果最好,所以本实验选定吐温20为增敏剂。同时准确吸取不同浓度的1∶5 000(V/V)的吐温20溶液进行实验,结果表明吐温20用量为1 mL时ΔF最大,所以本实验选用体积比为1∶5 000的吐温20溶液1 mL。
2.6 pH对体系的影响
以乙酸缓冲溶液为介质,调节测定体系的pH,研究pH对体系的影响。ΔF随pH的升高先增大后减小,当pH=7时,ΔF最大,故选择pH=7的乙酸缓冲体系为反应介质。
2.7 反应时间和温度对体系的影响
体系在5 min后反应完全,并且在30 min内ΔF基本不变,为方便测定故实验选择在10 min后测定。设定不同的温度:20 ℃、30 ℃、40 ℃、50 ℃,进行反应7 min,用流水冷却3 min。结果表明:不同温度条件下ΔF保持相对稳定,故实验选择在室温下进行。
2.8 标准曲线与检出限
按实验方法配制0、0.05、0.06、0.08、0.2、0.3、0.4、0.6、0.8、1.0、2.0、3.0、4.0 μmol·L-1Be -H溶液,以未加Be -H溶液的空白溶液作参比,于激发波长346 nm处测定荧光强度。实验结果表明,Be -H的浓度在5.0×10-8~4.0×10-6mol·L-1范围内的线性回归方程为:ΔF=332.1c+99.7(c:μmol·L-1),相关系数r2=0.9935。求得其标准偏差(S)为0.854,利用3S/K公式求得检出限为7.7×10-9mol·L-1。
2.9 样品的测定
取盐酸小檗碱片10粒,研细,称取40 mg细粉至烧杯中,加沸水适量使其溶解,冷却至室温,过滤后,移取滤液1 mL定容到100 mL容量瓶中。中药的处理:称取过筛的中药细粉2 g,加入40 mL无水乙醇和20 mL二次蒸馏水,在70 Hz功率下,超声提取数次,过滤,滤液定容到100 mL容量瓶中[11]。按实验方法测定,结果如表1。

表1 样品测定结果和回收率
3 结论
本实验在水溶液中以2-巯基苯并噻唑为稳定剂,D -甘露糖为还原剂,HAuCl4为原料,在80 Hz的超声波下制备AuNCs,用荧光光谱研究了经吐温20增敏的AuNCs作为荧光探针对中药盐酸小檗碱的检测。结果表明在中性环境中,室温下反应10 min后,体系荧光强度下降,且荧光强度在一定范围内与盐酸小檗碱的浓度成正比,线性范围为5.0×10-8~4.0×10-6mol·L-1,检出限为7.7×10-9mol·L-1,回收率为97.5%~105%。
参考文献:
[1] Liu D B,Chen W W,Wei J H.Analytical Chemistry,2012,84:4185.
[2] Zheng J,Zhou C,Yu M X.The Royal Society of Chemistry,2012,4:4073.
[3] XIA Q,LI C M.Chinese Traditional Patent Medicine(夏荃,李灿明.中成药),2008,30(7):1018.
[4] XU Y,ZHOU S W,TANG J L,et al.Journal of Third Military Medical University(徐颖,周世文,汤建林,等.第三军医大学学报),2007,29(2):179.
[5] LIU C J.Chinese Traditional Patent Medicine(刘存军.中成药),2007,29(12):1864.
[6] YU H Y,TANG Y J,WANG W B,et al.China Journal of Chinese Materia Medica(虞和永,汤永玖,王文博,等.中国中药杂志),2004,29(9):
[7] Liu J M,Chen J T,Xiu P Y.Analytical Chemistry,2013,85:3238.
[8] WU C I,WU W X.Acta Chinese Medicine of He Nan(吴成立,吴卫新.河南中医药学刊),2000,15(5):43.
[9] XU Y Y,MAO S Z.Chinese Journal of Hospital Pharmacy(徐英瑜,毛书征.中国医院药学杂志),2001,21(12):27.
[10] Li S R.Chemical Physics Letters,2013,76:561.
[11] Wu X,He X X.The Royal Society of Chemistry,2010,2:2244.

