多电子转移镁/铝电池体系能量密度热力学计算
曹文卓,汪君洋,陈汝颂,索鎏敏,李 泓
多电子转移镁/铝电池体系能量密度热力学计算
曹文卓1,2,汪君洋1,2,陈汝颂1,2,索鎏敏1,2,李 泓1,2
(1中国科学院物理研究所,北京 100190;2中国科学院大学,北京 100049)
镁离子电池和铝离子电池因其高能量密度、地壳储量丰富、安全等优良特性有望成为下一代新型高能量密度储能体系,是未来二次电池研究的热点之一。本文采用热力学方法计算和分析了近300种镁离子和铝离子电池体系的理论质量能量密度、体积能量密度和电压。在所得数据的基础上,以目前商业化锂离子电池正极材料钴酸锂为对比参考,综合考虑质量能量密度、体积能量密度、标准电极电位、毒性、腐蚀性、易燃性、环境友好性等诸多因素,逐步筛选出符合条件的一系列镁离子正极材料(O2、S、MnO2、MoO3、Fe2O3、Fe3O4、NiO、MoO2、CuO、Cu2O)和铝离子的正极材料(O2、S、MnO2、MoO3、NiO、CuO、Cu2O)。
镁离子电池;铝离子电池;质量能量密度;体积能量密度;正极
二次电池目前已经广泛应用于消费电子、电动车、智能电网和可再生能源储能等诸多领域,成为支撑社会可持续发展的重要动力。与此同时,社会的不断发展对能量储存系统提出了更高的要求,开发高能量密度、高功率密度、高安全、低成本的电池已经成为研发热点。其中寻找能量密度更高的二次电池体系,是研究人员的重要研发目标。
多电子转移反应体系是一类有潜力实现电池能量密度成倍增长的重要电化学储能体系。通常意义上讲,多电子转移体系指1 mol活性材料发生氧化还原反应能够提供数倍´1 mol电子转移[1],根据反应机理的不同可以分为3大类,第一类是基于一价阳离子的反应体系,以锂离子电池、钠离子电池为代表,典型的电极材料有Li2MSiO4(M=Fe或Mn)、Si、金属氧化物等。第二类是基于高价阳离子的反应体系,以二价碱土金属镁、钙、锌以及主族金属铝为基础的二次电池体系。第三类是非金属族的氧气、单质硫为正极活性物质的金属-空气电池、金属-硫电池[2]。
锂离子电池为目前最广泛使用的动力电池商业化体系,随着其应用市场不断扩大,基础锂资源的价格不断攀升,人们开始担忧未来锂资源的供给,尤其是对未来在能量密度要求不高但价格极其敏感的储能电网中大规模应用方面。因此研究者开始将目光转向其它替代电池体系。金属镁、铝与锂化学性质接近,且地壳储量丰富,成本低廉,并且为多电子转移体系使得在能量密度方面有较强的优势,近年来逐渐成为新的研究热点。加之,电动汽车的蓬勃发展对电池的能量密度提出了更高的要求。2020年,中国政府制定的量产电池电芯能量密度300 W·h/kg的目标[3]。要想达到指标,多价电子转移体系将会是一个非常有前景的高能量密度电池体系。
本文选取了多价电子转移体系中最具代表性的两类电池体系:镁离子电池、铝离子电池体系作为研究对象,介绍二次镁离子电池、二次铝离子电池的研究现状;对已经报道的和未来可能构成电化学电对的镁离子和铝离子体系做统一归纳和梳理,从热力学方面对近300种镁离子/铝离子电池体系的理论质量能量密度、体积能量密度和理论电压进行了初步的计算、分析和评估。力求让相关研究者对相关体系的理论能量密度有一个更为全面直观的认识并从中得到有研究价值的体系。
1 镁离子电池、铝离子电池简述
镁、铝在地壳中储量丰富以及其廉价易得的特性,且相对锂离子电池来说更安全,使得其在大负荷用途方面相比锂离子电池更有优势[4]。金属镁和铝的理论质量比容量是除锂以外最高的体系,更重要的是其体积比容量具有绝对优势,较锂而言,铝是其大约4倍,镁是其大约2倍(表1)。
对镁离子电池、铝离子电池的研究早在19世纪50年代就展开了,但是到目前都迟迟没有商业化。主要有如下原因:第一,镁的化学活性很强,电解质很容易在其表面还原生成一层致密的钝化膜,与锂电池中负极形成SEI钝化膜不同,该层钝化膜不是镁离子导体,镁离子无法穿越,从而阻碍可逆的电化学反应;其次,镁离子半径比锂离子小,但是所带电荷是锂离子的两倍,这一方面导致镁离子溶剂化比锂离子更强,镁离子去溶剂化过程所需能量更高;另一方面导致其在固体晶格中的传输受到更强的电荷相互作用使得其离子传输受限,扩散困难[8]。与之相似,铝离子电池除了同样存在与镁离子电池类似的前两点问题外,由于铝本身特有的物理化学性质,其不但化学性质活泼,而且为两性金属,即酸性或中性条件下容易发生析氢反应,碱性条件下铝成流反应和腐蚀反应产物均为Al(OH)3,胶状Al(OH)3无催化剂条件下很难转化为可溶的Al(OH)4-,降低电解质的电导率,增大极化,使电池可逆性变差[9]。
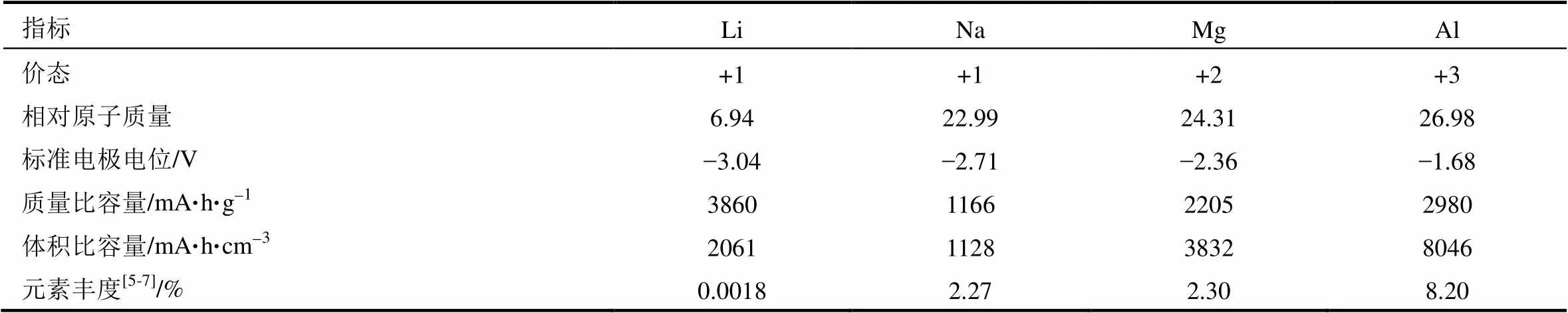
表1 金属锂、钠、镁、铝电极对比
从目前关于镁离子电池和铝离子电池已有的研究经验看,该体系无法像钠离子电池一样借鉴锂离子电池相关成熟研究经验。电解液更多是路易斯酸碱理论下形成的复杂配位电解质体系,而且目前报道的可以实现镁离子和铝离子可逆脱嵌的正极材料少之又少。常用的镁离子电池正极材料有过渡金属氧化物、过渡金属硫化物、普鲁士蓝类似物、聚阴离子型化合物、硼化物和有机材料等。常见镁离子电池正极材料见表2。

表2 常见镁离子电池正极材料

续表2
常见铝离子电池的正极材料有过渡金属氧化物、过渡金属硫化物、普鲁士蓝类似物、含碳材料、导电聚合物、金属氯化物、聚阴离子型化合物、S、Cl2等非金属单质。常见铝离子电池正极材料见表3。

表3 常见铝离子电池正极材料
2 热力学计算原理
二次电池依靠化学能与电能的互相转换来工作。电池在标准状态(298.15 K、101.325 kPa)下化学反应前后体系能量变化为产物标准Gibbs生成能与反应物标准Gibbs生成能之差,即为该反应的标准吉布斯生成能。
如果将一个反应的通式表示为式(1)
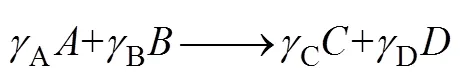
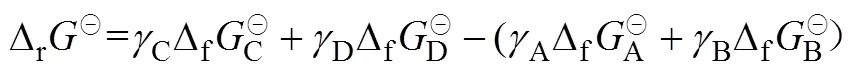
写为通式即为式(3)
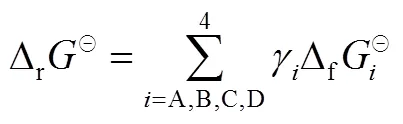
对于等温等压下(标准状态)的可逆反应,标准Gibbs生成能的减少量等于该反应过程对外做最大的非体积功。式(4)描述的即为当非体积功全部为电功时的情况。
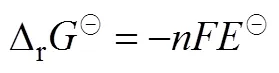
电池体系的能量密度主要有两种表示方法,即质量能量密度、体积能量密度。
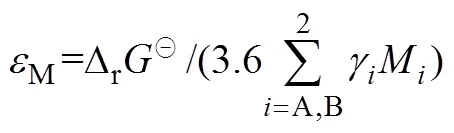
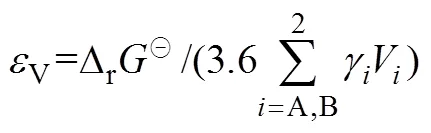
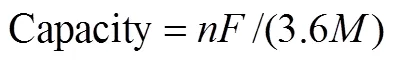
从式(2)、式(6)、式(7)可以看出,反应体系的生成物的Gibbs生成能越低,反应物的Gibbs生成能越高,反应物摩尔质量、摩尔体积越小时,电化学体系能量密度越高。标准状态下的物质的Gibbs生成能可通过热力学手册查得。热力学手册未收录的物质的热力学数据一般要查阅相关文献获知。对于Gibbs生成能尚不清楚的物质,可以通过基于第一性原理(First Principles)的密度泛函理论(Density Functional Theory-DFT)计算。
3 计算体系的选取以及原始数据来源
本文采用热力学方法共计算了近300种镁电池或铝电池体系的理论能量密度。相关体系的计算均建立在以金属镁或金属铝为负极,且正极不含镁或铝的正极体系,其中包括过渡金属化合物、非金属单质及其化合物。过渡金属主要选取了第四周期(除钪以外)元素和第五周期的Zr、Nb、Mo。考虑到原子序数增大会导致理论容量的降低,进而影响体系能量密度,因此本文为涉及原子序数小于Mo的材料。除此之外,原子序数比Mo小的元素剔除了Sc、Y,主要是考虑到这两种元素在地壳中的含量太少,相关化合物作为正极会导致较高的成本。过渡金属化合物正极材料的选取情况见表4。非金属及其化合物作为正极材料往往可以获得比较高的能量密度,但技术上存在很多难题,本文选取了27种较为常见的非金属单质及其化合物作为正极,见表5。
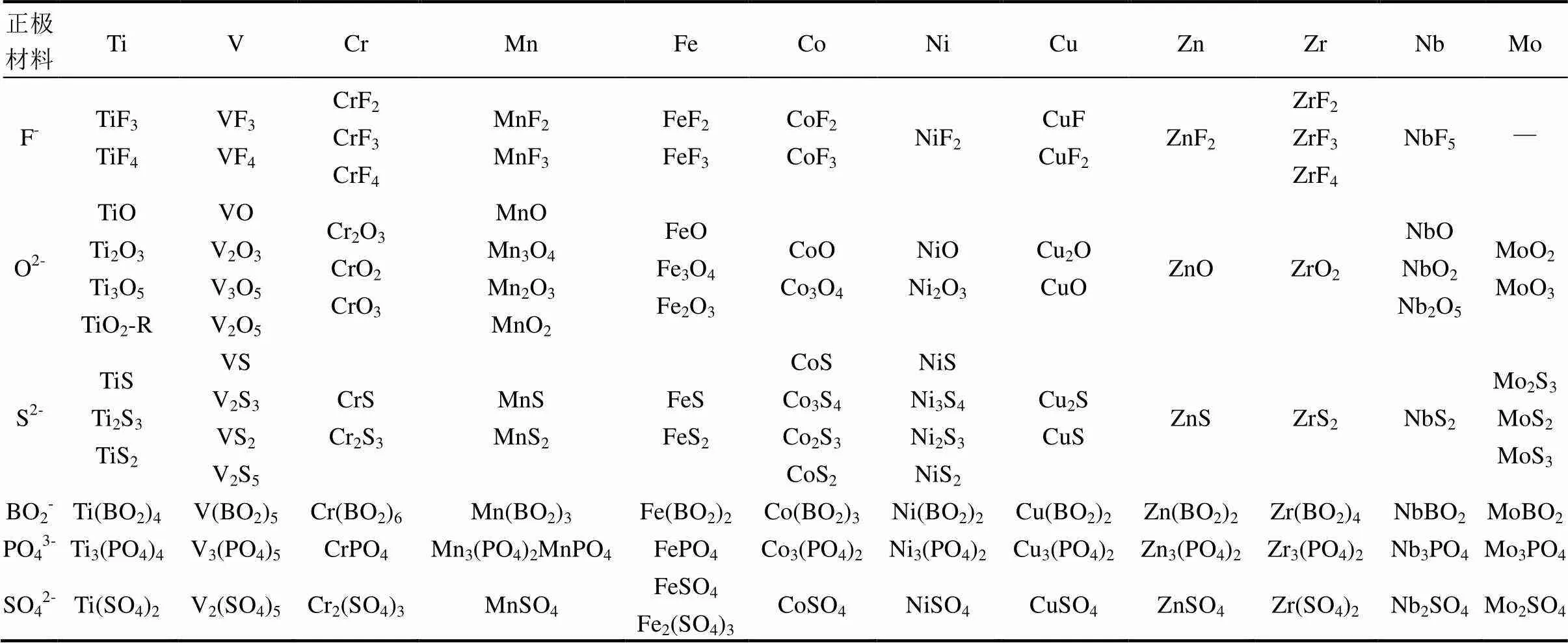
表4 过渡金属化合物正极材料
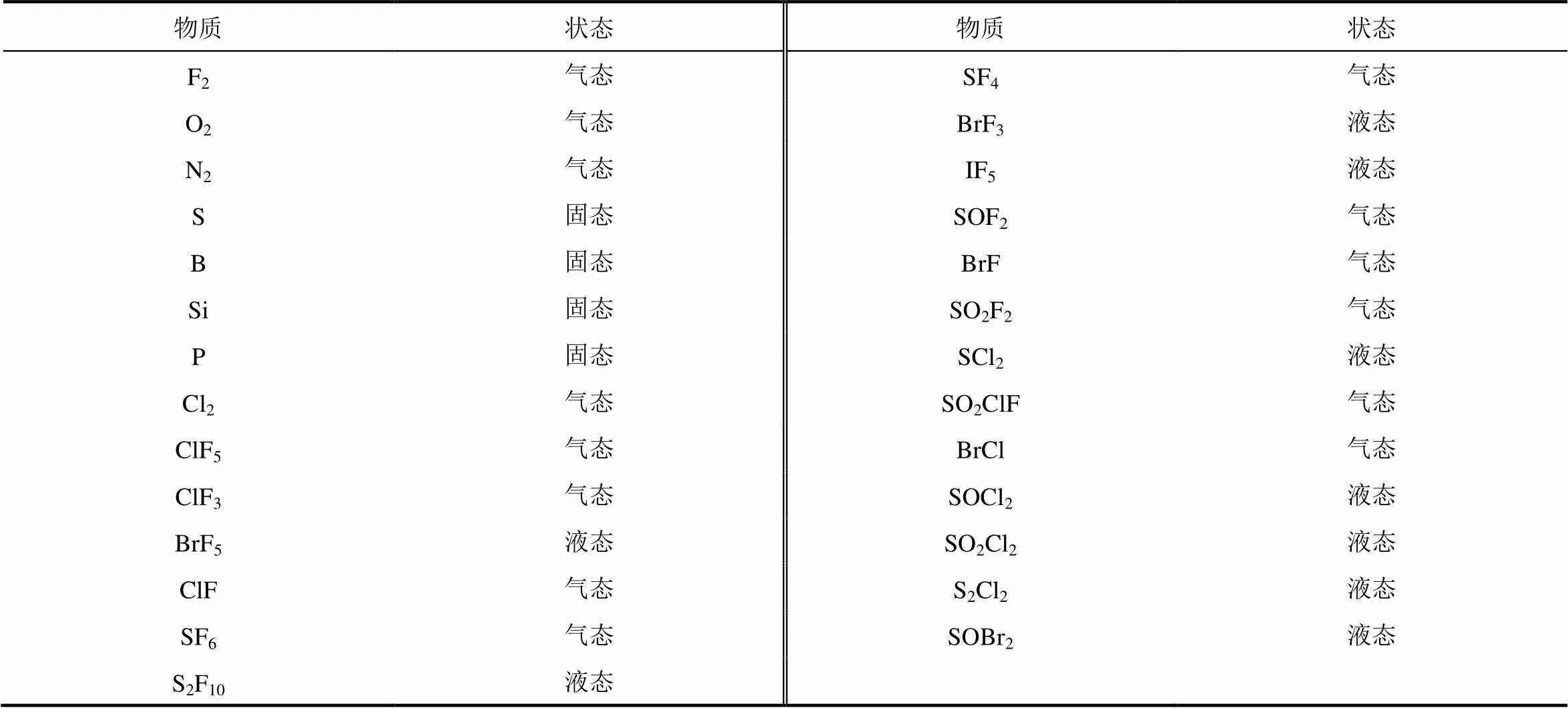
表5 非金属单质及其化合物的状态(27种)(298.15 K,101.325 kPa)
计算所需要的原始数据主要通过热力学手册查询[35-37]和National Institute of Standards and Technology (NIST)-JANAF Thermochemical Tables获得[38]。
4 结果分析
4.1 质量能量密度分析
图1和图2分别为计算所得理论质量能量密 度最高的20种镁电池或铝电池体系。以Mg为负 极的理论质量能量密度最高的是Mg/F2体系, 4776 W·h/kg。质量能量密度位列第2的是Mg/O2体系,3924 W·h/kg;位列第3的是Mg/ClF5体系;质量能量密度高达3861 W·h/kg。以Al为负极的理论质量能量密度最高是Al/F2体系,4734 W·h/kg。位列第二的是Al/O2体系,4311 W·h/kg;位列第3的是Al/ClF5体系,质量能量密度高达3688 W·h/kg。
从图1、图2中可以看出,理论质量能量密度最高的10种镁电池和铝电池体系中正极材料及其排序是完全一样的,正极均为非金属单质及其化合物。20种理论质量能量密度最高的体系中非金属单质及其化合物作为正极的体系分别占到了80%和70%。出现这样的结果很大程度上是因为非金属单质及其化合物的相对分子质量比较小,且参与氧化还原反应的元素占分子总质量比重较大(非金属单质及其化合物作为正极时,按照能发生氧化还原反应的元素全部反应,且生成常温下常见价态的化合物来计算)。
非金属单质及其化合物作为正极,一般来说有较高的理论质量能量密度。但是计算的27种正极材料中,有21种具有腐蚀性或毒性,详见表6。因此,综合考虑腐蚀性、毒性、导电性、标准电极电势等因素,非金属单质及其化合物中比较有研究价值的、有望应用于商业化的正极材料被逐步缩小为O2、S。其中O2、S作为正极的镁离子电池和铝离子电池目前已经有一些研究进展,但是多为一次电池,其充放电机理尚未弄清楚,如何实现Mg/O2、Mg/S、Al/O2和Al/S电池二次化仍然存在巨大技术挑战,用第一性原理加快对于充放电过程中表面产物的表征是目前研究的重点和难点[39]。
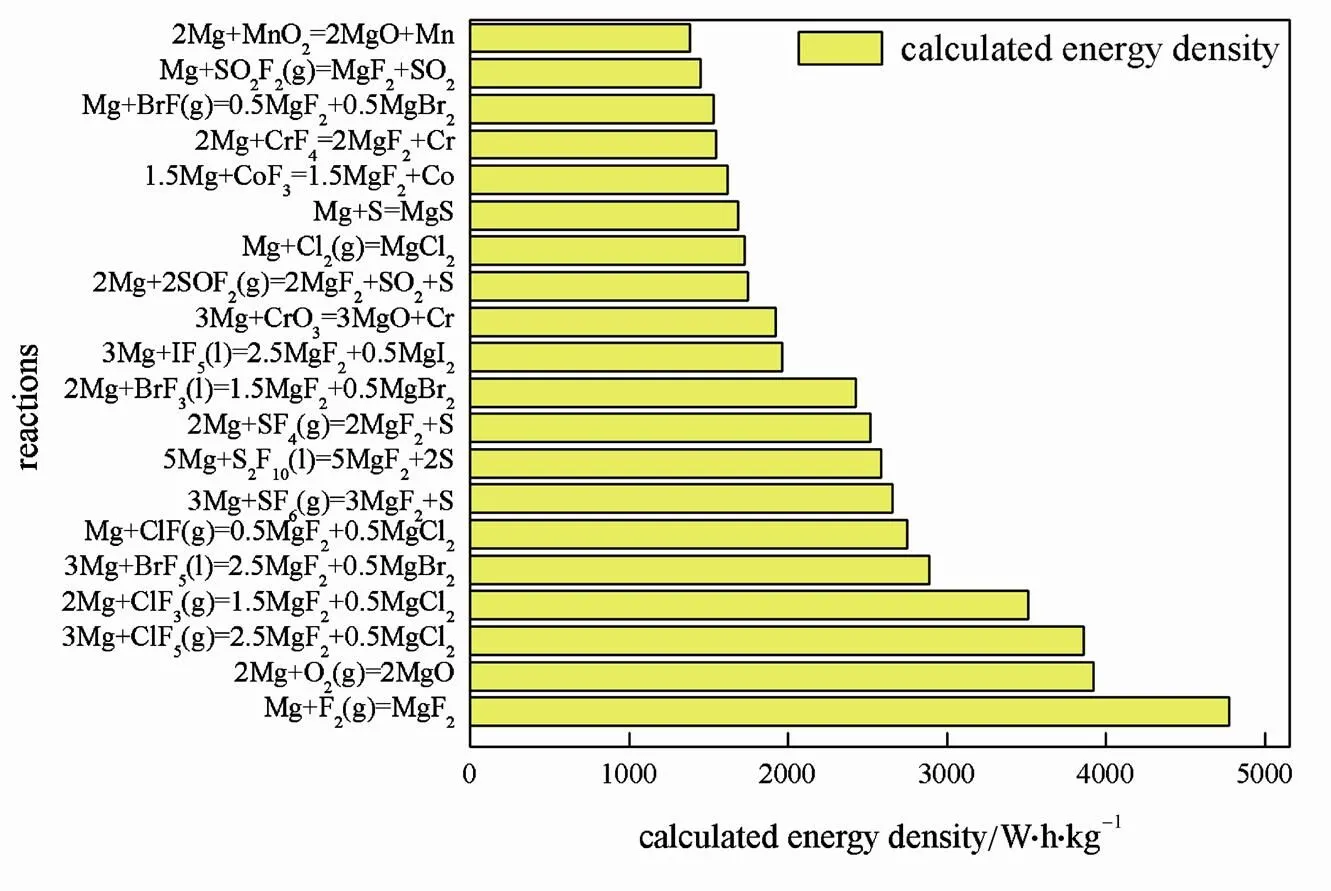
图1 质量能量密度最高的20种镁电池体系
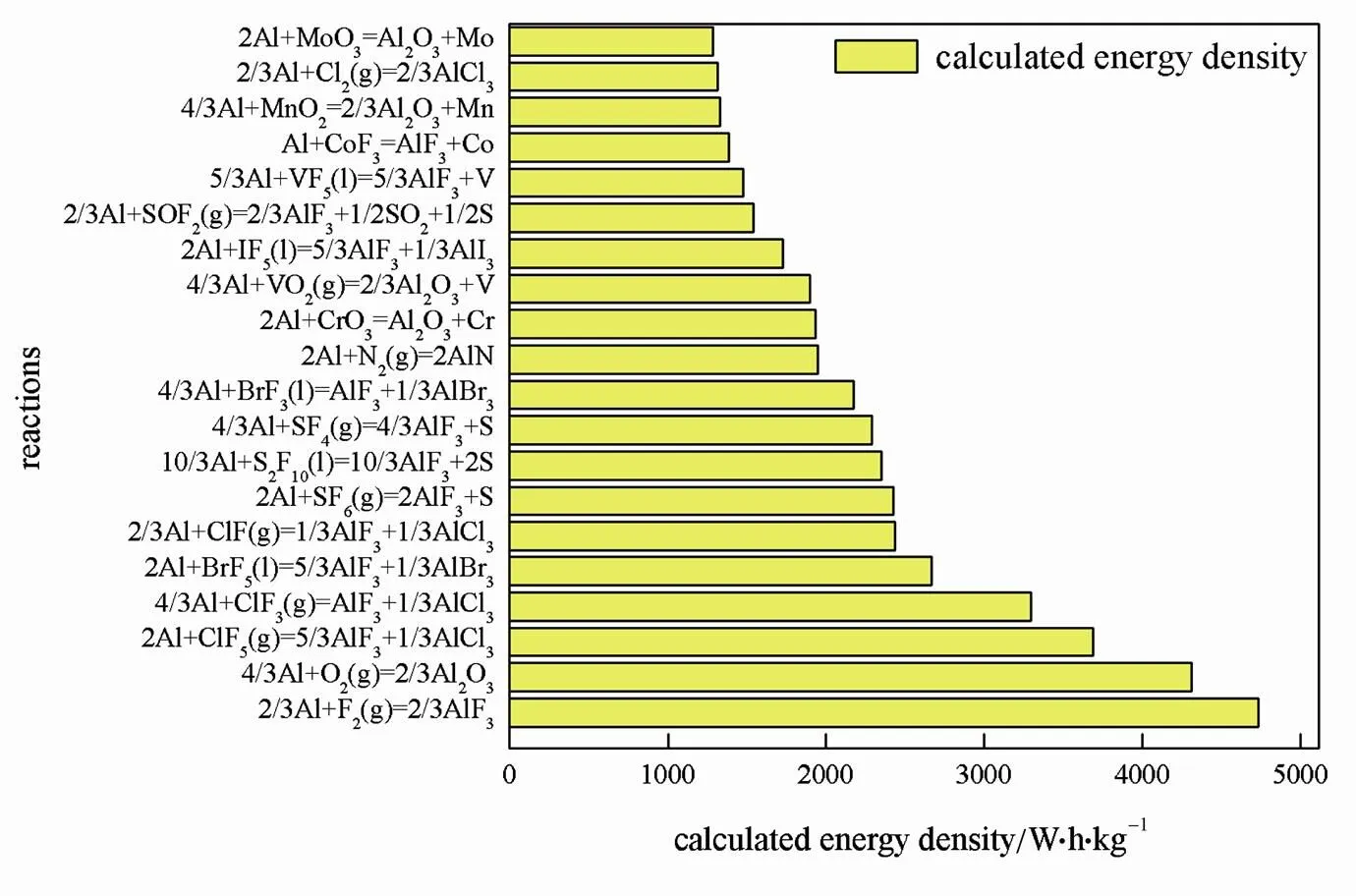
图2 质量能量密度最高的20种铝电池体系
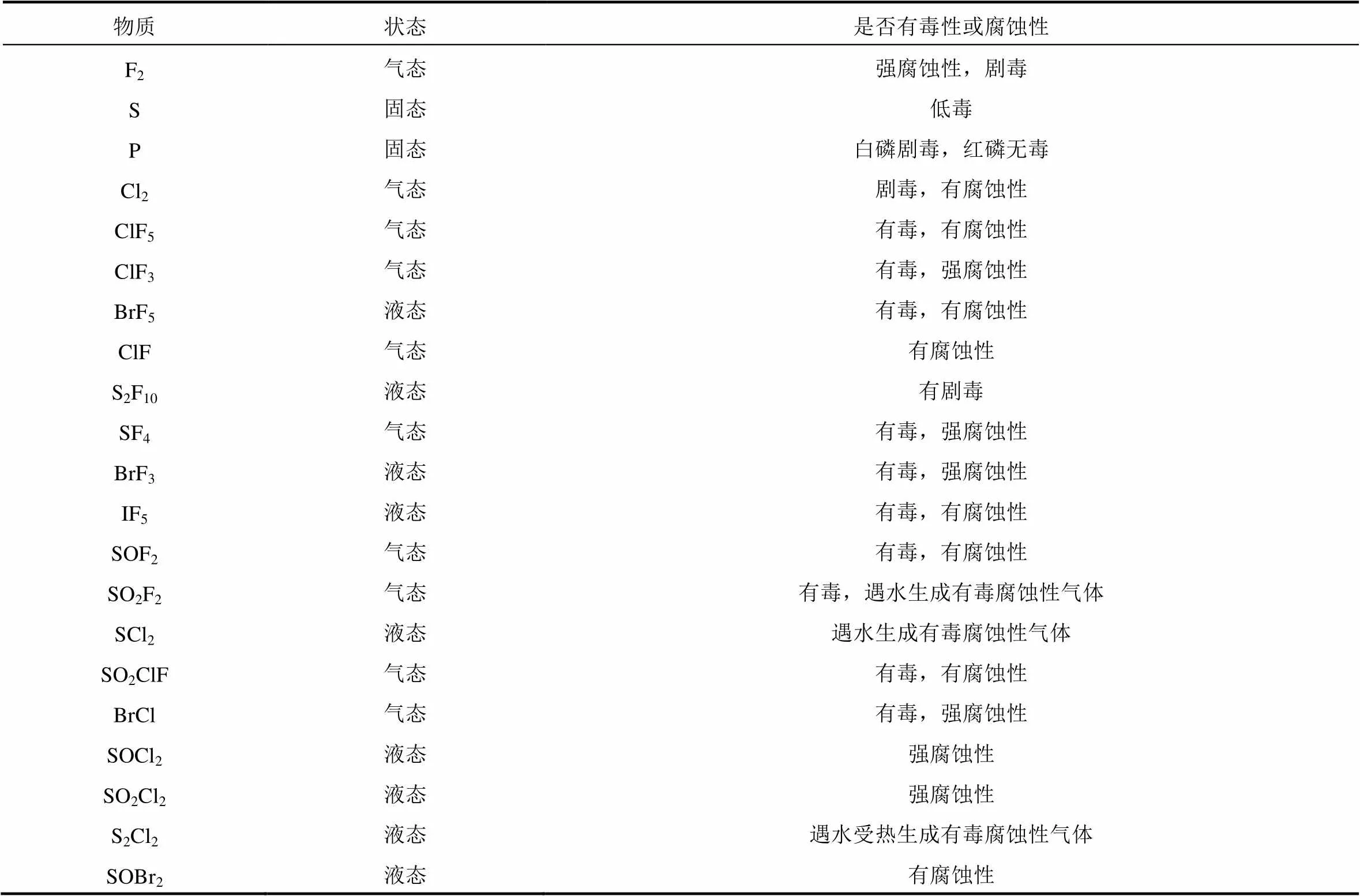
表6 有腐蚀性或毒性的非金属单质及其化合物正极材料(21种)
此外,由于此处计算的27种非金属单质及其化合物多为气体或液体(298.15 K、101.325 kPa,即标准状态下),且多半有腐蚀性或毒性不便于利用,因此我们将计算范围扩展到过渡金属化合物。
分别以Mg、Al为负极,过渡金属化合物为正极的理论质量能量密度最高的20种电池体系见图3和图4。从计算结果可以发现,能量密度最高的体系均为氟化物或者氧化物,其中有两种过渡金属化合物不是固体,分别为气态的VO2(g)和液态的VF5(l),由于未能找到固体的热力学数据,因此计算了这两种正极材料非固体时电池体系的理论能量密度作为参考。
以Mg为负极、过渡金属化合物为正极的理论质量能量密度最高的20种电池体系中,理论质量能量密度最高的是Mg/CrO3体系,1920 W·h/kg。质量能量密度位列第二的是Mg/CoF3体系,1618 W·h/kg,位列第三的是Mg/CrF4体系,质量能量密度高达1549 W·h/kg。
以Al为负极、过渡金属化合物为正极的理论质量能量密度最高的20种电池体系中,理论质量能量密度最高的是Al/CrO3体系,1930 W·h/kg。质量能量密度位列第二的是Al/VO2(g)体系,1899 W·h/kg,位列第三的是Al/VF5(l)体系,质量能量密度高达1472 W·h/kg。
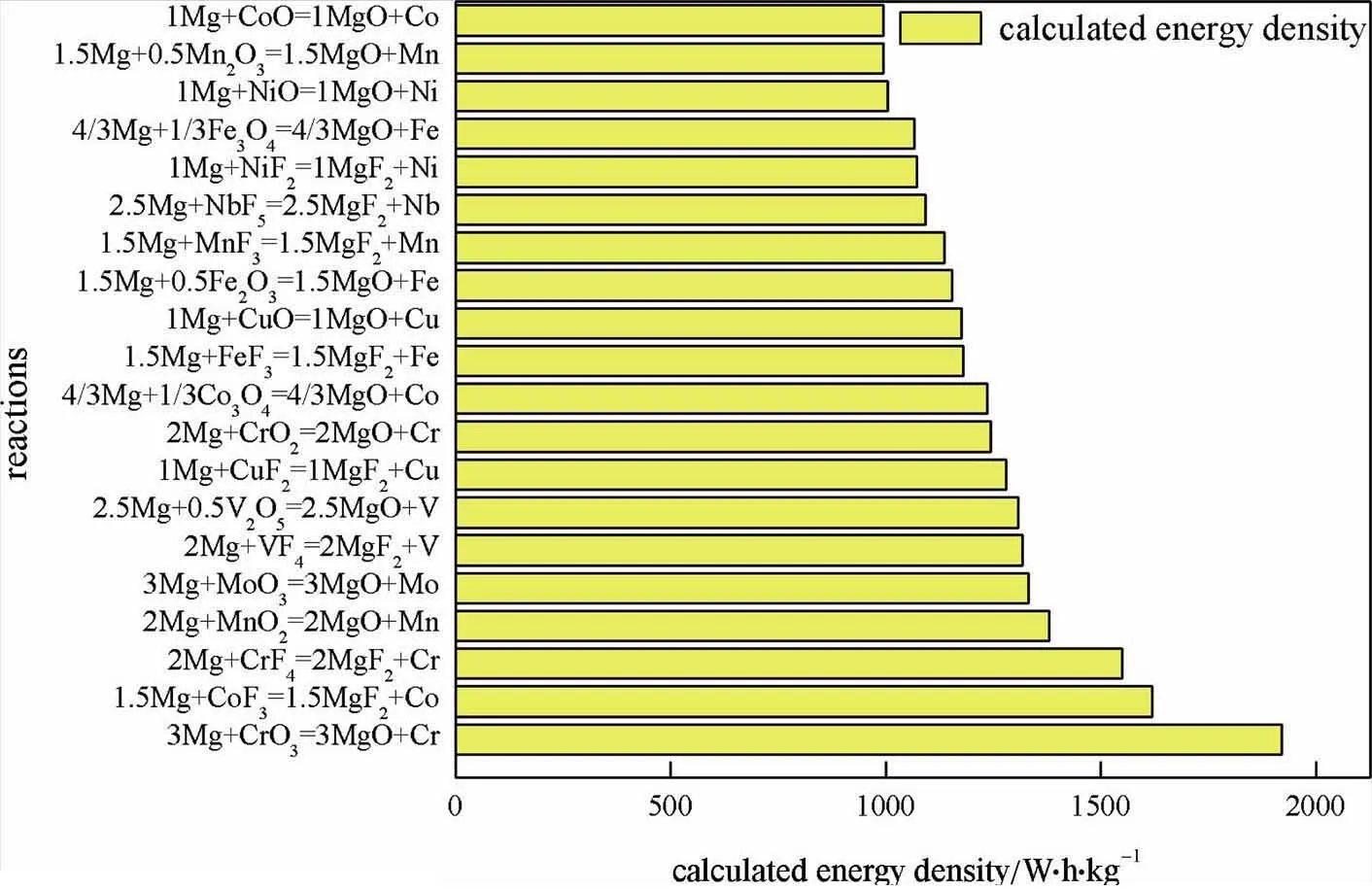
图3 质量能量密度最高的20种Mg过渡金属化合物正极
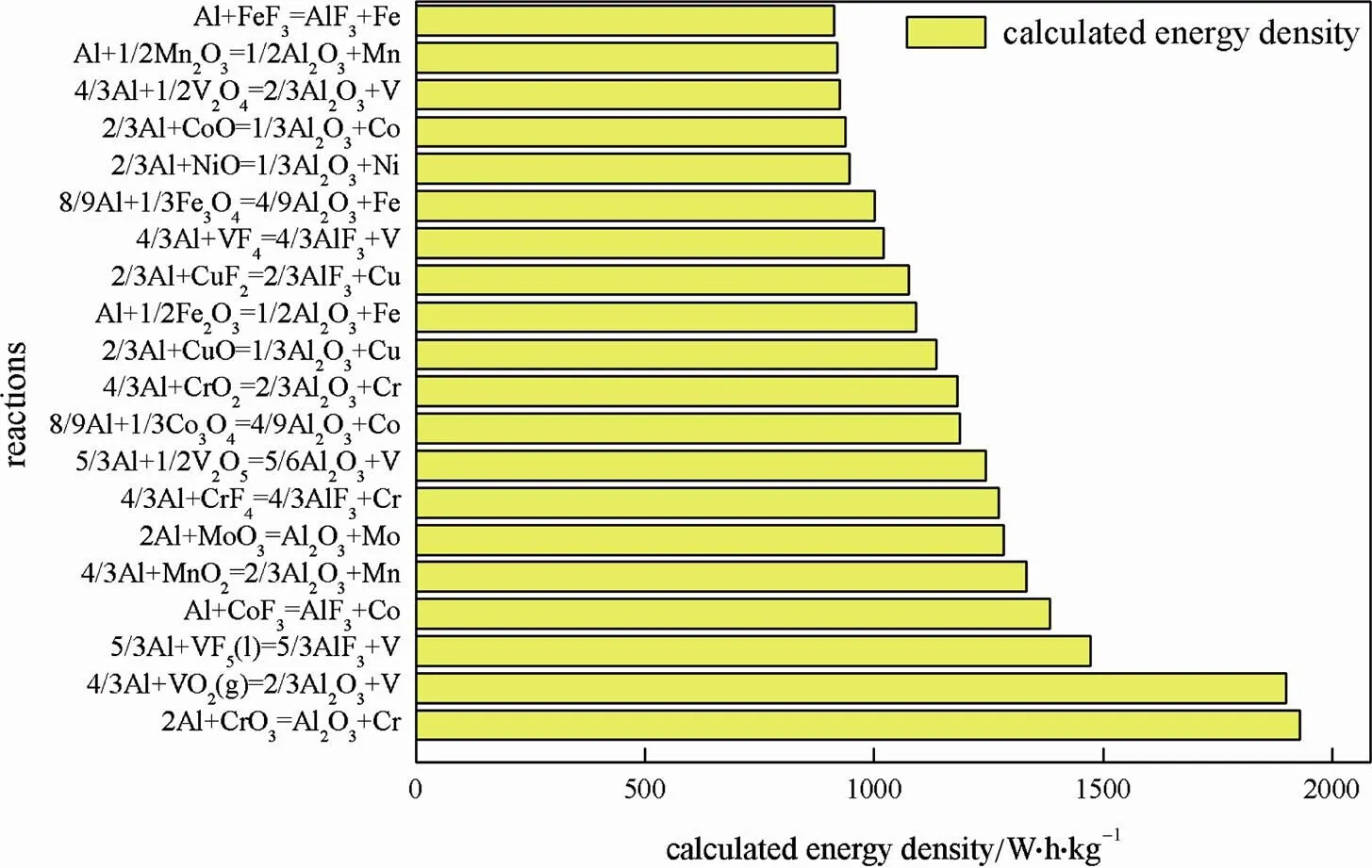
图4 质量能量密度最高的20种铝过渡金属化合物正极
考虑到镁电池或铝电池未来作为下一代高能量密度体系,我们将能量密度筛选阈值设置为现有商用锂离子电池钴酸锂体系,其质量能量密度按照正极容量140 mA·h/g,放电电压3.7 V计算为518 W·h/kg。表7、表8列出理论质量能量密度大于518 W·h/kg的Mg电池和Al电池体系。
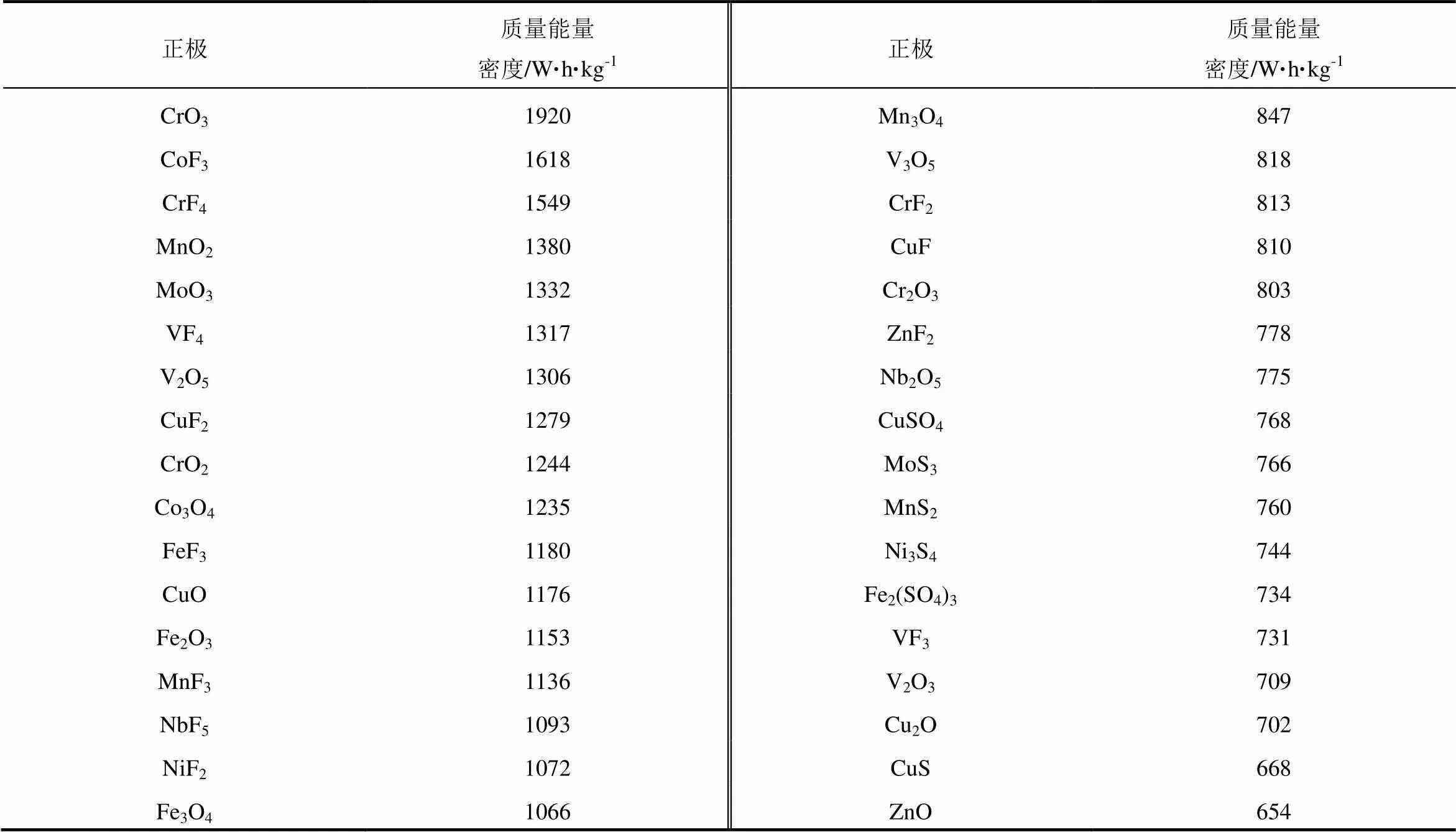
表7 质量能量密度大于518 W·h/kg的镁离子正极 (60种)
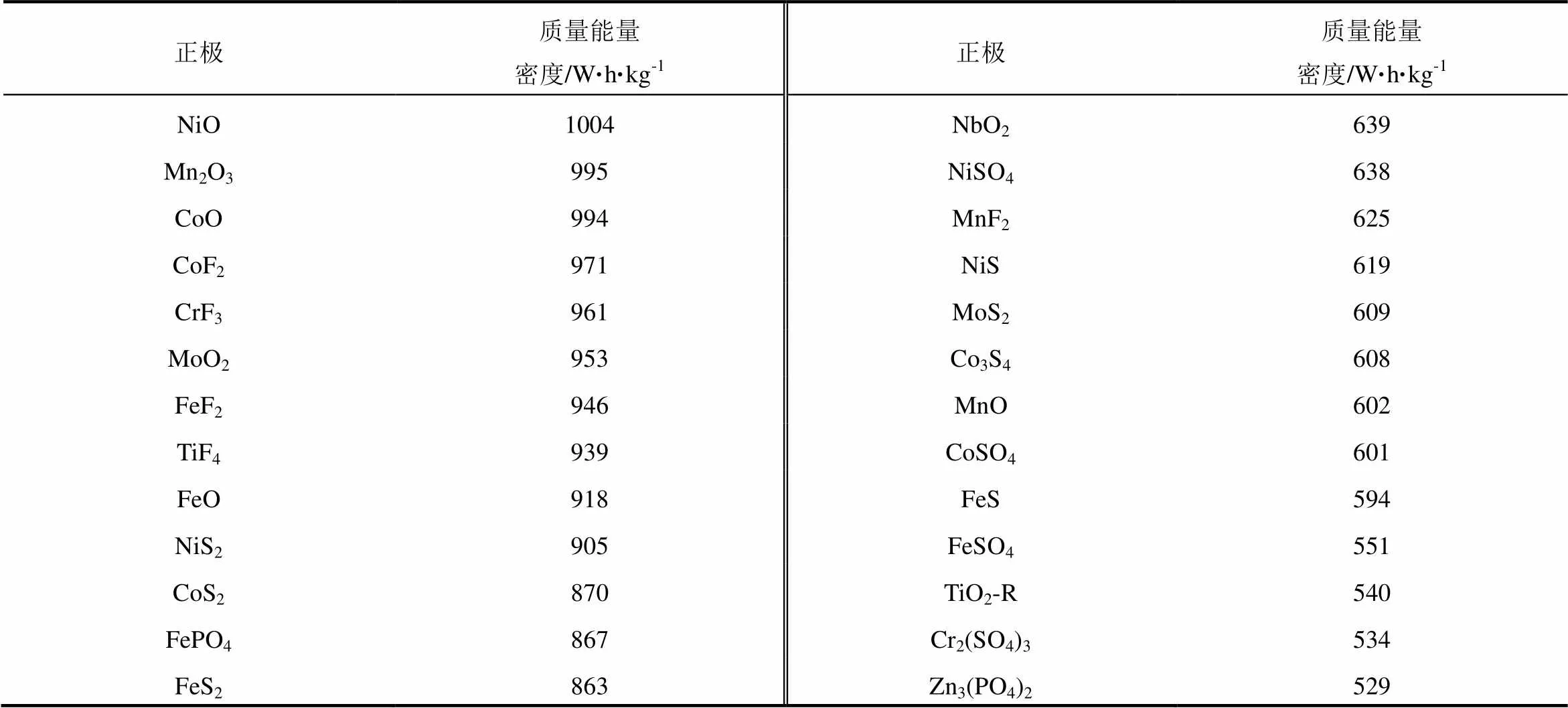
续表
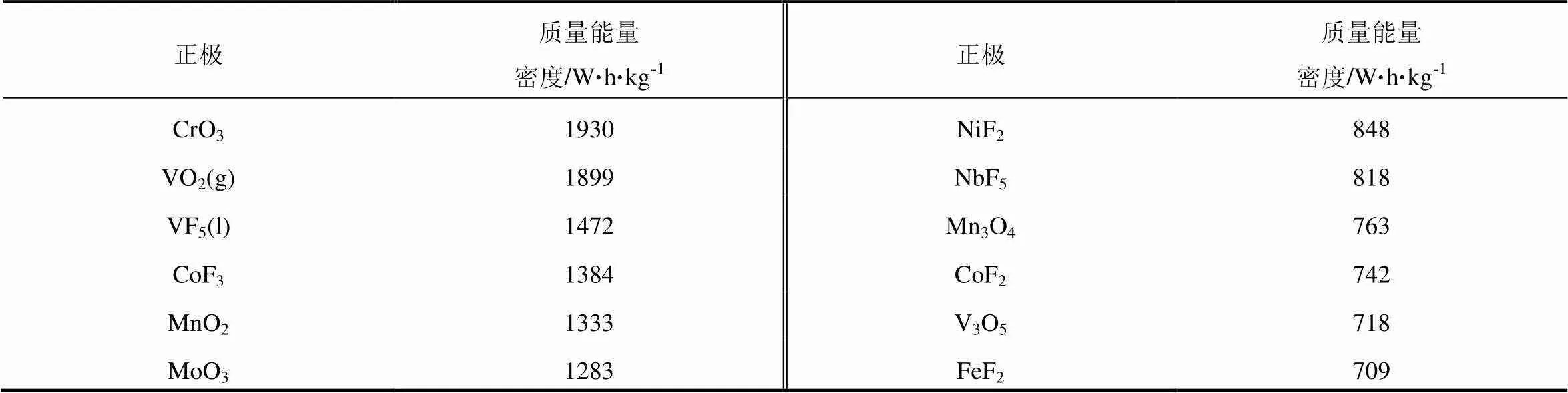
表8 质量能量密度超过518 W·h/kg的过渡金属铝离子正极 (45种)
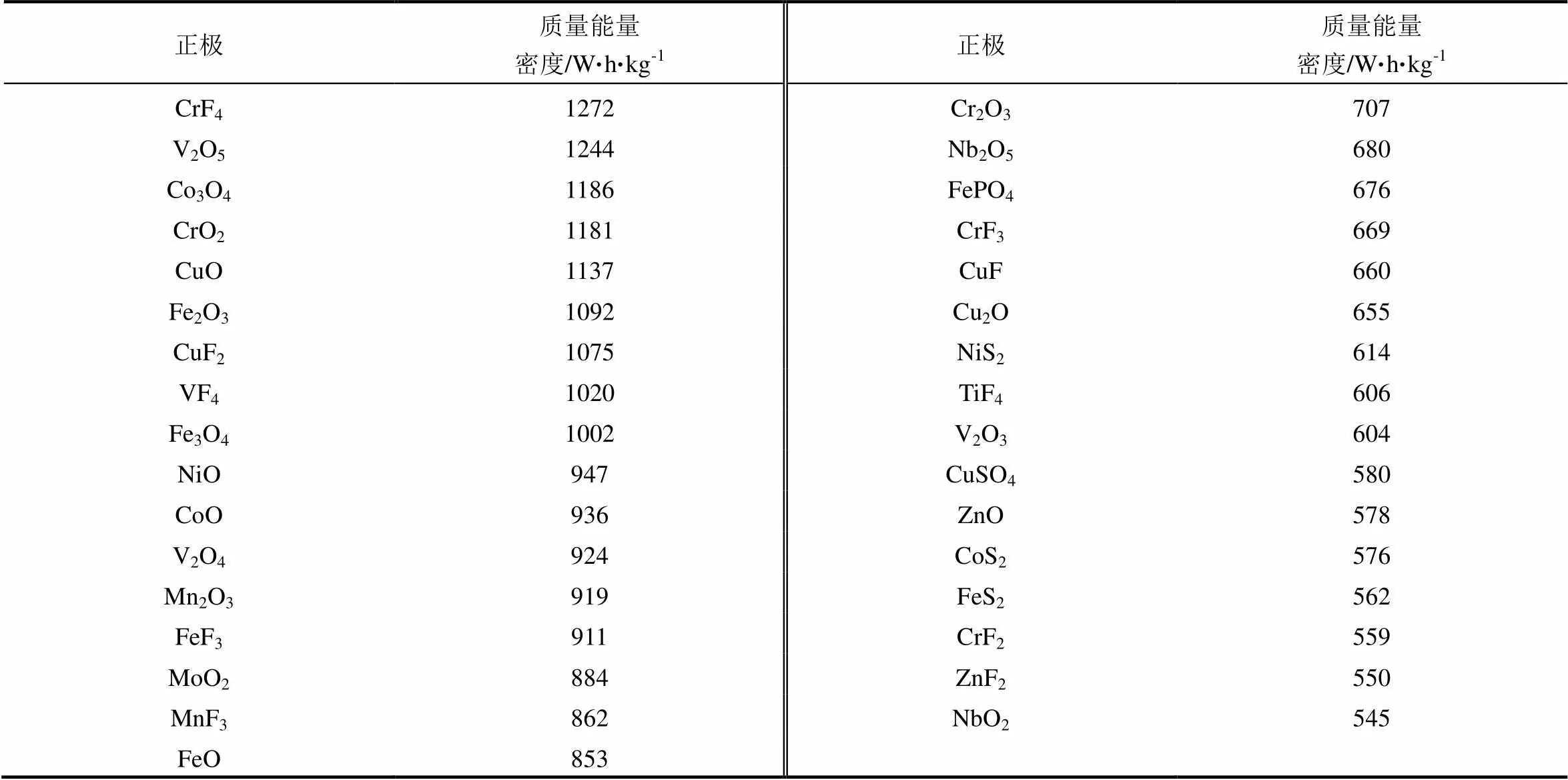
续表
4.2 体积能量密度分析
关于体积能量密度的计算,分别以Mg、Al为负极,过渡金属化合物为正极,计算参数选取了相关体系理论质量能量密度和材料本身理论密度,并未考虑材料实际填充密度和粉体电极预留空隙率等相关电极制造因素。图5和图6分别给出了理论体积能量密度最高的20种镁电池和铝电池体系。
过渡金属化合物正极均为氟化物或者氧化物。镁离子电池中,理论体积能量密度最高的是Mg/CoF3体系,4851 W·h/L。体积能量密度位列第二的是Mg/CuO体系,4595 W·h/L,位列第三的是Mg/Co3O4体系,体积能量密度高达4382 W·h/L。
铝离子电池中,理论体积能量密度最高的是Al/ VO2(g)体系,6962 W·h/L。体积能量密度位列第二的是Al/CuO体系,5754 W·h/L,位列第三的是Al/ Co3O4体系,体积能量密度高达5617 W·h/L。
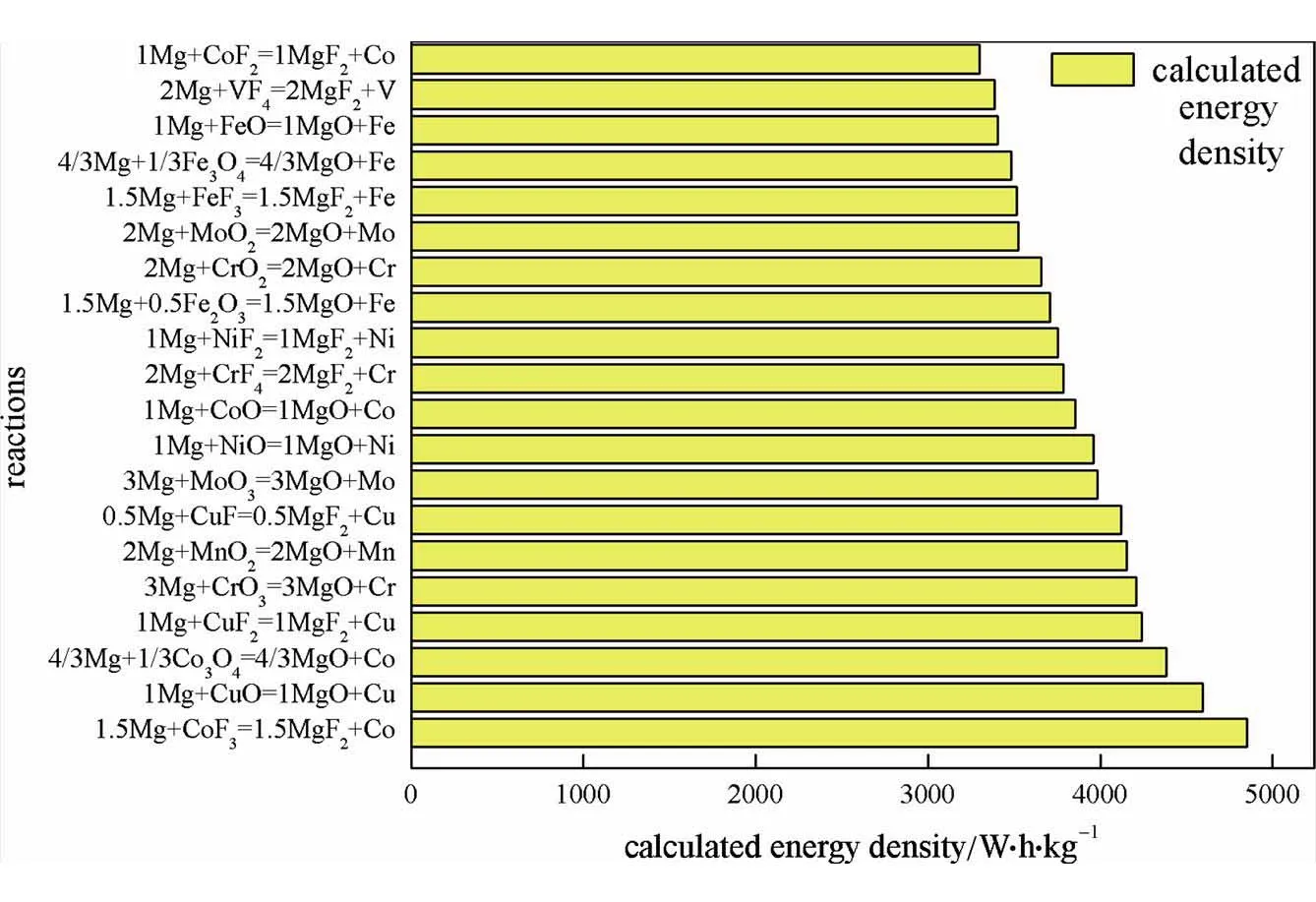
图5 体积能量密度最高的20种镁离子过渡金属化合物正极
4.1节提到,商业化钴酸锂正极的质量能量密度约为518 W·h/kg,钴酸锂理论密度约为5.1 g/cm,据此计算理论体积能量密度约为2642 W·h/L。因此2642 W·h/L作为筛选阈值在表7和表8的基础上进行进一步优化,删去不符合体积能量密度指标的正极后得到表9和表10。
4.3 电压分析
考虑到电池输出电压是选取正极材料时的一个重要的指标,因此这里以碱性锌锰电池标称电压为界限,限定电压应该至少在1.5 V以上。
在表9、表10的基础上,删去不符合电压指标的正极后得到表11、表12。
4.4 环境友好性分析
考虑到氟化物不稳定,水解或者热解会产生剧毒和有腐蚀性的HF,因此氟化物很难应用于生产实践。图3,图4中出现了几种含Cr和Co的氧化物和氟化物。但是多半有毒,且对环境有较恶劣的影响,因此也不是环境友好的正极材料。V的氧化物多半有较强的毒性,不适合大规模工业化生产和应用。
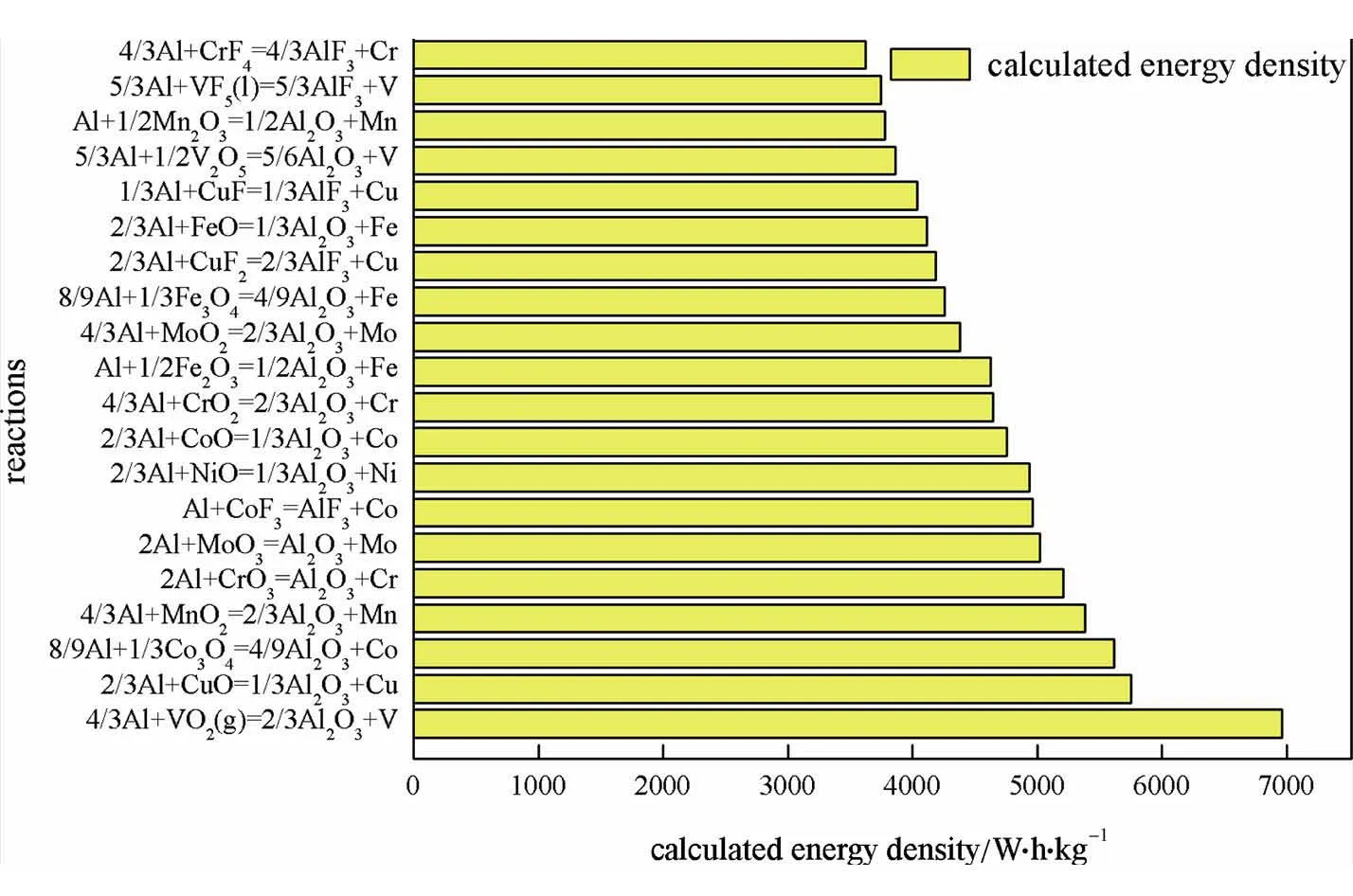
图6 体积能量密度最高的20种过渡金属化合物铝正极
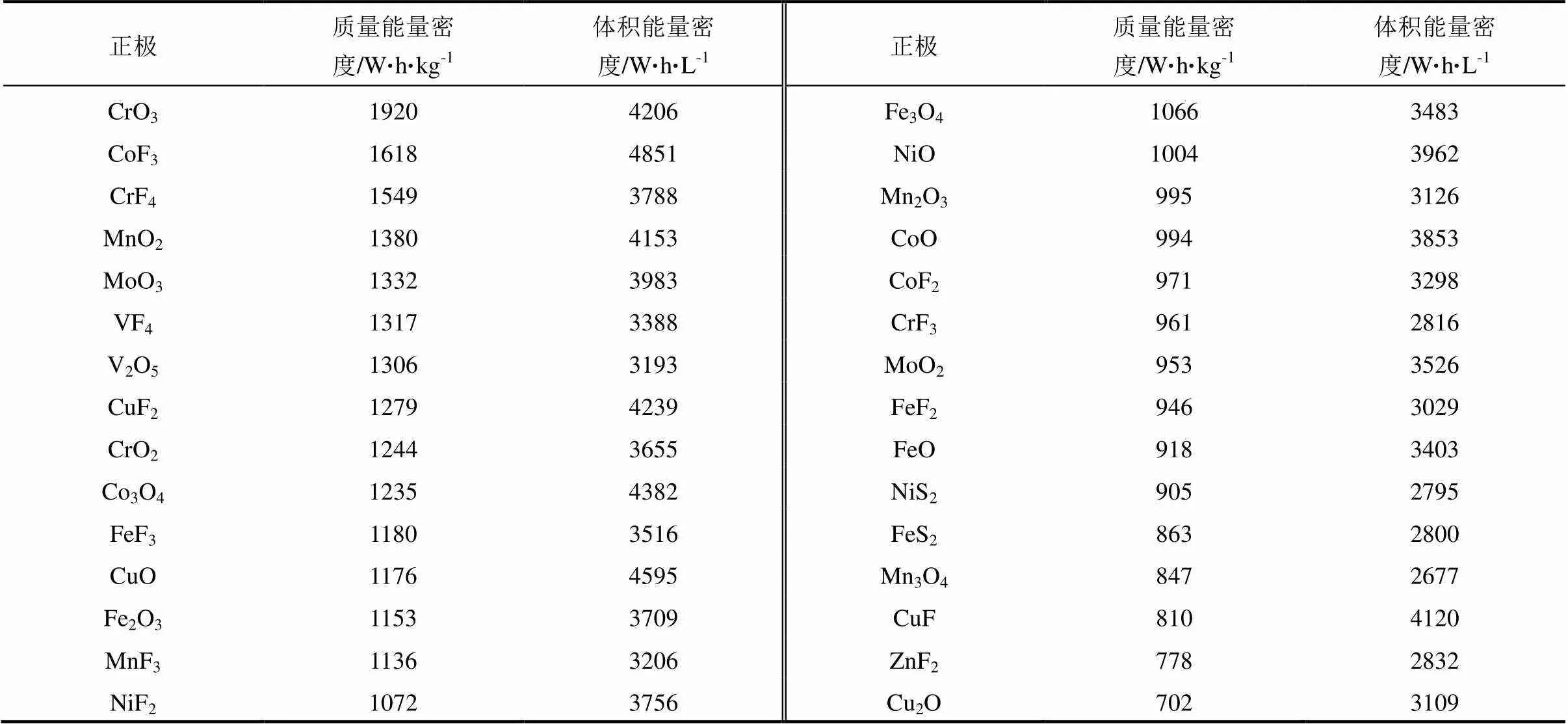
表9 质量能量密度超过518 W·h/kg、体积能量密度超过2642 W·h/L的过渡金属镁正极(30种)
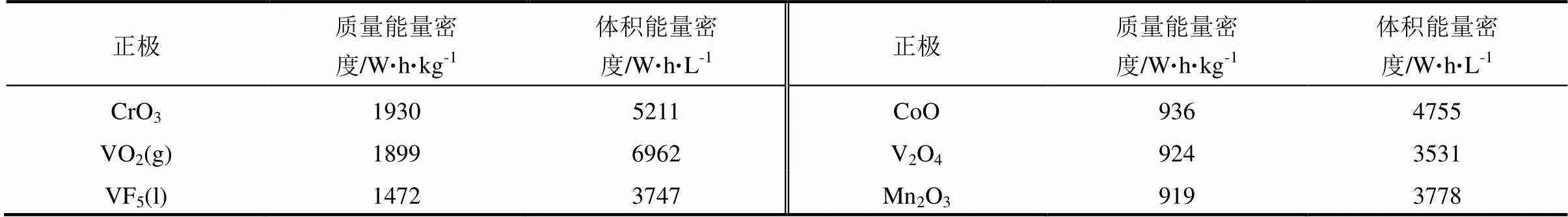
表10 质量能量密度超过518 W·h/kg、体积能量密度超过2642 W·h/L的过渡金属铝正极(32种)
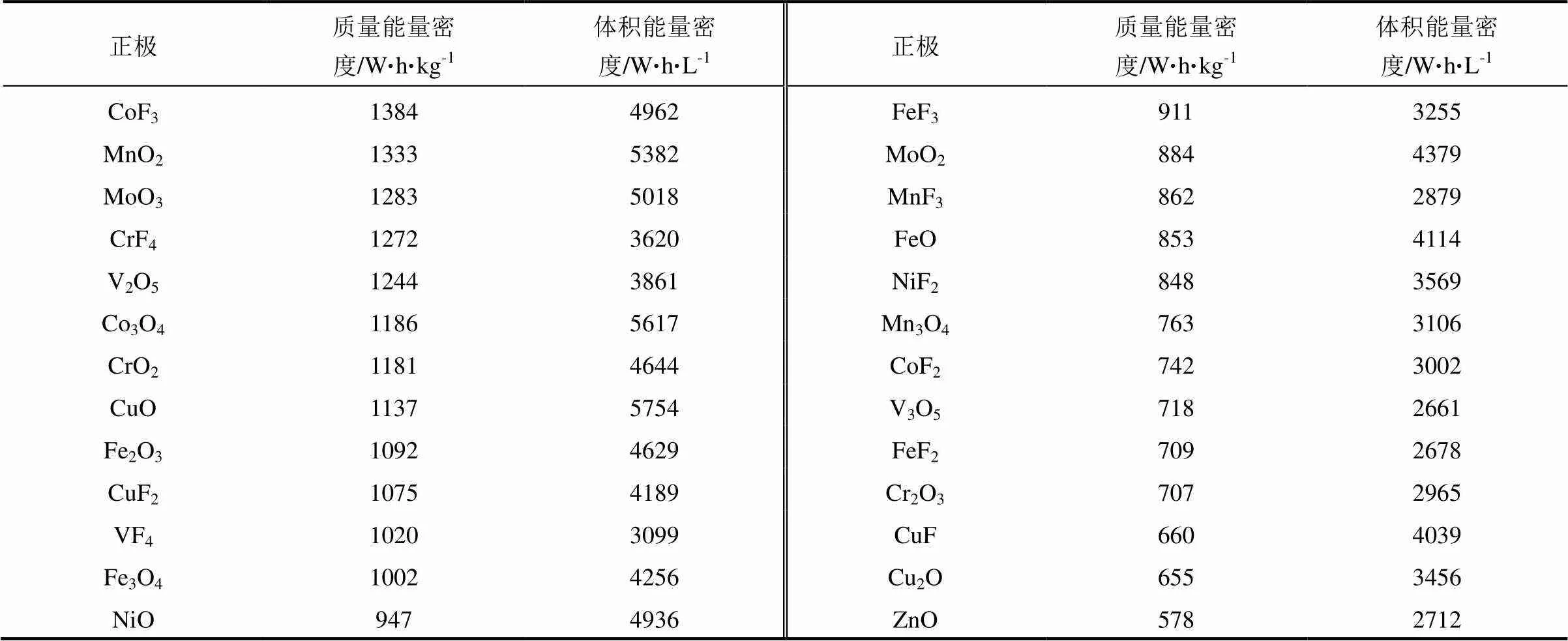
续表
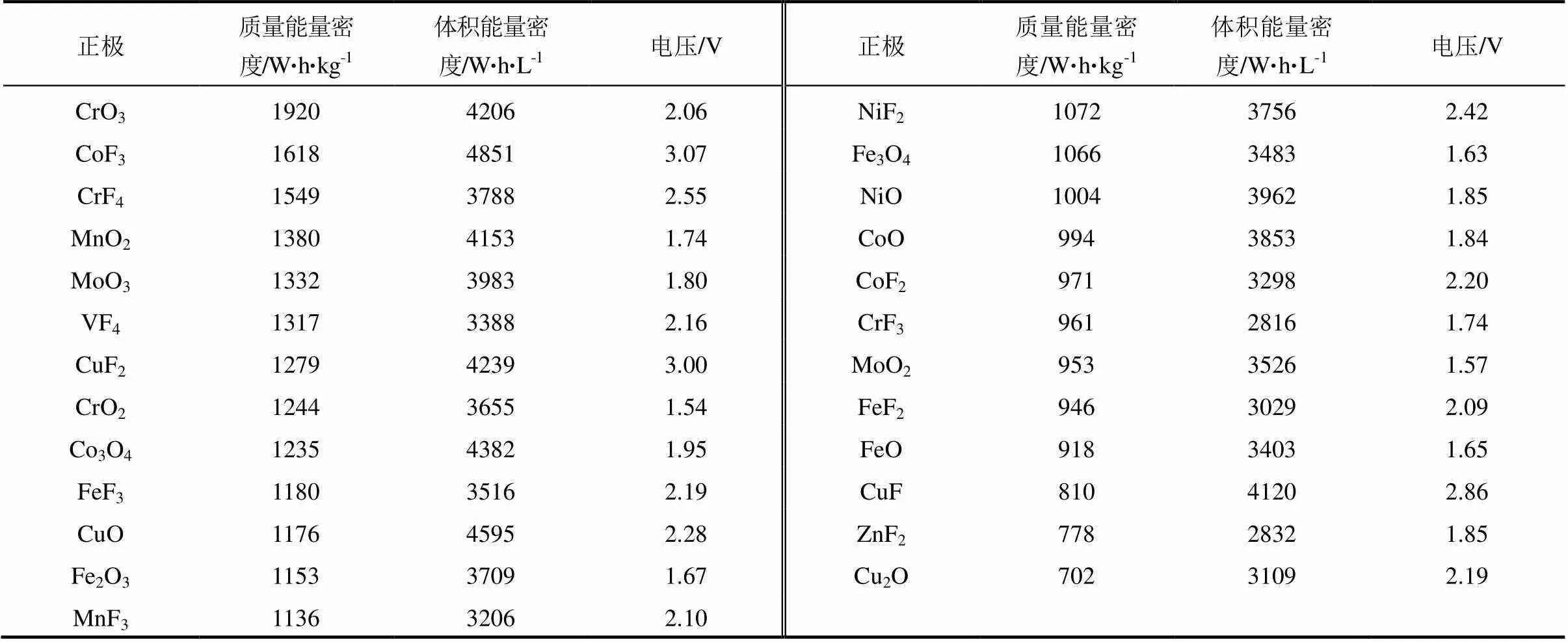
表11 质量能量密度超过518 W·h/kg、体积能量密度超过2642 W·h/L、电压大于1.5 V的镁离子正极(25种)

表12 质量能量密度超过518 W·h/kg、体积能量密度超过2642 W·h/L、电压超过1.5 V的铝离子正极(18种)
因此最终考虑在以上分析的基础上,加上对于环境友好性分析,得出高能量密度、高电压、环境友好的有潜力的镁离子、铝离子电池正极材料见表13、表14。

表13 质量能量密度超过518 W·h/kg、体积能量密度超过2642 W·h/L、电压超过1.5 V的环境友好镁离子正极材料(8种)

表14 质量能量密度超过518 W·h/kg、体积能量密度超过2642 W·h/L、电压超过1.5 V的环境友好铝离子正极材料 (5种)
4.5 理论容量与实际容量对比
对于镁离子电池,计算的100多种体系中,V2O5、MoO3、MnO2、Mn3O4、Mn2O3、Co3O4、MoS2、TiS2已经被作为正极材料做过一些研究。实验正极容量和理论正极容量的对比情况见表15。

表15 镁离子正极材料理论容量与实际容量对比
注:①K-α MnO2:钾稳定的α MnO2;②THF:四氢呋喃;③HMDSAlCl3:六甲基二硅叠氮化铝氯化物;④MMOITFSI:阳离子为1,2-二甲基-3-R-咪唑鎓与丁基,阴离子为双(三氟甲磺酰)酰亚胺的离子液体。
对于铝离子电池,计算的100多种体系中,V2O5、VO2、TiO2、FeS、FeS2、Cl2、S、Mo6S8、TiS2已经被作为正极材料做过一些研究。实验正极容量和理论正极容量的对比情况见表16。
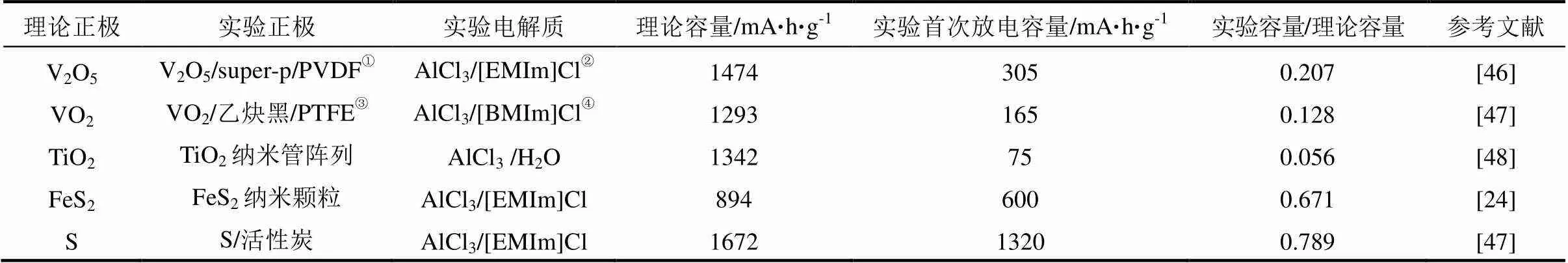
表16 铝离子正极材料理论比容量与实际比容量对比
注:①PVDF: 聚偏二氟乙烯;②[EMIm]Cl: 1-乙基-3-甲基咪唑鎓氯化物;③PTFE: 聚四氟乙烯;④[BMIm]Cl:1-丁基-3-甲基咪唑鎓氯化物。
5 结 语
近年,镁离子电池和铝离子电池作为一种绿色廉价的新型高能量密度二次电池体系被广泛关注,其相关研究热度正在逐年提高。热力学计算表明,在所有的研究体系中,F2、O2、ClF5作为正极的电池体系具有最高的理论质量能量密度,但综合考虑能量密度、电极电势、毒性、腐蚀性、易燃性以及环境友好性等因素,镁离子正极材料的范围被逐一缩小至O2、S、MnO2、MoO3、Fe2O3、Fe3O4、NiO、MoO2、CuO和Cu2O等;铝离子正极材料的范围被逐一缩小至O2、S、MnO2、MoO3、NiO、CuO和Cu2O。与此同时,需要指出的是本文单单只是从材料热力学角度出发计算了不同材料作为镁离子或铝离子正极的理论能量密度和电压,而并未考虑如果作为电极材料还需满足的其他因素,诸如电子电导、离子电导、电极与电解液界面问题以及负极SEI钝化膜等等因素的影响,以及由此产生的电解液兼容和适配性问题。因此,究竟何种材料会成为未来镁电池和铝电池正极材料还需要时间的检验,相信随着研究的不断深入在不久的将来会给出最终答案。
[1] WU CHUAN B Y, WU FENG, et al. Novel ternary metal boride Mg-Co-B alloys as anode materials for alkaline secondary batteries[J]. Electrochemistry Communications, 2009, 11(11): 2173-2176.
[2] 罗锐, 黄永鑫, 陈人杰, 吴锋. 基于多电子反应机制的高比能二次电池[C]// 第三届全国储能科学与技术大会, 2016.
LUO Rui, HUANG Yongxin, CHEN Renjie, WU Feng. Secondary battery with high specific energy based on multi-electron reaction mechanism[C]// Proceedings of the Third National Conference on Energy, 2016.
[3] 李泓, 许晓雄. 固态锂电池研发愿景和策略[J]. 储能科学与技术, 2016, 5(5): 607-614.
LI Hong, XU Xiaoxiong. R&D vision and strategies on lithium batteries[J]. Energy Storage Science and Technology, 2016, 5(5): 607-614.
[4] AURBACH D, LU Z, SCHECHTER A, et al. Prototype systems for rechargeable magnesium batteries[J]. Nature, 2000, 407(6805): 724-727.
[5] RANKIN W J. Minerals, metals and sustainability: Meeting future material needs[M]//PRESS C. Boca Raton, Fla. 2011.
[6] B SAHOO N C, A SAMANTARAY, P KUMAR. Inorganic chemistry[M]. PHI Learning, 2012.
[7] HARRIS J. Nature's building blocks: an A-Z guide to the elements[J]. Interdisciplinary Science Reviews, 2002, 27(1): 79-80.
[8] 郑育培, 努丽燕娜, 杨军, 陈强, 王久林. 可充镁电池正极材料研究进展[J]. 化工进展, 2011, 30(5): 1024-1032.
ZHENG Yupei, NULI Yanna, YANG Jun, et al. Research progress of cathode materials for rechargeable magnesium batteries[J]. Chemical Industry and Engineering Progress, 2011, 30(5): 1024-1032.
[9] 马正青, 左列, 庞旭, 曾苏民. 铝电池研究进展[J]. 船电技术, 2008, 28(5): 257-261.
MA Zhengqing, ZUO Lie, PANG Xu, et al. Advance in Aluminum Batteries[J]. Ship Electricity Technology, 2008, 28(5): 257-261.
[10] NOVAK P, DESILVESTRO J. Electrochemical insertion of magnesium in metal oxides and sulfides from aprotic electrolytes[J]. J. Electrochem. Soc., 1993, 140(1): 140-144.
[11] BRUCE P G, KROK F, NOWINSKI J, et al. Chemical intercalation of magnesium into solid hosts[J]. J. Mater. Chem., 1991, 1(4): 705-706.
[12] KUMAGAI N, KOMABA S, SAKAI H, et al. Preparation of todorokite-type manganese-based oxide and its application as lithium and magnesium rechargeable battery cathode[J]. Journal of Power Sources, 2001, 97/98: 515-517.
[13] GREGORY T D, HOFFMAN R J, WINTERTON R C. Nonaqueous electrochemistry of magnesium-applications to energy-storage[J]. J. Electrochem. Soc., 1990, 137(3): 775-780.
[14] LI X L, LI Y D. MoS2nanostructures: Synthesis and electrochemical Mg2+intercalation[J]. J. Phys. Chem. B, 2004, 108(37): 13893-13900.
[15] MAKINO K, KATAYAMA Y, MIURA T, et al. Electrochemical insertion of magnesium to Mg0.5Ti2(PO4)3[J]. Journal of Power Sources, 2001, 99(1-2): 66-69.
[16] FENG Z, YANG J, NULI Y, et al. Sol-gel synthesis of Mg1.03Mn0.97SiO4and its electrochemical intercalation behavior[J]. Journal of Power Sources, 2008, 184(2): 604-609.
[17] WANG R Y, WESSELLS C D, HUGGINS R A, et al. Highly reversible open framework nanoscale electrodes for divalent ion batteries[J]. Nano Letters, 2013, 13(11): 5748-5752.
[18] NULI Y, GUO Z, LIU H, et al. A new class of cathode materials for rechargeable magnesium batteries: Organosulfur compounds based on sulfur-sulfur bonds[J]. Electrochemistry Communications, 2007, 9(8): 1913-1917.
[19] GIRAUDET J, CLAVES D, GUERIN K, et al. Magnesium batteries: Towards a first use of graphite fluorides[J]. Journal of Power Sources, 2007, 173(1): 592-598.
[20] REED L D, MENKE E. The roles of V2O5and stainless steel in rechargeable Al-ion batteries[J]. J. Electrochem. Soc., 2013, 160(6): A915-A917.
[21] KULISH V V, MANZHOS, S. Comparison of Li, Na, Mg and Al-ion insertion in vanadium pentoxides and vanadium dioxides[J]. RSC Adv., 2017, 7(30): 18643-18649.
[22] LIU S, HU J J, YAN N F, et al. Aluminum storage behavior of anatase TiO2nanotube arrays in aqueous solution for aluminum ion batteries[J]. Energy & Environmental Science, 2012, 5(12): 9743-9746.
[23] JURAN T R, SMEU M. Hybrid density functional theory modeling of Ca, Zn, and Al ion batteries using the Chevrel phase Mo6S8cathode[J]. Phys. Chem. Chem. Phys., 2017, 19(31): 20684-20690.
[24] MORI T, ORIKASA Y, NAKANISHI K, et al. Discharge/charge reaction mechanisms of FeS2cathode material for aluminum rechargeable batteries at 55 degrees C[J]. Journal of Power Sources, 2016, 313: 9-14.
[25] PHILLIPS J, GIBBARD H F. Thermodynamics of Li(Al)-FeS battery system[J]. J. Electrochem. Soc., 1978, 125(8): C369.
[26] LIU S, PAN G L, LI G R, et al. Copper hexacyanoferrate nanoparticles as cathode material for aqueous Al-ion batteries[J]. J. Mater. Chem. A, 2015, 3(3): 959-962.
[27] XU J T, DOU Y H, WEI Z X, et al. Recent progress in graphite intercalation compounds for rechargeable metal (Li, Na, K, Al)-ion batteries[J]. Adv. Sci., 2017, 4(10): 14.
[28] RANI J V, KANAKAIAH V, DADMAL T, et al. Fluorinated natural graphite cathode for rechargeable ionic liquid based aluminum-ion battery[J]. J. Electrochem. Soc., 2013, 160(10): A1781-A1784.
[29] HUDAK N S. Chloroaluminate-doped conducting polymers as positive electrodes in rechargeable aluminum batteries[J]. J. Phys. Chem. C, 2014, 118(10): 5203-5215.
[30] DONAHUE F M, MANCINI S E, SIMONSEN L. Secondary aluminum iron(III) chloride batteries with a low-temperature molten-salt electrolyte[J]. J. Appl. Electrochem., 1992, 22(3): 230-234.
[31] SUTO K, NAKATA A, MURAYAMA H, et al. Electrochemical properties of al/vanadium chloride batteries with AlCl3-1-ethyl-3-methylimidazolium chloride electrolyte[J]. J. Electrochem. Soc., 2016, 163(5): A742-A747.
[32] BRABSON G D, FANNIN A A, KING L A, et al. Prototype high-power density aluminum-chlorine battery[J]. J. Electrochem. Soc., 1973, 120(3): C85.
[33] GAO T, LI X G, WANG X W, et al. A rechargeable Al/S battery with an ionic-liquid electrolyte[J]. Angewandte Chemie-International Edition, 2016, 55(34): 9898-9901.
[34] ZU Chenxi, LI H. Thermodynamics analysis on energy densities of batteries[J]. Energy & Environmental Science, 2011, 4(8): 2614-2624.
[35] HAYNES W M. CRC handbook of chemistry and physics,97th edition[M]. Boca Raton: CRC Press, 2016-2017.
[36] JAMES G SPEIGHT. Lange's handbook of chemistry,16th edition[M]. New York: McGraw Hill, 2005.
[37] BARIN I. Thermochemical date of pure substances, 3rd edition[M]. New York: VCH publisher, 1995.
[38] National Institute of Standards and Technology (NIST)-JANAF Thermochemical Tables[DB/OL]. https://janaf.nist.gov/
[39] SMITH J G, NARUSE J, HIRAMATSU H, et al. Theoretical limiting potentials in Mg/O2batteries[J]. Chemistry of Materials, 2016, 28(5): 1390-1401.
[40] IMAMURA D, MIYAYAMA M. Characterization of magnesium- intercalated V2O5/carbon composites[J]. Solid State Ionics, 2003, 161(1-2): 173-180.
[41] 司玉昌, 孙文军, 王贺孔, 邓昌辉, 牟心红, 焦丽芳, 袁华堂. MoO3纳米材料的合成及电化学嵌镁性能研究[J]. 南开大学学报(自然科学版), 2010, 43(6): 5-8.
SI Yuchang, SUN Wenjun, WANG Hekong, et al. Synthesis and Electrochemical insertion of magnesium in MoO3nanomaterials[J]. Acta Scientiarum Naturalium Universitatis Nankaiensis(Natural Science Edition), 2010, 43(6): 5-8.
[42] ARTHUR T S, ZHANG R G, LING C, et al. Understanding the electrochemical mechanism of K-alpha MnO2for magnesium battery cathodes[J]. ACS Appl. Mater. Interfaces, 2014, 6(10): 7004-7008.
[43] WANG L, ASHEIM K, VULLUM P E, et al. Sponge-like porous manganese(II,III) oxide as a highly efficient cathode material for rechargeable magnesium ion batteries[J]. Chemistry of Materials, 2016, 28(18): 6459-6470.
[44] SUTTO T E, DUNCAN T T. Electrochemical and structural characterization of Mg ion intercalation into Co3O4using ionic liquid electrolytes[J]. Electrochim Acta, 2012, 80: 413-417.
[45] LIU Y C, JIAO L F, WU Q, et al. Synthesis of rGO-supported layered MoS2for high-performance rechargeable Mg batteries[J]. Nanoscale, 2013, 5(20): 9562-9567.
[46] JAYAPRAKASH N, DAS S K, ARCHER L A. The rechargeable aluminum-ion battery[J]. Chem. Commun., 2011, 47(47): 12610-12612.
[47] DAS S K, MAHAPATRA S, LAHAN H. Aluminium-ion batteries: Developments and challenges[J]. J. Mater. Chem. A, 2017, 5(14): 6347-6367.
[48] LIU Y, SANG S, WU Q, et al. The electrochemical behavior of Cl-assisted Al3+insertion into titanium dioxide nanotube arrays in aqueous solution for aluminum ion batteries[J]. Electrochim Acta, 2014, 143: 340-346.
Thermodynamic calculation on energy densities of multi-electron transfer Mg/Al batteries
CAO Wenzhuo1,2, WANG Junyang1,2, CHEN Rusong1,2, SUO Liumin1,2, LI Hong1,2
(1Institute of Physics, Chinese Academy of Sciences, Beijing 100190, China;2University of Chinese Academy of Sciences, Beijing 100049,China)
Magnesium (Mg) ion batteries and aluminum (Al) ion batteries have become new hot spots in beyond lithium ion batteries due to their high energy densities, abundant reserves as well as safety. In this work, the theoretical gravimetric energy densities (GED), volumetric energy densities (VED) and output voltage (OV) of nearly 300 electrochemical couples of Mg/Al ion batteries are calculated by thermodynamic method. As our evaluation, considering of gravimetric energy density, volumetric energy density, output voltage, toxicity, corrosion, flammability and environmental friendliness and so on, a series of materials are screened out as promising candidates including Mg ion cathodes (O2, S, MnO2, MoO3, Fe2O3, Fe3O4, NiO, MoO2, CuO and Cu2O) and Al ion cathodes (O2, S, MnO2, MoO3, NiO, CuO and Cu2O).
magnesium ion batteries; aluminum ion batteries; gravimetric energy density; volumetric energy density; cathode
10.12028/j.issn.2095-4239.2018.0063
O 646.21
A
2095-4239(2018)03-0437-13
2018-04-01;
2018-04-13。
曹文卓(1995—),女,硕士研究生,研究方向为固态锂电池,E-mail:caowenzhuo17@mails.ucas.ac.cn;
李泓,研究员,研究方向为锂电池和固态离子学,E-mail:hli@iphy.ac.cn。

