5-氮杂-2-脱氧胞苷及曲古抑菌素A对人胃癌SNU-1细胞系中DLC-1基因启动子甲基化及mRNA表达的影响
贾 皑,秦 洁,任 莉,范修德
西安交通大学第一附属医院 1.消化内科; 2.感染科,陕西 西安 710061
胃癌的病因复杂,其发生、发展是一个多因素参与的多阶段复杂过程,抑癌基因启动子区甲基化成为胃癌发生、发展的早期事件。抑癌基因表达量减少是发生胃癌的关键性因素[1]。DLC-1基因是与胃癌相关的重要抑癌基因之一,DLC-1基因的缺失表达与胃癌的发生、发展有密切关系[2]。本实验选择抑癌基因DLC-1为研究靶点,以人胃癌SNU-1细胞株为研究对象,应用甲基化特异性聚合酶链式反应(methylation-specific-polymerase chain reaction, MSP)和实时荧光定量PCR的实验方法,分析5-Aza-dC和曲古抑菌素A (trichostatin A, TSA)对DLC-1基因在胃癌细胞SNU-1中的甲基化水平和mRNA表达的影响,为5-Aza-dC和TSA应用于胃癌的临床治疗提供新的线索。
1 材料与方法
1.1一般材料细胞株:人胃癌SNU-1细胞株购自ATCC库。5-Aza-dC、TSA(Sigma公司,美国)。基因组DNA提取试剂盒(OMEGA公司,美国)。重亚硫酸盐修饰试剂盒(MILLIPORE公司,美国)。RPMI 1640培养基干粉、胎牛血清(Gibco公司,美国);DMSO(北京索莱宝科技有限公司,中国)、引物合成(南京金斯瑞科技有限公司,中国);Tap Mix(热启动Taq酶)、6×DNA上样缓冲液、DNA marker、6×DNA上样缓冲液(北京天根生物科技有限公司,中国)。
1.2方法
1.2.1 细胞培养:人胃癌SNU-1细胞株用质量浓度为100 g/L的FBS血清RPMI 1640培养基置于37 ℃、体积分数为5%的CO2和95%湿度空气的恒温密闭式培养箱中贴壁培养。此细胞为单层贴壁细胞,每天观察细胞生长情况,根据培养液颜色变化,2~3 d更换1次培养液,等待细胞生长处于对数生长期时,予质量浓度为2.5 g/L的胰蛋白酶消化传代。
1.2.2 细胞株分组:采用体外培养的人胃癌SNU-1细胞系,将实验分成4组:(1)对照组:未加入任何药物。(2)5-Aza-dC组:加入浓度为5 μmol/L的5-Aza-dC培养液;(3)TSA组:加入浓度为300 nmol/L的TSA培养液;(4)5-Aza-dC+TSA组:向培养瓶内加入浓度为5 μmol/L的5-Aza-dC培养24 h后,再加入浓度为300 nmol/L的TSA培养液共同培养;以上每组细胞均培养72 h,每24 h更换1次培养液。
1.2.3 MSP:采用MSP方法检测以上各组药物干预72 h后人胃癌SNU-1细胞DLC-1基因启动子区甲基化状态。取对数生长期的细胞,以酚/氯仿法提取DNA,并对其行亚硫酸氢盐修饰,将修饰后的DNA用Wizard DNA clean-up Systerm纯化体系混匀、过柱,经脱盐、纯化回收,洗脱进50 μl的双蒸水中,脱去硫化基团,制备DNA。以修饰后的DNA为模板行MSP扩增(见表1),25 μl的扩增体系:DNA 200 ng,2 mmol/L NTP 1.5 μl,10×PCR缓冲液3 μl,25 mmol/L的MgCl22.4 μl,上下游引物各1 μl, 5 U/μl TaqDNA聚合酶12.5 μl,100倍SYBR Green I 0.1 μl,用ddH2O将总体积补齐至25 μl。条件为:95 ℃ 5 min; 然后以95 ℃ 30 s,55 ℃ 30 s,72 ℃ 30 s,扩增30个循环;72 ℃时延伸5 min。取PCR产物,用质量浓度为25 g/L的琼脂糖凝胶进行电泳,凝胶分析仪行拍照分析。

表1 甲基化特异性PCR引物Tab 1 Specific PCR primers for methylation
1.2.4 qPCR检测5-Aza-dC及TSA对人胃癌SNU-1细胞株DLC-1 mRNA表达的影响:采用qPCR方法检测以上各组药物干预72 h后人胃癌SNU-1细胞DLC-1基因mRNA表达水平。细胞总RNA提取及其qPCR法测定药物作用细胞后,常规收集细胞,并提取总RNA(按Trizol说明书操作)。进行反转录及PCR扩增。反转录体系为:67.2 ng RNA与1 μl Oligo(dT)混匀后,70 ℃处理5 min,立即冰浴,再加入2 μl 5×gDNA Eraser Buffer、1 μl gDNA Eraser、无RNA酶水补足体系至10 μl,5×PrimeScript×Buffer 2 4 μl、PrimeScript×RT Enzyme Mix 1 μl、混匀后37 ℃温育60 min。PCR反应体系为:SYBR Premix TaqTMⅡ(2×)12.5 μl,模板cDNA 2 μl,上下游引物各1 μl(10 μmol/L),去离子水补足至25 μl。PCR产物于质量浓度为20 g/L的琼脂糖凝胶电泳后观察,UVP凝胶成像仪摄像,其中DLC-1细胞为阳性对照,GAPDH为内参对照。用Quantity One 4.5.2图像分析软件分别读取SNU-1细胞和SNU-1细胞DLC-1及GAPDH的斑点密度扫描值,进行相对定量,实验重复3次。序列及扩增条件如表2所示。

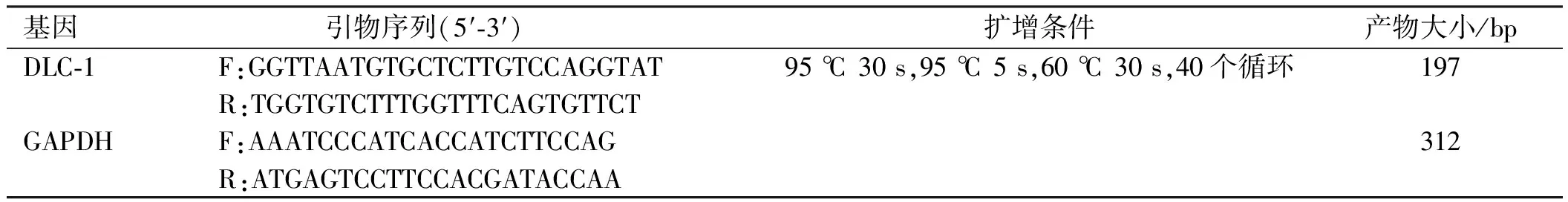
表2 qPCR引物设计Tab 2 Primer design for qPCR
2 结果
2.1MSP检测药物干预对DLC-1启动子甲基化水平的影响本实验经MSP检测胃癌细胞经过72 h药物干预后对DLC-1基因甲基的表达水平。以DLC-1基因组DNA为模板,经过MSP扩增后,产物琼脂糖凝胶电泳出现了以下3种甲基化状态(见图1),非甲基化:非甲基化产物中有目的条带,甲基化产物中无目的条带;半甲基化:甲基化产物和非甲基化产物同时出现目的条带;全甲基化:甲基化产物中出现目的条带,非甲基化产物中无目的条带。
在胃癌SNU-1细胞中,未加任何药物干预的对照组中DLC-1基因呈甲基化状态;经过5-Aza-dC药物干预后的胃癌细胞,DLC-1基因出现明显的非甲基化条带,甲基化条带亮度减弱;胃癌细胞经TSA作用后,条带无明显变化;胃癌细胞经过5-Aza-dC+TSA联合干预后,DLC-1基因甲基化条带明显减弱,并出现非甲基化条带。
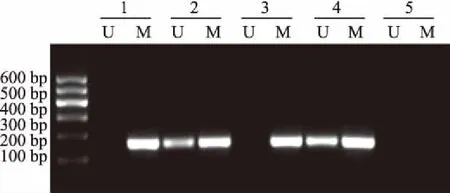
注:U:非甲基化引物;M:甲基化引物;1:对照组;2:5-Aza-dC
2.2qPCR检测药物干预对DLC-1mRNA水平的影响各组细胞中DLC-1基因mRNA相对表达量以对照组的mRNA水平作为1,其他三组加药细胞的mRNA表达量平均相对含量与对照组比较:5-Aza-dC组DLC-1 mRNA表达量是对照组的2.22倍,TSA组DLC-1 mRNA表达量是对照组的2.20倍,5-Aza-dC+TSA组DLC-1 mRNA表达量是对照组的4.50倍(见图2)。故5-Aza-dC、TSA、5-Aza-dC+TSA组DLC-1 mRNA相对表达量与对照组比较,差异有统计学意义(P<0.05);5-Aza-dC组、TSA组DLC-1 mRNA相对表达量与5-Aza-dC+TSA组比较,差异有统计学意义(P<0.05)。
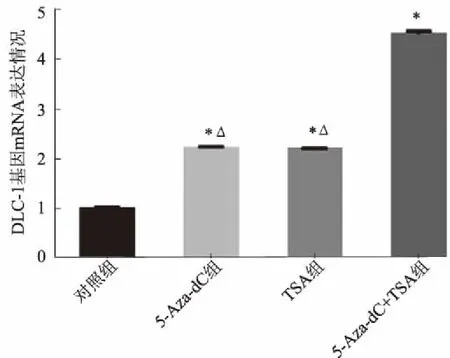
注:与对照组比较,*P<0.05; 与5-Aza-dC+TSA组比较,ΔP<0.05。
3 讨论
本实验所研究的DLC-1基因,全称为肝癌缺失基因,是YUAN等[3-4]对多种肝癌细胞系进行研究时分离得到的一种重要的抑癌基因。研究[5]表明,正常组织中DLC-1 mRNA均有表达,且启动子无甲基化,而胃癌组织中DLC-1 mRNA呈低表达或缺失表达,且甲基化率约为35.3%。DLC-1的启动子过甲基化与DLC-1 mRNA表达呈负相关,且DLC-1 mRNA表达缺失的胃癌组织均出现启动子区过甲基化。随着肿瘤组织分化程度降低而DLC-1 mRNA表达逐渐减弱,有淋巴结转移的胃癌组织DLC-1 mRNA呈明显低表达[6]。可见DLC-1作为一种抑癌基因,与肿瘤的分化及转移等有密切相关性。YUAN等[4,7-9]进一步证实了启动子区域的高甲基化可能导致肝脏、结直肠、前列腺、胃癌等多种肿瘤细胞系DLC-1基因的失活。
由于发现甲基化及乙酰化作用具有可逆性,目前各地学者们将以逆转基因甲基化及乙酰化状态作为治疗肿瘤新的切入点[10-12]。他们成功地将5-Aza-dC运用在乳腺癌、肺癌、前列腺癌等体外培养的肿瘤细胞株,逆转了Rb、VHL、p15、p16、E-cadherin等多个抑癌基因启动子区甲基化状态,使原本沉默的抑癌基因重新表达,进而有效地抑制了肿瘤的发生、发展[13-15]。研究[4]显示,缺失DLC-1 mRNA表达的细胞系给予5-Aza-dC后DLC-1 mRNA表达明显增强,且肿瘤细胞的生长受到明显抑制,转入裸鼠体内其致瘤性也明显降低。而组蛋白去乙酰化酶抑制剂—TSA,可以恢复组蛋白乙酰化水平,对染色质结构进行修饰,有效上调抑癌基因的表达,诱导肿瘤细胞分化,阻滞肿瘤生长、细胞周期和选择性凋亡,从而抑制多种肿瘤细胞的生长,TSA目前已应用于皮肤T淋巴细胞瘤和血液系统等恶性肿瘤中[16-17]。
KIM等[18]研究发现,5-Aza-dC及TSA单独或联合对人胃癌细胞有明显的抑制作用,为了证实本实验中5-Aza-dC及TSA单独或联合对人胃癌细胞SNU-1细胞的抑制作用与DLC-1基因表达上调有关,我们采用MSP及免疫荧光PCR检测5-Aza-dC及TSA处理DLC-1启动子区CpG岛去甲基化及mRNA表达情况。实验发现,胃癌SNU-1细胞株启动子区CpG岛为甲基化状态,经过药物干预72 h后,5-Aza-dC能逆转DLC-1启动子的甲基化状态,使因甲基化转录沉默的DLC-1基因恢复转录活性,其mRNA得以重新表达,从而发挥DLC-1的肿瘤抑制作用。而TSA对启动子区甲基化作用无明显影响,其mRNA表达量升高,可能与TSA恢复组蛋白乙酰化或通过甲基化结合蛋白乙酰化,从而使转录失活的抑癌基因DLC-1基因mRNA重新表达。经MSP检测后,5-Az-dC+TSA联合用药与单药5-Aza-dC作用相似,可以逆转DLC-1基因启动子区CpG岛的甲基化状态;而在免疫荧光PCR中,5-Aza-dC+TSA联合用药较5-Aza-dC单药作用强,DLC-1基因mRNA表达量明显升高,二者联合具有协同作用,可能与DNA去甲基化、组蛋白乙酰化通过甲基化结合蛋白相互作用有关。
总之,胃癌细胞的抑癌基因启动子区甲基化异常的现象较为普遍,5-Aza-dC及TSA药物主要针对整个基因组,而非某一个特定基因。药物干预后可逆转基因启动子区异常甲基化,使其重新表达进而发挥抑癌基因的作用。DLC-1基因在胃癌SNU-1细胞系内存在异常甲基化的现象,影响了该基因的正常表达,通过5-Aza-dC及TSA干预后逆转胃癌细胞系DLC-1基因启动区异常甲基化,提高了其mRNA表达量,发挥抑癌作用。两药物联合使用后起到协同作用,增强了单药的药效,为5-Aza-dC及TSA应用于临床提供了实验基础。
[1] WATANABE Y, KIM H S, CASTORO R J, et al. Sensitive and specific detection of early gastric cancer with DNA methylation analysis of gastric washes [J]. Gastroenterology, 2009, 136(7): 2149-2158. DOI: 10.1053/j.gastro.2009.02.085.
[2] LIU J B, WU X M, CAI J, et al. CpG island methylator phenotype and Helicobacter pylori infection associated with gastric cancer [J]. World J Gastroenterol, 2012, 18(36): 5129-5134. DOI: 10.3748/wjg.v18.i36.5129.
[3] LIU X, PAN Y J, ZHENG J N, et al. The role of tumor suppressor DLC-1: far from clear [J]. Anticancer Agents Med Chem, 2017, 17(7): 896-901. DOI: 10.2174/1871520616666160907142754.
[4] YUAN B Z, DURKIN M E, POPESCU N C. Promoter hypermethylation of DLC-1, a candidate tumor suppressor gene, in several common human cancers [J]. Cancer Genet Cytogenet, 2003, 140(2): 113-117.
[5] HE D, ZHANG Y W, ZHANG N N, et al. Aberrant gene promoter methylation of p16, FHIT, CRBP1, WWOX, and DLC-1 in Epstein-Barr virus-associated gastric carcinomas [J]. Med Oncol, 2015, 32(4): 92. DOI: 10.1007/s12032-015-0525-y.
[6] KIM T Y, JONG H S, SONG S H, et al. Transcriptional silencing of the DLC-1 tumor suppressor gene by epigenetic mechanism in gastric cancer cells [J].Oncogene, 2003, 22(25): 3943-3951. DOI: 10.1038/sj.onc.1206573.
[7] 喻军, 齐健, 李梦颖, 等. SFRP1基因启动子甲基化和肝细胞癌关系的Meta分析[J]. 胃肠病学和肝病学杂志, 2017, 26(4): 376-380. DOI: 10.3969/j.issn.10065709.2017.04.005.
YU J, QI J, LI M Y, et al. SFRP1 gene hypermethylation and hepatocellular carcinoma: a Meta-analysis [J]. Chin J Gastroenterol Hepatol, 2017, 26(4): 376-380. DOI: 10.3969/j.issn.10065709.2017.04.005.
[8] JIANG Y, LI J M, LUO H Q. Clinicopathological significance of DLC-1 expression in cancer: a Meta-analysis [J]. Asian Pac J Cancer Prev, 2015, 16(16): 7255-7260.
[9] 孟莹, 朱圣韬, 李鹏, 等. 启动子区甲基化和组蛋白乙酰化对人食管鳞癌细胞SFRP1基因表达的影响[J]. 胃肠病学和肝病学杂志, 2015, 24(5): 506-509. DOI: 10.3969/j.issn.10065709.2015.05.005.
MENG Y, ZHU S T, LI P, et al. Effects of histone acetylation and promoter methylation on SFRP1 expression in human esophageal squamous cell carcinoma cells [J]. Chin J Gastroenterol Hepatol, 2015, 24(5): 506-509. DOI: 10.3969/j.issn.10065709.2015.05.005.
[10] CHOI S J, JUNG S W, HUH S, et al. Alteration of DNA mythylation in gastric cancer with chemotherapy [J]. J Microbiol Biotechnol, 2017, 27(8): 1367-1378. DOI: 10.4014/jmb.1704.04035.
[11] RONNEKLEIV-KELLY S M, SHARMA A, AHUJA N. Epigenetic therapy and chemosensitization in solid malignancy [J]. Cancer Treat Rev, 2017, 55: 200-208. DOI: 10.1016/j.ctrv.2017.03.008.
[12] BIAN X, LIANG Z, FENG A, et al. HDAC inhibitor suppresses proliferation and invasion of breast cancer cells through regulation of miR-200c targeting CRKL [J]. Biochem Pharmacol, 2018, 147: 30-37. DOI: 10.1016/j.bcp.2017.11.008.
[13] GUO S, LIU M, GODWIN A K. Transcriptional regulation of hTREX84 in human cancer cells [J]. PLoS One, 2012, 7(8): e43610. DOI: 10.1371/journal.pone.0043610.
[14] RONNEKLEIV-KELLY S M, SHARMA A, AHUJA N. Epigenetic therapy and chemosensitization in solid malignancy [J]. Cancer Treat Rev, 2017, 55: 200-208. DOI: 10.1016/j.ctrv.2017.03.008.
[15] FIALOVA B, LUZNA P, GURSKY J, et al. Epigenetic modulation of AR gene expression in prostate cancer DU145 cells with the combination of sodium butyrate and 5′-Aza-2′-deoxycytidine [J]. Oncol Rep, 2016, 36(4): 2365-2374. DOI: 10.3892/or.2016.5000.
[16] ECKSCHLAGER T, PLCH J, STIBOROVA M, et al. Histone deacetylase inhibitors as anticancer drugs [J]. Int J Mol Sci, 2017, 18(7). pii: E1414. DOI: 10.3390/ijms18071414.
[17] 何滔, 郭明洲. 表观遗传结合免疫治疗—肿瘤治疗的新策略[J]. 胃肠病学和肝病学杂志, 2017, 26(4): 361-364. DOI: 10.3969/j.issn.10065709.2017.04.001.
HE T, GUO M Z. Epigenetic therapy combined with immunotherapy: a novel strategy for cancer therapy [J]. Chin J Gastroenterol Hepatol, 2017, 26(4): 361-364. DOI: 10.3969/j.issn.10065709.2017.04.001.
[18] KIM J, MIN S Y, LEE H E, et al. Aberrant DNA methylation and tumor suppressive activity of the EBF3 gene in gastric carcinoma [J]. Int J Cancer, 2012, 130(4): 817-826. DOI: 10.1002/ijc.26038.

