一种正压式防护口罩对微生物气溶胶防护效果的研究
张柯,胡凌飞,靳爱军,李劲松,曹杰,李娜,李光熙
近年来,众多医务人员和病原微生物实验室的工作人员面临着流感、SARS、结核等经空气传播的微生物感染的威胁[1-3],佩戴防护口罩能够阻断病原微生物侵入人体,是预防呼吸道传染病的流行、保护人员健康的有效手段。根据国内外相关标准,评价防护口罩性能的一个重要参数是对微生物颗粒的过滤效率。目前,随着电子技术和超高滤网技术的发展,颗粒过滤效率为 99.99% 以上的防护口罩被研制面世,用来应对愈发频繁的高危生物污染环境作业。本文对一种高效正压式防护口罩对细菌和病毒气溶胶的过滤效率进行测试,以检验其对微生物气溶胶的防护效果。
1 材料与方法
1.1 材料
1.1.1 研究对象 正压式防护口罩由主机、空气软管和面罩组成,主机通过 USB 线缆进行充电,配备一个手持遥控器,控制主机的运行。主机设置三个气流速度,分别为 100、120 和 180 L/min。机器开启后,外部环境空气在风扇的带动下,通过主机内的主过滤器,将洁净空气经过空气软管送入面罩内。主过滤器采用超高效率空气过滤网(ULPA),滤网总面积为 0.3 m2,能够过滤最小直径为 10 nm 的颗粒物。
该正压式防护口罩与通过过滤器阻力呼吸的被动式面罩不同,采用产生正气压的“主动式”过滤技术,环境中的空气经由预过滤滤芯,滤除毛发以及颗粒杂质、灰尘后,进入强力推进的全密闭的风道,气流携带的超微颗粒物质被主过滤滤芯拦截,可以去除空气中的 PM2.5 和细菌、病毒等生物气溶胶。该口罩的主机尺寸为 26.5 cm × 19 cm ×5.5 cm,重量约为 1.7 kg,标称的过滤效率是对小至 10 nm 的颗粒物能够达到 99.9999% 以上,由北京泓兴浩杨科技有限公司研制。
1.1.2 菌株 选择粘质沙雷菌(ATCC 8039)为细菌的替代物;选择噬箘体 ΦX174(ATCCl3706-B1)为病毒的替代物,大肠杆菌(ATCCl3706)为其宿主菌。
1.1.3 试验仪器 头部模型、Andersen 六级空气微生物采样器由军事医学科学院微生物流行病研究所提供;MS-I 多功能空气微生物采样器购自青岛众瑞智能仪器有限公司;Φ90 一次性培养皿、APS 3321 空气动力学粒子分析仪均购自美国 TSI公司;气溶胶发生装置包括气溶胶密闭舱室、洁净气源系统(由空压机、除湿机、除油机、多级空气净化器和流量计组成)和气溶胶发生器 Collision250购自美国 BGI 公司。
1.1.4 主要试剂 普通营养琼脂培养基、普通营养肉汤为美国 BD 公司产品;上层琼脂培养基为上海根生生物科技有限公司产品。
1.2 方法
1.2.1 悬液制备 粘质沙雷菌和噬箘体 ΦX174的悬液制备参考文献[4-5]中的方法进行。
1.2.2 防护效果测试 在气溶胶密闭舱室中,将正压式防护口罩戴在头部模型上,用三通将头部模型鼻腔部位的抽气管道与 Andersen 六级采样器和 APS 3321 的进气口连接,以便采集口罩与面部形成的口罩内腔中的微生物气溶胶和气溶胶粒子;同时,在佩戴正压式防护口罩的头部模型旁 10 cm处放置采样胶管,将其另一端与 Andersen 六级采样器和 APS 3321 连接,采集密闭舱室中的口罩外部微生物气溶胶和总气溶胶粒子。气溶胶发生器固定于头部模型前上方发生生物气溶胶粒子,测试装置如图 1 所示。
关闭密闭舱室柜门,将正压式防护口罩主机风速调至 100 L/min,以 10 L/min 的气体流量发生微生物气溶胶,同时向舱室内补充洁净空气,待气溶胶发生 5 min 后,用 APS 3321 分别测试气溶胶密闭舱室内的总粒子浓度和口罩内腔中的总粒子浓度,然后同时开启两个 Andersen 六级采样器,采样流量为 28.3 L/min,气溶胶密闭舱室中的气溶胶采样时间为 0.5 min,口罩内腔采样时间为 5 min。关闭发生器并开启空气净化装置,待气溶胶密闭舱室内空气洁净后重复上述步骤依次做 3 组测试。改变正压式防护口罩主机风速,分别调至 120 L/min和 180 L/min,重复上述实验步骤。
采样结束后取出平皿,粘质沙雷菌放入 30 ℃温箱培养 24 h,获得每个平皿上存活的粘质沙雷菌菌落数 CFU。噬箘体 ΦX174 的采样平皿取出后,倒入上层宿主菌悬液,利用双层营养琼脂平板培养计数法获得噬菌体噬菌斑数 PFU。
1.2.3 结果计算
1.2.3.1 微生物气溶胶粒子数量中值直径的计算 根据 Andersen 六级采样器各级平皿上的菌落数(噬菌斑数),按照偏态分布 50% 中值直径的计算公式进行计算。具体算法是依据 Andersen 六级采样器每一级捕获的粒子大小不同,第一级 〉 7 μm、第二级为 4.8 ~ 7 μm、第三级为 3.4 ~ 4.7 μm、第四级为 2.1 ~ 3.3 μm、第五级为 1.1 ~ 2.0 μm、第六级为 0.6 ~ 1.0 μm,把六级采样器捕获的粒子作为 6 组大小不同数据,计算公式为:数量中值直径 P50= L +(i/f)(50%n – C)。公式中 L 为累计频数中值的组距下限;i 为累计频数中值的组距;f为累计频数中值的粒子数;50%n 为累计频数中值所在组的累计频数;C 为累计频数中值[6-7]。
图1 正压式防护口罩测试装置示意图Figure 1 Schematic diagram of test device for a positive pressure protective mask
1.2.3.2 防护效率的计算
按照 ⑴ 计算正压式防护口罩对气溶胶总粒子的防护效率。

式中:ηB是正压式防护口罩对气溶胶总粒子的防护效率;CTin是 APS 3321 检测到的口罩内腔中的气溶胶总粒子浓度;CT是 APS 3321 检测到的气溶胶密闭舱室中的气溶胶总粒子浓度。
按照 ⑵ 计算正压防护口罩对微生物气溶胶的防护效率。

式中:ηS是正压式防护口罩对微生物气溶胶粒子的防护效率;CAin是 Andersen 六级采样器检测到的口罩内腔中的微生物气溶胶粒子浓度;CA是Andersen 六级采样器检测到的气溶胶密闭舱室中的微生物气溶胶粒子浓度。
1.3 统计学处理
统计软件采用 SPASS23.0,分析方法采用单因素方差分析,P< 0.05 认为具有统计学意义。

图2 粘质沙雷菌气溶胶总粒子的粒谱分布图Figure 2 Distribution of particle spectra of the total Serratia marcescens aerosol
2 结果
2.1 微生物气溶胶粒子的粒谱分布
APS 3321 空气动力学粒子分析仪测定的是空气中所有气溶胶粒子的浓度分布,粘质沙雷菌气溶胶总粒子的粒谱分布及累积浓度分布如图 2 和图 3所示,5 μm 以下的粒子占粒子总数的 78.5%;噬箘体 ΦX174 的气溶胶总粒子的粒谱分布及累积浓度分布分别如图 4 和图 5 所示,5 μm 以下的粒子占粒子总数的 93%,两种微生物气溶胶粒子的大小和浓度分布相似。
根据 Andersen 六级采样器采样结果,其气溶胶中值直径结果如表 1 所示,粘质沙雷菌和噬箘体 ΦX174 的粒子数量中值直径为 1.8 μm 左右。
2.2 正压式防护口罩对气溶胶总粒子的防护性能
口罩内腔中经过高效过滤器过滤后的气溶胶粒子通过 APS 3321 检测到的粒谱分布分别如图 6 和图 7 所示,与口罩外气溶胶总粒子浓度进行比较,得出该防护口罩对空气中的气溶胶总粒子的防护效率,结果如表 2 所示。APS 3321 检测到包含粘质沙雷菌和噬箘体 ΦX174 的气溶胶总粒子浓度达到 106个/L 数量级,正压式防护口罩对总粒子的防护效率基本上在 99% 以上。经统计学分析发现,气溶胶总粒子中含有的微生物粒子的种类对正压式防护口罩的防护效率没有影响(P=0.36)。

图3 粘质沙雷菌气溶胶总粒子的累积浓度分布图Figure 3 Distribution of particle cumulative concentration of the total Serratia marcescens aerosol

图4 噬箘体 ΦX174 气溶胶总粒子的粒谱分布图Figure 4 Distribution of particle spectra of the total phage ΦX174 aerosol
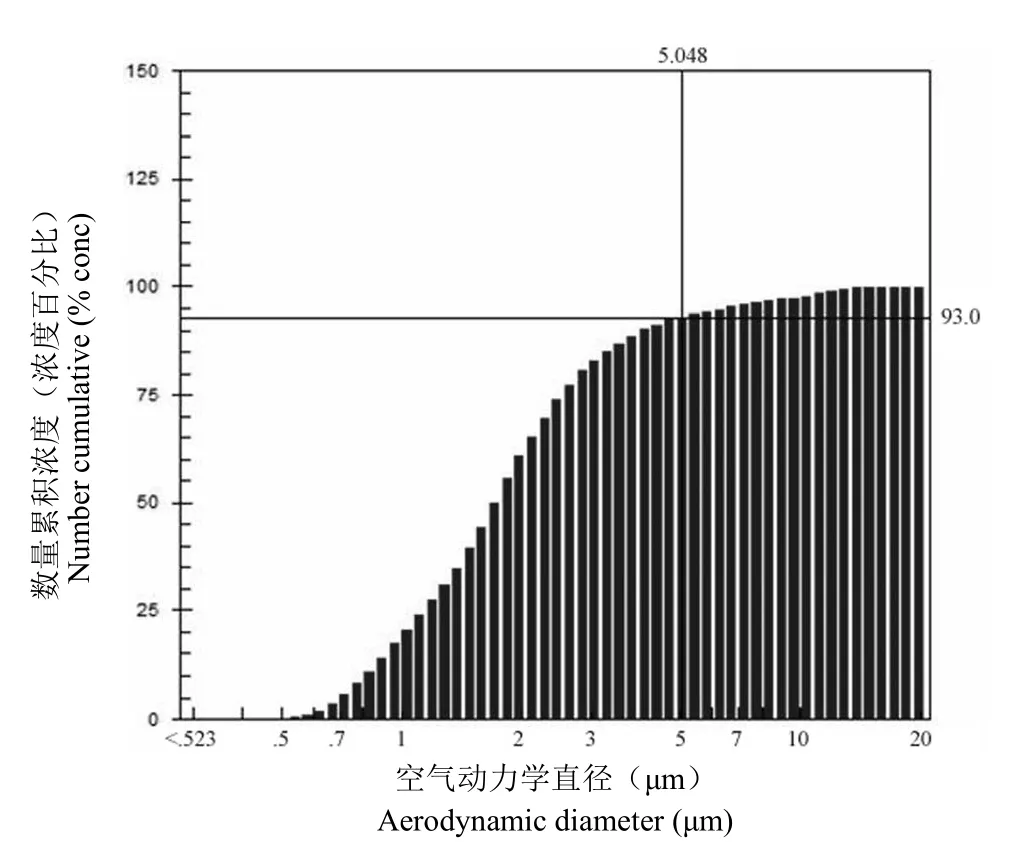
图5 噬箘体 ΦX174 气溶胶总粒子的累积浓度分布图Figure 5 Distribution of particle cumulative concentration of the total phage ΦX174 aerosol

表1 采样法计算测得的微生物气溶胶粒子直径Table 1 Diameter of aerosol calculated from sampling

图6 口罩内腔中粘质沙雷菌气溶胶粒子的粒谱分布图(CTin = 187 个/L)Figure 6 Distribution of particle spectra of the Serratia marcescens aerosol in the mask inner cavity (CTin =187 particles/L)
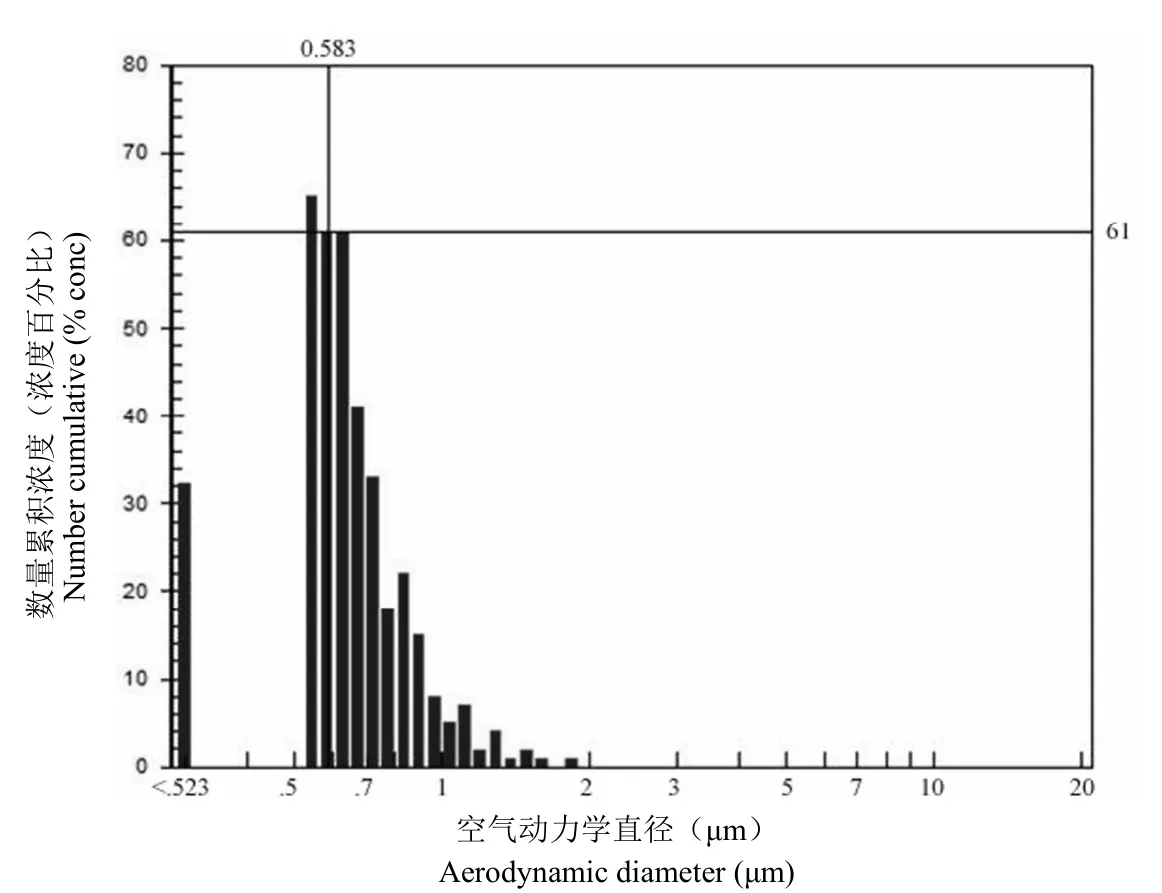
图7 口罩内腔中噬箘体 ΦX174 气溶胶粒子的粒谱分布图(CTin = 1264 个/L)Figure 7 Distribution of particle spectra of the phage ΦX174 aerosol in the mask inner cavity (CTin = 1264 particles/L)

表2 正压式防护口罩对气溶胶总粒子的防护效果Table 2 Protective efficiencies of positive pressure protective mask for total aerosol
表3 正压式防护口罩对微生物气溶胶的防护效率Table 3 Protective efficiencies of positive pressure protective mask for bioaerosol
2.3 正压式防护口罩对微生物气溶胶的防护效率
将 Andersen 六级采样器采样结果代入正压防护口罩对微生物气溶胶的防护效率计算公式 ⑵,结果如表 3 所示,口罩外部采集到的细菌和病毒气溶胶的浓度达到 105CFU/m3或 PFU/m3的数量级,远低于气溶胶总粒子浓度。在不同气流速度的送风量下,该正压式防护口罩对细菌和病毒气溶胶的防护效率有显著差异(对于粘质沙雷菌,F=113.58,P< 0.01,对于噬箘体 ΦX174,F= 28.24,P< 0.01),说明气流速度对微生物气溶胶的防护效率有影响,气流速度越大,口罩的防护效率越高。在 180 L/min 的送风气流下,口罩内腔中在 5 min内的微生物气溶胶浓度未能达到 Andersen 六级采样器能够采集到的最低浓度值,口罩对微生物气溶胶的防护效率高于 99.99%。
正压式防护口罩对气溶胶总粒子和对微生物气溶胶粒子的防护效率之间的差异不显著[F=0.43,P= 0.52(粘质沙雷菌);F= 3.04,P= 0.10(噬箘体 ΦX174)],对两种微生物气溶胶的防护效率也无显著差异(F= 0.16,P= 0.70)。
3 讨论
防护效率指在规定的气流速度下口罩滤料能够将气溶胶滤除的百分数,是口罩防护性能评价的重要指标之一。GB 19083-2010《医用防护口罩技术要求》以及 WSB 59-2003《自吸过滤式生物防护口罩通用规范》(中国人民解放军总后勤部卫生部标准)中规定口罩对空气动力学直径为 0.3 μm 颗粒防护效率大于 95%,对细菌气溶胶防护效率大于99%[8-9]。由于目前尚无针对正压式防护口罩的技术标准,检测参照医用防护口罩标准和生物防护口罩标准,该正压式防护口罩对细菌和病毒气溶胶的防护效率均满足标准要求。
该正压式防护口罩采用的是 ULPA 超高效空气过滤网,能够滤除小于或等于 0.1 μm 的超细颗粒,标称吸尘效率达到 99.99999% 以上,滤材对病毒过滤效率标称值为 99.9999% 或以上,本次实验结果与标称值差距较大。国内外对多个采用 N95过滤材料的医用防护口罩进行测试,防护效率均未达到标准值要求,最低值甚至才 23.200%[10],表明防护口罩的标称防护效率并不一定准确反映其实际防护效果[11]。口罩滤材的过滤效率测试是保证口罩合格的首要条件,但是滤材过滤效率高不能保证口罩佩戴时的实际防护效率也高,本次测试的分体式的防护口罩,滤材安装在主机上,其防护效果还与滤材的结构设计和安装以及整体的气密性有关系。该正压式防护口罩对细菌气溶胶和病毒气溶胶的防护效率都达到 99% 以上,且送风气流越大,防护效率越高,因此在保证人体佩戴舒适的前提下,在使用时尽量使用较高的送风气流。
利用微生物气溶胶评价防护装备的生物防护效率,能够真实地反映防护装备对微生物气溶胶粒子的防护效果[12-13],但是这种方法需要经过采样培养,耗时较长,对实验人员的实验技能具有较高的要求。空气动力学粒子分析仪 APS 3321 能够实时检测空气中气溶胶粒子的大小和浓度分布,本研究利用 APS 3321 检测所发生的微生物气溶胶总粒子的本底浓度,同时检测正压式防护口罩佩戴后内腔中的气溶胶粒子,利用粒子浓度比较的方式可以实时获得防护口罩对总粒子的防护效果,省时省力,检测结果与用 Andersen六级采样器采样得到的微生物气溶胶的防护效率没有显著差异,因此可以进一步研究用实时检测的方法来评价防护装备对微生物粒子的防护效果。
此外在评价口罩的实际防护效果时要考虑脸型密合度[14],由于个体差异,佩戴者的脸型也具有较大差异,口罩佩戴后与脸部之间如果达不到密合性要求,实际防护效果与标称值是不能等同的[15]。本次检测正压式防护口罩的防护效率,是佩戴在头部模型上,实验时尽可能将口罩与头部模型之间的缝隙密封,但还是存在密合性上的缺陷,造成测试结果上的差异。
[1] Chen JD, Yuan J, Yang ZC, et al. Investigation of first hospital infection event of H1N1 influenza in mainland. Chin J Nosocomiology,2010, 20(2):177-179. (in Chinese)陈建东, 袁俊, 杨智聪, 等. 国内首起甲型 H1N1流感医院感染暴发调查分析. 中华医院感染学杂志, 2010, 20(2):177-179.
[2] Pei LY, Gao ZC, Yang Z, et al. Investigation of the influencing factors on severe acute respiratory syndrome among health care workers.J Peking Univ (Health Sci), 2006, 38(3):271-275. (in Chinese)裴立英, 高占成, 杨震, 等. 医务人员感染严重急性呼吸综合征影响因素的调查研究. 北京大学学报(医学版), 2006, 38(3):271-275.
[3] Apisarnthanarak A, Mundy LM. Outbreak of influenza A (2009)H1N1 among Thai healthcare workers: is it time to integrate a vaccination program? Infec Control Hosp Epidemiol, 2010, 31(8):854-856.
[4] Li N, Wen ZB, Yang WH, et al. A study on protective effect of a positive pressure bio-protective clothing against bacterial aerosol. Bull Acad Milit Med Sci, 2011, 35(8):566-569. (in Chinese)李娜, 温占波, 杨文慧, 等. 一种正压生物防护服细菌气溶胶防护效果的研究. 军事医学, 2011, 35(8):566-569.
[5] Li N, Wen ZB, Yang WH, et al. Evaluation of the protective performance of a positive pressure bio-protective clothing against viral aerosol. Chin J Prev Med, 2012, 46(1):67-69. (in Chinese)李娜, 温占波, 杨文慧, 等. 某种正压生物防护服的病毒气溶胶防护性能评价. 中华预防医学杂志, 2012, 46(1):67-69.
[6] Wen ZB, Wang J, Li JS, et al. Evaluatation on the clean efficiency of microbiological aerosol by a complex type air cleaner. Chin J Disinfection, 2012, 29(5):367-369. (in Chinese)温占波, 王洁, 李劲松, 等. 一种多因子组合型空气净化器对微生物气溶胶净化效果的测试. 中国消毒学杂志, 2012, 29(5):367-369.
[7] Yu L, Li N, Jin AJ, et al. Evaluation on the bactericidal efficiency of a low temperature machine to microbiological aerosol. Chin J Disinfection, 2017, 34(10):902-904. (in Chinese)于龙, 李娜, 靳爱军, 等. 低温等离子体空气消毒机对微生物气溶胶杀灭效果的评价. 中国消毒学杂志, 2017, 34(10):902-904.
[8] General Administration of Quality Supervision, Inspection and Quarantine of the People's Republic of China, Standardization Administration of the People's Republic of China. GB 19083-2010 Technical requirements for protective face mask for medical use. (in Chinese)中华人民共和国国家质量监督检验检疫总局, 中国国家标准化管理委员会. GB 19083-2010 医用防护口罩技术要求.
[9] The General Logistics Department of the People's Liberation Army of China. WSB 59-2003 General specification for self-absorbed filter respirators. (in Chinese)中国人民解放军总后勤部卫生部. WSB 59-2003 自吸过滤式生物防护口罩通用规范.
[10] Zhang XY, Qin RL, Li YZ, et al. Evaluation on filtration property of protective respirators in aerosol. China Sa Sci J, 2011, 21(4):132-136.(in Chinese)张雪艳, 秦汝莉, 李玉珍, 等. 常用防护口罩对气溶胶的防护性能研究. 中国安全科学学报, 2011, 21(4):132-136.
[11] Balazy A, Toivola M, Adhikari A, et al. Do N95 respirators provide 95% protection level against airborne viruses, and how adequate are surgical masks? Am J Infect Control, 2006, 34(2):51-57.
[12] Wen ZB, Lu JC, Li JS, et al. Evaluation on the filtration efficiency of the mask filtration materials against non-biological particles and microbial aerosol. Chin J Disinfection, 2009, 26(5):487-490. (in Chinese)温占波, 鹿建春, 李劲松, 等. 口罩滤材对非生物颗粒气溶胶和微生物气溶胶过滤效率的评价. 中国消毒学杂志, 2009, 26(5):487-490.
[13] Wen ZB, Lu JC, Zhao JJ, et al. Evaluation of protective efficacy of high-efficiency filtration protective equipment against microorganism aerosol. Chin J Disinfection, 2007, 24(2):112-114. (in Chinese)温占波, 鹿建春, 赵建军, 等. 几种高效过滤器材对微生物气溶胶防护效果的评价. 中国消毒学杂志, 2007, 24(2):112-114.
[14] Bowen LE. Does that face mask really protect you? Appl Biosafety,2013, 15(2):67-71.
[15] Wen ZB, Chen JJ, Zhao JJ, et al. Evaluation of the efficacy of surgical mask in filtering bacterial aerosol. Chin J Disinfection, 2007, 24(4):306-309. (in Chinese)温占波, 陈洁君, 赵建军, 等. 医用外科口罩细菌气溶胶过滤效果评价. 中国消毒学杂志, 2007, 24(4):306-309.

