Ru-Sn-B催化剂制备及对苯二甲酸催化加氢反应的研究
宋义伟,郭慧军,崔慧山,纪 军,王 伟
(中国石油工程建设有限公司华北分公司,河北 任丘 062552)
对苯二甲醇是重要的有机化工中间体,可以通过含羰基的化合物如醛、酮、羧酸及其酯或酐等加氢制得。由于碳氧双键有较大的空间位阻和弱的极性使得羧酸酯还原成醇十分困难[1],工业上通常用铜锌、铜铬等复合氧化物催化羧酸及其酯加氢[2-5]。Cu-Cr催化剂的缺点是对环境可能产生污染,随着环保要求越来越高,开发新型高效环境友好的催化剂用于该类反应成为当前研究的热点。其中以添加锡、铂、铼等的负载型Ru系催化剂成为研究重点[6-8]。Mitsuo等[9]采用Ru-Sn-Re/C催化剂,在230 ℃、9.0 MPa氢压下进行1,4-环己烷二甲酸加氢,反应3.5 h,1,4-环己烷二甲醇收率为75%。本工作以Al2O3为载体,以RuCl3和SnCl2作为活性组分,通过NaBH4还原制备了Ru-Sn-B催化剂,并应用于对苯二甲酸加氢制备对苯二甲醇的催化反应中,得到了理想的实验结果。
1 实 验
1.1 试剂与仪器
三氯化钌(RuCl3·3H2O),CP;氯化亚锡(SnCl2·2H2O),AR;硼氢化钠(NaBH4,>96%);精对苯二甲酸(C8H6O4),工业级。
1.2 催化剂制备
将RuCl3·3H2O水溶液与SnCl2·2H2O水溶液混合,加入Al2O3搅拌均匀,静置老化后取一定量NaBH4溶液加入,在70~90 ℃干燥6 h后研磨得粉末状催化剂,加热并于氢气流速为150 mL/min下还原2 h,即得催化剂产品。改变各催化剂中载体和起始物的用量,制得不同活性组分的催化剂(记为RSmBp,其中R代表金属Ru,S代表金属Sn,B代表B元素,m表示n(Sn)/n(Ru),p表示n(B)/n(Sn+Ru))。
1.3 催化剂表征
1.3.1比表面积和孔径测定
载体的比表面及平均孔径采用美国麦克(Micromeritrics)公司的ASAP 2010M 物理吸附仪进行测定(77 K,N2吸附)。
1.3.2程序升温还原/脱附测定
程序升温装置所用的色谱仪为上海分析仪器厂的102型气相色谱分析仪,热导池检测器。
程序升温还原(TPR)分析条件:催化剂装入U-型石英反应器中,在N2气气氛中升温至120 ℃进行预处理。反应器冷却后开启色谱,采用H2-N2混合气按20 ℃/min速率升温至600 ℃停止。
程序升温脱附(TPD)分析条件:催化剂装入U-型石英反应器中升温至230 ℃,40 mL/min的H2流量下还原1 h,冷却到室温,N2吹扫至色谱基线稳定后,以10 ℃/min速率升温至880 ℃停止。
1.3.3化学吸附测定
催化剂装入U-型石英反应器中。升温至设定温度,通入氢气还原1 h后冷却到室温,将反应器置入冷阱中,采用N2色谱载气,脉冲定量进样O2和CO,当被吸附气体的色谱峰达到最大时,继续进样3~5次,停止进样。通过分析二者峰面积变化,计算其吸附量。
1.4 对苯二甲醇合成及收率测定
按比例将反应物料、溶剂水和催化剂加入到高压反应釜中,通入氢气,搅拌加热,反应结束后停止加热和搅拌,冷却,真空抽滤得滤液。采用酸值法分别测定反应液和催化剂PTA含量,计算PTA转化率。反应液组成及BDM收率测定采用气相色谱仪,内标法测定,分析条件:OV-1701毛细管色谱柱,氢火焰检测器。柱温170 ℃,气化温度270 ℃,检测温度270 ℃,桥电流120 mA,载气压力0.07 MPa,分流气速10 mL/20 s,衰减比1∶1,灵敏度×2,进样0.4 μL。
将催化剂抽滤洗涤3次,除去表面吸附的有机物,然后在70 ℃下干燥4 h,用于考察催化剂的稳定性。
2 结果与讨论
2.1 催化剂表征
2.1.1TPR
2.1.1.1不同Sn含量的催化剂
图1是Sn含量对催化剂TPR峰型的影响。
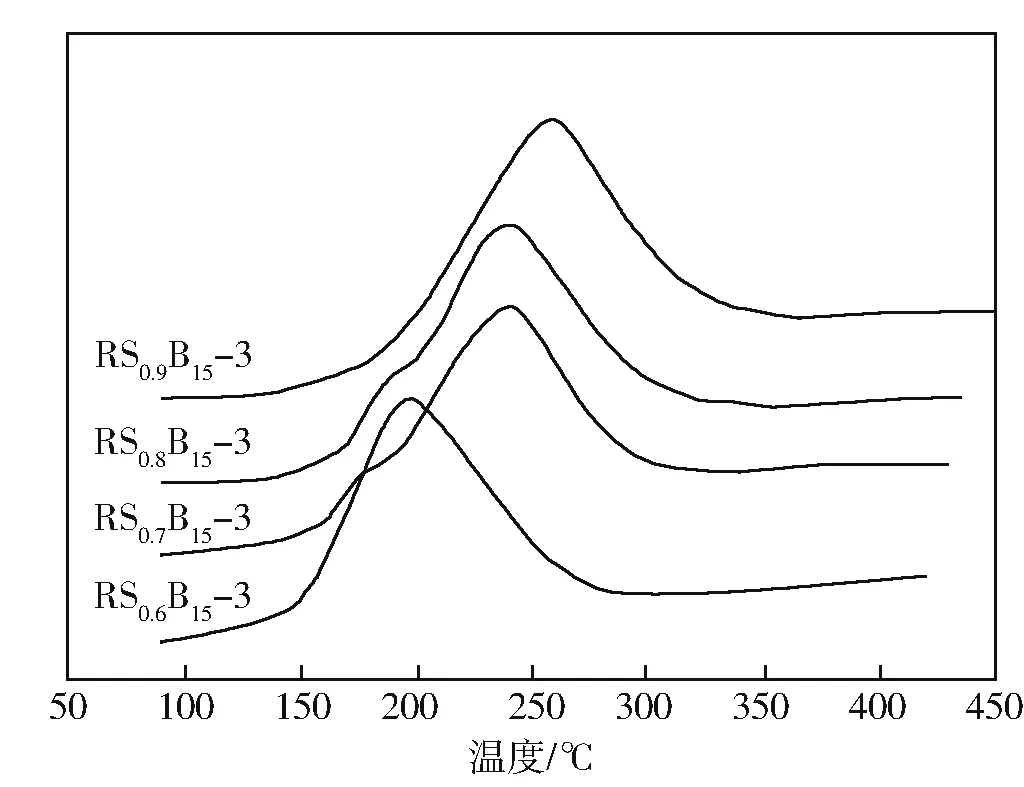
图1 不同Sn含量的RSmB15催化剂TPR曲线
根据文献[10],Sn(Ⅱ)在低温区域不会被还原。图中出现的还原峰主要为Ru(0),从图1可以看到,当催化剂中Sn含量较低((n(Sn)/n(Ru)≤0.6)时,催化剂较易还原,在谱图上仅显示一个还原峰(195 ℃)。说明在Sn(Ⅱ)含量较少的情况下,Sn(Ⅱ)和Ru(0)很难发生相互作用,Ru(Ⅲ)被直接还原为Ru(0)。随着Sn含量增加,TPR谱图中还原峰向高温漂移,说明在还原过程中Ru-Sn间发生相互作用,当n(Sn)/n(Ru)在0.7~0.8时,在TPR谱图上出现两个明显的还原峰。在180~190 ℃出现的H2消耗峰可能是Ru(0)的生成。而在240 ℃附近出现的峰则可能是Ru(0)和SnO(Sn处于Sn(Ⅱ)或Sn(Ⅳ))发生相互作用的结果[11]。当(n(Sn)/n(Ru)≥0.9)时,RSmB15催化剂的还原峰漂移至260 ℃,且在200 ℃以下不再出现肩峰。这是因为随着Sn(Ⅱ)的增加,Ru原子和Sn(Ⅱ)相互作用加强,从而使得Ru原子不能单独存在[12]。
2.1.1.2不同B含量的催化剂
图2为采用不同NaBH4的量还原的RS0.8Bp催化剂TPR曲线。

图2 RS0.8Bp催化剂的TPR曲线
从图2可以看出,随着NaBH4用量增加,TPR谱图中的还原峰向高温漂移,分别出现在225,240和265 ℃,这是因为加入NaBH4造成催化剂表面Ru的减少[12],从而使得n(Sn)/n(Ru)比例增加,造成H2还原峰向高温区漂移。同时,随着NaBH4用量的增加,催化剂表面的B含量也有一定程度的增加。而氢气消耗量相应发生变化,这一结果可以认为由于NaBH4用量的增加造成的[13]。
2.1.2CO和O2化学吸附研究
2.1.2.1不同Sn含量的催化剂
图3显示了RSmB15催化剂的CO和O2化学吸附实验结果。
从图3可以看出,随着n(Sn)/n(Ru)的增加,CO吸附量有逐渐减少的趋势,而催化剂对O2的吸附则呈现出相反的变化趋势,催化剂CO化学吸附能力弱于O2化学吸附能力。这是因为CO只能被Ru金属表面化学吸附[14],Sn(Ⅱ)和Al2O3表面不能化学吸附CO。而O原子既可以吸附在Ru金属表面上也可以吸附在Sn(Ⅱ)上[15]。随着催化剂中Sn含量的增加,催化剂表面的Ru(0)比例减少,催化剂对CO的吸附量逐渐下降。而对O2吸附增加。
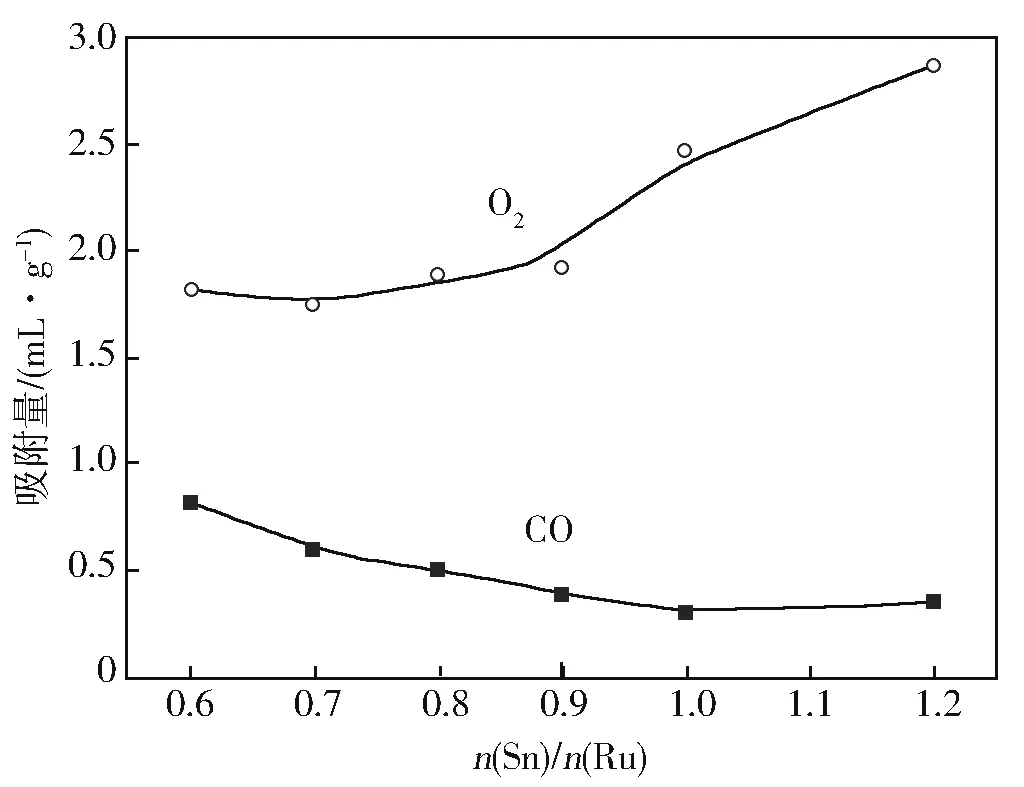
图3 RSmB15催化剂CO和O2吸附曲线
当n(Sn)/n(Ru)大于0.9以后O2的吸附量的增长明显加快。这是因为由于Sn含量的增加,使得Sn富集于催化剂表面,而部分Ru(0)被覆盖,由于O与Sn的结合能(-285 kJ/mol)小于O与Ru的结合能(-239.3 kJ/mol),使得在Sn(Ⅱ)的表面O2更容易吸附。两者共同作用的结果,显示催化剂对O2的总吸附量有一个较大的提高。
2.1.2.2不同B含量
图4是不同NaBH4的量还原制备的RS0.8Bp催化剂化学吸附曲线。
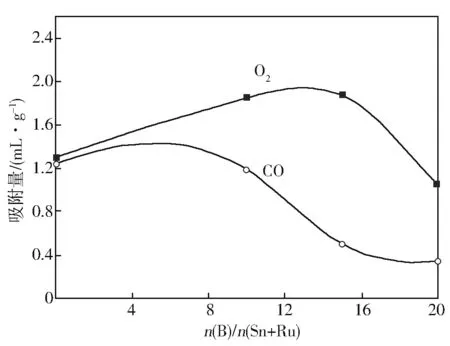
图4 RS0.8Bp催化剂CO和O2吸附曲线
随着催化剂中B含量的增加,CO吸附量有逐渐减小的趋势。当n(B)/n(Ru+Sn)从10增加到15的过程时,CO吸附量明显减少。而O2吸附量则先增加然后降低,主要是催化剂表面Ru原子、Sn(Ⅱ)及载体对CO和O2选择吸附及NaBH4使催化剂表面Ru(0)比例减少造成的。
康宁早在20世纪80年代就以电视技术和消费产品进入了中国市场。自此,康宁深耕中国市场近四十载,见证并推动了国内光通信、显示科技、生命科学器皿、汽车和移动消费电子产品五大市场的迅猛发展。康宁把握中国改革开放及产业升级的时代契机,在中国大陆地区投资已超过40亿美元,建立了18个业务运营公司和工厂,以及一座康宁中国研发中心,拥有近5000名员工。凭借行业领先的技术和产品,以及在研发上的不断投入,康宁始终与时俱进,满足不断升级的市场需求,开发出改变人类生活的创新产品。
2.1.3TPD
2.1.3.1不同Sn含量的催化剂
图5为不同n(Sn)/n(Ru)的RSmB15催化剂的H2-TPD曲线。
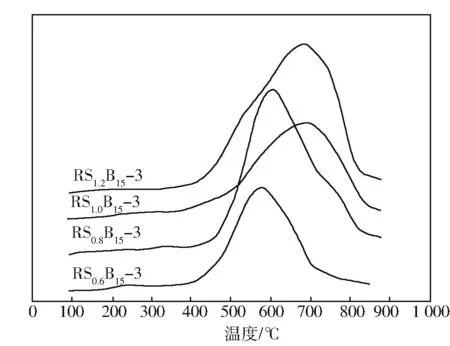
图5 RSmB15催化剂的TPD曲线
从图5可以看出,对于不同n(Sn)/n(Ru)的RSmB15催化剂,均只有一个H2脱附峰,同时,最高脱附温度随着n(Sn)/n(Ru)的增加而增高。这说明H和Ru的结合能随着Sn含量的增加而增大。氢气脱附峰的峰面积说明了催化剂的H吸附能力,从图中可以看出RSmB15催化剂吸附氢气的能力最大。吸附能力的增加可能是因为由于Sn的加入,使得催化剂表面的RuB粒径的分布发生变化[16]。
2.1.3.2不同B含量
图6为不同B含量的RS0.8Bp催化剂的H2-TPD曲线。
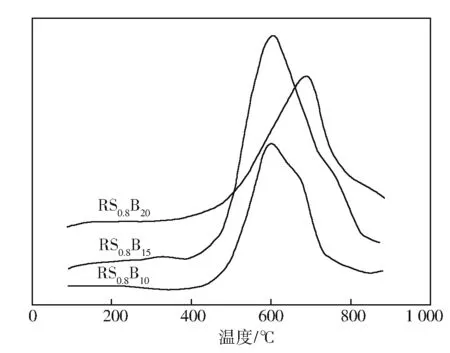
图6 RS0.8Bp催化剂的TPD曲线
如图6所示,3种不同n(B)/n(Ru+Sn)的RS0.8Bp催化剂H2-TPD曲线中,均只显示了一个脱附峰。同时,在催化剂中B含量较小时,脱附峰在600 ℃左右,随着B含量增加,TPD谱图中最高脱附温度增加(RS0.8B20增加至680 ℃左右)。这说明随着NaBH4用量的增加,催化剂表面和H的结合能力增强。从图6还可以看到,RS0.8B15催化剂的脱附峰面积相对较大。即对H2的吸收能力较强,显示此催化剂具有较高的催化活性。
2.2 催化剂性能评价
2.2.1Sn含量对催化剂性能的影响
不同n(Sn)/n(Ru)制备的RSmB15催化剂对反应结果见图7。
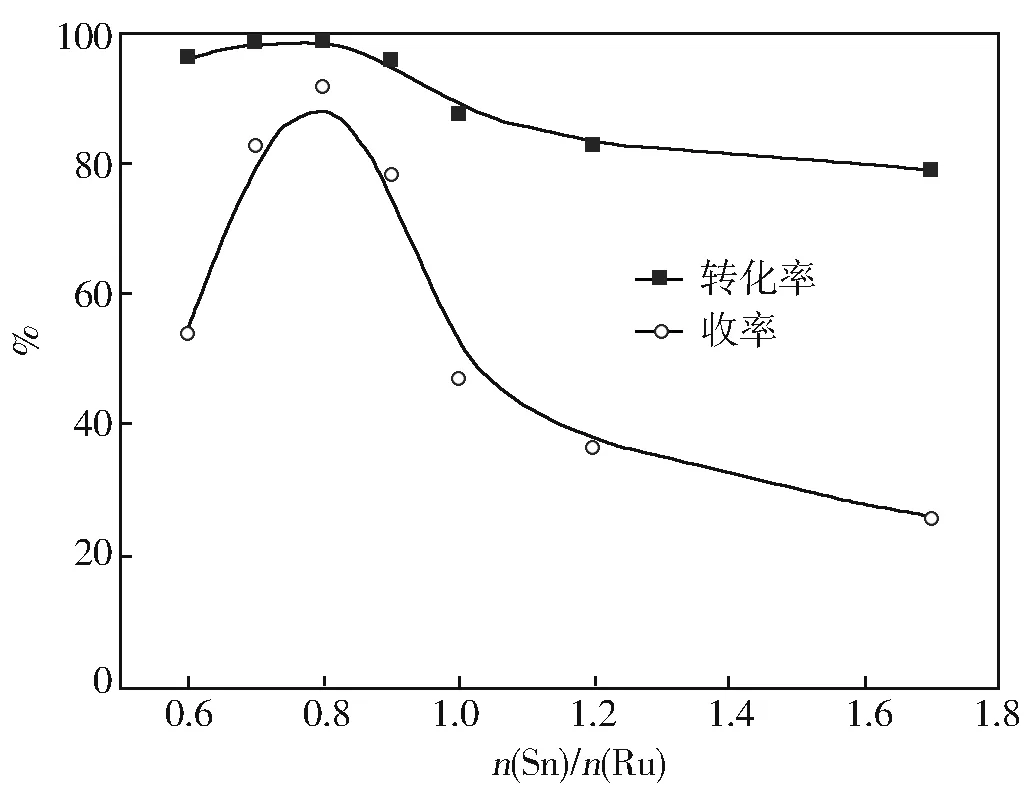
图7 Sn含量对RSmB15催化性能的影响
由图7可见,n(Sn)/n(Ru)从0.6增加到0.8的过程中,PTA转化率均在96%以上,而BDM收率逐渐增加,当n(Sn)/n(Ru)=0.8时,BDM收率达到最大值91.6%。当n(Sn)/n(Ru)>1.0时,BDM的收率有明显的下降。通常认为,羧酸的氢化过程包括:Sn活化羰基、Ru活化氢并使活化的氢和羰基反应[18]。因此,增加Sn含量并未提高催化剂活性,而是有利于羧基活化,从而提高生成醇的选择性[19]。但是,过量添加Sn组分,造成催化剂表面Sn含量增加,Ru浓度会相应降低,从而对氢的吸附能力降低,进而影响催化剂选择性。同时,大量羧基被吸附在催化剂表面的活性位上,将抑制H到达催化剂表面,使得催化剂活性和选择性降低[10,17-20]。所以,对于PTA加氢反应,存在一个合适的锡钌比。
2.2.2B含量对催化剂性能的影响
图8是B含量对RS0.8Bp催化剂性能的影响。
从图8可见,采用不同B含量的催化剂对PTA加氢均具有较高的活性。PTA转化率在96%以上,但催化剂选择性存在很大差别。未使用NaBH4还原的催化剂BDM收率只有25.6%,而采用NaBH4化学还原的催化剂BDM选择性均在80%以上。说明催化剂中B的存在对催化剂的选择性有很大的影响。这是因为B的存在增加了Ru周围电荷密度,使H2易于活化为H原子。增强催化剂中Ru对H的吸附能力[21],从而与被Sn(Ⅱ)活化的羰基反应的能力增强,使BDM收率提高。
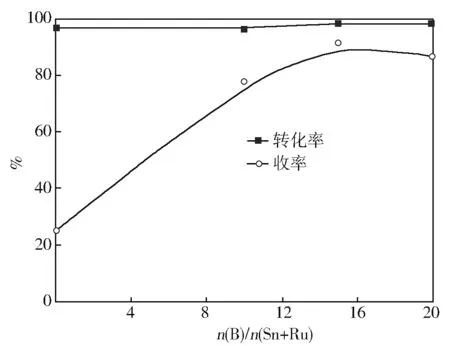
图8 B含量对RS0.8Bp催化剂性能的影响
3 结 论
a.采用共浸渍法以Al2O3为载体,制备了RSB催化剂,通过序升温还原(TPR)、CO和O2化学吸附以及程序升温脱附(TPD)表征表明,活性组分Ru极易被还原成金属态,随着Sn含量增加,Ru、Sn以及B和载体间发生相互作用。Sn含量过高时将富集于催化剂表面,当n(Sn)/n(Ru)=0.8,n(B )/n(Ru+Sn)=15时制备的催化剂具有最优活性。
b.将RSB催化剂用于PTA加氢制备BDM反应,得到的优化工艺条件是反应物料配比为n(催化剂)∶n(PTA)∶n(H2O)=1∶4∶40。在230 ℃和10 MPa下,反应5 h,转化率接近100%,BDM收率达到88.9%。
[1] McAlees A J, McCrindle R. Catalytic hydrogenations of cyclic imides and ayhydrides[J]. J Chem Soc C, 1969(19), 2425-2435.
[2] Pohl J, Franz-Josef C, Gerd G. Acid-resistant catalysts for the direct hydrogenation of fatty acids to fatty alcohols:US, 4855273[P].1989-08-08.
[3] Mizumoto T, Kamatani H. Process for preparing 1,4-1,4-cyclohexanedimethanol: JP,52000242[P].1977-01-05.
[4] 计伟荣,谭志斌,曾玉龙,等. Cu-Cr2O3/Al2O3催化剂上乳酸乙酯加氢制丙二醇研究[J].浙江工业大学学报,2013, 41(2):183-185、194.
[5] 邓天舒,茆福林,周小平.Cu-ZnO催化剂用于乳酸乙酯气相加氢制1,2-丙二醇的研究[J].现代化工, 2011,31(5):79-82.
[6] Yoshinori H, Kouetsu E. The drastic effect of platinum on carbon-supported ruthenium-tin catalysts used for hydrogenation reactions of carboxylic acids[J]. Applied Catalysis A: General, 2003, 239: 181-195.
[7] Kayou A, Nanba Y. Method for hydrogenating terephthalic acid: JP, 2002145824[P].2002-05-222.
[8] 罗鸽,闫世明,乔明华,等. RuSn/Al2O3催化剂用于乳酸乙酯加氢制1,2-丙二醇研究[J].石油化工,2004(3):1062-1064.
[9] Mitsuo K, Eizaburou U. Catalysts for hydrogenating terephthalic acid: JP, 2002060356[P].2002-02-26.
[10] Cheah K Y, Tang T S. Selective hydrogenation of oleic acid to 9-octadecen-1-ol: catalyst preparation and optium reaction conditions[J]. JAOCS,1994, 71: 501-506.
[11] Deshapande V M, Paterson W R, Narasimham C S. Studieson ruthenium-tin boride catalyst: 1. characterizatin[J]. J Catal, 1990,121:165-173.
[12] Kluson P, Cerveny L. Selective hydrogenation over ruthenium catalysts[J]. Applied Catalysis A: General, 1995, 128: 13-31.
[13] Pouilloux Y, Autin F, Guomon C, et al. Hydrogenation of fatty esters over ruthenium-tin catalysts; characterization and identification of active centers[J]. Journal of Catalysis, 1998, 176: 215-224.
[14] Galvagno S, Donato A. Selective hydrogenation of cinnamaldehyde over Ru-Sn catalysts[J]. Journal of Molecular Catalysis, 1993, 78: 227-236.
[15] Katsuhiko Tahara, Eiji Nagahara. Liquid-phase hydrogenation of carboxylic acid on supported bimetallic Ru-Sn-alumina catalysts[J]. Applied Catalysis A: General, 1997, 154: 75-86.
[16] Luo Ge, Yan Shirun, Qiao Minhua, et al. Effect of tin on Ru-B/γ-Al2O3catalyst for the hydrogenation of ethyl lactate to 1,2-propanediol[J]. Applied Catalysis A: General, 2004, 275: 95-102.
[17] Sexton B A, Hughes A E, Foger K. An X-ray photoelectron spectroscopy and reaction study of Pt-Sn catalysts[J]. Journal of Catalysis, 1984, 88: 466-477.
[18] Toba M, Tanaka S. Synthesis of alcohols and diols by hydrogenation of carboxylic acids and esters over Ru-Sn-Al2O3catalysts[J]. Applied Catalysis A: General, 1999, 189: 243-250.
[19] Pouilloux Y, Piccirili A. Selective hydrogenation into oleyl alcohol of methyl oleate in the presence of Ru-Sn/Al2O3catalyst[J]. Journal of Molecular Catalysis A: Chemical, 1996, 108: 161-166.
[20] 辛勤. 固体催化剂研究方法[M]. 北京: 科学出版社, 2004:291-296.
[21] Deshapande V M, Ramnrayan K, Narasimham C S. Studies on ruthenium-tin boride catalyst: 2. hydrogenation of fatty acid esters to fatty alcohols[J]. J Catal, 1990,121:174.

