磁性壳聚糖凝胶微球对水中Pb(Ⅱ)的吸附性能
蒲生彦,王可心,马 慧,杨 曾,候雅琪,陈虹宇 (1.成都理工大学,地质灾害防治与地质环境保护国家重点实验室,四川 成都 610059;2.成都理工大学,国家环境保护水土污染协同控制与联合修复重点实验室,四川 成都 610059;3.香港理工大学,土木及环境工程学系,中国 香港)
重金属在生物物质循环和能量交换中不能被分解破坏,只能改变其物理化学形态或转移其存在位置,加之重金属在环境中的迁移转化几乎涉及了所有可能的物理、化学和生物过程,因而治理难度很大[1].伴随现代工业的快速发展,重金属废水已成为对环境污染最严重的工业废水之一[2].现有重金属废水处理技术,如离子交换法、电解法、化学沉淀法等常规方法普遍存在处理工艺复杂,运行成本高,对低浓度重金属废水处理效果差的问题[3].相比之下,吸附法则具有适用范围广、反应速度快、可适应不同反应条件、环境友好等优点,受到了研究人员的高度关注[4].近年,研究较多的吸附材料有活性炭[5]、沸石[6]、膨润土[7]等.这些吸附剂对废水中重金属有一定的去除效果,但吸附完成后难以与水体分离,容易造成环境二次污染.与非生物质吸附剂相比,生物质基吸附剂富含大量吸附功能基团,对重金属离子有很强的吸附能力和较高吸附容量,而且具有资源丰富,可再生易降解,环境友好成本低的优点,较为适合水中重金属离子的富集与分离[8-9].常见的天然高分子吸附剂,如:壳聚糖[10]、纤维素[11]、木质素[12]等,其中以壳聚糖及其衍生物研究最为活跃.
壳聚糖是一种成本低廉,环境友好的天然生物高分子,其分子主链上大量氨基、羟基等官能团可络合金属离子,且这些官能团具有良好的反应性,可功能化改性[13].若将壳聚糖赋予磁性后,采用磁分离技术可使吸附剂回收和再生变得简易[14].目前,磁性壳聚糖吸附剂的制备方法有原位共沉淀法[15]、微乳液法[16]和水热法[17]等,其中原位共沉淀法通过溶液中的化学反应直接得到均一的材料,相比其他方法制备过程简单且环境友好,是应用最普遍的方法之一[18].目前已有的原位共沉淀法包括电喷雾技术[19],静电液滴(ESD)技术[20]和反向共沉淀法[21]等.
本研究采用原位共沉淀法结合柠檬酸钠交联制备了一种新型多孔磁性壳聚糖凝胶微球,在对其微观结构、物化性能进行充分表征的基础上,选取Pb(II)作为目标污染物考察了该凝胶微球的吸附性能,以期能为水中重金属富集去除提供一种新的思路和方法.
1 材料与方法
1.1 材料
试剂:壳聚糖(Chitosan,CS,脱乙酰度 80%~95%)购于上海阿拉丁生化科技股份有限公司;冰醋酸、氢氧化钠、柠檬酸钠购于成都科龙化学试剂厂;六水合氯化铁、四水合氯化亚铁和硝酸铅购于志远化学试剂厂;实验用水均采用超纯水.
仪器:KW-400恒温水浴振荡器,上虞佳星仪器厂;SCIENTZ-50F冷冻干燥机,宁波新芝生物科技股份有限公司;GGX-9火焰原子吸收分光光度计,北京海光仪器有限公司.
1.2 多孔磁性壳聚糖凝胶微球的制备
将0.8g壳聚糖溶于24mL 2%的乙酸溶液中,机械搅拌 30min,使得壳聚糖充分溶解;之后向溶液中加入2mL摩尔比为2:1的Fe3+/Fe2+混合溶液,继续搅拌30min,溶液由亮黄色变为棕红色后,将混合溶液用蠕动泵滴入 NaOH/柠檬酸钠混合浸泡液(NaOH 1.25mol/L, 柠檬酸钠0.1mol/L)中,静置陈化 10h;磁分离后用超纯水多次洗涤,除去残余的NaOH和柠檬酸钠,冷冻干燥30h.
无磁壳聚糖凝胶微球(CS)在不加 Fe3+/Fe2+混合溶液的条件下以相同方法制得作为实验对照组.
1.3 表征方法
采用德国 Sigma300型扫描电子显微镜(SEM)观察样品表面形貌,采用日本 FEI Tecnai-G20型透射电子显微镜(TEM)观察样品内部形貌,采用美国Nicolet-1170SX型傅里叶红外光谱仪(FTIR)进行红外谱图分析,采用美国 STA6000型热重分析仪(TGA)考察在壳聚糖凝胶微球中引入Fe3O4纳米颗粒的热力学效应.
1.4 对Pb(II)的静态吸附实验
将0.05g磁性壳聚糖凝胶微球投加到50mL 200mg/L的 Pb(II)溶液中,在 25℃下恒温振荡(150r/min),测定吸附量q随时间t的变化情况.吸附量采用公式(1)进行计算.
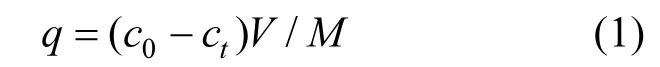
式中:c0和ct为在Pb(II)溶液的初始浓度和吸附t时间后的浓度,mg/L;V为 Pb(II)溶液的体积,L;M为吸附剂的投加量,g.
2 结果与讨论
2.1 多孔磁性壳聚糖凝胶微球制备
首先,壳聚糖溶液与Fe3+/Fe2+(摩尔比为2:1)经螯合作用形成 Fe3+-CS-Fe2+混合溶胶,然后,将混合溶胶通过蠕动泵滴入 NaOH/柠檬酸钠混合浸泡液形成凝胶微球.在此过程中,发生 Fe3+/Fe2+原位共沉淀反应生成 Fe3O4纳米颗粒,壳聚糖和柠檬酸钠发生交联反应.最后,将制得吸附剂用于水中重金属离子的静态吸附,并利用外加磁场将吸附剂分离回收,从而达到回收再利用,减少二次污染的目的.多孔磁性壳聚糖凝胶微球制备及重金属吸附实验流程如图1所示.
本实验所制得的磁性壳聚糖凝胶微球平均粒径约为(2.91±0.65)mm,将其冷冻干燥处理后平均粒径约为(2.42±0.51)mm,干燥后平均粒径约减小 16.8%,冷冻干燥后凝胶微球较好地保留原有圆球状形态及内部多孔结构.重;图 2(e)和(f)为多孔磁性壳聚糖凝胶微球和壳聚糖凝胶微球的内部结构扫描电镜图.由图可知,与壳聚糖凝胶微球内部紧密的结构相比,磁性壳聚糖凝胶微球内部具有良好的多孔结构,增大了吸附剂的比表面积,有利于吸附作用发生.
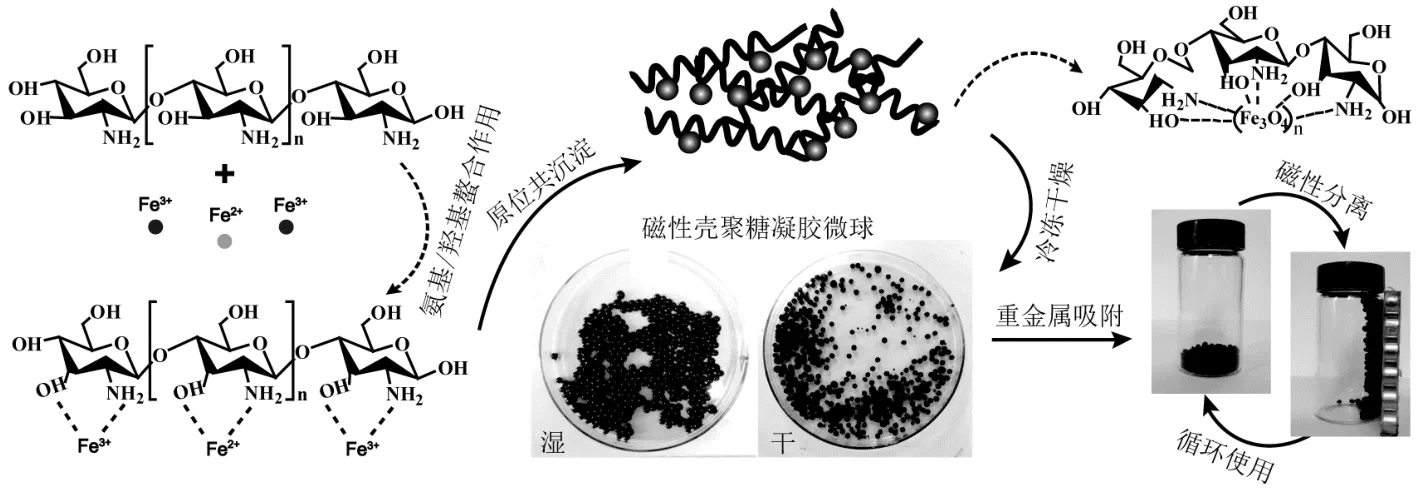
图1 磁性壳聚糖凝胶微球制备与重金属吸附实验流程Fig.1 Schematic illustration of preparation of magnetic chitosan hydrogel microspheres and its adsorption process

图2 壳聚糖凝胶微球和磁性壳聚糖凝胶微球SEMFig.2 SEM characterization results of chitosan hydrogel microsphere and magnetic chitosan hydrogel microspheres
为深入了解多孔磁性壳聚糖凝胶微球中Fe3O4纳米颗粒的形态,对样品进行了TEM分析.由图3可知,Fe3O4纳米颗粒在壳聚糖微球内部分布较均匀,未出现明显团聚现象,其平均粒径约为(4.79 ±1.09)nm(图 3(b)).
图 4为壳聚糖凝胶微球及吸附前后多孔磁性壳聚糖凝胶微球红外光谱图.壳聚糖、柠檬酸钠和Pb(II)之间的相互作用会影响特征峰的位置和强度,在壳聚糖凝胶微球的光谱中,1082cm-1,1027cm-1两处为 C-OH键的伸缩振动吸收峰,1383cm-1处为伯醇组-C-O键的伸缩振动吸收峰.1425cm-1处为C-N键的伸缩振动峰.壳聚糖固有的O-H和N-H伸缩振动峰出现在3444cm-1附近,在多孔磁性壳聚糖凝胶微球的两个光谱中也可观察到这一较宽的吸收峰.在吸附前多孔磁性壳聚糖凝胶微球的光谱中,1648cm-1处的N-H伸缩振动吸收峰移动到1640cm-1处.由于柠檬酸钠的交联和 Fe3O4与壳聚糖之间的弱相互作用,导致酰胺峰强度降低.在吸附前、后磁性壳聚糖凝胶微球光谱中,586cm-1处出现了Fe3O4的特征吸收峰,对应的是 Fe-O的伸缩振动峰,说明磁性纳米颗粒 Fe3O4已成功嵌入吸附剂中.而吸附了Pb(II)的凝胶微球光谱图4(b)和(d)中,1383cm-1和1425cm-1处特征吸收峰形状发生变化表明Pb(II)离子和壳聚糖发生络合反应,同时说明多孔磁性壳聚糖凝胶微球的羟基、氨基和羧基可以高效吸附金属阳离子.

图4 吸附前后壳聚糖凝胶微球和磁性壳聚糖凝胶微球的红外谱Fig.4 FTIR spectra of pure chitosan hydrogel microspheres, and magnetic hydrogel chitosan microspheres before and after adsorption
通过热重分析表征了壳聚糖凝胶微球中引入的Fe3O4纳米颗粒的热力学效应.图5为壳聚糖凝胶微球和多孔磁性壳聚糖凝胶微球的热重曲线图.

图5 磁性壳聚糖凝胶微球的热重分析曲线Fig.5 Thermo gravimetric curves of magnetic chitosan hydrogel microspheres
由热重分析曲线可知,壳聚糖凝胶微球重量损失发生在 3个阶段.第一阶段,当温度升至90℃左右,吸附剂中的自由水及通过氢键形成的结合水减少;第二阶段,在 90~320℃范围内,壳聚糖发生分解;第三阶段,壳聚糖发生碳化分解,在 800℃时所对应的重量为热解最终产物残余碳.多孔磁性壳聚糖凝胶微球在 25~120℃的范围内脱去自由水和结合水;在 320℃时壳聚糖完全分解;在600℃时,Fe3O4与碳反应生成单质铁;在 800℃时残余重量为碳和单质铁.多孔磁性壳聚糖凝胶微球的分解起始温度比壳聚糖凝胶微球高,说明 Fe3O4的存在有效地提高了吸附剂的热稳定性.
2.3 吸附时间和初始浓度对吸附效果的影响
图6(a)讨论了在0~840min内壳聚糖凝胶微球和多孔磁性壳聚糖凝胶微球对Pb(II)吸附量的变化.
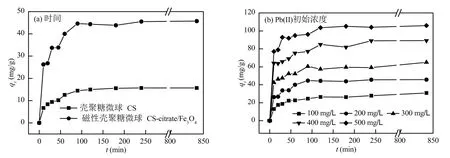
图6 时间和初始浓度对Pb(II)吸附的影响Fig.6 Influence of time and initial concentration on adsorption of Pb(II)
可以看出,壳聚糖凝胶微球的吸附作用主要发生在0~120min内,在120min后达到吸附平衡,平衡吸附量为 16.1mg/g.多孔磁性壳聚糖凝胶微球对Pb(II)的吸附与壳聚糖凝胶微球呈现相同的变化趋势,但平衡吸附量达到了45.3mg/g,为壳聚糖凝胶微球的 2.8倍,这是磁性复合吸附剂的高度多孔结构提供了较大的比表面积,使更大数目的活性基团与 Pb(II)接触产生的结果.吸附剂吸附量在0~120min内升高较快,说明Pb(II)与多孔磁性壳聚糖凝胶微球的基团发生螯合反应,被成功地吸附到样品表面上,使得溶液中 Pb(II)浓度下降.随着吸附反应的进行,吸附到多孔磁性壳聚糖凝胶微球的Pb(II)逐渐占据了大部分活性基团,导致活性基团的数目下降,在120min时吸附量趋于平衡.
本研究将铅离子初始浓度设置为100、200、300、400、500mg/L对多孔磁性壳聚糖凝胶微球的吸附性能进行了考察(图 6(b)).多孔磁性壳聚糖凝胶微球对不同初始浓度Pb(II)的吸附呈现类似的变化趋势,随着初始浓度增大,多孔磁性壳聚糖凝胶微球对Pb(II)的吸附量逐渐增大.
2.4 吸附动力学及吸附等温线
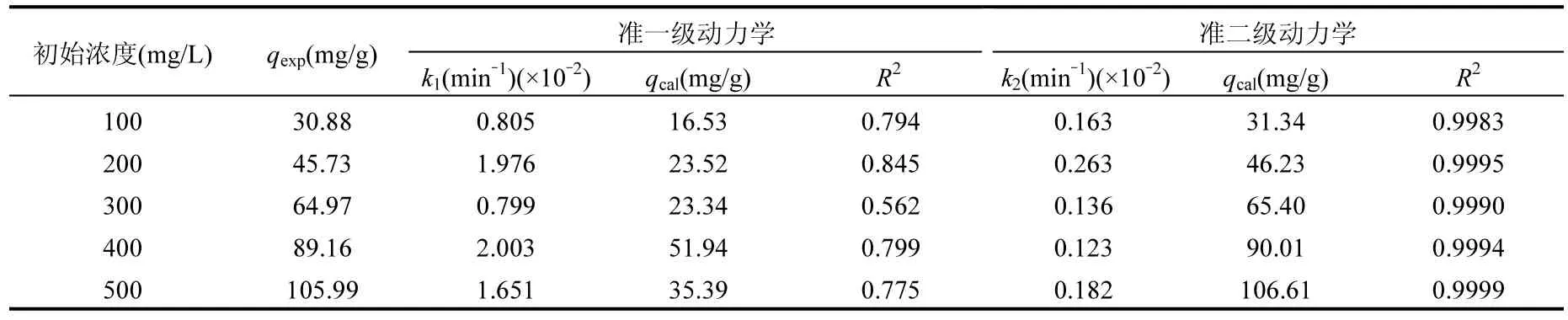
表1 Pb(II)吸附动力学方程的拟合Table 1 Fitting results of lead ions adsorption kinetics equations
2.4.1 吸附动力学 采用准一级和准二级动力 学模型对动力学数据进行拟合,计算出相应的速率常数,研究其吸附过程的动力学行为并探讨吸附机理.所用拟合方程的线性表达式如下:

式中:qt为t时刻吸附剂对Pb(II)的吸附量,mg/g;qe为平衡吸附量,mg/g;k1为准一级速率常数,min-1;k2为准二级速率常数,mg/(g⋅min).qe、k2可分别由截距和直线斜率求得.分析结果见表1和图7.
准一级动力学相关系数最高为 0.845,而准二级动力学相关系数均高于 0.99,因此准二级动力学方程能更好地描述整个吸附过程.这证实了多孔磁性壳聚糖凝胶微球吸附剂对Pb(II)的吸附为化学吸附,比表面积是吸附的重要影响因素.

图7 吸附动力学曲线Fig.7 Absorption kinetic curve
2.4.2 吸附等温线 使用 Langmuir和Freundlich吸附等温线模型来解释吸附机理.Langmuir方程假设吸附过程为单层吸附,线性表达式如下:
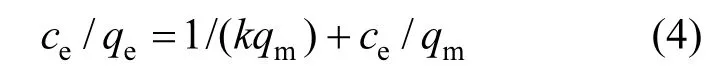
式中:qe表示吸附质的吸附量,mg/g;ce表示其在溶液中的平衡浓度,mg/L;b为Langmuir吸附平衡常数,L/mg;qm为在吸附剂上单层形成的最大吸附能力,mg/g.
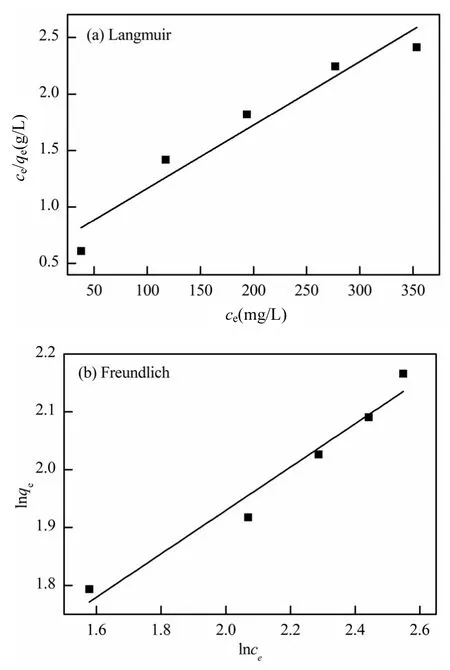
图8 等温吸附曲线Fig.8 Sorption isotherm
Freundlich等温线是用于描述非均相表面的经验方程,它的线性表达式如下:
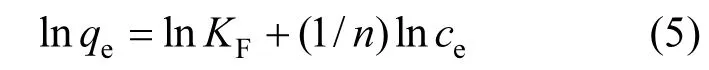
式中:KF是Freundlich常数;1/n为吸附指数.将Pb(II)起始浓度范围为100~500mg/L的5组吸附实验数据进行吸附等温线拟合,结果见图 8和表2. Langmuir模型和Freundlich模型均具有良好的拟合度,且后者线性拟合相关系数更高,大于0.95,可能是由于吸附剂表面基团分布不均,导致吸附过程呈现非均质吸附特性.吸附指数 1/n的值为 0.3749,有报道称 1/n<1表明吸附容易进行[22].相较其他生物质基吸附材料吸附铅离子研究,如甘蔗渣对铅最大吸附量为 41.32mg/g[23],改性木质素磺酸钠对铅最大吸附量为 55.22mg/g[24],N-(2-磺乙基)壳聚糖对铅最大吸附量为99.79mg/g[25],本研究中磁性壳聚糖微球对铅的吸附容量178.25mg/g均大于上述吸附材料.表明磁性壳聚糖微球对Pb(II)具有良好的吸附效果.

表2 Pb(II)吸附等温线拟合参数Table 2 Fittingof lead ions adsorption isotherm equations
3 结论
3.1 采用原位共沉淀法和柠檬酸钠交联法制备得到的多孔磁性壳聚糖凝胶微球内部孔隙丰富,比表面积大,磁性良好,可外加磁场分离.Fe3O4纳米颗粒在壳聚糖基质中分布均匀,增加了吸附剂的热稳定性.
3.2 多孔磁性壳聚糖凝胶微球对水中 Pb(II)具有良好的吸附性能,约在2h达吸附平衡,当Pb(II)初始浓度从100mg/L增加到500mg/L时,平衡吸附量从30.88mg/g增加到105.99mg/g.
3.3 吸附剂对水中 Pb(II)的吸附过程满足准二级动力学方程,并较好的符合 Freundlich等温吸附方程,最大吸附容量可达178.25mg/g.
参考文献:
[1]唐 黎,李秋华,陈 椽,等.贵州普定水库沉积物重金属分布及污染特征 [J]. 中国环境科学, 2017,37(12):4710-4721.
[2]范小杉,罗 宏.工业废水重金属排放区域及行业分布格局 [J].中国环境科学, 2013,33(4):655-662.
[3]Fu F, Wang Q. Removal of heavy metal ions from wastewaters: A review [J]. Journal of Environmental Management, 2011,92(3):407-418.
[4]Bailey S E, Olin T J, Bricka R M, et al. A review of potentially low-cost sorbents for heavy metals [J]. Water Research, 1999,33(11):2469-2479.
[5]包汉峰,杨维薇,张立秋,等.污泥基活性炭去除水中重金属离子效能与动力学研究 [J]. 中国环境科学, 2013,33(1):69-74.
[6]孙 岩,吴启堂,许田芬,等.土壤改良剂联合间套种技术修复重金属污染土壤:田间试验 [J]. 中国环境科学, 2014,34(8):2049-2056.
[7]丁述理,孙晨光.膨润土吸附水中 Cr(Ⅵ)的影响因素研究 [J].非金属矿, 2006,(3):45-48.
[8]梁 莎,冯宁川,郭学益.生物吸附法处理重金属废水研究进展[J]. 水处理技术. 2009,(3):13-17.
[9]王建龙,陈 灿.生物吸附法去除重金属离子的研究进展 [J].环境科学学报, 2010,(4):673-701.
[10]张安超,向 军,路 好,等.酸-碘改性壳聚糖-膨润土脱除单质汞特性及机理分析 [J]. 中国环境科学, 2013,33(10):1758-1764.
[11]周书葵,曾光明,刘迎九,等.改性羧甲基纤维素对铀吸附机理的试验研究 [J]. 中国环境科学, 2011,31(9):1466-1471.
[12]路 瑶,魏贤勇,宗志敏,等.木质素的结构研究与应用 [J]. 化学进展, 2013,(5):838-858.
[13]Muzzarelli R A A. Potential of chitin/chitosan-bearing materials for uranium recovery: An interdisciplinary review [J].Carbohydrate Polymers, 2011,84(1):54-63.
[14]Feng Y, Gong J, Zeng G, et al. Adsorption of Cd (II) and Zn (II)from aqueous solutions using magnetic hydroxyapatite nanoparticles as adsorbents [J]. Chemical Engineering Journal,2010,162(2):487-494.
[15]Kim D K, Zhang Y, Voit W, et al. Synthesis and characterization of surfactant-coated superparamagneticmonodispersed iron oxide nanoparticles [J]. Journal of Magnetism and Magnetic Materials,2001,225(1/2):30-36.
[16]Gupta A K, Gupta M. Synthesis and surface engineering of iron oxide nanoparticles for biomedical applications [J]. Biomaterials,2005,26(18):3995-4021.
[17]Li G, Jiang Y, Huang K, et al. Preparation and properties of magnetic Fe3O4-chitosan nanoparticles [J]. Journal of Alloys and Compounds, 2008,466(1/2):451-456.
[18]宋艳艳,孔维宝,宋 昊,等.磁性壳聚糖微球的研究进展 [J]. 化工进展, 2012,31(2):345-354.
[19]Liu Z, Bai H, Sun D D. Facile fabrication of porous chitosan/TiO2/Fe3O4microspheres with multifunction for water purifications [J].NEW Journal of Chemistry, 2011,35(1):137-140.
[20]Wang C, Yang C, Huang K, et al. Electrostatic droplets assisted in situ synthesis of superparamagnetic chitosan microparticles for magnetic-responsive controlled drug release and copper ion removal [J]. Journal of Materials Chemistry B. 2013,1(16):2205-2212.
[21]程三旭,李克智,齐乐华,等.反向共沉淀法制备纳米 Fe3O4及其粒径控制 [J]. 材料研究学报, 2011,(5):489-494.
[22]Bulut Y, Gozubenli N, Aydin H. Equilibrium and kinetics studies for adsorption of direct blue 71from aqueous solution by wheat shells [J].Journal of Hazardous Materials, 2007,144(1/2):300-306.
[23]王珏珏,张越非,池汝安,等.改性木质素磺酸钠对铅离子的吸附行为研究 [J]. 武汉工程大学学报, 2017,39(1):12-18.
[24]涂艳梅,杨汉培,聂 坤,等.磺乙基化与传统壳聚糖对比研究其对水体中铅有效性降低效应 [J]. 环境科技, 2016,29(2):1-6.
[25]王春云,闫新豪,符纯美.基于甘蔗渣生物吸附重金属污染物的研究 [J]. 当代化工. 2017,(1):61-63.

